2018年北京市西城区高三化学二模物理带答案word版
北京市海淀西城朝阳东城2018届高三二模化学试题及答案(官方版)

专业 K12 教研共享平台
(3)C 的结构简式是______。 (4)D→F 的反应类型是______,F→G 的化学方程式是______。 (5)J 的结构简式是______。 (6)K 含有六原子环结构,K→L 的化学方程式是______。 (7)G 和 L 经过 3 步反应合成 N,路线如下:
(4)取代反应(或酯化反应)
北京市西城区 2018 年 5 月高三理科综合 第12页(共15页)
专业 K12 教研共享平台
(5) (6) (7) 26. (12分, (1)和(3)第一空1分,其他每空2分) (1) (2)① ② 温度越高,反应速率越快 反应温度过高,乙二醇会深度加氢生成乙醇,乙二醇的产率降低 (3)负 CO2 + 6H+ + 6e− == CH3OH + H2O (4)abc 27. (13分, (1)1分,其他每空2分)
北京市西城区 2018 年 5 月高三理科综合 第2页(共15页)
专业 K12 教研共享平台
11. 在金属 Pt、Cu 和铱(Ir)的催化作用下,密闭容器中的 H2 可高效转化酸性溶液中的硝态 氮(NO3−)以达到消除污染的目的。其工作原理的示意图如下:
下列说法不正确 的是 ...
Ir
北京市西城区 2018 年 5 月高三理科综合 第1页(共15页)
专业 K12 教研共享平台
B.加入少量 CH3COONa 固体后,溶液 pH 升高 C.加 0.1 mol·L−1 CH3COONa 溶液使 pH>7,则 c(CH3COO−)=c(Na+) D.与等体积 pH=11 的 NaOH 溶液混合,所得溶液呈中性 9.下列说法正确的是 A.分别向等物质的量浓度的Na2CO3和NaHCO3溶液中滴加2滴酚酞溶液,后者红色更深 B.分别向2 mL5%H2O2溶液中滴加1 mL 0.1 mol·L−1 FeCl3和CuSO4溶液,产生气泡快慢不相同 C.蛋白质溶液遇饱和 Na2SO4 溶液或醋酸铅溶液均产生沉淀,沉淀均可溶于水 D.加热 NH4Cl 和 Ca(OH)2 固体的混合物,可将二者分离
北京市西城区2018届高三二模试题理科综合试卷含答案
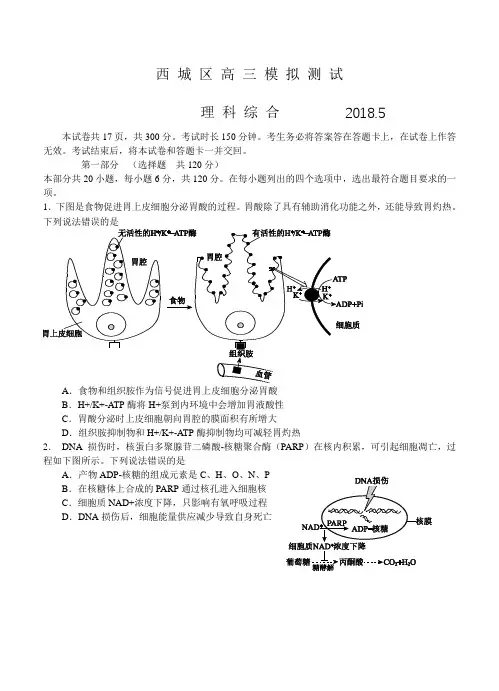
西城区高三模拟测试理科综合2018.5本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
1.下图是食物促进胃上皮细胞分泌胃酸的过程。
胃酸除了具有辅助消化功能之外,还能导致胃灼热。
下列说法错误的是A.食物和组织胺作为信号促进胃上皮细胞分泌胃酸B.H+/K+-ATP酶将H+泵到内环境中会增加胃液酸性C.胃酸分泌时上皮细胞朝向胃腔的膜面积有所增大D.组织胺抑制物和H+/K+-ATP酶抑制物均可减轻胃灼热2.DNA损伤时,核蛋白多聚腺苷二磷酸-核糖聚合酶(PARP)在核内积累,可引起细胞凋亡,过程如下图所示。
下列说法错误的是A.产物ADP-核糖的组成元素是C、H、O、N、PB.在核糖体上合成的PARP通过核孔进入细胞核C.细胞质NAD+浓度下降,只影响有氧呼吸过程D.DNA损伤后,细胞能量供应减少导致自身死亡3.脱落酸(ABA)和赤霉素(GA)在种子萌发中起重要作用。
用35S-甲硫氨酸“饲喂”不同激素处理的大麦种子,提取蛋白质进行电泳,结果如右图。
下列说法错误的是A.在图中所示的蛋白质中,α-淀粉酶分子最大B.35S-甲硫氨酸是合成淀粉酶等蛋白质的原料C.ABA能拮抗GA诱导的α-淀粉酶合成D.GA通过抑制某些蛋白质合成抑制萌发4.栎树是某森林中主要的生产者,舞毒蛾啃食栎树。
栎树盛果期时丰富的果实会把白尾鹿吸引到森林中,鹿身上的扁虱会跳到森林地面产卵。
大量的栎树果实也吸引着白足鼠,扁虱卵孵化出的幼虫吸食白足鼠血和人血,同时会将白足鼠体内的螺旋菌传播给人类,使人类患上莱姆病。
下列相关分析错误的是A.扁虱与鼠、鹿、人之间的寄生关系导致螺旋菌传播到人B.舞毒蛾数量增加使栎树减产,人类患莱姆病的风险增加C.栎树盛果期时,该区域人类患上莱姆病的风险明显提高D.生物多样性是维持生态系统结构和功能稳态的必要条件5.利用竞争酶联免疫检测技术,检测抗虫棉中Bt抗虫蛋白表达量,原理如下图所示。
西城区2018届高三二模理综化学试题及答案

99.9
94.7
62.3
220
99.9
92.4
46.1
由上表可知,温度越高,EC 的转化率越高,原因是______。
温度升高到 220 ℃时,乙二醇的产率反而降低,原因是______。
(3)用稀硫酸作电解质溶液,电解 CO2 可制取甲醇,装置如下图所示,电极 a 接电源的______
极(填“正”或“负”),生成甲醇的电极反应式是______。
(1)ClO− + H2O OH− + HClO (2)ClO− + 2I− + H2O == I2 + Cl− + 2OH− (3)① 向 pH=10 的 NaOH 溶液中加入少量滴有淀粉溶液的碘水,振荡,蓝色褪去
② 碘水 右侧碘水棕黄色变浅,电流表的指针偏转
(4)①Cl2 ②溶液中的 Cl2 或 HClO 也可将 I−氧化为 I2,使溶液变蓝 加热 pH=2 的溶液至无色,使黄绿色气体(或 Cl2)充分逸出,使 HClO 完全分解,冷却后再 加入 KI 溶液
12.D
(2) (4)取代反应(或酯化反应)
(3)
(5)
(6)
(7) 26.(12分,(1)和(3)第一空1分,其他每空2分) (1)
(2)①
② 温度越高,反应速率越快
反应温度过高,乙二醇会深度加氢生成乙醇,乙二醇的产率降低
(3)负
CO2 + 6H+ + 6e− == CH3OH + H2O
27.(13分,(1)1分,其他每空2分)
(4)abc
(1)CaO + O2 + V2O3焙==烧== Ca(VO3)2 (2)① Ca(VO3)2 + 4H+ == 2VO2+ + Ca2+ + 2H2O
北京市西城区2018年5月高三模拟测试(二模)理科综合试题及答案

西城区高三模拟测试理科综合2018.5本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
1.下图是食物促进胃上皮细胞分泌胃酸的过程。
胃酸除了具有辅助消化功能之外,还能导致胃灼热。
下列说法错误..的是A.食物和组织胺作为信号促进胃上皮细胞分泌胃酸B.H+/K+-ATP酶将H+泵到内环境中会增加胃液酸性C.胃酸分泌时上皮细胞朝向胃腔的膜面积有所增大D.组织胺抑制物和H+/K+-ATP酶抑制物均可减轻胃灼热北京市西城区2018年5月高三理科综合第1页(共35页)2.DNA损伤时,核蛋白多聚腺苷二磷酸-核糖聚合酶(PARP)在核内积累,可引起细胞凋亡,过程如下图所示。
下列说法错误..的是A.产物ADP-核糖的组成元素是C、H、O、N、PB.在核糖体上合成的PARP通过核孔进入细胞核C.细胞质NAD+浓度下降,只影响有氧呼吸过程D.DNA损伤后,细胞能量供应减少导致自身死亡北京市西城区2018年5月高三理科综合3.脱落酸(ABA)和赤霉素(GA)在种子萌发中起重要作用。
用35S-甲硫氨酸“饲喂”不同激素处理的大麦种子,提取蛋白质进行电泳,结果如右图。
下列说法错误..的是A.在图中所示的蛋白质中,α-淀粉酶分子最大B.35S-甲硫氨酸是合成淀粉酶等蛋白质的原料C.ABA能拮抗GA诱导的α-淀粉酶合成D.GA通过抑制某些蛋白质合成抑制萌发4.栎树是某森林中主要的生产者,舞毒蛾啃食栎树。
栎树盛果期时丰富的果实会把白尾鹿吸引到森林中,鹿身上的扁虱会跳到森林地面产卵。
大量的栎树果实也吸引着白足鼠,扁虱卵孵化出的幼虫吸食白足鼠血和人血,同时会将白足鼠体内的螺旋菌传播给人类,使人类患上莱姆病。
下列相关分析错误..的是A.扁虱与鼠、鹿、人之间的寄生关系导致螺旋菌传播到人B.舞毒蛾数量增加使栎树减产,人类患莱姆病的风险增加C.栎树盛果期时,该区域人类患上莱姆病的风险明显提高D.生物多样性是维持生态系统结构和功能稳态的必要条件5.利用竞争酶联免疫检测技术,检测抗虫棉中Bt抗虫蛋白表达量,原理如下图所示。
9答案-西城二模物理2018.5

西城区高三模拟测试-物理参考答案及评分标准 2018.513.A 14.B 15.C 16.D 17.B 18.B 19.D 20.D 21.(18分)(1)C (4分)(2)①A 2,R 1 ②乙 ③如右图所示④0.68 ⑤ B说明:①~④每空2分,作图2分,⑤ 4分 22.(16分)(1)(4分)由匀强电场中电势差与场强的关系得=U E d(2)a. (6分)粒子在磁场中运动时根据牛顿第二定律 2=mv qvB RL=2R解得 2qBLP mv ==b. (6分)粒子在电场中运动时根据动能定理 212=qU mv解得 m= 228qB LU23.(18分) (1)(4分)以飞机和金属棒为研究对象根据动量守恒定律 Mv 0 =(M + m )v解得它们共同的速度 0Mv v M m=+ (2)(6分)飞机钩住金属棒后它们以速度v 开始在安培力的作用下做减速运动,所以当它们速度为v 时安培力最大,此时由安培力产生的加速度也最大 根据牛顿第二定律 BIL =(M + m )a根据全电路欧姆定律 B L vI R r =+ 联立以上两式解得 2202()()B L Mv a R r M m =++(3)(8分)以飞机和金属棒为研究对象,在很短的一段时间∆t 内根据动量定理 BiL ·∆t =(M + m )∆v ①在某时刻根据全电路欧姆定律 BLv i R r=+i② 由①②两式得 ()BLv BL t M m v R r∆=+∆+i③ 飞机经时间t 停下来,对③式在时间t 内求和22()B L x M m v R r=++ 解得 022()Mv R r x B L +=24.(20分)(1)a. (2分)在x 方向,因为小球不受力的作用,所以影子做匀速直线运动;在y 方向,因为小球仅受重力的作用,初速度为0,所以影子做初速度为 零的匀加速直线运动。
b. (5分)此时x 方向的影子速度 v x = v 0 = 20m/s y 方向的影子速度 v y = gt = 20m/s小球的速度v =代入数据解得2m /s =28.2m /sv = 20120y xv tg v θ===, θ = 45° 速度方向与x 方向成45°角(2)a. (6分)以小球A 为研究对象,设它经过平衡位置O 时的速度为v ,当它从O 运动到最大位移处,根据机械能守恒有221122mv kR =,由此得v =①。
2018届北京市西城区高三二模化学试题及答案 精品

北京市西城区2018年高三二模试卷2018.5【PGS35】选择题(共20题每小题6分共120分)6.下列物质与危险化学品标志的对应关系不正确...的是7.化学与生产、生活密切相关。
下列叙述正确的是A.煤的干馏和煤的液化均是物理变化B.海水淡化的方法有蒸馏法、电渗析法等C.天然纤维和合成纤维的主要成分都是纤维素D.用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同答案:B8.下列解释事实的化学方程式不正确...的是A.金属钠在空气中加热,生成淡黄色固体:2Na+O2 === Na2O2B.向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O=Al(OH)3↓+3NH4+C.铁在潮湿的环境中生锈:3Fe+4H2O= Fe3O4+4H2↑△D .二氧化氮溶于水有硝酸生成:3NO 2+H 2O=2HNO 3+NO 答案:C9.下列说法不正确...的是 A .为除去FeSO 4溶液中的Fe 2(SO 4)3,可加入铁粉,再过滤 B .为除去溴苯中的溴,可用NaOH 溶液洗涤,再分液 C .为除去乙炔气中少量的H 2S ,可使其通过CuSO 4溶液 D .为除去CO 2中少量的SO 2,可使其通过饱和Na 2CO 3溶液 答案:D10示意图如下。
下列说法不正确...A .O 2在电极b 上发生还原反应B .溶液中OH —向电极a 移动C .反应消耗的NH 3与O 2D .负极的电极反应式为:2NH 3-6e —+6OH —=N 2+6H 2O 答案:C11.依据下列实验现象,得出的结论正确的是答案:D12.恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g) 反应过程中测定的部分数据见下表:下列说法正确的是A.0~2 min内的平均速率为υ (CO)=0.6 mol/(L·min) B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol 的SO2C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)=0.6 mol答案:B25.(17分)可降解塑料PCL其合成路线如下。
西城区2018届高三二模理综化学试题及答案(word版)
西 城 区 高 三 模 拟 测 试理 科 综 合 2018.5本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分 (选择题 共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
6.下列物质的分离方法中,利用粒子大小差异的是A .过滤豆浆B .酿酒蒸馏C .精油萃取D .海水晒盐7.4种短周期元素在周期表中的位置如下图,X 原子最外层有6个电子。
下列说法不正确...的是 A .离子半径:X 2−<Y 2− B .非金属性:W <XC .还原性:Y 2−<Z − D .酸性:H 2YO 4<HZO 48.下列关于pH =3的CH 3COOH 溶液的叙述正确的是 A .溶液中H 2O 电离出的c (OH −)=1.0×10−3 mol·L −1 B .加入少量CH 3COONa 固体后,溶液pH 升高C .加0.1 mol·L −1 CH 3COONa 溶液使pH >7,则c (CH 3COO −)=c (Na +)D .与等体积pH =11的NaOH 溶液混合,所得溶液呈中性 9.下列说法正确的是A .分别向等物质的量浓度的Na 2CO 3和NaHCO 3溶液中滴加2滴酚酞溶液,后者红色更深W XYZB.分别向2 mL5%H2O2溶液中滴加1 mL 0.1 mol·L−1 FeCl3和CuSO4溶液,产生气泡快慢不相同C.蛋白质溶液遇饱和Na2SO4溶液或醋酸铅溶液均产生沉淀,沉淀均可溶于水D.加热NH4Cl和Ca(OH)2固体的混合物,可将二者分离10.聚氨酯类高分子材料PU用途广泛,其合成反应为:下列说法不正确的是...A.HO(CH2)4OH的沸点高于CH3CH2CH2CH3B.高分子材料PU在强酸、强碱中能稳定存在C.合成PU的两种单体的核磁共振氢谱中均有3个吸收峰D.以1,3-丁二烯为原料,可合成HO(CH2)4OH11.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3−)以达到消除污染的目的。
2018.5西城高三化学二模答案
西城区高三模拟测试理科综合参考答案及评分标准2018.5第一部分共20小题,每小题6分,共120分。
6.A7.C8.B9.B10.B11.C12.D第二部分共11小题,共180分。
25~28题其他正确答案可参照本标准给分25.(17分,(1)1分,其他每空2分)(1)羟基(2(3(4)取代反应(或酯化反应)(5(6(726.(12分,(1)和(3)第一空1分,其他每空2分)(1②温度越高,反应速率越快反应温度过高,乙二醇会深度加氢生成乙醇,乙二醇的产率降低(3)负CO2 + 6H+ + 6e− == CH3OH + H2O(4)abc27.(13分,(1)1分,其他每空2分)焙烧(1)CaO + O2 + V2O3 ====Ca(VO3)2(2)①Ca(VO3)2 + 4H+ ==2VO2+ + Ca2+ + 2H2O②酸度大于3.2%时,钒的溶解量增大不明显,而铝的溶解量增大程度更大(3)①调节溶液的pH,并提供Ca2+,形成Ca3(VO4)2沉淀(富集钒元素)②Ca3(VO4)2的浊液中存在平衡Ca3(VO4)2(s)3Ca2+(aq) + 2VO43−(aq) ,(NH4)2CO3溶液中的CO32−与Ca2+结合生成更难溶的CaCO3沉淀,c(Ca2+)降低,平衡正向移动,使钒从沉淀中溶出③pH>8时,钒的主要存在形式不是VO3−(4)91(c1b1-5c2b2)/(1000a)28.(16分,(1)和(4)①1分,其他每空2分)(1)ClO− + H2O OH− + HClO(2)ClO− + 2I− + H2O ==I2 + Cl− + 2OH−(3)①向pH=10的NaOH溶液中加入少量滴有淀粉溶液的碘水,振荡,蓝色褪去②碘水右侧碘水棕黄色变浅,电流表的指针偏转(4)①Cl2②溶液中的Cl2或HClO也可将I−氧化为I2,使溶液变蓝加热pH=2的溶液至无色,使黄绿色气体(或Cl2)充分逸出,使HClO完全分解,冷却后再加入KI溶液③3ClO− + I− ==3Cl− + IO3−。
北京市西城区高三理综(化学部分)5月模拟测试(二模)试题
北京市西城区2018届高三理综(化学部分)5月模拟测试(二模)试题6.下列物质的分离方法中,利用粒子大小差异的是7.4种短周期元素在周期表中的位置如下图,X原子最外层有6个电子。
下列说法不正确的是A.离子半径: X2-<Y2-B.非金属性:W<XC.还原性: Y2-<Z-D.酸性: H2YO4< HZO48.下列关于pH=3的CH3COOH溶液的叙述正确的是A.溶液中H2O电离出的c(OH-)=1.0×10-3mol/LB.加入少量CH3COONa固体后,溶液pH升高C.加0.1mol/LCH3COONa 溶液使pH>7,则c(CH3COO-)=c(Na+)D.与等体积pH=11的NaOH溶液混合,所得溶液呈中性9.下列说法正确的是A.分别向等物质的量浓度的Na2CO3和NaHCO3溶液中滴加2滴酚酞溶液,后者红色更深B.分别向2mL5%H2O2溶液中滴加1mL0.1mol/LFeCl3和CuSO4溶液,产生气泡快慢不相同C.蛋白质溶液遇饱和Na2SO4溶液或醋酸铅溶液均产生沉淀,沉淀均可溶于水D.加热NH4Cl和Ca(OH)2固体的混合物,可将二者分离10. 聚氨酯类高分子材料PU用途广泛,其合成反应为:下列说法不正确的是A.HO(CH2)4OH 的沸点高于CH3CH2CH2CH3B.高分子材料PU 在强酸、强碱中能稳定存在C.合成PU的两种单体的核磁共振氢谱中均有3个吸收峰D.以1,3-丁二烯为原料,可合成HO(CH2)4OH11.在金属Pt、Cu和铱(Ir) 的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-) 以达到消除污染的目的。
其工作原理的示意图如下:下列说法不正确的是A.Ir的表面发生反应: H2+N2O N2+H2OB.导电基体上的负极反应: H2-2e-=2H+C.若导电基体上只有单原子铜,也能消除含氮污染物D.若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量12.某同学用如下装置进行实验①和②,在相同时间内,记录现象如下(溶液的温度变化均不明显)。
北京市西城区2017-2018学年高三二模理综物理试卷 Word版含解析
2017-2018学年北京市西城区高三二模物理试卷一、单选题(共8小题)1.关于两个分子之间的相互作用力和分子势能,下列判断正确的是()A.两分子处于平衡位置,分子间没有引力和斥力B.两分子间距离减小,分子间的引力和斥力都增大C.两分子间距离减小,分子势能一定减小D.两分子间距离增大,分子势能一定增大考点:分子力分子动理论与统计观点答案:B试题解析:两分子处于平衡位置,分子间引力和斥力相等,故A错;分子间的引力和斥力均随分子距离的减小而增大,故B正确;分子势能增大或减小,取决于分子间引力和斥力做的总攻,比如,当分子间的斥力大于引力,减小分子间的距离,分子间总的作用力做负功,分子势能增大,而增大分子间的距离,分子间总的作用力做正功,分子势能减小,故从C,D均错;2.下列几个光现象中,属于衍射现象的是()A.水中的气泡看起来特别明亮B.白光通过三棱镜在屏上出现彩色光带C.在阳光照射下肥皂泡上出现彩色花纹D.通过两支铅笔夹成的狭缝看点亮的日光灯出现彩色条纹考点:光答案:D试题解析:水中的气泡看起来特别明亮属于光的全反射;白光通过三棱镜在屏上出现彩色光带属于光的色散;在阳光照射下肥皂泡上出现彩色花纹属于薄膜干涉;通过两支铅笔夹成的狭缝看点亮的日光灯出现彩色条纹属于单缝衍射;故选D;3.为纪念中国航天事业的成就,发扬航天精神,自2016年起,将每年的4月24日设立为“中国航天日”。
在46年前的这一天,中国第一颗人造卫星发射成功。
至今中国已发射了逾百颗人造地球卫星。
关于环绕地球做圆周运动的卫星,下列说法正确的是()A.卫星的向心加速度一定小于9.8m/s2B.卫星的环绕速度可能大于7.9km/sC.卫星的环绕周期一定等于24hD.卫星做圆周运动的圆心不一定在地心上考点:万有引力定律及其应用万有引力定律答案:A试题解析:卫星做匀速圆周运动时,其加速度会随着高度的增大而减小,9.8是最大的向心加速度,故A正确;卫星做匀速圆周运动时,其线速度会随着高度的增大而减小,7.9是最大的线速度,故B错误;只有地球同步卫星的周期是24,其他种类的卫星不是24,故C错误;卫星做匀速圆周运动,万有引力全部提供向心力,故圆心一定在地球的球心,故D错误;4.如图所示,有一圆形匀强磁场区域,O为圆的圆心,磁场方向垂直纸面向里。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
西城区高三模拟测试-物理2018.513.碳12的原子核是由6个质子和6个中子构成的,各质子之间存在着三种相互作用力,万有引力、库仑力和核力。
这三种相互作用力的大小由弱到强的顺序是 A .万有引力、库仑力、核力 B .万有引力、核力、库仑力 C .库仑力、万有引力、核力 D .核力、万有引力、库仑力14.一束激光照在一个很小的圆盘上,在屏上观察到如图所示的图样,在影的中心有一个亮斑,这就是著名的“泊松亮斑”。
下列说法正确的是 A .圆盘中心有个小孔,这是光的衍射现象 B .圆盘中心是不透光的,这是光的衍射现象 C .圆盘中心有个小孔,这是光的干涉现象 D .圆盘中心是不透光的,这是光的干涉现象15.下列说法正确的是A .光波的传播需要介质B .在真空中电磁波的传播速度小于光速C .X 射线、γ射线都是电磁波D .发声体振动时在空气中产生的声波是横波16.如图所示为交流发电机的示意图,从线圈通过如图所示的位置开始计时。
如果发电机产生的交变电流的频率为50Hz ,电动势的最大值为400V ,则发电机产生的电动势瞬时值表 达式为A . e = 400sin50t (V )B . e = 400cos50t (V )C . e = 400sin100πt (V )D . e = 400cos100πt (V )17.火星有两颗卫星,分别记作火卫一和火卫二,它们的轨道近似为圆形。
已知火卫一的运行周期为7小时39分,火卫二的运行周期为30小时18分。
由此可以判断,这两颗卫星 A .火卫一距火星表面较近且线速度较小B .火卫一距火星表面较近且向心加速度较大C .火卫二距火星表面较近且线速度较大D .火卫二距火星表面较近且角速度较小18.一种巨型娱乐器械可以使人体验超重和失重。
一个可乘十多个人的环形座舱套装在竖直柱子上,由升降机送上几十米的高处,然后让座舱自由落下。
落到一定位置时,制动系统启动,座舱做减速运动,到地面时刚好停下。
在上述过程中,关于座舱中的人所处的状态,下列判断正确的是A .座舱在自由下落的过程中人处于超重状态B .座舱在减速运动的过程中人处于超重状态C .座舱在整个运动过程中人都处于失重状态D .座舱在整个运动过程中人都处于超重状态19.我们通常用阴极射线管来研究磁场、电场对运动电荷的作用,如图所示为阴极射线管的示意图。
玻璃管已抽成真空,当左右两个电极连接到高压电源时,阴极会发射电子,电子在电场的加速下,由阴极沿x 轴方向飞向阳极,电子掠射过荧光屏,屏上亮线显示出电子束的径迹。
要使电子束的径迹向z 轴正方向偏转,在下列措施中可采用的是 A .加一电场,电场方向沿z 轴正方向 B .加一电场,电场方向沿y 轴负方向 C .加一磁场,磁场方向沿z 轴正方向 D .加一磁场,磁场方向沿y 轴负方向20.电动汽车由于节能环保的重要优势,越来越被大家认可。
电动汽车储能部件是由多个蓄电池串联叠置组成的电池组,如图所示。
某品牌电动小轿车蓄电池的数据如下表所示。
下列说法正确的是A .将电池组的两极直接接在交流电上进行充电B .电池容量的单位Ah 就是能量单位C .该电池组充电时的功率为4.4kWD .该电池组充满电所储存的能量为1.4╳108J21.(18分)(1)在做“用油膜法估测分子的大小”实验时,先配制好一定浓度的油酸酒精溶液,并得到1滴油酸酒精溶液的体积为V 。
往浅盘里倒入约2cm 深的水,然后将痱子粉均匀地撒在水面上。
用注射器往水面上滴1滴油酸酒精溶液,油酸立即在水面散开,形成一块薄膜,薄膜上没有痱子粉,可以清晰地看出它的轮廓,如图1所示。
待薄膜形状稳定后量出它的面积为S 。
在这个实验中,下列说法正确的是 。
A .根据Vd S =就可以粗略地测量酒精分子的直径 B .根据Vd S=就可以精确地测量油酸分子的直径C .选择油酸作为被测物质,是因为油酸的物理性质有助于油酸在水面上形成单分子膜(2)在做“描绘小灯泡的伏安特性曲线”的实验中,选用的小灯泡规格为“3.8 V ,0.3 A ”。
① 除了导线和开关外,有以下一些器材可供选择:电流表:A 1(量程3A ,内阻约0.1Ω)、A 2(量程0.6 A ,内阻约0.3Ω); 电压表:V (量程5 V ,内阻约5kΩ);滑动变阻器:R 1(阻值范围0~10Ω)、R 2(阻值范围0~2kΩ); 电源:E (电动势为4 V ,内阻约为0.04Ω)。
为了调节方便,测量准确,实验中应选用电流表_______,滑动变阻器________。
(填器材的符号)② 为尽量精准的描绘小灯泡的伏安特性曲线,应选用的实验电路为图2中的+乙+图2图1③ 某同学记录了多组数据,并且将这些数据的对应点标在了图3的坐标纸上,请根据这些点 在图3中画出I -U 图线。
④ 从图线可知,当灯泡两端电压为2.6V 时,小灯泡的功率等于 W (保留两位有效数字)。
⑤ 将实验所用小灯泡接入如图4所示的电路中,其中A 是电流传感器。
当开关S 闭合前后,结合以上所作的I -U 图线,分析判断通过小灯泡的电流随时间变化的图像,应该是图5所示四个图像中的 。
22.(16分)如图所示,两平行金属板间距为d ,两板间的电势差为U ,板间电场可视为匀强电场。
金属板上方有磁感应强度为B 的匀强磁场。
电荷量为+q 的微观粒子,由静止开始从正极板出发,经电场加速后射出,从M 点进入磁场做匀速圆周运动,最后从N 点离开磁场。
忽略重力的影响。
(1)求匀强电场场强的大小E ;(2)若测得M 、N 两点间距离为L , 求:a. 粒子从电场射出时的动量P ;b. 粒子的质量m 。
× × × × × × × × × AS 图4图5A B I 图323.(18分)2012年11月,“歼15”舰载机在“辽宁号”航空母舰上着舰成功,它的阻拦技术原理是,飞机着舰时利用阻拦索的作用力使它快速停止。
随着电磁技术的日趋成熟,新一代航母已准备采用全新的电磁阻拦技术,它的阻拦技术原理是,飞机着舰时利用电磁作用力使它快速停止。
为研究问题的方便,我们将其简化为如图所示的模型。
在磁感应强度为B 、方向如图所示的匀强磁场中,两根平行金属轨道MN 、PQ 固定在水平面内,相距为L ,电阻不计。
轨道端点MP 间接有阻值为R 的电阻。
一个长为L 、质量为m 、阻值为r 的金属导体棒ab 垂直于MN 、PQ 放在轨道上,与轨道接触良好。
质量为M 的飞机以水平速度v 0迅速钩住导体棒ab ,钩住之后关闭动力系统并立即获得共同的速度。
假如忽略摩擦等次要因素,飞机和金属棒系统仅在安培力作用下很快停下来。
求:(1)飞机钩住金属棒后它们获得的共同速度v 的大小; (2)飞机在阻拦减速过程中获得的加速度a 的最大值;(3)从飞机钩住金属棒到它们停下来的整个过程中运动的距离x 。
R aN24.(20分)合成与分解是物理常用的一种研究问题的方法,如研究复杂的运动就可以将其分解成 两个简单的运动来研究。
请应用所学物理知识与方法,思考并解决以下问题。
(1)如图1所示,将一小球以v 0=20m/s 的初速度从坐标轴原点O 水平抛出,两束平行光分别沿着与坐标轴平行的方向照射小球,在两个坐标轴上留下了小球的两个“影子”,影子的位移和速度描述了小球在x 、y 两个方向的运动。
不计空气阻力的影响,g =10m/s 2。
a .分析说明两个“影子”分别做什么运动;b .经过时间t = 2s 小球到达如图1所示的位置,求此时小球的速度v 。
(2)如图2所示,把一个有孔的小球A 装在轻质弹簧的一端,弹簧的另一端固定,小球穿在沿水平x 轴的光滑杆上,能够在杆上自由滑动。
把小球沿x 轴拉开一段距离,小球将做振幅为R 的振动,O 为振动的平衡位置。
另一小球B 在竖直平面内以O ′为圆心,在电动机的带动下,沿顺时针方向做半为径R 的匀速圆周运动。
O 与O ′在同一竖直线上。
用竖直向下的平行光照射小球B ,适当调整B 的转速,可以观察到,小球B 在x 方向上的“影子”和小球A 在任何瞬间都重合。
已知弹簧劲度系数为k ,小球A 的质量为m ,弹簧的弹性势能表达式为212kx ,其中k 是弹簧的劲度系数,x 是弹簧的形变量。
a .请结合以上实验证明:小球A振动的周期2T = b .简谐运动的一种定义是:如果质点的位移x 与时间t 的关系遵从正弦函数的规律,即它的振动图像(x-t 图像)是一条正弦曲线,这样的振动叫做简谐运动。
请根据这个定义并结合以上实验证明:小球A 在弹簧作用下的振动是简谐运动,并写出用已知量表示的位移x 与时间t 关系的表达式。
西城区高三模拟测试-物理参考答案及评分标准 2018.513.A 14.B 15.C 16.D 17.B 18.B 19.D 20.D平行光图2图1平行光影子y 平行光21.(18分) (1)C (4分)(2)①A 2,R 1 ②乙 ③如右图所示④0.68 ⑤ B说明:①~④每空2分,作图2分,⑤ 4分 22.(16分)(1)(4分)由匀强电场中电势差与场强的关系得=U E d(2)a. (6分)粒子在磁场中运动时根据牛顿第二定律 2=mv qvB RL=2R解得 2qBLP mv ==b. (6分)粒子在电场中运动时根据动能定理 212=qU mv解得 m= 228qB L U23.(18分) (1)(4分)以飞机和金属棒为研究对象根据动量守恒定律 Mv 0 =(M + m )v解得它们共同的速度 0Mv v M m=+ (2)(6分)飞机钩住金属棒后它们以速度v 开始在安培力的作用下做减速运动,所以当它们速度为v 时安培力最大,此时由安培力产生的加速度也最大 根据牛顿第二定律 BIL =(M + m )a根据全电路欧姆定律 B L vI R r =+ 联立以上两式解得 2202()()B L Mv a R r M m =++(3)(8分)以飞机和金属棒为研究对象,在很短的一段时间∆t 内根据动量定理 BiL ·∆t =(M + m )∆v ①在某时刻根据全电路欧姆定律 BLv i R r=+i② 由①②两式得 ()BLv BL t M m v R r∆=+∆+i③ 飞机经时间t 停下来,对③式在时间t 内求和22()B L x M m v R r=++ 解得 022()Mv R r x B L+=24.(20分)(1)a. (2分)在x 方向,因为小球不受力的作用,所以影子做匀速直线运动;在y 方向,因为小球仅受重力的作用,初速度为0,所以影子做初速度为 零的匀加速直线运动。
b. (5分)此时x 方向的影子速度 v x = v 0 = 20m/s y 方向的影子速度 v y = gt = 20m/s小球的速度v =代入数据解得2m /s =28.2m /sv = 20120y xv tg v θ===, θ = 45° 速度方向与x 方向成45°角(2)a. (6分)以小球A 为研究对象,设它经过平衡位置O 时的速度为v ,当它从O 运动到最大位移处,根据机械能守恒有221122mv kR =,由此得v =①。
