高一化学知识小卡片·硫化氢的实验室制法(51)
氯化氢、硫化氢、二氧化硫、乙炔、乙酸乙酯de实验室制法

氯化氢的实验室制法实验室里制取氯化氢是利用食盐和浓硫酸在不加热或稍微加热的条件下进行反应。
化学方程式是:NaCl+H2SO4(浓)=NaHSO4+HCl↑这个反应是属于固体粉末与液体反应制取气体的类型,所用制气装臵与实验室制取氯气的一样(参看氯气的实验室制法)。
氯化氢极易溶于水,密度比空气大,只能用向上排空气法进行收集。
氯化氢有很强的刺激性气味,收集氯化氢后的剩余尾气,不能逸散在室内,可用水进行吸收。
硫化氢的实验室制法实验室里通常是用硫化亚铁跟稀盐酸或稀硫酸反应制取硫化氢,它们的化学方程式是:FeS+2HCl=FeCl2+H2S↑FeS+H2SO4(稀)=FeSO4+H2S↑制取硫化氢使用的是块状固体与液体反应制取气体的仪器装臵(参看《初中卷》使用固体和液体药品制备气体的仪器装臵)。
硫化氢易溶于水,密度比空气大,应使用向上排空气法收集。
检验集气瓶内是否已集满硫化氢,可将润湿的醋酸铅试纸放在集气瓶口,若试纸立即变黑,证明瓶内硫化氢气已集满。
二氧化硫的实验室制法在实验室里,常用亚硫酸钠跟浓硫酸起反应制取二氧化硫。
化学方程式是:Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑制气装臵是用固体粉末与液体反应制取气体的仪器装臵(参看《初中卷》使用固体和液体药品制备气体的仪器装臵)。
二氧化硫易溶于水,密度比空气大,收集二氧化硫是用向上排空气集气法。
氨的实验室制法实验室里常用的是给铵盐和碱的混合物加热的方法制取氨气。
一般是用加热氯化铵和氢氧化钙的混合物,化学方程式是:2NH4Cl+Ca(OH)=2CaCl2+2H2O+2NH3↑制气装臵是用给固体药品加热制取气体的仪器装臵。
氨气极易溶于水,密度比空气小,要用向下排空气法收集。
检验集气瓶中是否已集满氨气,可把润湿的红色石蕊试纸放在瓶口;若试纸立即变蓝,证明集气瓶内已集满氨气。
铵根离子的检验检验铵根离子是利用铵盐能跟碱起反应放出氨气的性质。
检验方法是:把少量铵盐晶体放入试管里,然后用胶头滴管滴入少量较浓的氢氧化钠溶液,给试管加热。
硫化氢的制取

硫化氢的制取硫化氢是一种重要的有毒气体,它在熔炼、电池制造、医药及其他工业和农业生产中都有重要的作用。
硫化氢是指氢原子与一个硫原子结合而成的分子,有明确的分子式H2S,它是气态,沸点为-60℃,在某些情况下它会形成液态或固态。
因其具有腐蚀性,故在硫化氢的制取和使用过程中,必须采取严格的安全措施。
硫化氢的制取主要有水解、烧碱反应和电解等方法。
其中水解方法是最常用的制取硫化氢的方法。
这是一种以水加热分解含硫物质制取硫化氢的过程,原料常用的有腐熟硫、硫磺、蓖麻油,这些原料均含有硫,在进行水解反应时,由于热力作用,产生催化作用,在水中释放出硫化氢。
水解法虽然已经相对成熟,但其酸性条件较为复杂,而且容易产生沉淀物,降低回收率及硫化氢的浓度,并会产生一些有毒物质。
烧碱反应法是利用悬浮液中氢离子代替水解法中的水,同时利用碱性物质作为催化剂。
这种方法使反应过程简单,反应产率高,但其反应温度较高,且反应比较长,控制起来较为困难。
电解法主要是在碱性环境中进行,利用电压进行电解。
电解法可以得到高浓度的硫化氢,而且其反应十分灵敏,可以控制硫化氢的浓度,弥补水解法低浓度,电解法较为成熟,其工艺稳定性高,可以得到无杂质的硫化氢。
硫化氢的制取具有相当大的危险性,因此在实际操作时,应该严格按照相应的安全规范来处理。
一般应该采取空气分流、通风除尘、设备设施的隔离等措施,以减轻和消除硫化氢的危害。
同时,还要配备有关的消防和防护装备,以防止硫化氢发生意外泄漏,保证人身和财产的安全。
综上所述,硫化氢的制取是一项危险的工作,需要严格按照安全规范来操作。
目前常用的硫化氢制取方法有水解法、烧碱反应法和电解法。
选择合适的截止方法,严格遵守安全操作规程,以保证人员及设备的安全。
硫化氢的实验室制法

1。药品: 2。反应原理: 3。发生装置: 4。除杂装置: 5。收集装置: 6。尾气吸收装置:
实验室制取硫化氢的方法:
一、药品: 硫化亚铁和稀硫酸(或稀盐 酸)
二、反应原理:
FeS+H2SO4==FeSO4+H2S
FeS+2HCl==FeCl2+H2S
氧 气 ( O2 ) 氢 气 ( H2 ) 药品 氯酸钾或高锰酸钾 锌和稀硫酸
6 FeS, 7 双氧水,8稀HCl,9浓HCl
B
可制备的气 A中盛放的 B中盛放的
体
药品
药品
O2
7
3
CO2
8
1
H2S
8或5
6
从两个方面考虑: (1)反应的条件。 (2)药品的状态。
氧 气 的 发 生 装 置
此装置使用于什么样的反应
氢 气 的 发 生 装 置
此装置使用于什么样的反应
适用于反应物是固 体且需加热
适用于反应物有两种 (固体+液体)且不 需加热
Cl2的制备、提纯、吸收 Cl2中混有HCl和H2O(g)
三、实验室制取硫化氢气体的装置
反应 原理
2KClO3 =M=n=O= 22KCl + 3O2 2KMnO4 == K2MnO4+MnO2+O2
Zn+H2SO4 =ZnSO4 +H2
氢 气( H2 )
收集方法
排水法( 因为氧 气不易 溶于水) 向上排气法(因为 氧气 的密度比空 气略大)
A.长颈漏斗下端管口没有插 到液面以下。 B.导气管插到液面以下。 C.用向下排气法收集。 D.导管没有插到接近集气瓶 底部。
高一化学知识小卡片·硫化氢的实验室制法(51)
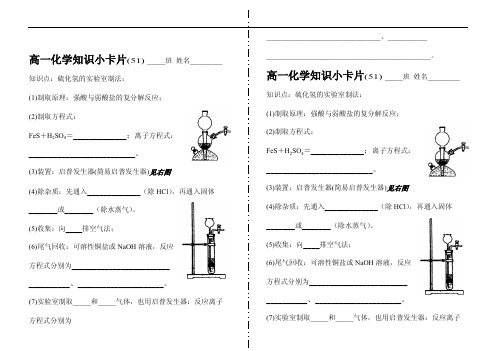
高一化学知识小卡片(51)_____班 姓名_________知识点:硫化氢的实验室制法:(1)制取原理:强酸与弱酸盐的复分解反应;(2)制取方程式:FeS +H 2SO 4=_____________;离子方程式:__________________________。
(3)装置:启普发生器(简易启普发生器)见右图(4)除杂质:先通入_____________(除HCl ),再通入固体_______或_______(除水蒸气)。
(5)收集:向____排空气法;(6)尾气回收:可溶性铜盐或NaOH 溶液,反应方程式分别为__________________________________、_____________________。
(7)实验室制取_____和_____气体,也用启普发生器:反应离子方程式分别为________________________________、_________________________________________________________。
高一化学知识小卡片(51) _____班 姓名_________知识点:硫化氢的实验室制法:(1)制取原理:强酸与弱酸盐的复分解反应;(2)制取方程式:FeS +H 2SO 4=_____________;离子方程式:__________________________。
(3)装置:启普发生器(简易启普发生器)见右图(4)除杂质:先通入_____________(除HCl ),再通入固体_______或_______(除水蒸气)。
(5)收集:向____排空气法;(6)尾气回收:可溶性铜盐或NaOH 溶液,反应方程式分别为__________________________________、_____________________。
(7)实验室制取_____和_____气体,也用启普发生器:反应离子方程式分别为________________________________、_________________________________________________________。
高一化学知识小卡片_硫化氢的实验室制法.doc
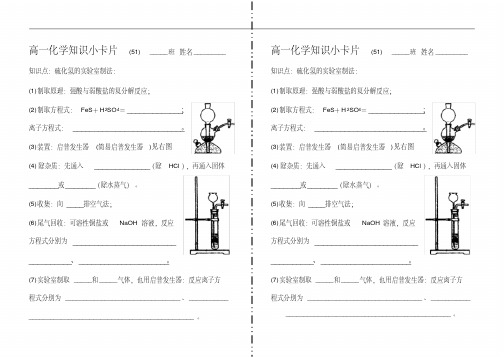
高一化学知识小卡片(51) _____班姓名_________ 知识点:硫化氢的实验室制法:(1)制取原理:强酸与弱酸盐的复分解反应;(2)制取方程式:FeS+H2SO4=_____________;离子方程式:__________________________。
(3)装置:启普发生器(简易启普发生器)见右图(4)除杂质:先通入_____________(除HCl),再通入固体_______或_______(除水蒸气)。
(5)收集:向____排空气法;(6)尾气回收:可溶性铜盐或NaOH溶液,反应方程式分别为__________________________________、_____________________。
(7)实验室制取_____和_____气体,也用启普发生器:反应离子方程式分别为________________________________、___________ ______________________________________________。
高一化学知识小卡片(51) _____班姓名_________ 知识点:硫化氢的实验室制法:(1)制取原理:强酸与弱酸盐的复分解反应;(2)制取方程式:FeS+H2SO4=_____________;离子方程式:__________________________。
(3)装置:启普发生器(简易启普发生器)见右图(4)除杂质:先通入_____________(除HCl),再通入固体_______或_______(除水蒸气)。
(5)收集:向____排空气法;(6)尾气回收:可溶性铜盐或NaOH溶液,反应方程式分别为__________________________________、_____________________。
(7)实验室制取_____和_____气体,也用启普发生器:反应离子方程式分别为________________________________、___________ ______________________________________________。
硫化氢的实验室制法

排水法( 因为氧 气不易 溶于水) 向上排气法(因为 氧气 的密度比空 气略大)
排水法(因为氢气难 溶于水)
向下排气法(因为氢 气的密度比空气小)
带火星的木条伸 检验方法 入集气瓶,木条
复燃,为氧气
点燃气体能燃烧, 生成物只有水,为 氢气
氧
氢
气
气
的
ቤተ መጻሕፍቲ ባይዱ
的
发
发
生
生
装
装
置
置
讨论:选择实验室制取气体装置的
思路与方法。
可供选药品:1 大理石, 2 锌粒,
A
3 MnO 2 , 4 浓H2SO4 , 5 稀H2SO4
6 FeS, 7 双氧水,8稀HCl,9浓HCl
B
可制备的气 A中盛放的 B中盛放的
体
药品
药品
O2
7
3
CO2
8
1
H2S
8或5
6
排水法 向上排气法 向下排气法
2、收集方法: 向上排气法( H2S的密度比空气大)
不能用排水法( H2S能溶于水)
收集仪器: 1、集气瓶 2、玻璃片
实验室制取硫化氢的装置 :
3、检验方法:
使湿润的醋 酸铅(PbAc2)试 H2S 纸变黑。
思考:
1。如何验证集气瓶内的气体已满?
2。尾气如何吸收?
Cl2的制备、提纯、吸收 Cl2中混有HCl和H2O(g)
三、实验室制取硫化氢气体的装置
1、发生装置(制取氢气的装置相似 )
发生仪器: 1、长颈漏斗
(或分液漏斗) 2、锥形瓶 3、双孔橡皮塞 4、导气管
2、在选择收集装置时应以什么为依据? 主要应以物理 (1)气体的密度与空气比较 性质两个方面:(2)气体在水中的溶解性
硫化氢的实验室制法及原理

硫化氢的实验室制法及原理
硫化氢(H2S)是一种有毒、有臭味的气体,常被用作工业原料和化学试剂。
在实验室中,常用的制法有以下几种:
1、硫酸与钠反应制法:将硫酸和钠混合在一起,加热至80-90°C,即可生成硫化氢气体。
具体反应方程式为:
H2SO4 + Na → NaHSO4 + H2
NaHSO4 + Na → Na2SO4 + H2
2、硫酸与铜反应制法:将硫酸和铜混合在一起,加热至80-90°C,即可生成硫化氢气体。
具体反应方程式为:
Cu + H2SO4 → CuSO4 + H2
3、硫酸与铁反应制法:将硫酸和铁混合在一起,加热至80-90°C,即可生成硫化氢气体。
具体反应方程式为:
Fe + H2SO4 → FeSO4 + H2
这三种制法的原理均为还原反应,即在反应过程中硫酸的硫原子被还原为硫化氢分子。
注意:制备硫化氢时要格外小心,因为它是有毒的。
使用时应注意安全措施,并且使用时应穿戴防毒面具。
高纯硫化氢的用途和制备方法

高纯硫化氢的用途和制备方法高纯硫化氢,这玩意儿听起来是不是有点吓人呀?但可别小瞧它,它在很多领域那可是有着大用处呢!
在化工领域,高纯硫化氢就像一个神奇的小精灵。
它可以用于合成一些重要的化合物,就好比是搭建化学大厦的一块关键砖头。
比如一些含硫的有机化合物,没有它还真不行呢!它就像是一个幕后英雄,默默为各种化学产品的诞生贡献着自己的力量。
在金属加工行业,高纯硫化氢也能一展身手。
它可以帮助处理金属表面,让金属变得更加光亮、坚韧。
这就好像给金属做了一次高级美容护理,让它们焕发出新的光彩。
那高纯硫化氢是怎么制备出来的呢?这可就有讲究啦!一种常见的方法是通过硫化物与酸反应来制取。
就好像是一场化学反应的奇妙舞会,硫化物和酸在特定的条件下相遇,然后就蹦出了高纯硫化氢这个小精灵。
还有其他的一些方法,每种方法都有它独特的地方,就像不同的厨师有不同的烹饪技巧一样。
想象一下,如果没有高纯硫化氢,那些需要它的化工过程会变得多么艰难呀!就像做菜没有了盐,总觉得少了点什么。
而且制备高纯硫化氢也不是随随便便就能成功的,需要严格控制各种条件,稍有不慎可能就会前功尽弃呢!
我们的生活中有很多看似不起眼的东西,其实都有着大大的用途。
高纯硫化氢就是这样的一个例子。
它在我们看不见的地方默默发挥着
作用,为我们的生活带来便利和改变。
所以呀,可别因为高纯硫化氢的名字听起来有点吓人就对它敬而远之。
它可是有着自己独特价值的呢!我们应该正确地认识它、利用它,让它为我们的生活增添更多的精彩。
你说是不是呢?。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
知识点:硫化氢的实验室制法:
(1)制取原理:强酸与弱酸盐的复分解反应;
(2)制取方程式:FeS+H2SO4=_____________;离子方程式:__________________________。
(3)装置:启普发生器(简易启普发生器)见右图发生器:反应离子方程式分别为________________________________、___________
______________________________________________。
高一化学知识小卡片(51)_____班姓名_________
(5)收集:向____排空气法;
(6)尾气回收:可溶性铜盐或NaOH溶液,反应方程式分别为________________________
__________、_____________________。
(7)实验室制取_____和_____气体,也用启普发生器:反应离子方程式分别为________________________________、___________
(4)除杂质:先通入_____________(除HCl),再通入固体_______或_______(除水蒸气)。
(5)收集:向____排空气法;
(6)尾气回收:可溶性铜盐或NaOH溶液,反应方程式分别为________________________
__________、_____________________。
知识点:硫化氢的实验室制法:
(1)制取原理:强酸与弱酸盐的复分解反应;
(2)制取方程式:FeS+H2SO4=_____________;离子方程式:__________________________。
(3)装置:启普发生器(简易启普发生器)见右图
(4)除杂质:先通入_____________(除HCl),再通入固体_______或_______(除水蒸气)。
______________________________________________。
