研究物质性质的方法和程序
高一化学知识点总结必修一12研究物质性质的方法和程序

1.2 研究物质性质的方法和程序一、研究物质性质的基本方法:研究物质的性质,经常用到观察法、实验法、分类法和比较法1、观察法:(1) 概念:观察法是一种有计划、有目的用感官考察研究对象的方法感官包括:➢眼看:直接用肉眼观察物质的颜色、状态➢鼻闻:用鼻子闻物质的气味,闻有毒气体时,不能直接靠近➢借助仪器:可以借助仪器来观察,从而提高观察的灵敏度(2) 要求:观察要有明确而具体的目的,要对观察到的现象进行分析2、实验法:(1) 概念:是验证对物质性质的预测或者探究物质未知性质的方法(2) 要求:➢实验前:要明确实验目的要求、实验用品、实验步骤➢实验中:要仔细研究实验现象,并做好实验记录➢实验后:写好实验报告,并对实验结果进行分析3、分类法:运用分类的方法,分门类对物质性质及其变化研究,可总结出各类物质的一般性质和特性4、比较法:运用比较的方法,可以找出物质性质间的异同二、观察法例子:可以通过实验法来研究钠的物理性质和钠与水反应的相关性质1、钠的物理性质:➢颜色:银白色➢两点:熔沸点低➢两度:硬度、密度小(密度比水小)2、钠与水反应(1) 实验现象:➢钠浮在水面上,说明钠的密度比水小➢钠块熔成闪亮的小球,说明钠的熔点低,反应放热➢发出嘶嘶的响声,说明反应生成气体(经检验可知该气体为H2) ➢小球迅速向各个方向游动,是因为反应产生的气体推动小球运动➢滴有酚酞的溶液变红色,说明反应生成了碱因此:钠与水反应的化学方程式:2Na+2H2O====2NaOH+H2↑(2) 注意事项:➢取金属钠时要用镊子,不能直接用手拿➢实验时切取的钠不能太多,一般黄豆粒大小就可以了➢切完后,剩余的钠必须要放回原瓶,不可随意乱丢知识点补充:钠与水溶液的反应情况(1)钠与酸溶液的反应:钠与水反应的实质是钠与水电离出来的极少量的H+反应生成H2,在酸溶液中,酸电离出的H+浓度远大于水,因此钠在酸溶液中,先与酸反应,当酸反应完时,剩余的钠再与水反应。
研究物质性质的方法和程序

研究物质性质的方法和程序1.基本方法:观察法、实验法、分类法、比较法2.基本程序:第三步:用比较的方法对观察到的现象进行分析、综合、推论,概括出结论。
化学方程式反应现象应用2Mg+O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+O2点燃或Δ2CuO 红色金属变为黑色固体4Al+3O2点燃或Δ2Al2O3 银白金属变为白色固体3Fe+2O2点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热4Fe + 3O2高温2Fe2O3C+O2 点燃CO2 剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 点燃SO2 剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2 点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2 点燃2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2点燃2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2 Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4+MnO2+O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgOΔ2Hg+O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO+H2O+CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O +CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4 =MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4=Al2(SO4)3+3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2 Δ 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 Δ3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2 点燃或光照2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2C O+O2点燃2CO2 蓝色火焰煤气燃烧C + CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4+2C高温3Fe + 2CO2↑ 冶炼金属C + CO2 高温2COCO2 + H2O = H2CO3 碳酸使石蕊变红证明碳酸的酸性H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+H2O+CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温CaO+ CO2↑ 工业制备二氧化碳和生石灰CaCO3+2HCl=CaCl2+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl=2NaCl+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl=MgCl2+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO +COΔ Cu + CO2 黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO高温2Fe+3CO2 冶炼金属原理Fe3O4+4CO高温3Fe+4CO2 冶炼金属原理WO3+3CO高温W+3CO2 冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2点燃2CO2+4H2OC2H5OH+3O2点燃2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4=Cu+FeSO4 银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4= Fe+ MgSO4 溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+ Cu (NO3)2Cu+2AgNO3=2Ag+ Cu(NO3)2 红色金属表面覆盖一层银白色物质镀银Zn+CuSO4= Cu+ZnSO4 青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl=2FeCl3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl=2AlCl3+3H2O 白色固体溶解Na2O+2HCl=2NaCl+H2O 白色固体溶解CuO+2HCl=CuCl2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HCl=ZnCl2+ H2O 白色固体溶解MgO+2HCl=MgCl2+ H2O 白色固体溶解CaO+2HCl=CaCl2+ H2O 白色固体溶解NaOH+HCl=NaCl+ H2O 白色固体溶解Cu(OH)2+2HCl=CuCl2+2H2O 蓝色固体溶解Mg(OH)2+2HCl=MgCl2+2H2O 白色固体溶解Al(OH)3+3HCl=AlCl3+3H2O 白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl=FeCl3+3H2O 红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl=CaCl2+2H2OHCl+AgNO3= AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解CuO+H2SO4=CuSO4+H2O 黑色固体溶解、溶液呈蓝色ZnO+H2SO4=ZnSO4+H2O 白色固体溶解MgO+H2SO4=MgSO4+H2O 白色固体溶解2NaOH+H2SO4=Na2SO4+2H2OCu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解Ca(OH)2+H2SO4=CaSO4+2H2OMg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解、溶液呈黄色Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3=2NaNO3+H2O 白色固体溶解CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解NaOH+HNO3=NaNO3+ H2OCu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解、溶液呈黄色3NaOH + H3PO4=3H2O + Na3PO43NH3+H3PO4=(NH4)3PO42NaOH+CO2=Na2CO3+ H2O 吸收CO、O2、H2中的CO2、2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成CuSO4+5H2O= CuSO4?H2O 蓝色晶体变为白色粉末CuSO4?H2OΔ CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl = AgCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓ 有白色沉淀生成CaCO3+2HCl=CaCl2+H2O+CO2 ↑MgCO3+2HCl= MgCl2+H2O+ CO2 ↑NH4NO3+NaOH=NaNO3+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+ KOH= KCl+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体电解质和非电解质1.定义:①条件:水溶液或熔融状态;②性质:能否导电;③物质类别:化合物。
研究物质性质的方法和程序

实验记录:
实验内容 实验现象 结论 钠由银白色 钠被迅速氧 金属钠在空 变暗,失去 化生成氧化 气中放置 金属光泽 钠(Na2O) 激烈反应发 燃烧生成 在空气中加 出黄色火焰 过氧化钠 热金属钠 生成淡黄色 ( Na2O2) 固体
三 小结:
在研究物质性质时,运用分类的方法,分门别 类地对物质及其变化进行研究,可以总结出各 类物质的通性和特性;运用比较的方法,可以 找出物质性质间的异同,认识物质性质间的内 在联系;而最常用的观察和实验的方法要有明 确而具体的目的,要对观察到的现象进行分析 和综合。合理而有效地运用这四种方法会使我 们的研究变得简单易行。
化学性质
根据所学的知识和已有的知识经验,推 测金属可能具有哪些共同的性数有特殊颜色
有延展性 、导电性、导热性
比较Na的两种氧化物
氧化钠
化学式 颜色 状态 类别 与水反应 Na2O
过氧化钠
Na2O2
白色固体粉末(晶体) 淡黄色固体粉末 碱性氧化物
Na2O+H2O=2NaOH
反应放热,钠熔点低
①钠与水剧烈反应,活泼金属,强还原剂. 2Na+2H2O=2NaOH+H2↑ ②钠能与盐酸溶液反应吗? 2Na+2HCl=2NaCl+H2↑ ③钠能硫酸铜溶液发生置换反应吗? 2Na+CuSO4+2H2O=Cu(OH)2↓+Na2SO4+H2↑
交 流 研 讨
2 探究金属钠与氧气的反应。 认识条件控制 在实验研究中的意义。
(一).金属钠的物理性质
观察记录
状态
研究物质性质的方法和程序

研究物质性质的基本方法三:分类法
在研究物质性质时,运用分类的方法, 法分门别类地对物质及其变化进行研究, 可以总结出各类物质的一般性质和特性;反 之,知道某物质的类别,我们就可推知 该物质的一般性质。
研究物质性质的基本方法四:比较法
运用比较的方法,可以找出物质性质间 的异同,认识物质性质间的内在联系, 对物质的性质进行归纳和概括。
一、研究物质性质的基本方法
1. 观察法 2. 实验法 3. 分类法 4. 比较法
1、观察法: 观察金属钠的物理性质
及钠与水反应的现象 明确观察目的
在实验中用感官或仪器观察
记录观察结果 分析、思考和综合
自己动手,大胆 做一做!
严禁用手触摸钠 !! 严禁任意丢弃 !! 严禁比黄豆粒大 !!
正确观察现象 , 及时记录实验现象.
我要观察什么?
1、认识金属钠的状态、颜色、硬度 的相对大小、密度的相对大小、 熔点的相对高低。
2、观察金属钠与水的反应。
观察记录:
金属钠的物理性质
我观察到了什么? 马上记下来!
1、金属钠的状态—- 固态
2、金属钠的密度的相对大小—-ρ钠>ρ煤油
3、金属钠硬度的相对大小—- 硬度小,
可用小刀切割
4、金属钠的颜色—- 银白色、有金属光泽
恩格斯说:“单凭观察所得 的经验是决不能充分证明必然的”。
要跳出单纯的经验的圈子要敢于 提出有科学根据的假设,并通过设计 实验加以检验。
研究物质性质的方法和程序
巩固复习
第二课时
1.研究物质性质的方法有哪些?
2.通过观察你知道了钠的哪些性质?
3.简述钠与水反应的现象?书写反应的 方程式?
【知识解析】研究物质性质的基本方法
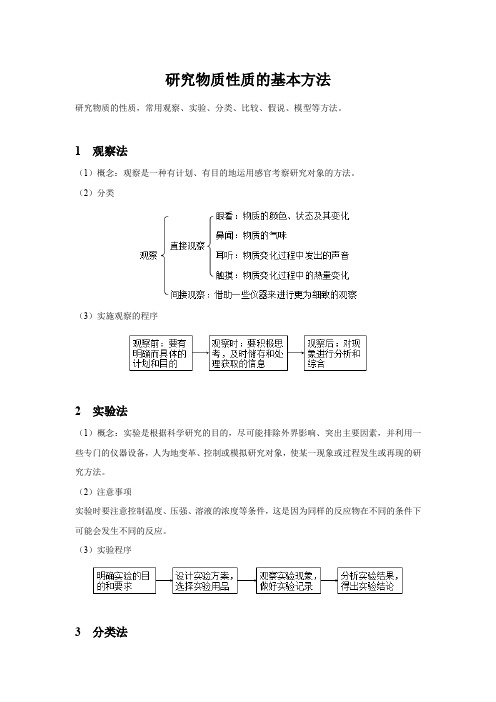
研究物质性质的基本方法研究物质的性质,常用观察、实验、分类、比较、假说、模型等方法。
1 观察法(1)概念:观察是一种有计划、有目的地运用感官考察研究对象的方法。
(2)分类(3)实施观察的程序2 实验法(1)概念:实验是根据科学研究的目的,尽可能排除外界影响、突出主要因素,并利用一些专门的仪器设备,人为地变革、控制或模拟研究对象,使某一现象或过程发生或再现的研究方法。
(2)注意事项实验时要注意控制温度、压强、溶液的浓度等条件,这是因为同样的反应物在不同的条件下可能会发生不同的反应。
(3)实验程序3 分类法(1)概念:分类是根据研究对象的共同点和差异点,将它们区分为不同种类和层次的科学方法。
(2)分类的目的①分门别类地对物质及其变化进行研究,可以总结出各类物质的一般性质;②可以根据物质所属的类别预测物质的性质。
4 比较法含义:找出各类物质性质之间的异同,认识各类物质性质之间的内在联系。
5 假说概念:在已有事实和科学理论的基础上,对有关现象或规律的本质以及未知物质或现象进行推测性说明。
6 模型概念:以客观事实为依据建立起来的,通过建构模型对物质或物质的变化进行简化模拟。
注意运用假说和模型所做的预测或说明是否正确还需要通过实验来验证。
典例详析例1-1(2021河南郑州月考)用如图1-2-1所示的方法研究某气体的性质,这种方法属于()图1-2-1A.实验法B.观察法C.分类法D.比较法解析◆题图所示为闻物质气味的正确方法。
直接用肉眼观察物质的颜色、状态以及用鼻子闻物质的气味等都属于观察法。
答案◆B警示◆许多同学误认为这是实验法,实际上该方法是一种有计划、有目的地运用感官考察研究对象的方法。
例1-2(2021北京一零一中学期中)下列有关研究物质性质的方法中,说法不正确的是()A.研究物质的性质时,常用观察、实验、分类、比较、模型、假说等方法B.观察是一种有计划、有目的地运用感官考察研究对象的方法C.科学家提出的假说一定能成为科学理论D.使用模型有助于人们研究物质的性质解析◆观察、实验、分类、比较、模型、假说等是研究物质性质时常用的方法,A项正确;观察是一种有计划、有目的地运用感官考察研究对象的方法,B项正确;假说提出后需要通过实验来验证,才有可能成为科学理论,C项错误;通过建构模型对物质或物质的变化进行简化模拟,有助于人们研究物质的性质,D项正确。
研究物质性质的方法和程序

研究物质性质的方法和程序
研究物质性质的方法和程序(教学设计)
【课标要求】
一、知识与技能
1.了解金属钠的主要性质(钠与水、氧气的反应),知道钠是一种很活泼的金属。
2.了解氯气的主要性质(氯气与金属单质、非金属单质、及水的反应。
3.进一步熟练药品的取用、加热等实验基本操作。
二、过程与方法
1.通过观察分析实验现象,体验科学合理地运用观察方法的过程
2.实验探究钠与氧气的反应及氯气的性质,体会实验方法在化学研究中的作用,并认识实验过程中控制实验条件的重要性以及研究物质性质的一般程序。
3.在归纳金属钠的性质及预测氯气性质的过程中,体验分类、比较等研究方法在学习和研究物质性质过程中的应用。
【知识链接】
Cl2 的性质
1、物理性质:在通常情况下,氯气是一种________色、有_________气味的有毒气体。
与其它气体相比沸点__________(填较高或较低)_________ (填难或易)液化。
密度比空气大,氯气能溶于水,1 体积水约溶解_____体积的氯气。
______(填溶或难溶)于饱和食盐水。
思考:①常见的易液化的气体除Cl2 外,还有__________、
____________。
《研究物质性质的方法和程序》 知识清单
《研究物质性质的方法和程序》知识清单一、研究物质性质的基本方法1、观察法观察是研究物质性质的第一步。
通过用肉眼观察物质的颜色、状态、光泽等外观特征,用鼻子闻物质的气味,用耳朵听物质在反应时可能产生的声音等,获取物质的初步信息。
例如,观察金属钠的颜色是银白色,状态为固体,具有金属光泽。
在观察时,要注意观察的条件和环境,确保观察的准确性和全面性。
同时,要善于捕捉细微的变化和特征,为后续的研究提供基础。
2、实验法实验是研究物质性质的重要手段。
通过设计和进行实验,可以控制变量,深入探究物质的性质和变化规律。
在进行实验时,要明确实验目的,设计合理的实验方案,选择适当的实验仪器和试剂,严格按照实验操作步骤进行实验,并注意观察实验现象,记录实验数据。
例如,通过钠与水的实验,可以观察到钠浮在水面上、迅速熔化成小球、在水面上四处游动并发出“嘶嘶”的响声,溶液变红等现象,从而得出钠的密度比水小、熔点低、能与水剧烈反应生成氢气和氢氧化钠等性质。
3、分类法分类法是根据物质的组成、结构、性质等方面的相似性和差异性,将物质进行分类研究。
通过分类,可以将众多的物质归纳为不同的类别,便于系统地研究和掌握物质的性质。
例如,根据物质的组成可以分为纯净物和混合物;根据物质在常温常压下的状态可以分为固体、液体和气体等。
4、比较法比较是研究物质性质的常用方法之一。
通过将一种物质与其他类似物质进行比较,可以更清晰地认识该物质的独特性质。
比如,比较钠、镁、铝三种金属的活泼性,可以通过它们与水、酸反应的剧烈程度来判断。
二、研究物质性质的基本程序1、观察物质的外观首先,对所要研究的物质进行仔细的观察,包括物质的颜色、状态、气味、硬度、密度等物理性质。
2、预测物质的性质基于已有的知识和经验,结合物质的类别和组成,对物质可能具有的性质进行预测。
3、设计并实施实验根据预测的性质,设计合理的实验方案,选择适当的实验方法和仪器设备,进行实验探究。
在实验过程中,要注意控制实验条件,确保实验的安全性和准确性。
研究物质性质的方法和程序
化学性质
研究物质的方法之三、四:分类法、比较法
(三) 钠的存在与保存
• 1.由于钠的化学性质很活泼,所以在自然界 中钠全部以化合态存在,如:
NaCl、Na2SO4、NaNO3、Na2CO3等 • 2.由于钠的化学性质很活泼,易与空气中的 水和氧气反应,所以钠应当密封保存,少 量的钠通常保存在煤油中。
2 P + 3Cl2 2 P + 5Cl2
2PCl3(白雾) 2PCl5
(白烟)
点燃
思考:氯气与铜、氢气反应时,分别产生了
烟、雾的现象,那么烟和雾有何区别呢? 烟:大量细小固体颗粒分散在气体中的现象。
雾:大量液滴分散在气体中的现象。
3、与水的反应
Cl2+H2O=HCl+HClO
2HClO=2HCl+O2↑
将盛满氯气的试管倒置在水 中,水面上升,并呈浅黄绿 色,气体颜色变浅
将盛满氯气的试 管倒置在水中, 水面上升,并呈 黄绿色
化学性质
1、与金属反应 (一般生成高价化合物)
与铜反应的实验演示
现象:剧烈燃烧,充满棕黄色的烟,最后溶液成蓝色。
写出反应的化学方程式。
Cu+Cl2 点燃
=
CuCl2
提问:氯气既能与活泼金属反应,又能与不活泼金 属反应,而且一般生成高价化合物,那么,铁与氯 气反应的产物应该是什么呢? 与铁反应的实验演示 铁存在几 种化合价
【问题·∙思考】 实验室中多余的氯气是如何处理的? 为什么?
用碱液吸收多余的氯气
(1)氯气有毒,污染空气.
(2)氯气可与碱液反应
课堂练习:
1、下列物质属于纯净物的是:
A
A、液氯
B、氯水
高中化学《研究物质性质的方法和程序》教案(2)总结
研究物质性质的方法和程序【教课目的】1.知识与技术目标:使学生认识金属钠的物理性质及主要的化学性质(钠跟水、氯气的反响),认识钠是一种很开朗的金属。
使学生认识氯气的物理性质和主要的化学性质(氯气跟金属单质、非金属单质及水的反响)。
进一步娴熟药品的取用,加热等基础实验操作。
2.过程与方法目标:经过指引学生察看、剖析实验现象,让他们领会如何科学、合理地运用察看方法。
经过对钠跟氧气的反响及氯气性质的实验研究,让学生领会实验方法在化学研究中的作用,并认识到实验过程中控制实验条件的重要性。
在归纳金属钠的性质及展望氯气性质的过程中,让学生体验分类、比较等研究方法在学习和研究物质性质过程中的应用。
3.感情态度与价值观目的:经过对金属钠和氯气性质的研究,激发学生学习化学的兴趣,让他们乐于研究物质变化的神秘;利用阅读资料《含氯化合物的漂白与消毒作用》培育学生将化学知识与生产、生活实践相联合的意识。
【教课要点、难点】1.知识上要点、难点:金属钠和氯气的化学性质2.方法上要点、难点:使学生初步学会以察看、实验、比较、分类等方法在研究物质性质中的运用,初步掌握研究物质的一般程序。
【教课准备】1.讲堂活动记录及报告(详赐教课过程)活动沟通·商讨:活动察看·思虑:察看金属钠的物理性质及钠与水反响的现象活动活动·研究金属钠与氧气反响的实验活动沟通·商讨活动研究氯气的性质2.将学生为4- 6 人小组3.试验试剂和仪器:见讲堂活动记录及报告【教课方法】察看、实验研究、对照法【教课过程】〖发放讲堂活动记录及报告〗在前方的学习中我们知道,化学科学是在原子、分子水平上研究物质的构成、构造、性质、变化、制备和应用的一门自然科学。
认识物质的性质是化学研究的一项重要任务,且只有深入地研究物质的性质,才能更好地利用物质为人类生产、生活服务。
比如,经过对氢气的可燃性研究,可用作绿色能源和火箭的推动剂;经过对溴化银感光性的研究,制成了感光胶卷;经过对叠氮化钠(NaN3, 在激烈撞击的状况下能快速分解并产生大批氮气)性质的研究,制成了汽车安全气囊因而可知,研究物质的性质是十分重要的。
研究物质的性质的方法和程序教案
研究物质的性质的方法和程序教案一、教学目标:1.了解研究物质性质的重要性和意义。
2.掌握研究物质性质的常用方法和程序。
3.能够应用所学方法和程序进行相关实验和观测。
二、教学内容:1.物质性质的概念和分类。
2.研究物质性质的常用方法和程序。
三、教学过程:1.导入(10分钟)教师通过引入如下问题进行导入:你知道物质的性质有哪些?它们对于我们的生活有什么作用?导入问题激发学生思考,开启学习兴趣,并引导学生认识到物质性质的重要性和意义。
2.知识讲解(20分钟)(1)物质性质的概念和分类教师通过简洁明了的讲解,向学生介绍物质性质的概念,并详细解释其分类,如物质的物理性质、化学性质、机械性质等。
(2)研究物质性质的常用方法和程序教师向学生介绍常用的研究物质性质的三种方法:观察法、实验法和测试法,并结合具体实例,解释它们的应用场景和操作步骤。
3.案例分析与讨论(20分钟)教师提供一些经典的案例,引导学生运用已学知识,分析并讨论如何使用合适的方法和程序来研究物质性质。
例如:如何判断一种未知溶液中是否含有盐类物质?4.实验操作(30分钟)学生按照教师的指导,进行实验操作,通过实际操作来学习研究物质性质的方法和程序。
例如:利用观察法,观察不同物质在加热过程中的变化。
5.学生实践(20分钟)学生根据教师的要求,选取一种物质,并自主设计实验步骤和程序,研究其特定性质。
学生可以选择观察法、实验法或测试法,来得出相应的结论。
6.总结归纳(10分钟)教师和学生共同总结本节课所学内容,强调学习物质性质的重要性和意义,并回顾整个研究物质性质的方法和程序,以及实验操作的要点。
四、拓展延伸:学生可以进一步扩大实验范围,设计更复杂的实验来进一步研究物质的性质。
同时,学生还可以利用图书馆、互联网等资源进行实证研究,深入探究物质性质的更多方面。
五、教学评估:1.课堂参与度评估:对学生在讨论与实验环节的积极参与程度进行评估。
2.实验报告评估:根据学生实验报告的设计合理性、操作方法准确性以及实验结论的科学性等方面进行评价。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2012-2013学年度上学期高一化学导学案2012.09
第一章认识化学科学
第二节研究物质性质的方法和程序(第二课时)
【学习目标】
1、了解氯气的物理性质和主要的化学性质(氯气与金属单质、非金属单质、水、碱的反应)
2、通过氯气性质的实验探究,体会实验方法在化学研究中的应用。
在预测氯气性质的过程中,体验分类,比较等研究方法在学习和研究物质性质过程中的作用
3、利用阅读材料,增强将化学知识与生产、生活实践相结合的意识。
【课前预习区】
1、研究物质性质的一般程序为观察_______________、预测_______________、_______________、_______________。
2、回忆氧气的性质,用化学方程式表示(各举一例)。
3、氯气和氧气一样,都属于______单质,试预测氯气可能与哪些类别的物质反应。
4、认识了物质的性质后,要探究产生相关性质的原因,这涉及____________方面的问题,即物质的性质由_____________决定。
一般利用__________、_________等方法进行研究。
【课堂互动区】
1、认识氯气的物理性质:
⑴取一只盛满氯气的集气瓶,观察氯气的颜色;稍打开玻璃片,用手轻轻地在瓶口扇动,使少量的氯气飘进鼻孔,闻氯气的气味。
⑵取一盛满氯气的试管,将其倒扣在水槽中,静置一段时间后观察现象。
【小结】通过观察可以得出氯气的颜色为、状态为、有气味、密度比空气。
取一支盛满氯气的试管,将其倒扣在水槽中,静置一段时间后,现象为:
结论是:。
预测:从分类的观点来看氯气属于。
氯气与的性质相似,可能与、
等发生化合反应。
2、探究氯气的化学性质
(一)验证氯气与金属单质(例如铁、铜)、非金属单质(氢气)的反应(二)探究氯气与水的反应
【预测与假设】氯气能够溶于水,氯气溶于水仅仅是物理变化吗?氯气溶于水后除了氯气和水外还有什么成分?根据P15“实验探究”中提供的试剂和仪器设计实验验证氯水(氯气溶于水后形成的溶液)中的成分?
【小结】
1、氯气与水的反应,试写出化学方程式__________________________________
2、氯水的成分:_______ _____________
3、设计实验证明有漂白作用的是氯气还是次氯酸
4、在实验室中未用完的氯气能够随便排放吗?为什么?你将如何处理剩余的氯气(试用用方程式表示)?
(三)氯气与碱的反应
(1)次氯酸盐是常用漂白剂和消毒剂的主要成分。
例如,84消毒液的有效成分就是次氯酸钠,可由氯气与NaOH溶液反应制得,2NaOH+Cl2=
[阅读自学] 阅读《含氯化合物的漂白与消毒作用》一文,解决下面问题
(2)次氯酸的性质
HClO具有作用和作用,但是它不适合直接做漂白剂和消毒剂,因为它不稳定,见光或
受热易分解:,它还是一种弱酸,酸性比碳酸。
(3)漂白粉的制取原理
试着用化学方程式表示漂白粉失效原理、
【课堂检测】
1、自来水常用氯气来消毒,用自来水配置下列物质的溶液时,药品不会变质的是()
A、AgNO3
B、Na2CO3
C、NaOH
D、AlCl3
2、下列氯化物中,即能由金属和氯气直接反应制得,又能又金属和盐酸反应值得的是()
A 、CuCl2B、FeCl2 C、FeCl3 D 、AlCl3
3、在对游泳池水中通入氯气消毒发生氯气泄漏时,应立即关闭氯气罐,还应该采取下列自救方法中()
A、用湿润的毛巾捂住口鼻跑向低处
B、用浸湿小苏打或者肥皂水的毛巾捂住口鼻跑向高处
C、用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处
D、用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
4、下列关于氯水的叙述中,正确的是()
A.新制氯水中只含有Cl2和H2O分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.久置的氯水pH将变小
D.氯水经光照有气泡逸出,该气体为HCl
5、漂白粉是的混合物,其有效成分是,用漂白粉进行漂白时,需要使漂白粉跟或空气中的反应,有关反应的化学方程式
【课后巩固区】
1、下列物质属于纯净物的是()
A 盐酸
B 氯水
C 液氯
D 漂白粉
2、用氯气跟单质化合不能制取的物质是()
A.KCl B.FeCl2C.FeCl3 D.CuCl23、把石蕊试液滴加到新制的氯水中,出现的现象是()
A.溶液变红色B.溶液变蓝色
C.溶液变紫色D.溶液颜色先变红,后立即消失
4、潮湿的氯气、新制的氯水、次氯酸钠及漂白粉的水溶液均能使有色布条褪色,原因是它们均含有()
A.氯气B.次氯酸C.次氯酸根D.氯化氢
5、漂白粉在空气中容易变质的原因是()
A.CaCl2易吸收空气中的水分B.Ca(ClO)2易与盐酸反应
C.Ca(ClO)2见光易分解D.Ca(ClO)2易与空气中的CO2和水作用
6、在新制的氯水中含有多种微粒,①使氯水呈现黄绿色的是_______②能使硝酸银溶液产生白色沉淀的是______③能使紫色石蕊试液显红色的是______④能使红纸褪色的是________⑤能使无水硫酸铜变蓝的是________⑥能与碳酸氢钠溶液反应放出气体的是________。
