一些二元恒沸物的组成及沸点
具有最低恒沸点二元体系的沸点组成图的绘制

物理化学实验报告班级:14级制药一班姓名:王丹妮学号:14220125实验一具有最低恒沸点二元体系的沸点组成图的绘制一、实验目的1、绘制在一定压力下环已烷-乙醇双液系的气液平衡图,了解相图和相律的基本概念。
2、掌握测定双组分液系恒沸点的方法,找出恒沸点混合物的组成和最低恒沸点。
3、用回流冷凝法测定沸点时气相与液相的组成,绘制双液系相图。
并找出恒沸点混合物的组成及恒沸点的温度。
4、掌握用折光率确定二元液体组成的方法。
5、掌握阿贝折射仪的测量原理及使用方法。
二、实验原理(一)沸点的基本概念:液体的沸点是指液体的饱和蒸汽压和外压相等时的温度。
在一定外压下,纯液体的沸点有确定的值。
但对于完全互溶的双液系,沸点不仅与外压有关,而且还与双液系的组成有关。
(二)恒沸点化合物:如果液体与拉乌尔定律的偏差不大,在T-X图上溶液的沸点介于A,B二纯液体的沸点之间,实际溶液由于A,B二组分的相互影响,常与拉乌尔定律有较大偏差,在T-X图上会有最高或最低点的出现,这些点称为恒沸点,其相应的溶液称为恒沸点化合物。
常温下,两种液态物质以任意比例相互溶解所组成的体系称为完全互溶双液系。
在恒定压力下,表示溶液沸点与组成关系的相图称为沸点—组成图,即为T-x相图。
完全互溶双液系的T-x图可分为三类:(1)理想双液系,溶液沸点介于两纯物质沸点之间如图(a);(2)各组分对拉乌尔定律发生正偏差,溶液具有最低恒沸点(图中最低点)如图(b);(3)各组分对拉乌尔定律发生负偏差,溶液具有最高恒沸点(图中最高点)如图(c);(三)本实验采用回流冷凝的方法绘制环己烷-乙醇体系的T-x图。
其方法是用Abbe折射仪测定不同组成体系在沸点时气液两相的折光率。
在折光率-组成图(标准曲线)找出未知浓度溶液的折光率,就可从曲线上查出相对应的组成。
三、仪器试剂沸点仪1套;阿贝折光仪1台;移液管2支;滴管2支环己烷(A.R.);无水乙醇(A.R.)四、实验步骤1. 根据给定的折射率与组成的关系,绘制工作曲线。
[参考实用]常见的共沸物
![[参考实用]常见的共沸物](https://img.taocdn.com/s3/m/ac1ff34b02768e9951e7384f.png)
常见的共沸物又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分与沸点均保持不变。
这实际是表明,此时沸腾产生的蒸汽与液体本身有着完全相同的组成。
共沸物是不可能通过常规的蒸馏或分馏手段加以分离的。
并非所有的二元液体混合物都可形成恒沸物,一些例子列在了下面。
这类混合物的温度-组分相图有着显著的特征,即,其气相线(气液混合物和气态的交界)与液相线(液态和气液混合物的交界)有着共同的最高点或最低点。
如此点为最高点,则称为正恒沸物;如此点为最低点,则称为负恒沸物。
大多数恒沸物都是负恒沸物,即有最低沸点。
非均相共沸精馏分离叔丁醇和水的方法专利号:20XX10016030本发明公开了一种非均相共沸精馏分离叔丁醇和水方法。
采用包括精馏塔的精馏装置,非均相共沸精馏分离叔丁醇和水,其过程,常压下将叔丁醇与水的恒沸物或混合物,按恒沸物或混合物与共沸剂环已烷的质量比为0.3~1.5,加入精馏塔的塔釜中,在塔釜为60-80℃进行全回流,全回流结束后,采出分相器中富集的水,当塔顶在64~83℃,塔釜在70~87℃,以回流比为1~5,采出三元共沸物收集在分相器中,分相器上层的环己烷和叔丁醇有机相采出备用。
再以回流比1-4,在塔顶62-82℃下由塔顶采出环己烷-水及少量环己烷-叔丁醇的混合物后,在塔釜82-88℃,塔顶82-83℃下从塔顶得到纯度为98.2wt%的叔丁醇产品。
本发明的优点是,共沸剂的用量少,叔丁醇的一次收率高。
乙醇沸点78.3乙醇与水二元共沸沸点78.1二元共沸组成:水4.4%,乙醇95.5%要想精馏得到无水乙醇需加人苯,三元共沸。
«【PDF下载】化学滴定分析用标准溶液的制备(国标)15种常用有机溶剂的纯化»常见的共沸混合物的组成及共沸点化学世界|共沸物,又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分与沸点均保持不变。
这实际是表明,此时沸腾产生的蒸汽与液体本身有着完全相同的组成。
二元恒沸体系的组分数和自由度

二元恒沸体系的组分数和自由度
二元恒沸体系是指由两种物质组成的恒温恒压的体系,它是热力学及其应用中最基础的概念。
它由一种物质A和另一种物质B组成,两者共同构成体系恒定温度和压强。
二元恒沸体系最重要的特征是,当系统中的温度及压强保持不变时,它的组分与自由度将会保持不变,而整个系统也会保持原状。
二元恒沸体系的组分数取决于其中含有的物质种类,如果只有两个物质,那么它的组分数就等于2;如果有3个物质,那么它的组分数就等于3,依此类推。
自由度是指体系中温度和压强方面的自由度。
对于二元恒沸体系,其自由度等于2,也就是说,它可以自由地控制两个状态变量——温度和压强,而其余参数可以作为被动变量,它们随着温度和压强的变化而变化。
二元恒沸体系的组分数和自由度的确是热力学的基础,它们能够帮助我们更好地理解物质如何在热力学分析过程中运行和变化,从而对它们的性质和操作有更深入的了解。
常见的共沸混合物的组成及共沸点
共沸物,又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分与沸点均保持不变。
这实际是表明,此时沸腾产生的蒸汽与液体本身有着完全相同的组成。
共沸物是不可能通过常规的蒸馏或分馏手段加以分离的。
并非所有的二元液体混合物都可形成共沸物,科学堂在下列表格列出了一些常用的共沸物组成及其共沸点。
这类混合物的温度-组分相图有着显著的特征,即,其气相线(气液混合物和气态的交界)与液相线(液态和气液混合物的交界)有着共同的最高点或最低点。
如此点为最高点,则称为正共沸物;如此点为最低点,则称为负共沸物。
大多数共沸物都是负共沸物,即有最低沸点。
值得注意的是:任一共沸物都是针对某一特定外压而言。
对于不同压力,其共沸组分和沸点都将有所不同;实践证明,沸点相差大于30K的两个组分很难形成共(恒)沸物(如水与丙酮就不会形成共沸物)。
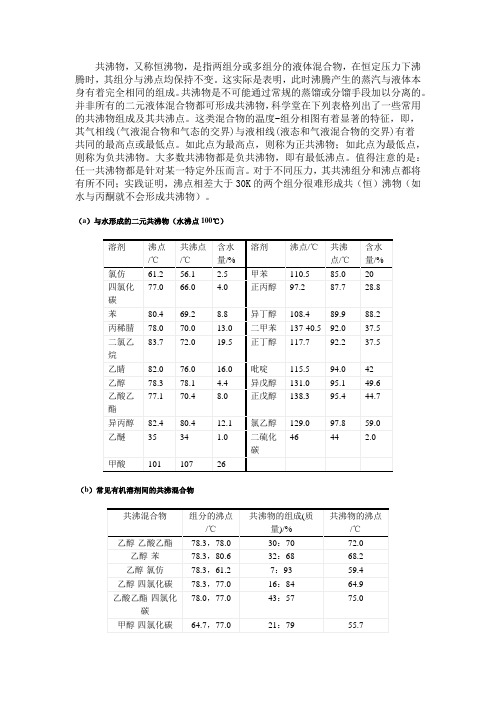
(a)与水形成的二元共沸物(水沸点100℃)(b)常见有机溶剂间的共沸混合物常见的共沸物共沸物组分的沸点(度)组成(w/w) 共沸点(度)水--乙醇 100--78.5 5--95 78.15水--正丙醇--97.2 28.8--71.2 87.7水--异丙醇--82.4 12.1--87.9 80.4水--正丁醇--117.7 37.5--62.5 92.2水--异丁醇--108.4 30.2--69.8 89.9水--叔丁醇--82.5 11.8--88.2 79.9水--异戊醇--131.0 49.6--50.4 95.1水--正戊醇--138.3 44.7--55.3 95.4水--氯乙醇--129.0 59.0--41.0 97.8水--乙醚--35 1.0--99.0 34水--乙腈--81.5 14.2--85.8 76水--丙烯腈--78.0 13.0--87 70.0水--甲酸--101 26--74 107水--丙酸--141.4 82.2--17.8 99.1水--乙酸乙酯--78 9.0--91 70水--二氧六环--101.3 18--82 87.8水--氯仿--61.2 2.5--97.5 56.1水--四氯化碳--77.0 4.0--96 66.0水--二氯乙烷--83.7 19.5--80.5 72.0水--苯--80.4 8.8--91.2 69.2水--甲苯--110.5 20--80 85.0水--二甲苯--137-140.5 37.5--62.5 92.0水--吡啶--115.5 42--58 94.0水--二硫化碳--46 2.0--98.0 44甲醇--二氯甲烷 64.7--41 7.3--92.7 37.8甲醇--氯仿--56.2 12--88 55.5甲醇--四氯化碳--77.0 21--79 55.7甲醇--丙酮--56.2 12--88 55.5甲醇--苯--80.6 39.1--60.9 57.6甲醇/甲酸甲酯/环己烷 17.8/48.6/33.6 50.8乙醇--乙酸乙酯 78.3--78.0 30--70 72.0乙醇--苯--80.6 32--68 68.2乙醇--氯仿--61.2 7--93 59.4乙醇--四氯化碳--77.0 16--84 65.1乙醇/苯/水78.3/80.6/100 19/74/7 64.9 乙酸乙酯--四氯化碳78.0--77.0 43--57 75.0乙酸乙酯--环己烷 46--54 71.6 乙酸甲酯--环己烷83--17 54.9 氯仿--丙酮 61.2--56.4 80--20 64.7 甲苯--乙酸 101.5--118.5 72--28 105.4。
常见共沸物及其沸点

共沸物,又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分与沸点均保持不变。
这实际是表明,此时沸腾产生的蒸汽与液体本身有着完全相同的组成。
共沸物是不可能通过常规的蒸馏或分馏手段加以分离的。
并非所有的二元液体混合物都可形成共沸物,科学堂在下列表格列出了一些常用的共沸物组成及其共沸点。
这类混合物的温度-组分相图有着显著的特征,即,其气相线(气液混合物和气态的交界)与液相线(液态和气液混合物的交界)有着共同的最高点或最低点。
如此点为最高点,则称为正共沸物;如此点为最低点,则称为负共沸物。
大多数共沸物都是负共沸物,即有最低沸点。
值得注意的是:任一共沸物都是针对某一特定外压而言。
对于不同压力,其共沸组分和沸点都将有所不同;实践证明,沸点相差大于30K的两个组分很难形成共(恒)沸物(如水与丙酮就不会形成共沸物)。
(a)与水形成的二元共沸物(水沸点100℃)
(b)常见有机溶剂间的共沸混合物。
二元体系沸点-组成图测绘

二元体系沸点‐组成图测绘实验日期:20年月日姓名:学号:班级:一、实验目的及要求(1)在大气压下,测定环己烷-乙醇体系气、液平衡相图(沸点-组成图)。
(2)掌握阿贝折光仪的测量原理和使用方法。
二、实验原理一个完全互溶的二元体系,两个纯液体组分,在所有组成范围内完全互溶。
在定压下,完全互溶的二元体系的沸点‐组成图可分为三类,如图C7.1所示。
a.溶液的沸点介于两纯组分沸点之间,如苯‐甲苯体系;b.溶液有最低恒沸点,如环己烷‐乙醇体系;c.溶液有最高恒沸点,如丙酮‐氯仿体系。
b、c两类溶液在最高或最低恒沸点时气、液两相组成相同,加热蒸发只能使气相总量增加,气、液相组成及溶液沸点保持不变,此温度称恒沸点,相应组成称恒沸组成。
图C7.1 二元体系T-x图下面以a为例,简单说明绘制沸点-组成图的原理。
加热总组成为x1的溶液,体系的温度上升,达液相线上1点时溶液开始沸腾,组成为x2的气相开始生成,但气相量很少(趋于0),x1、x2二点代表达到平衡时液、气两相组成。
继续加热,气相量逐渐增多,沸点继续上升,气、液二相组成分别在气相线和液相线上变化,当达某温度(如2点),并维持温度不变时,则x3、x4为该温度下液、气两相组成,气相、液相的量之比按杠杆规则确定。
当外压恒定时,在气、液两相共存区域自由度等于1,当温度一定时,则气、液两相的组成也就确定,总组成一定,由杠杆规则可知两相的量之比也已确定。
因此,在一定的实验装置中,全回流的加热溶液,在总组成、总量不变时,当气相的量与液相的量之比也不变时(达气-液平衡),则体系的温度也就恒定。
分别取出气、液两相的样品,分析其组成,得到该温度下,气、液两相平衡时各相的组成。
改变溶液总组成,得到另一温度下,气、液两相平衡时各相的组成。
测得溶液若干总组成下的气液平衡温度及气、液相组成,分别将气相点用线连接即为气相线,将液相点用线连接即为液相线,得到沸点‐组成图。
气相、液相的成份分析采用折光率法:先绘出折光率~组成(n~x)的等温线,方法是在定温下测定已知各种组成(x)的折光率(n),绘出n~x等温线。
常见的共沸物

常见的共沸物又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分和沸点均保持不变。
这实际是表明,此时沸腾产生的蒸汽和液体本身有着完全相同的组成。
共沸物是不可能通过常规的蒸馏或分馏手段加以分离的。
并非所有的二元液体混合物都可形成恒沸物,一些例子列在了下面。
这类混合物的温度-组分相图有着显著的特征,即,其气相线(气液混合物和气态的交界)和液相线(液态和气液混合物的交界)有着共同的最高点或最低点。
如此点为最高点,则称为正恒沸物;如此点为最低点,则称为负恒沸物。
大多数恒沸物都是负恒沸物,即有最低沸点。
非均相共沸精馏分离叔丁醇和水的方法专利号:2本发明公开了一种非均相共沸精馏分离叔丁醇和水方法。
采用包括精馏塔的精馏装置,非均相共沸精馏分离叔丁醇和水,其过程,常压下将叔丁醇和水的恒沸物或混合物,按恒沸物或混合物和共沸剂环已烷的质量比为0.3~1.5,加入精馏塔的塔釜中,在塔釜为60-80℃进行全回流,全回流结束后,采出分相器中富集的水,当塔顶在64~83℃,塔釜在70~87℃,以回流比为1~5,采出三元共沸物收集在分相器中,分相器上层的环己烷和叔丁醇有机相采出备用。
再以回流比1-4,在塔顶62-82℃下由塔顶采出环己烷-水及少量环己烷-叔丁醇的混合物后,在塔釜82-88℃,塔顶82-83℃下从塔顶得到纯度为98.2wt%的叔丁醇产品。
本发明的优点是,共沸剂的用量少,叔丁醇的一次收率高。
乙醇沸点78.3 乙醇和水二元共沸沸点 78.1 二元共沸组成:水4.4 %,乙醇95.5% 要想精馏得到无水乙醇需加人苯,三元共沸。
« 【下载】化学滴定分析用标准溶液的制备(国标)15种常用有机溶剂的纯化»常见的共沸混合物的组成及共沸点化学世界 |共沸物,又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分和沸点均保持不变。
这实际是表明,此时沸腾产生的蒸汽和液体本身有着完全相同的组成。
二元恒沸混合物的组成

二元恒沸混合物的组成一、引言二元恒沸混合物是指由两种成分组成的混合物,在特定温度下,其蒸汽与液体处于平衡状态,且具有相同的沸点。
本文将介绍二元恒沸混合物的组成及其相关知识。
二、二元恒沸混合物的概念二元恒沸混合物是指由两种成分组成的混合物,在一定温度下,其蒸汽与液体处于平衡状态,且具有相同的沸点。
这种混合物的组成可以是不同的,但其蒸汽和液体的组成比例是恒定的。
三、二元恒沸混合物的组成1. 组成比例二元恒沸混合物的组成比例是指其蒸汽和液体中两种成分的比例关系。
在恒沸混合物中,两种成分的比例保持不变,无论是在蒸汽相还是在液体相中,其成分比例都保持一致。
2. 成分的选择二元恒沸混合物的成分选择主要取决于两种物质之间的化学性质和物理性质。
通常情况下,选择的两种成分具有相似的化学性质和物理性质,这样才能在特定温度下形成恒沸混合物。
3. 形成条件二元恒沸混合物的形成需要满足一定的条件。
首先,选择的两种成分之间必须具有相似的化学性质和物理性质,这样才能在特定温度下形成恒沸混合物。
其次,需要选择适当的温度,使得两种成分的蒸汽和液体能够达到平衡状态。
四、二元恒沸混合物的应用1. 蒸馏分离二元恒沸混合物的应用之一是在蒸馏分离中。
由于恒沸混合物的蒸汽和液体成分比例恒定,可以通过蒸馏的方式将两种成分有效地分离出来。
这在化工工艺中具有重要的应用价值。
2. 溶剂提取二元恒沸混合物的应用之二是在溶剂提取中。
由于恒沸混合物的蒸汽和液体成分比例恒定,可以利用这一特性进行溶剂的提取。
通过选择适当的溶剂和调节温度,可以实现对特定成分的有效提取。
3. 质量分析二元恒沸混合物的应用之三是在质量分析中。
由于恒沸混合物的组成比例恒定,可以通过测量蒸汽和液体中两种成分的比例来确定样品中特定成分的含量。
这在化学分析和质量检测中具有重要的意义。
五、总结二元恒沸混合物是由两种成分组成的混合物,在特定温度下,其蒸汽和液体处于平衡状态,且具有相同的沸点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
63.5
36.5
水
异丁酸甲酯
100.0
92.3
77.7
6.8
93.2
水
异丁酸乙酯
100.0
110.1
85.2
15.2
84.8
水
异丁酸正丙酯
100.0
133.9
92.2
30.8
69.2
水
异丁酸异丁酯
100.0
147.3
95.5
39.4
60.6
水
异丁酸异戊酯
100.0
168.9
97.4
56.0
44.0
Ⅰ
Ⅱ
Ⅰ
Ⅱ
混合物(Mixture)
Ⅰ
Ⅱ
水
乙醇
100.0
78.4
78.1
4.5
95.5
水
正丙醇
100.0
97.2
87.7
28.3
71.7
水
异丙醇
100.0
82.5
8.04
12.1
87.9
水
正丁醇
100.0
117.8
92.4
38.0
62.0
水
异丁醇
100.0
108.0
90.0
33.2
66.8
水
仲丁醇
100.0
122.9
89.0
25.0
75.0
水
甲酸(最大值)
100.0
100.8
107.3
22.5
77.5
水
乙酸
100.0
118.1
无(no)
无(no)
无(no)
水
丙酸
100.0
141.1
99.98
82.3
17.7
水
丁酸
100.0
163.5
99.4
81.6
18.4
水
异丁酸
100.0
154.5
99.3
79.0
21.0
97.3
59.0
41.0
水
苯甲醚
100.0
153.9
95.5
40.5
59.5
水
间苯二酚二乙醚
100.0
235.0
99.7
91.0
9.0
水
甲酸正丙酯
100.0
80.9
71.9
3.6
96.4
水
甲酸正丁酯
100.0
106.8
83.8
15.0
85.0
水
甲酸异丁酯
100.0
98.4
80.4
7.8
92.2
水
甲酸正戊酯
93.8
水
乙酸正丁酯
100.0
126.2
90.2
28.7
71.3
水
乙酸异丁酯
100.0
117.2
87.5
19.5
80.5
水
乙酸正戊酯
100.0
148.8
95.2
41.0
59.0
水
乙酸异戊酯
100.0
142.1
93.8
36.2
63.8
水
乙酸苄甲酯
100.0
214.9
99.6
87.5
12.5
水
乙酸苯酯
100.0
水
异戊酸甲酯
100.0
116.3
87.2
19.2
80.8
水
异戊酸乙酯
100.0
134.7
92.2
30.2
69.8
水
异戊酸正丙酯
100.0
155.8
96.2
45.2
54.8
水
异戊酸异丁酯
100.0
168.7
97.4
55.8
44.2
水
异戊酸异戊酯
100.0
193.5
98.8
74.1
25.9
水
己酸乙酯
100.0
52.5
47.5
水
氢碘酸(最大值)
100.0
-34.0
127.0
43.0
57.0
水
甲基乙基酮
100.0
79.6
73.5
11.0
89.0
水
甲基正丙基酮
100.0
102.0
83.3
19.5
80.5
水
甲基异丁基酮
100.0
115.9
87.9
24.3
75.7
水
异丙亚基丙酮
100.0
129.5
91.8
34.8
水
丁酸甲酯
100.0
102.7
82.7
11.5
88.5
水
丁酸乙酯
100.0
120.1
87.9
21.5
78.5
水
丁酸正丙酯
100.0
142.8
94.1
36.4
63.6
水
丁酸正丁酯
100.0
165.7
97.2
53.0
47.0
水
丁酸异丁酯
100.0
156.8
96.3
46.0
54.0
水
丁酸异戊酯
100.0
178.5
1.3
98.7
水
二异丙醚
100.0
68.4
62.2
4.5
95.5
水
乙基正丙基醚
100.0
63.6
59.5
4.0
96.0
水
二异丁基醚
100.0
122.2
88.6
23.0
77.0
水
二异戊基醚
100.0
172.6
97.4
54.0
46.0
水
二苯醚
100.0
259.3
99.3
96.8
3.2
水
苯乙醚
100.0
170.4
表中给出的沸点值是在大气压(101.325kPa)下测得的。
二元恒沸混合物的组成和沸腾温度
Compositions and Boiling Points of Constant Boiling Binary Mixtures
组分名称
(Name)
沸点
(Boiling point)
/℃
质量百分比
(Mass percentage)/%
99.9
91.0
9.0
水
糠醇
100.0
169.4
98.5
80.0
20.0
水
苯
100.0
80.2
69.3
8.9
91.1
水
甲苯
100.0
110.8
84.1
19.6
80.4
水
二氯乙烷
100.0
83.7
72.0
8.3
91.7
水
二氯丙烷
100.0
96.8
78.0
12.0
88.0
水
乙醚
100.0
34.5
34.2
65.2
水
双丙酮醇
100.0
166.0
98.8
87.3
12.7
水
丁醛
100.0
75.7
68.0
6.0
94.0
水
糠醛
100.0
161.5
97.5
65.0
35.0
水
吡啶
100.0
115.5
92.6
43.0
57.0
甲醇
乙酸甲酯
64.7
57.0
53.8
18.7
81.3
38.5
61.5
水
3-戊醇
100.0
115.4
91.7
36.0
64.0
水
正己醇
100.0
157.9
97.8
75.0
25.0
水
正庚醇
100.0
176.2
98.7
83.0
17.0
水
正辛醇
100.0
195.2
99.4
90.0
10.0
水
烯丙醇
100.0
97.0
88.2
27.1
72.9
水
苯甲醇
100.0
205.2
水
硝酸(最大值)
100.0
86.0
120.5
32.0
68.0
水
高氯酸(最大值)
100.0
110.0
203.0
28.4
71.6
水
氢氟酸(最大值)
100.0
19.4
120.0
63.0
37.0
水
氢氯酸(最大值)
100.0
-84.0
110.0
79.76
20.24
水
氢溴酸(最大值)
100.0
-73.0
126.0
195.7
98.9
75.1
24.9
水
丙酸甲酯
100.0
79.9
71.4
3.9
96.1
水
丙酸乙酯
100.0
99.2
81.2
10.0
90.0
水
丙酸正丙酯
100.0
122.1
88.9
