基础化学习题解答(第四章)
基础化学习题答案1-8

基础化学习题答案1-8基础化学习题答案习题答案第一章绪论1、求0.010kgNaOH、0.100kg(1Ca2+)、0.10kg(1Na2CO3)的物质的量。
22解:(1)m(NaOH) = 0.010kg M(NaOH) = 40gmol-1n(NaOH) =21040= 0.25 (mol)2(2)m(1Ca2+) = 0.100kg M(1Ca2+) = 40gmol-1 n(1Ca2+) =2__= 5.0(mol)12(3)m(Na2CO3) = 0.10kg M(Na2CO3) = 53gmol-121n(Na2CO3) =__= 1.89 (mol)2、下列数值各有几位有效数字?(1)1.026 4位(2)0.0208 3位(3)0.003 1位(4)23.40 4位(5)3000 无数位(6)1.0×10-3 2位3、应用有效数字计算规则,计算下列各式:(1)21.10 - 0.263 + 2.3 = 23.1 (2)3.20×23.45×8.912 = 667(3)3.22 23.171.26 103= 5.93×10 (4)-35.4 4.32 102.325 2.1524.6×10-24、(1) 以H2SO4为基本单元,M(H2SO4)=98g/mol;(2) 以HSO4-为基本单元,M(HSO4-)=97g/mol;(3) 以3H2SO4为基本单元,M(3H2SO4)=294g/mol。
5、答:甲的报告更为合理,百分比小数点后保留两位有效数字。
基础化学习题答案第二章溶液与胶体1、在25oC时,质量分数为0.0947的稀硫酸溶液的密度为1.06gL-1,在该温度下纯水的密度为0.997 gL-1。
计算H2SO4的物质的量分数、物质的量浓度和质量摩尔浓度。
解:设取稀硫酸溶液1L,则n(H2SO4) = n(H2O) =1.06 1000 0.0__1.06 1000 (1 0.0947)18= 1.02 (mol) = 53.31(mol)c(H2SO4) =n(H2SO4)V= 1.02 (moll-1)1.021.02 53.31x(H2SO4) =b(H2SO4) =n(H2SO4)n(H2SO4) n(H2O)== 0.0188n(H2SO4)m(H2O)=1.021000 1.06 (1 0.0947)= 0.106(molkg-1)2、醚的正常沸点为34.5℃,在40℃时往100g乙醚中至少加入多少摩尔不挥发溶质才能防止乙醚沸腾?解:Tb Kb bB )2.02 (40-34.5n0.1n = 0.22mol3、苯的凝固点为5.50℃,Kf = 5.12 Kkgmol-1。
基础化学第四章习题答案

1.能够抵抗少量酸、碱或加水稀释,而本身pH 值基本保持不变的溶液,称为缓冲溶液。
2.缓冲容量是衡量缓冲能力大小的尺度。
通常用使单位体积缓冲溶液的pH 改变1个单位时,所需加入一元强酸或一元强碱的物质的量表示缓冲容量。
影响缓冲容量的主要因素是缓冲系的总浓度和缓冲比;缓冲比一定时,总浓度越大,缓冲容量越大;总浓度一定时,缓冲比越接近于1,缓冲容量越大。
缓冲容量与缓冲系中共轭酸的p K a 无关。
所以总浓度相同的HAc-NaAc 和H 2CO 3-HCO 3-缓冲系的缓冲容量相同。
3.(1)(2)(4)(5).4. 配制pH = 3的缓冲溶液,选HCOOH —HCOO -最合适,因为HCOOH 的pK a = 3.75,与所需的pH 值最接近。
5. 此混合溶液为HCO 3- -CO 32-组成的缓冲溶液。
查表4-1,H 2CO 3的p K a2=10.25。
m o l m o l g g H C O n 119.00.840.10)(13=⋅=--mol094.0molg 106g0.10)CO(123=⋅=--n代入式(4.4)得15.10mol119.0mol 094.0lg2510)HCO)CO lgp pH 323a =+⋅=+=--((n n K6. H 2C 2O 4:pKa 1 = 1.23 pKa 2 = 4.19∴应选择---242242O C O HC 缓冲体系 1]O[C ]O [HC ]O[C ]O [HC lgpKa pH 2424224242=⇒-=----则:3:2V :V NaOH O C H422=7. HAc + NaOH = NaAc + H 2O初(mol ):100×0.10 50×0.10平 (mol): 50×0.10 50×0.10c a =301501005=+(mol·L -1) c b =301501005=+(mol·L -1)pH=pKa-lg754301301754.lg.c c ba =-= 8.设需加入0.10 mol·L -1HCl 溶液x 毫升,NH 3·H 2O + HCl = NH 4Cl + H 2O生成NH 4Cl 的浓度 = 0.10x /(500+x) (mol·L -1) 剩余NH 3·H 2O 的浓度 = (0.10×500 – 0.10x )/ (500+x) (mol·L -1)pOH = 14-10 = 4 x1.0x 1.050lg75.4)x 500/(x 10.0)x 500/()x 500(10.0lg75.44--=++--=625101050.x.x .=- x = 75.5(mL) 设需加入NH 4Cl 的浓度为y mol·L -1,y1.0lg75.44-= 62.5y1.0= y = 0.018(mol/L)需加入固体NH 4Cl = 0.018×0.5×53.5 = 0.48(g)1]O[C ]O [HC ]O[C ]O [HC lgpKa pH 2424224242=⇒-=----则:3:2V :V NaOH O C H422=9.加入的NaOH 为0.20g÷40g·mol -1=0.005mol 、c (OH -)=0.005mol ÷0.100L=0.05mol ·L -1设原溶液中共轭碱 [B -]原=xmol·L -1,则加入NaOH 后,[HB]=0.25mol·L -1-0.05mol·L -1=0.20mol·L -1, [B -]=0.05mol·L -1+xmol·L -1 ,代入式(4.2)]HB []B [lga p pH -+=K11Lmol 20.0L mol )x 05.0(lg30.560.5--⋅⋅++=[B -]原=xmol·L -1=0.35mol·L -1原溶液45.5Lmol 25.0Lmol 35.0lg30.5pH 11=⋅⋅+=--10. 阿司匹林以HAsp 表示,解离后以Asp -表示。
2020年智慧树知道网课《基础化学》课后章节测试满分答案

第一章测试1【单选题】(1分)在使用物质的量单位(mol)时,要注意基本单元的表示。
若n(H2O)=1.0mol,则n(1/2H2 O)的数值为()A.0.5molB.1.0molC.3.0molD.2.0mol第二章测试1【判断题】(1分)对于非电解质稀溶液,其渗透浓度在数值上等于其质量摩尔浓度。
A.对B.错2【判断题】(1分)临床上将葡萄糖溶液与溶液作为等渗溶液使用。
如将此两溶液以任意比例混合,则所得混合液也必然是等渗溶液。
A.对B.错3【判断题】(1分)渗透浓度为的NaCl溶液和的葡萄糖溶液,它们的渗透压相等,则它们的物质的量浓度也相等。
A.对B.错4【判断题】(1分)由于0℃的冰与0℃的NaCl溶液温度相同,所以该两相可以共存。
A.错B.对5【判断题】(1分)难挥发非电解质稀溶液的沸点升高、凝固点降低均由溶液的蒸气压下降引起。
A.对B.错6【判断题】(1分)无论溶质是电解质还是非电解质,凝固点降低值较小的溶液的渗透压一定低于凝固点降低值较大的溶液。
A.错B.对7【判断题】(1分)由于苯比水易挥发,故在相同温度下,苯的蒸气压比水大。
A.对B.错8【判断题】(1分)将相同质量的葡萄糖和甘油分别溶于1L水中,则两溶液的△p1=△p2,△T b1=△T b2,π1=π(T一定)。
2A.对B.错9【判断题】(1分)纯溶剂通过半透膜向溶液渗透的压力称为渗透压。
A.对B.错10【判断题】(1分)渗透浓度均为的NaCl溶液和葡萄糖溶液,NaCl溶液的渗透压大。
A.错B.对11【判断题】(1分)渗透压较高的溶液其物质的量浓度一定较大。
A.对B.错12【单选题】(1分)下列方法最适用于测定蛋白质相对分子质量的是()A.沸点升高法B.蒸气压下降法C.渗透压法D.凝固点降低法13【单选题】(1分)已知水的,测得某人血清的凝固点为-0.56℃,则该血清的渗透浓度为()A.506mmol·L-1B.560mmol·L-1C.408mmol·L-1D.301mmol·L-114【单选题】(1分)已知苯的凝固点为5.35℃,。
高一化学(必修一)《第四章 核素》练习题-附答案解析

高一化学(必修一)《第四章核素》练习题-附答案解析班级:___________姓名:___________考号:___________一、单选题1.中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。
关于Lv的叙述错误的是( ) A.原子序数116 B.中子数177 C.最外层电子数6 D.相对原子质量2932.某公司原计划发射77颗卫星,以实现全球卫星通信,这一数字与铱(Ir)元素的原子核外电子数恰好相等,因此称为“铱星计划”。
已知铱的一种同位素的质量数为191,则其核内中子数与质子数之差是()A.77 B.114 C.37 D.2683.2018年5月,美国宣布退出伊朗核协议,23592U的浓缩是焦点问题。
下列有关23592U的说法正确的是A.23592U原子核中含有92个中子B.23592U原子核外有143个电子C.23592U与23892U互为同位素D.23592U与23892U互为同素异形体4.核素15N常用作生物医药示踪剂。
下列关于15N的说法不正确...的是A.质子数是7 B.电子数是8 C.中子数是8 D.质量数是155.已知阳离子 M2+的原子核内有 n个中子,M 原子的质量数为 A,则 m g M2+中所含电子的物质的量是A.(A-n-2)/Am mol B.m(A-n)/n mol C.m(A-n-2)/A mol D.m(A-n+2)/A mol6.下列化学用语描述正确的是()A.可用于考古断代的一种核素的符号:136CB.氚的原子结构模型:C.182O 的结构示意图:D.14C和14N互为同位素7.在元素周期表中,应用于计算机芯片的硅元素如图所示,下列有关硅的说法正确A .原子核外有14个电子B .原子个数是14C .硅原子的相对原子质量是28.09D .质量数是28.098.在63Li 、73Li 、2311Na 、2412Mg 、146C 、147N 中,下列说法不正确的是( ) A .表示6种核素B .63Li 和73Li 为同种元素的不同核素,互称同位素 C .146C 和147N 的质量数相同,属于同主族元素 D .2311Na 和2412Mg 的中子数相同9.通过对用14C 标记的C 60进行跟踪研究,医学界发现了一种C 60的羧酸衍生物在特定的条件下可通过断裂DNA 杀死艾滋病病毒。
普通化学第四章课后习题解答

第四章化学平衡原理参考答案P 68~69综合思考题:解:①根据θθmf B m r H v H ∆=∆∑(其中B v 对生成物取正值,反应物取负值)有: ),()1(),()1(),(),(2g B H g A H g E H g D H H m f m f m f m f m r θθθθθ∆-+∆-+∆+∆=∆=2×(-4RT 1)+(-2.606RT 1)+3.5RT 1+2.5RT 1 =-4.606RT 1同理:),()1(),()1(),(),(2g B S g A S g E S g D S S m m m m m r θθθθθ-+-++=∆=2×(0.25RT 1)+(0.5RT 1)-0.3RT 1-0.7RT 1 =0.0根据吉“布斯-赫姆霍兹”方程θθθmr m r m r S T H G ∆-∆=∆有: 31100.0298606.4-⨯⨯--=∆RT G m r θ=-4.606RT 1×10-3(kJ.mol -1)<0 ∴反应正向自发。
②根据θθK RT G m r ln -=∆有:606.41010606.4ln 3131=⨯⨯--=∆-=--RT RT RT G K m r θθK θ=100.0③求Q ,根据]/[]/[]/[]/[2θθθθP P P P P P P P Q B A E D ⋅⋅=有: ]3.101/3.1015.0[]3.101/3.1010.1[]3.101/3.1015.0[]3.101/3.1015.0[2kPa kPa kPa kPa kPa kPa kPa kPa Q ⨯⋅⨯⨯⋅⨯==0.25 ∵Q<K θ∴平衡向正反应方向移动④根据)(ln 211212T T TT R H K K m r ⋅-∆=θθθ有:1606.4RT H m r -=∆θ,T 1=298K ,0.1001=θK ,T 2=398K ,?2=θK 将有关数据代入式子中得:)398298298398(298606.40.100ln2⨯-⋅⨯-=R R K θ解得:K θ2=31.4 ⑤∵K θ2< K θ1,∴由T 1升至T 2平衡向逆反应方向移动(即吸热反应方向移动)。
《基础化学》课后习题参考答案(有机部分)
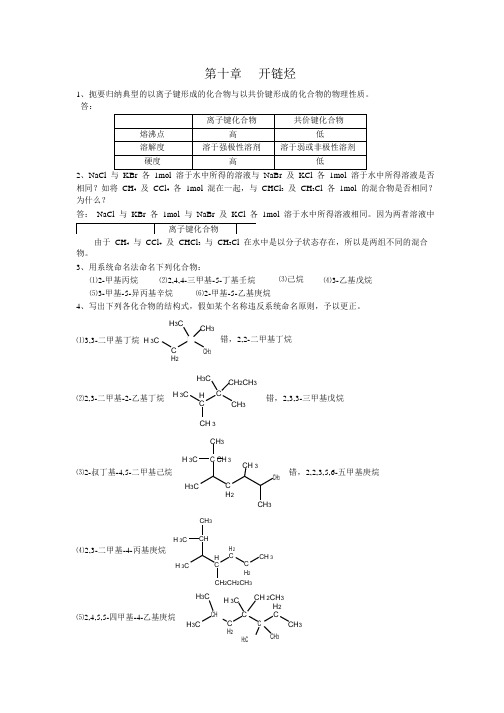
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
基础化学习题04
第四章 缓冲溶液 首 页 难题解析 学生自测题 学生自测答案 章后习题答案 难题解析 [TOP]例4-1 现有1.0L 缓冲溶液,内含0.01mol H 2PO 4-、0.030mol HPO 42-。
(1) 计算该缓冲溶液的pH ;(2) 往该缓冲溶液中加入0.005 0 mol HCl 后,pH 等于多少?析 题设缓冲系:H 2PO 4-HPO 42-+ H +,用公式 pH =p K a +lg )PO (H )(HPO 4224--n n 计算。
若加入HCl ,H +与HPO 42- 反应生成H 2PO 4-。
解 (1)根据H 3PO 4: p K a1=2.16; p K a2=7.21; p K a3=12.32pH =p K a +lg )PO (H )(HPO 4224--n n =7.21+lg mol 010.0mol 030.0=7.68 (2)加入0.005 0 mol HCl 后:pH =p K a +lg )PO (H )(HPO 4224--n n =7.21+lg 0.0050mol 0.010mol 0.0050mol 0.030mol +-= 7.42 例4-2 柠檬酸(缩写H 3Cit )常用于配制供培养细菌的缓冲溶液。
如用500mL 的0.200 mol·L -1柠檬酸,须加入0.400 mol·L -1的NaOH 溶液多少毫升,才能配成pH 为5.00的缓冲溶液?(已知柠檬酸的p Ka 1=3.14,p Ka 2= 4.77,p Ka 3=6.39)析 要配pH5.00的缓冲溶液,应选p K a 2,缓冲系NaH 2Cit-Na 2HCit ,用NaOH 与H 3Cit 完全反应生成NaH 2Cit ,再与NaH 2Cit 部分反应生成Na 2HCit 。
解 设H 3Cit 全部转化为NaH 2Cit 需NaOH 溶液V 1 mL :0.200 mol·L -1×500 mL = 0.400 mol·L -1×V 1 mL解得: V 1 = 250设NaH 2Cit 部分转化,组成NaH 2Cit -Na 2Hcit 缓冲系,需NaOH 溶液V 2 mL :NaH 2Cit + NaOH Na 2HCit + H 2On (Na 2HCit )= 0.400 mol·L -1×V 2 mL= 0.400V 2 mmoln (NaH 2Cit )= 0.200 mol·L -1×500 mL -0.400 mol·L -1×V 2 mL= (100-0.400 V 2)mmolpH = p Ka 2 + lg )Cit NaH ()HCit Na (22n n = 4.77+lg )mmol0.400-(100mmol 400.022V V = 5.00 解得: V 2 = 157共需加入NaOH 溶液的体积: V 1 mL + V 2 mL = 250 mL + 157 mL = 407 mL例4-3 今有500mL 总浓度0.200 mol·L -1、pH4.50的HAc -NaAc 缓冲溶液,欲将pH 调整到4.90,需加NaOH 多少克?调整后缓冲溶液的缓冲容量是多少?解 查表得HAc 的p K a= 4.76,在pH4.50的缓冲溶液中:4.50 = 4.76 + lg (HAc)(NaAc)L 0.200mol -1c c -⋅ 解得 c (HAc )= 0.130mol·L -1c (NaAc )= 0.200 mol·L -1-0.130 mol·L -1= 0.070mol·L -1加入固体NaOH m g : 4.90 = 4.76 + lg 1-1-1-1-mol g 40g L 50.0L mol 130.0mol g 40gL 50.0L mol 070.0⋅-⨯⋅⋅+⨯⋅m m 解得: m = 0.92在pH4.90的缓冲溶液中:[HAc] = 0.130 mol·L -1-L50.0mol g 40g 92.01-⨯⋅= 0.084mol·L -1 [Ac -] = 0.070 mol·L -1+L50.0mol g 40g 92.01-⨯⋅= 0.116mol·L -1 缓冲容量为: β = ][Ac [HAc]][HAc][Ac 2.303--+⨯=1-1--1-1L 0.116mol L 0.084mol L 0.116mol L 0.084mol 2.303⋅+⋅⋅⨯⋅⨯= 0.112 mol·L -1 例4-4 用0.025 mol·L -1的H 3PO 4和0.10 mol·L -1的NaOH ,配制pH7.40的缓冲溶液100 mL ,求所需H 3PO 4和NaOH 的体积比。
基础化学第四章 沉淀平衡练习答案
基础化学第四章习题答案1、何谓沉淀-溶解平衡?同物质的量的BaCl 2和H 2SO 4混合溶液中,含有哪些离子?这些离子浓度之间存在着哪些关系?答:难溶电解质溶解和沉淀速度相等,固体的量和溶液中分子或离子的量不再改变的状态,称为沉淀-溶解平衡。
Ba 2+、Cl -、SO 42-、H +、OH -[Ba 2+/c θ][SO 42-/ c θ]=K sp θ,[H +][OH -]= K w 等2、 活度积、溶度积、离子积之间有何区别与联系?答:活度积、溶度积指平衡状态下的活度积或浓度积,对给定的难溶电解质其活度积只与温度有关,溶度积不但与温度有关,还和溶液离子强度有关,对于MA 型难溶电解质:θsp A M apK K =γ⋅γ-+θ。
离子积指任意状态下的浓度积,其值是任意的。
3、 无副反应时,沉淀的溶度积与溶解度有何关系?溶度积小的物质,它的溶解度是否一定小?举例说明。
答:θspc nm K S nm nm +θ=不同类型难溶电解质的溶解度不能根据溶度积数值大小直接判断。
溶度积小的物质,它的溶解度是不一定小,如Ag 2CrO 4与AgCl 。
4、 除了沉淀物质本性以外,影响沉淀溶解度的主要因素有哪些?答:除了沉淀物质本性以外,影响沉淀溶解度的主要因素还有:同离子效应、盐效应、酸效应、配位效应等。
5、判断下列操作中可能发生的反应和现象并予以解释:(1)将少量CaCO 3固体放入稀HCl 中。
(2)将少量Mg (OH )2放入NH 4Cl 溶液中。
(3)向少量MnSO 4溶液中加入数滴饱和H 2S 水溶液,再逐滴加入2mol ·L -1的氨水。
(4)向盛少量PbS 固体的试管中,滴入H 2O 2溶液。
(5)向盛少量AgCl 沉淀的试管中,滴入KI 溶液。
(6)向盛少量Cu (OH )2沉淀的试管中,滴入2mol ·L -1NH 3·H 2O 溶液。
答:(1)CaCO 3固体溶解,有无色无味气体产生。
基础化学课后习题答案
基础化学 第一章 习题参考答案3. (1) 5位,(2) 3位,(3) 2位,(4)1位,(5)2位。
4. %1.0001.01024.00001.01024.01024.01023.0-=-=-=-=RE5. kPa}){}{}({m N 10}){}{}({dm m N }){}{}({ L J }){}{}({K mol K J L mol }){}{}({ ])[][]([}){}{}({][}{][}{][}{2331111-T R c T R c T R c T R c T R c T R c T R c T T R R c c cRT Π⨯⨯=⋅⨯⨯⨯=⋅⋅⨯⨯=⋅⨯⨯=⨯⋅⋅⨯⋅⨯⨯=⨯⨯⋅⨯⨯=⋅⨯⋅⨯⋅==-----式中,花括号代表量的值,方括号代表量的单位。
6. 1 mi 3 = 1.609 3443 km 3 = 4.168 182 km 3, 所以水资源的总体积V = (317 000 000 + 7 000 000 + 2 000 000 + 30 000) × 4.168 182 km 3 =1.3590 ×109 km 37.m ol 0.25 kg 1g1000 m ol g )00.10.160.23(kg 0.010(NaOH)1-=⨯⋅++=nmol1.89 kg 1g 1000 mol g )00.16301.1299.222(21kg 0.100 )CO Na 21(mol4.99 kg 1g1000 mol g 08.4021kg 0.100 )Ca 21(1-321-2=⨯⋅⨯++⨯⨯==⨯⋅⨯=+n n8. m ol 2.57 m ol g )35.45 239.65(g350)(ZnCl 1-2=⋅⨯+=n1-21-2k mol 3.95 kg 1g1000 650mol 2.57 )(ZnCl L mol 3.48 L1mL1000 mL 39.57mol 2.57)(ZnCl g g b c ⋅=⨯=⋅=⨯=9. 1-1--3L mmol 5.1 mol 1mmol1000 L 1L 100mL 1000 mol g 9.13g 10 20 )(K ⋅=⨯⨯⨯⋅⨯=+c1-1--3-L mmol 103 mol1mmol 1000 L 1L 100mL 1000 mol g 5.453g 10 366 )(Cl ⋅=⨯⨯⨯⋅⨯=c10. 设称取含结晶水的葡萄糖(C 6H 12O 6·H 2O)的质量为m ,052600. molg 16.0)1.01g/[(2 50)-(1000 mol 0.28mol0.278 )O H (C Lmol 0.278 mol g )0.16601.1120.126(L g 0.05 )O H (C g 27.5L g 50.0 L.50001g )0.1601.120.16601.1120.126(g)0.16601.1120.126( O)H O H (C 1-61261-1-1-61261-26126=⋅+⨯+=⋅=⋅⨯+⨯+⨯⋅==⋅=⨯+⨯+⨯+⨯+⨯⨯+⨯+⨯⨯=⋅x c m m ρ11. L .41 L g .091g 3.02g )5.350.23( g 5.0 (NaCl)1-=⋅⨯+⨯=V12. ∵ 10KI + 2KMnO 4 + 8H + = 12K + + 2MnO 2 + 5I 2 + 4H 2O∴ mol 0.004 mol g )9.1262(21g 0.508 )I 21( )KMnO 51 (KI 1-24=⋅⨯⨯==+n n基础化学 第二章 习题参考答案1. 根据 BA AA n n n x +=,mol 56.5mol 18.0g 100g O)(H 1-2=⋅=n mol 0292.0molg 342g 0.10)(1=⋅=-蔗糖n 995.0mol0292.0mol 56.5mol 56.5)(O)(H O)(H O)(H 222=+=+=蔗糖n n n xkPa 33.2995.0kPa 34.2O)(H 20=⨯==x p p2. (1) mol 004912.0molg 342g68.1)(1=⋅=-甲n mol 003551.0molg 690g45.2)(1=⋅=-乙n 1kg mol 2456.0kg0200.0mol004912.0-⋅==(甲)b1kg mol 1775.0kg0200.0mol003551.0-⋅==(乙)b溶液乙的蒸气压下降小,故蒸气压高。
大学化学基础(邓建成第二版)第四章思考题、习题
答:电负性是描述化学键中各原子对共用电子对的吸引能力。 同周期元素,从左到右,电负性数值逐渐增加,但同 周期过渡元素的电负性变化不大。 同主族元素,从上到下,电负性数值逐渐降低。
7、如何理解共价键具有方向性和饱和性? 答: 共价键的形成条件之一是原子中必须有成单电子,而 且形成的共价键的数目受到未成对电子数的限制。在形成共价 键时几个未成对的电子只能与几个自旋相反的单电子配位成键。 这说明共价键具有饱和性。 在形成共价键时,原子间总是尽可能沿着原子轨道最大重 叠的方向成键,轨道重叠越多,形成的共价键也就越稳定。原
⑤ CO2气体分子之间存在色散力。
10、晶体有几种主要类型?以下物质各属于何种晶体? ① NaCl; ④ 冰; ② SiC; ③ 石墨; ⑤ 铁。
答:晶体主要有:离子晶体、分子晶体、金属晶体、原 子晶体和过渡型晶体。 ① NaCl为离子晶体; ② SiC为原子晶体;③ 石墨为过渡 型晶体﹙混合型晶体﹚; ④ 冰为分子晶体; ⑤ 铁为金属晶
分别与三个Cl原子的p轨道重叠成键,因此 NCl3为三角锥形。
12、用分子间力说明下列事实: ① 常温下F2、Cl2是气体,Br2是液体,碘是固体; ② NH3易溶于水,而CH4却难溶于水;
③ 水的沸点高于同族其它氢化物的沸点。
答: ① F2 、 Cl2 、 Br2 、碘分子都为非极性分子,其分子量逐
体。
11、试用离子极化的观点解释AsF溶于水,AsCl、AsBr、 AsI难溶于水,溶解度由AsCl到AsI依次减少。 答:阴离子半径越大,受阳离子的极化影响,其电子云的变 形性越大,阴、阳离子的电子云重叠也就越多。离子中的共价键 成分也越多。 由于F¯ 、Cl¯ 、Br¯ 、I¯ 从左到右,离子半径逐渐增大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
思考与习题一、填空题:1.可逆反应 2A(g) + B(g) 2C(g) ;Δr H m θ< 0 。
反应达到平衡时,容器体积不变,增加B 的分压,则C 的分压 ___增大_______,A 的分压 ___减小________ ;减小容器的体积,B 的分压 _____减小______, K θ___不变________。
2.由N 2和H 2合成NH 3的反应中,Δr H m θ < 0,当达到平衡后,再适当降低温度则正反应速率将________减小 _____,逆反应速率将___减小__________,平衡将向___右 _____方向移动。
3.一定温度下,反应 PCl 5(g) PCl 3(g) + Cl 2 (g) 达到平衡后,维持温度和体积不变,向容器中加入一定量的惰性气体,反应将____不 _______ 移动。
4. 基元反应 2NO + Cl 2 → 2NOCl 是_3 _分子反应,是 3_级反应,其速率方程为__)Cl (·)NO ( 2c c k ⋅=υ____。
5.在密闭容器中进行N 2(g)+3H 2(g)→2NH 3(g)的反应,若压力增大到原来的2倍,反应速率增大 __16___ 倍。
6.可逆反应: I 2+H 2 2HI 在713K 时K θ=51,若将上式改写为 :21I 2 +21H 2 HI 则其K θ为 __51 ____ 。
7.已知下列反应的平衡常数: H 2(g) + S(s)H 2S(g) K θ1 S(s) + O 2(g) SO 2(g) K θ2则反应 H 2(g) + SO 2(g) O 2(g) + H 2S(g)的K θ为( θ1K /θ2K )。
8.反应:2Cl 2 (g) + 2H 2O (g)4HCl (g) + O 2 (g) Δr H m θ>0 ,达到平衡后进行下述变化,对指明的项目有何影响?① 加入一定量的O 2,会使n (H 2O ,g) 增大 ,n (HCl) 减小 ; ② 增大反应器体积,n (H 2O ,g) 减小 ;③ 减小反应器体积,n (Cl 2) 增大 ;④ 升高温度,K θ 增大 ,n (HCl) 增大 ;⑤ 加入催化剂,n (HCl) 减小 。
二、选择题1.对于一个给定条件下的反应,随着反应的进行 ( C )。
A .速率常数k 变小B .平衡常数K 变大C .正反应速率降低D .逆反应速率降低2.对反应 2X + 3Y → 2Z ,下列速率表达式正确的是 ( C )。
A . t c t c 2d )Y (d 3d )X (d =B . tc t c 3d )X (d 2d )Z (d = C . t c t c 3d )Y (d 2d )Z (d = D .t c t c 2d )X (d 3d )Y (d = 3.某一化学反应:2A + B → C 是一步完成的。
A 的起始浓度为 2 mol/L ,B 的起始浓度是4 mol/L ,1 s 后,A 的浓度下降到 1 mol/L ,该反应的反应速率为 ( A )。
A . 0.5 mol/(L ·s)B . -0.5 mol /(L ·s)C . -1 mol/(L ·s)D . 2 mol/(L ·s)4.某一可逆反应达平衡后,若反应速率常数k 发生变化时,则平衡常数K θ ( A ) 。
A . 一定发生变化B . 不变C . 不一定变化D .与k 无关5.N 2(g) + 3H 2 (g) → 2NH 3 (g) ,Δr H m θ = -92.4 kJ/mol,升高温度时,正反应速率 和逆反应速率 ' 的变化为 ( C )。
A . 增大, ' 减小B . 减小, ' 增大C . 增大, ' 增大D . 减小, ' 减小6.某反应物在一定条件下的平衡转化率为 35%,当加入催化剂时,若反应条件与前相同,此时它的平衡转化率是 ( B )。
A .大于35%B . 等于35%C . 小于35%D .无法知道7.反应 C(s) + O 2(g) → CO 2(g) 的Δr H mθ < 0,欲增加正反应速率,下列措施中无用的是( D )。
A . 增加氧的分压B .升温C . 使用催化剂D .减少CO 2 的分压 8. 500K 时,反应 SO 2 (g)+21O 2 (g) SO 3 (g) 的K θ = 50, 在同温下, 反应2SO 3 (g) 2SO 2 (g)+ O 2 (g) 的K θ等于 ( D )。
A .100B .2×10-2C .2500D .4×10-49.在一定条件下,一个反应达到平衡的标志是 ( B )。
A .各反应物和生成物的浓度相等B .各物质浓度不随时间改变而改变C .Δr G m θ = 0D .正逆反应速率常数相等10.已知在一定温度下SnO 2 (s) + 2CO(g)Sn(s) + 2CO 2 (g) 的K θ = 0.024 CO(g) + H 2O(g) CO 2 (g) + H 2(g) 的K θ= 0.034则在相同条件下,反应SnO 2 (s) + 2H 2(g) Sn(s) + 2H 2O(g) 的K θ为 ( B )。
A . 0.058B .21C . 8.2×10-4D . 0.7111.可使任何反应达到平衡时增加产率的措施是 ( C )。
A .升温B .加压C .增加反应物浓度D .加催化剂12.在恒压下进行合成氨反应 3H 2(g)+N 2 (g)2NH 3(g)时,若系统中积聚不参与反应的氩气量增加时,则氨的产率将 ( A )。
A .减小B .增加C .不变D .无法判断 13.可逆反应X + 2Y 2Z Δr H m θ>0,X ,Y ,Z 是三种气体,为了有利于Z 的生成,应采用的反应条件是( A )。
A .高温高压B .常温常压C .低温高压D .高温低压 14.反应NO(g) + CO(g) 21N 2(g) + CO 2(g) Δr H m θ = -427kJ/mol ,下列哪一个条件有利于使NO 和CO 取得较高转化率( B )。
A .高温、高压B .低温、高压C .低温、低压D .高温、低压15.下列反应的平衡常数可以用K θ=1/p ˊ(H 2)表示的是 ( C )。
A .H 2 (g)+S(g)H 2S(g) B .H 2 (g)+S(s) H 2S(g) C . H 2 (g)+S(s) H 2S(l) D .H 2 (l)+S(s) H 2S(s)三、是非题 (下列叙述中对的打“√”,错的打“×”)1. 催化剂只能缩短反应达到平衡的时间而不能改变平衡状态。
( √ )2. 凡速率方程式中各物质的浓度的指数等于反应方程式中其化学计量数时,此反应必为基元反应。
( √ )3. 一种反应物的转化率随另一种反应物的起始浓度不同而异。
(×)4. 分几步完成的化学反应的总平衡常数是各步平衡常数之和。
(×)5. 当一个化学反应处于平衡时,平衡混合物中各种物质的浓度都相等。
(×)6. 在一容器中,反应 2SO2 (g) + O2 (g) 2SO3 (g),达到平衡,加一定量N2气体保持总压力不变,平衡向正方向移动。
(×)7. N2(g) + 3H2(g) 2NH3(g),反应达到平衡后,把p(NH3),p(H2) 各提高到原来的 2 倍, p(N2)不变,则平衡向正反应方向移动。
(×)8. 反应CaCO3 (s) CaO(s) + CO2 (g),在一定条件下达到平衡后,若压缩容器体积,平衡向正反应方向移动。
(× )四、问答题1.采取哪些措施可以使下列平衡向正反应方向移动。
(1)C (s) + CO2 (g) 2CO (g) Δr H mθ>0答案:增加CO2的分压或减小CO的分压,升高温度,减小总压,增大固体C的接触面积答案关键词:压力,温度,接触面积。
(2)2CO (g) + O2 (g) 2CO2 (g) Δr H mθ<0答案:增加O2的分压,减小温度,增大总压。
(3)CO2 (g) + H2 (g) CO (g) + H2O (g) Δr H mθ>0答案:分别增加CO2或H2的分压或同时增加CO2、或减小CO和H2O的分压,升高温度答案关键词:压力,温度。
(4)3CH4 (g) + Fe2O3 (s) 2Fe (s) + 3CO (g) + 6H2 (g) Δr H mθ>0答案:减小总压,升高温度,增大固体Fe2O3的接触面积2.写出下列反应的标准平衡常数表达式(1) N2 (g) + O2 (g) 2NO (g);答案:(){}(){}(){}θθθPPPPPkONNO222=(2)C (s) + CO2 (g) 2CO (g);答案:(){}()θθθPPPPKCOCO22 =(3) CH 4 (g) + H 2O (g)CO (g) + 3H 2 (g); 答案:(){}(){}(){}(){}θθθθθP P P P P P P P K O H CH H CO 2423= (4)Fe 3O 4 (s) + 4H 2 (g)3Fe (s) + 4H 2O (g)。
答案:{}(){}θθθP P P P KH O H 224= 五、计算题1.已知反应A (g) + 2B (g) C (g)为基元反应。
某温度下,当c (A) = 0.5mol/L ,c(B) =0.6mol/L 时的反应速率为0.018mol/(L·min),求该温度下反应的速率常数。
解 由)(· )( 2B c A c k ⋅=υ 得 k = 0.018/0.5×0.62 = 0.1L 2/(mol 2·min)计算的最后结果数字:k = 0.1L 2/(mol 2·min) 2.实验测得反应:2SO 2(g) + O 2 2SO 3(g) 在1000K 温度下达到平衡时,各物质的平衡分压为:p (SO 2) = 27.7kPa ;p (O 2) = 40.7kPa ;p (SO 3) = 32.9kPa 。
计算该温度下的反应的标准平衡常数K θ。
解 {}{}{} )( )( )( 22223θO p SO p SO p K '⋅''=)100/7.40()100/7.27()100/9.32(22⨯= 3.47 计算的最后结果数字:47.3θ=K3.已知二氧化碳气体与氢气的反应为:CO 2 (g) + H 2 (g) CO (g) + H 2O (g)。
