四大晶体的比较
晶体的四种基本类型和特点

晶体的四种基本类型和特点晶体是由于原子、分子或离子排列有序而形成的固态物质。
根据晶体的结构特点,晶体可以分为四种基本类型:离子晶体、共价晶体、金属晶体和分子晶体。
1. 离子晶体离子晶体由正离子和负离子通过离子键结合而成。
正负离子之间的电荷吸引力使得离子晶体具有高熔点和脆性。
离子晶体的晶格结构稳定,形成高度有序的排列。
常见的离子晶体有氯化钠(NaCl)、氧化镁(MgO)等。
离子晶体在溶液中能够导电,但在固态下通常是绝缘体。
2. 共价晶体共价晶体由共价键连接的原子或分子组成。
共价键是由原子间的电子共享形成的,因此共价晶体具有很高的熔点和硬度。
共价晶体的晶格结构复杂多样,具有很高的化学稳定性。
典型的共价晶体包括金刚石(C)和硅(Si)。
共价晶体通常是绝缘体或半导体,由于共价键的稳定性,其导电性较弱。
3. 金属晶体金属晶体由金属原子通过金属键结合而成。
金属键是由金属原子间的电子云形成的,因此金属晶体具有良好的导电性和热传导性。
金属晶体的晶格结构常为紧密堆积或面心立方等紧密排列。
金属晶体的熔点通常较低,而且具有良好的延展性和韧性。
典型的金属晶体有铁(Fe)、铜(Cu)等。
4. 分子晶体分子晶体由分子通过弱相互作用力(如范德华力)结合而成。
分子晶体的晶格结构不规则,分子间的距离和角度较大。
由于分子间的相互作用力较弱,分子晶体通常具有较低的熔点和软硬度。
典型的分子晶体有水(H2O)、冰、石英(SiO2)等。
分子晶体在固态下通常是绝缘体,但某些分子晶体在溶液中能够导电。
总结起来,离子晶体由正负离子通过离子键结合,具有高熔点和脆性;共价晶体由共价键连接,具有高熔点和硬度;金属晶体由金属原子通过金属键结合,具有良好的导电性和热传导性;分子晶体由分子通过弱相互作用力结合,具有较低的熔点和软硬度。
这四种基本类型的晶体在结构、性质和应用上都有明显的差异。
研究晶体的类型和特点对于理解物质的性质和应用具有重要意义。
21、四种晶体比较表
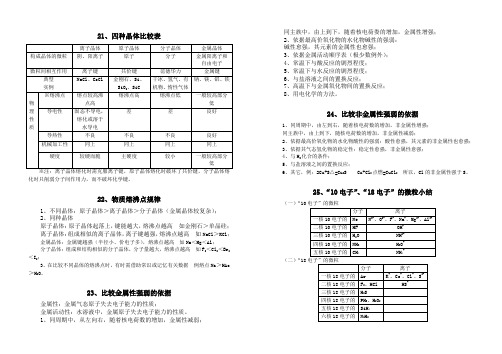
21、四种晶体比较表※注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只削弱分子间作用力,而不破坏化学键。
22、物质熔沸点规律1、不同晶体:原子晶体>离子晶体>分子晶体(金属晶体较复杂);2、同种晶体原子晶体:原子晶体起落上,键能越大,熔沸点越高如金刚石>单晶硅;离子晶体:组成相似的离子晶体,离子键越强,熔沸点越高如NaCl>KCl;金属晶体:金属键越强(半径小、价电子多),熔沸点越高如Na<Mg<Al;分子晶体:组成和结构相似的分子晶体,分子量越大,熔沸点越高如F2<Cl2<Br2<I2;3、在比较不同晶体的熔沸点时,有时需借助常识或记忆有关数据例熔点Na>HAc >H2O。
23、比较金属性强弱的依据金属性:金属气态原子失去电子能力的性质;金属活动性:水溶液中,金属原子失去电子能力的性质。
1、同周期中,从左向右,随着核电荷数的增加,金属性减弱;同主族中,由上到下,随着核电荷娄的增加,金属性增强;2、依据最高价氧化物的水化物碱性的强弱:碱性愈强,其元素的金属性也愈强;3、依据金属活动顺序表(极少数例外);4、常温下与酸反应的剧烈程度;5、常温下与水反应的剧烈程度;6、与盐溶液之间的置换反应;7、高温下与金属氧化物间的置换反应;8、用电化学的方法。
24、比较非金属性强弱的依据1、同周期中,由左到右,随着核电荷数的增加,非金属性增强;同主族中,由上到下,随核电荷数的增加,非金属性减弱;2、依据最高价氧化物的水化物酸性的强弱:酸性愈强,其元素的非金属性也愈强;3、依据其气态氢化物的稳定性:稳定性愈强,非金属性愈强;4、与H2化合的条件;5、与盐溶液之间的置换反应;6、其它,例:2Cu+S△=Cu2S Cu+Cl2点燃=CuCl2所以,Cl的非金属性强于S。
25、“10电子”、“18电子”的微粒小结(一)“10(二)“18。
高中化学四种晶体类型的比较

高中化学四种晶体类型的比较TYYGROUP system office room 【TYYUA16H-TYY-TYYYUA8Q8-四种晶体类型的比较物质熔沸点高低的比较方法物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下:1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。
例如:NaBr(固)>Br2>HBr(气)。
2、不同类型晶体的比较规律一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。
这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。
原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。
例如:金刚石>食盐>干冰3、同种类型晶体的比较规律A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,原子半径越小,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。
如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C<C—Si<?Si—Si,所以熔沸点高低为:金刚石>碳化硅>晶体硅。
B、离子晶体:熔、沸点的高低,取决于离子键的强弱。
一般来说,①离子所带电荷越多,②离子半径越小,离子键就越强,熔、沸点就越高,反之越低。
例如:MgO>CaO,NaF>NaCl>NaBr>NaI。
KF>KCl>KBr>KI,CaO>KCl。
C、金属晶体:金属晶体中①金属价电子数越多,②原子半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。
如:Na<Mg<Al,Li>Na>K。
合金的熔沸点一般说比它各组份纯金属的熔沸点低。
四种晶体比较表
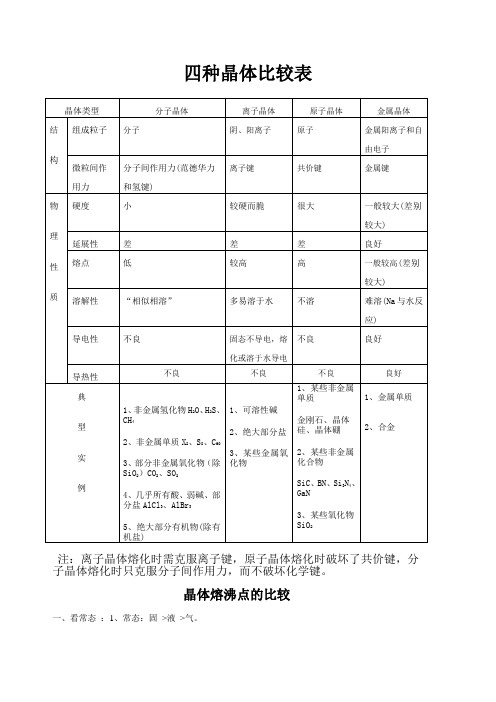
四种晶体比较表注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。
晶体熔沸点的比较一、看常态:1、常态:固>液>气。
2、一般情况下,原子晶体>离子晶体(金属晶体)>分子晶体。
3、原子晶体:共价键(取决于原子半径)。
4、离子晶体:离子键(取决于离子半径和离子电荷)5、金属晶体:金属键(取决于金属原子半径和价电子数)6、分子晶体:①结构相似,分子量越大,熔沸点越高。
②分子量相等,正>异>新。
③氢键反常二、看类型三、分类比较18.请完成下列各题:(1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。
(2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。
Ga原子的电子排布式为。
在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。
在四大晶体类型中,GaN属于晶体。
(3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是(填化学式)。
19.生物质能是一种洁净、可再生的能源。
生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。
写出基态Zn原子的核外电子排布式。
(2)根据等电子原理,写出CO分子结构式。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子中碳原子轨道的杂化类型为。
②甲醛分子的空间构型是;1mol甲醛分子中σ键的数目为。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为。
四种晶体类型的比较之欧阳地创编

四种晶体类型的比较物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下:1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。
例如:NaBr (固)>Br2>HBr(气)。
2、不同类型晶体的比较规律一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。
这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。
原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。
例如:金刚石>食盐>干冰3、同种类型晶体的比较规律A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。
如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C<C—Si< Si—Si,所以熔沸点高低为:金刚石>碳化硅>晶体硅。
B、离子晶体:熔、沸点的高低,取决于离子键的强弱。
一般来说,离子半径越小,离子所带电荷越多,离子键就越强,熔、沸点就越高,反之越低。
例如:MgO>CaO,NaF>NaCl>NaBr>NaI。
KF>KCl>KBr >KI,CaO>KCl。
C、金属晶体:金属晶体中金属阳离子所带电荷越多,半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。
如:Na<Mg<Al,Li>Na>K。
合金的熔沸点一般说比它各组份纯金属的熔沸点低。
如铝硅合金<纯铝(或纯硅)。
D、分子晶体:熔、沸点的高低,取决于分子间作用力的大小。
分子晶体分子间作用力越大物质的熔沸点越高,反之越低。
(具有氢键的分子晶体,熔沸点反常地高)如:H2O>H2Te>H2Se>H2S,C2H5OH>CH3—O—CH3。
四种晶体的熔沸点

四种晶体的熔沸点
晶体是一种具有有序排列的分子、原子或离子结构的固体。
它们具有一定的熔沸点,也就是在一定的温度下能够融化或沸腾。
以下是四种常见晶体的熔沸点。
1. 钠氯化物晶体:钠氯化物晶体是一种由钠离子和氯离子组成的离子化合物。
它的熔点约为801℃,沸点约为1413℃。
2. 碳晶体:碳晶体是由碳原子组成的晶体,包括金刚石和石墨。
金刚石的熔点非常高,约为3927℃,而石墨的熔点相对较低,约为3730℃。
3. 冰晶体:冰晶体是由水分子组成的晶体。
它的熔点在标准大气压下约为0℃,沸点约为100℃。
4. 硫晶体:硫晶体是由硫原子组成的晶体。
它的熔点约为115℃,沸点约为444℃。
这些晶体的熔沸点与它们的化学结构、分子大小、相互作用力等有关。
熔沸点的知识在材料科学、化学工程等领域中有着广泛的应用。
- 1 -。
四种晶体比较
四种晶体比较表注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。
晶体熔沸点的比较一、看常态:1、常态:固>液>气。
2、一般情况下,原子晶体>离子晶体(金属晶体)>分子晶体。
)取决于原子半径( 、原子晶体:共价键3.) 取决于离子半径和离子电荷(4、离子晶体:离子键) 取决于金属原子半径和价电子数(5、金属晶体:金属键熔沸点越高。
6、分子晶体:①结构相似,分子量越大,>异>新。
②分子量相等,正③氢键反常二、看类型三、分类比较18.请完成下列各题:(1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。
(2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。
Ga原子的电子排布式为。
在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。
在四大晶体类型中,GaN属于晶体。
(3)在极性分子NCl中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl水解的主要产物是33(填化学式)。
19.生物质能是一种洁净、可再生的能源。
生物质气(主要成分为CO、CO、H等)与H混合,催化合成222甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。
写出基态Zn原子的核外电子排布式。
(2)根据等电子原理,写出CO分子结构式。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)的碱性溶液反应生成CuO沉淀。
22子原;甲醛分子中碳①甲醇的沸点比甲醛的高,其主要原因是。
轨道的杂化类型为键的数目1mol ;甲醛分子中σ②甲醛分子的空间构型是。
为。
Cu在③1个原子数目为Cu晶胞中(结构如图所示),所包含的O2。
高考化学晶体结构:晶体类型与性质比较
高考化学晶体结构:晶体类型与性质比较在高考化学中,晶体结构是一个重要的知识点,其中晶体类型与性质的比较更是常考的内容。
理解和掌握不同晶体类型的特点及其性质差异,对于我们解决相关问题、提高化学成绩具有关键作用。
晶体,是由原子、离子或分子在空间按一定规律周期性地重复排列构成的固体物质。
根据构成晶体的粒子种类以及粒子间相互作用力的不同,晶体可以分为离子晶体、分子晶体、原子晶体和金属晶体这四大类型。
首先来看看离子晶体。
离子晶体是由阴、阳离子通过离子键结合而成的晶体。
常见的离子晶体有氯化钠、氯化铯等。
离子晶体具有较高的熔点和沸点,因为离子键是一种较强的化学键,要破坏离子键需要消耗大量的能量。
例如氯化钠,在通常情况下是固体,需要加热到 801℃才会熔化。
而且离子晶体在熔融状态或水溶液中能够导电,这是因为离子可以自由移动。
但在固态时,由于离子被束缚在晶格中,不能自由移动,所以不能导电。
接下来是分子晶体。
分子晶体是由分子通过分子间作用力(范德华力或氢键)结合而成的晶体。
像干冰(固态二氧化碳)、冰等都是典型的分子晶体。
分子晶体的熔点和沸点通常较低,因为分子间作用力相对较弱。
例如干冰,在常温常压下就会直接升华变成气体。
分子晶体一般不导电,除非其溶于水后形成了能够自由移动的离子。
再说说原子晶体。
原子晶体是由原子通过共价键结合而成的空间网状结构的晶体。
金刚石、晶体硅、二氧化硅等是常见的原子晶体。
原子晶体具有很高的熔点和沸点,硬度大。
这是因为共价键的强度很大,要破坏共价键需要很高的能量。
比如金刚石,是自然界中最硬的物质之一,其熔点高达 3550℃。
最后是金属晶体。
金属晶体是由金属阳离子和自由电子通过金属键结合而成的晶体。
大多数金属单质都属于金属晶体,如铁、铜、铝等。
金属晶体具有良好的导电性、导热性和延展性。
这是因为自由电子能够在金属阳离子之间自由移动。
金属晶体的熔点和沸点差异较大,这取决于金属键的强弱。
在性质方面,除了熔点、沸点和导电性有所不同外,晶体的硬度和溶解性也各有特点。
高中化学四种晶体熔沸点比较
高中化学四种晶体熔沸点比较在化学的世界里,晶体的熔点和沸点可真是个有趣的话题,嘿,咱们今天就来聊聊高中化学里那四种晶体的熔沸点比较,听起来是不是很有意思?想象一下,咱们的晶体就像各个性格各异的朋友,有的热情似火,有的冷漠孤傲,有的则温和如水。
好啦,先从离子晶体说起吧。
这种晶体的熔点通常很高,就像不轻易被感动的老顽固,离子之间的静电吸引力可不是盖的。
想象一下,钠和氯一见面就火花四溅,合成了美味的盐,熔点高得让人咋舌,一般得超过800度呢,这可不是一般的朋友关系,真是让人佩服。
咱们再来看看分子晶体,哎呀,这一类就有趣了。
分子晶体像是朋友圈里那种温柔善良的姑娘,平时可爱得不得了,熔点嘛,通常就低得多,像冰淇淋在阳光下融化,唰唰的变得越来越软。
比如说冰,想想看,零下几度就能化成水,真是个容易感动的家伙。
不过,别看她熔点低,分子间的弱相互作用也有她的独特魅力,让人忍不住想要多了解她。
然后,咱们说说金属晶体,这个可真是大块头,铸铁般的坚硬,熔点可高得很,真是威风凛凛。
金属晶体就像个在沙滩上晃荡的大汉,越热越兴奋,熔点动辄就几百度,铁、铜都在其中,热情得让人无可奈何。
金属原子们团结得紧紧的,像兄弟一样,彼此之间的金属键牢不可破,真是让人羡慕的友情。
别忘了网络的主角,晶体管的化学朋友们,网络中的共价晶体。
它们就像一群极为聪明的书呆子,熔点超高,像钻石一样耀眼,硬得让人无从下手。
碳的同素异形体,嘿,真是牛得不要不要的,熔点高得惊人,达到几千度,简直像天上掉下来的明星,闪闪发光。
共价晶体的强大,让人想要一探究竟,真是难得一见的奇珍异宝。
所以说,四种晶体熔沸点的比较就像是一次聚会,大家各显风采,有的高冷、有的温柔、有的热情,还有的闪耀。
每种晶体都有自己的特色,就像每个人都有自己的个性。
这不禁让人思考,化学其实就是这样一个奇妙的世界,各种元素和分子在这里交织碰撞,构成了我们眼前的一切,真是美妙啊!相信只要咱们深入探索,就能发现更多的奥秘和乐趣,化学的魅力无穷无尽,真是让人乐此不疲。
四大晶体
【跟踪练习】 1.下列各项所述的数字不是6的是 C +最近的且距离相等 A.在NaCl晶体中,与一个Na 的Cl-的个数 B.在金刚石晶体中,最小的环上的碳原子个数 C.在二氧化硅晶体中,最小的环上的原子个数 D.在NaCl晶体中,与一个Cl-最近的且距离相等 的Na+的个数 2.某物质由A、B、C三种元素组成,其晶体中微粒 的排列方式如图所示:该晶体的化学式是 B A AB3C3 B AB3C C A2B3C D A2B2C
强碱、大多数盐、 金刚石、Si、 金属氧化物、金属 B单质、SiO 、 金属单质、 2 合金 氢化物、过氧化钠、 SiC、BN、 铵盐等
部分非金属单质、 部分非金属氧化 物、非金属氢化 物、 几乎所有的 酸、 绝大多数有 机物
【跟踪练习】 1.下列式子中,真实表示分子组成的是 A A H2SO4 B NH4Cl C SiO2 D Na 2.在下列有关晶体的叙述中错误的是 C A 离子晶体中,一定存在离子键 B 原子晶体中,只存在共价键 C 原子晶体的熔点一定比金属晶体的高 D 晶体中有阴离子就一定有阳离子
1. 不同晶体类型的物质: 原子晶体>离子晶体>(金属晶体)>分子晶体 2. 同种晶体类型的物质: 晶体内微粒间作用力越大,熔沸点越高 ⑴离子晶体 离子所带电荷越 多 、离子半越 小 , 晶格能越大,离子键越强,晶体熔沸点 越 高 、硬度越 大 。 ⑵原子晶体 原子半径越 小 、键长越 短 、键能越大, 高 共价键越强,晶体熔沸点越 、硬度 越 大 。 金属原子半径越 小 、单位体积内自由电 ⑶金属晶体 子数目越 多 ,金属键越强,晶体熔沸点 越 高 、硬度越 大 。
5、过渡型晶体 范德华力 在石墨晶体中,层与层之间是以 结合,同一 层内C原子与C原子以 共价键 结合成平面网状结构, 故石墨为混合型晶体或过渡型晶体。 在同一层中,每个C原子与 3 个C原子形成C-C 键,键角为120° ,其中最小的环为六 元环,每个C 原子被 3 个六元环共有,每个C-C键被 2 个六元环 共有;每个六元环拥有的C原子数为_,拥有的C-C 2 键数为__,则C原子数 3 2:3 与C-C键数之比为_____。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
知识2、原子晶体结构 1、金刚石结构
109º28´
共价键
金刚石的晶胞结构
2、晶体硅的结构
3、二氧化硅的结构
Si O
180º 109º28´
共价键
4、碳化硅的结构
微粒是原子
课时小结 原子晶体
总结感悟 原子间以共价键结合
一般,原子半径越小,共价键键长越短,键能越大, 物质的熔沸点越高,硬度越大。
①铯离子和氯离子的位置: Cs+:体心 Cl-:顶点;或反之。 ②每个晶胞含Cs+、Cl-个数: 1 ③与Cs+等距离且最近的Cs+、ClCs+:6个;Cl-:8个(配位数)
(3)CaF2型晶胞
①一个CaF2晶胞中 4个Ca2+和8个F¯
②Ca2+的配位数: 8 F-的配位数: 4
(4)ZnS型晶胞
如熔点:金刚石>碳化硅>晶体硅。
二、分子晶体 1、概念: 只含分子的晶体
2、组成微粒: 分子
内:共价键结合; 3、粒子间作用力:
间:分子间作用力或氢键
4、物理特性:
。
(1)较低的熔点和沸点,易升华; 分子间作用力较弱
注: ①分子间作用力越大,熔沸点越高(相对分子质量,分子极性,氢键 ) ②(2)熔较化小时的一硬般度只破坏分分子子间间作作用用力力较,弱不破坏化学键。
, (2) 非密堆积如:C60、干冰 、I2、O2。
有分子间氢键——氢键具有方向性,使晶体中的空间利率不高,留 有相当大的空隙。这种晶体不具有分子密堆积特征。 如:HF 、NH3、冰(每个水分子周围只有4个紧邻的水分子)
课时小结
只有范德华力,无分子间氢键-分子密堆积 有分子间氢键-不具有分子密堆积特征如冰等 。
(3)一般是绝缘体,熔融态也不导电。(有些在水溶液中可以导电)
知识2、分子的堆积 1、干冰的晶体结构
(与CO2分子距离最近的CO2分子共有12个 )
碘晶体结构
氧(O2)的晶体结构
碳60的晶胞
2、冰的晶体结构
氢键具有方向性
冰中1个水分子周围有4个水分子
冰的结构
3、分子晶体结构特征: (1) 密堆积 只范德华力,无氢键。晶体每分子周围一般12个紧邻分子
四、金属晶体
1、金属晶体 金属离子与自由电子间较强的相互作用形成的晶体 (1)晶体中不存在单个分子 (2)金属阳离子被自由电子所包围
2、金属键的特征 由于自由电子为整个金属所共有,所以金 属键没有方向性和饱和性
3、金属共同的物理性质 容易导电、导热、有延展性、有金属光泽等。
金属晶体熔沸点的比较
①1个ZnS晶胞 4个阳离子 4个阴离子
②阳离子配位数: 4 阴离子配位数: 4
6、离子晶体的特点: ⑴无单个分子;无分子式。 ⑵熔沸点较高,硬度较大,难挥发难压缩。 ⑶一般易溶于水,难溶有机溶剂。 ⑷固态不导电,水溶液或熔融状态下导电。
7、离子晶体熔沸点的比较 离子带电荷越多,半径越小,晶格能越大,晶体的熔点越高 。
均位于顶角,并交错排列
①Na+和Cl-的位置: 钠离子:体心 棱中点
氯离子:面心 顶点,或反之。
②每个晶胞含钠离子、氯离子的个数:
Na+:
Cl-:
③与Na+等距离且最近的Na+ 有: 12个
与Na+等距离且最近的Cl¯ 有:6个 ④ NaCl的晶体结构配位数
---Cl--- Na+
CsCl晶体 ---Cs+ ---Cl-
五、石墨是层状结构的混合型晶体
知识拓展
同层内碳原子共价键结合, 层层间范德华力 石墨的熔点很高,化学性质稳定
谢谢!
四大晶体的比较
一、原子晶体 1、定义: 原子间以共价键相结合而形成的空间网状结构的晶体
2、构成微粒: 原子
3、微粒之间的作用: 共价键
4、气化或熔化时破坏的作用力: 共价键
5、物理性质: 熔沸点很高,硬度很大,难溶于一般溶剂。 (共价键键能越大,熔沸点越高,硬度越大)
6、常见原子晶体 ⑴非金属单质:硼(B)、硅(Si)、锗(Ge)、金刚石等 ⑵某些非金属化合物:SiC、BN等 ⑶某些氧化物:SiO2、Al2O3等
由分子构成
结 构 特 征
分子晶体
分子间用力
特 点
低熔点、升华、硬度很小等
分子晶 体熔沸 点的比 较
三、离子晶体 1、定义: 由阳离子和阴离子通过离子键结合而成的晶体。 2、成键粒子: 阴、阳离子 3、相互作用力: 离子键
4、常见的离子晶体: 强碱、活泼金属氧化物、大部分的盐类。
5、晶胞类型:
(1)氯化钠型晶胞
