电石中硫化氢,磷化氢检测的优化[1]
电石生产工艺论文

电石的生成方法有氧热法和电热发。
一般多采用电热发,电石的原料是生石灰和碳素元素(焦炭、无烟煤和石油等),在电石炉内依靠电弧高温熔化反应而生成电石,主要生产过程是:原料加工,配料,由电炉端的入口或管道将混合料加入电炉内。
在密闭电炉中加热至2300摄氏度,一次下列反应生成电石:CaO+3C →CaC2+CO,熔化了碳化钙。
从炉底取出后,经冷却,破碎后作为成品包装。
反应中生成的一氧化碳则依电石炉的类型以不同方式排出:在开放炉中,一氧化碳在料面上燃烧,产生的火焰随同粉尘—起向外四散;在半密闭炉中,一氧化碳的一部分被安置于炉上的吸气罩抽出,剩余的部分仍在料面燃烧;在密闭炉中,全部一氧化碳被抽出。
关键词:电石石灰焦炭电极1.绪论 (1)1. 1 电石的性质 (1)1.2. 电石的用途 (2)2. 电石生产主要设备 (2)2.1 电石炉的类型 (2)2.2 埃肯电石炉 (3)2.2.1埃肯电石炉简介 (3)2.2.2 电炉炉体 (4)2.2.3组合式把持器 (4)2.2.4电极压放程序 (7)2.2.5电路低压供电设备 (7)2.2.6炉盖 (8)2.2.7加料系统 (8)2.2.8水冷却系统 (9)2.2.9液压装置 (9)2.2.10电炉自控系统 (9)2.2.11碳材干燥 (10)3. 电石生产的原料 (11)3.1 焦炭 (11)3.2 石灰 (11)3.3 电极糊和电极 (12)3.3.1电极的特性 (12)3.3.2 电极糊 (12)3.3.3 制造电极糊的原料 (12)3.4 电极的烧结 (13)4.4.1电极糊烧结过程 (13)4. 电石生产工艺中工序流程 (13)4.1 碳材干燥 (13)4.2 配料站工艺流程图 (14)4.2.1配料站物料流程图(见下页) (14)4.2.2流程说明 (15)4.3 电石及破碎物料流程 (16)4.4 电石生产 (17)总结 (21)致谢 (22)参考文献 (23)1.绪论1. 1 电石的性质电石是指工业碳化钙(CaC2),由碳素元素(焦炭,无烟煤,石油等)与生石灰在电石炉内加热到1900~2200℃时,使碳与钙发生化学反应生成的产物。
乙炔发生生产过程危险分析
乙炔发生生产过程危险分析危险是指可能造成人员伤害、职业病、财产损失、作业环境破坏的根源或状态。
危险因素是指能使人造成伤亡,对物造成突发性损坏,或影响人的身体健康导致疾病,对物造成慢性损坏的因素。
通常为了区别客体对人体不利作用的特点和效果,分为危险因素(强调突发性和瞬间作用)和危害因素(强调在一定时间范围内积累作用)。
所有危险、有害因素尽管表现形式不同,但从本质上讲,之所以能造成危险、危害后果(伤亡事故、损害人身健康和物的损坏等)归结为存在能量、有害物质和能量、有害物质失去控制两方面因素的综合作用,并导致能量的意外释放或有害物质泄漏、散发的结果。
故存在能量、有害物质和失控是危险、有害因素产生的根本原因,都是危险、有害因素。
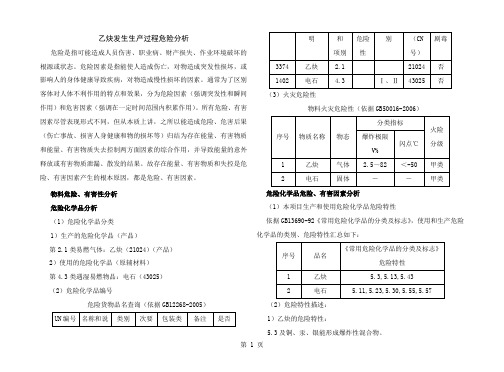
物料危险、有害性分析危险化学品分析(1)危险化学品分类1)生产的危险化学品(产品)第2.1类易燃气体:乙炔(21024)(产品)2)使用的危险化学品(原辅材料)第4.3类遇湿易燃物品:电石(43025)(2)危险化学品编号危险货物品名查询(依据GB12268-2005)(3)火灾危险性物料火灾危险性(依据GB50016-2006)危险化学品危险、有害因素分析(1)本项目生产和使用危险化学品危险特性依据GB13690-92《常用危险化学品的分类及标志》,使用和生产危险化学品的类别、危险特性汇总如下:(2)危险特性描述:1)乙炔的危险特性:5.3及铜、汞、银能形成爆炸性混合物。
5.13遇明火、高热会引起燃烧爆炸。
5.43 遇卤素会引起燃烧爆炸。
2)电石的危险特性5.11 遇明火极易燃烧爆炸。
5.23 遇水或潮湿空气会引起燃烧爆炸。
5.30 遇酸发生剧烈反应。
5.55 遇硫、磷会引起爆炸。
5.57 撞击、摩擦、振动有燃烧爆炸危险乙炔、电石的主要危险分析1、乙炔乙炔分子量26,熔点-80.5℃,沸点-84℃,气体密度1.1767 g/L(标准状态),是一种易燃易爆有毒的气体,毒性程度Ⅲ级(中度危害),浓度约在10%时就有轻微中毒感,随着浓度增大毒性亦增大。
【课堂新坐标】(教师用书)2021学年高中化学 课后知能检测8 新人教版选修3(1)

【课堂新坐标】(教师用书)2021-2021学年高中化学课后知能检测8 新人教版选修31.由两种元素X、Y,它们可组成以下分子,其中确信是极性分子的是( )A.XY B.XY2C.XY3D.XY4【答案】A2.以下化合物中,化学键的类型和分子的极性(或非极性)皆相同的是( )A.CO2和SO2B.CH4和SiO2C.BF3和NH3D.HCl和HI【解析】A中CO2为极性键组成的非极性分子,为直线形结构,SO2为V形结构,是极性分子;B中CH4为极性键组成的非极性分子,是正四面体结构,SiO2不是分子;C中BF3为极性键组成的非极性分子,是平面三角形结构,NH3为极性键组成的极性分子,是三角锥形结构;D中HCl和HI都是极性键组成的直线形结构,故都是极性分子。
【答案】D3.以下关于范德华力的表达正确的选项是( )A.是一种较弱的化学键B.分子间存在的较强的电性作用C.直接阻碍物质的熔、沸点D.稀有气体的原子间存在范德华力【答案】D4.(2021·锦阳高二检测)以下物质中不存在氢键的是( )A.冰醋酸中醋酸分子之间B.液态氟化氢中氟化氢分子之间C.氨水中氨分子与水分子之间D.可燃冰(CH4·8H2O)中甲烷分子与水分子之间【解析】甲烷中的碳原子电负性较小,不能与水分子形成氢键。
【答案】D5.以下物质的分子中含有极性键的非极性分子是( )A.H2O2B.CS2C.CCl4D.C2H5OH【解析】A、D中有H—O键、C—H键、C—O键是极性键,且H2O2、C2H5OH是极性分子;CS2、CCl4是非极性分子,但其中的C===S键、C—Cl键是极性键。
【答案】BC6.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。
以下关于PH3的表达不正确的选项是( )A.PH3分子中有未成键的孤电子对B.PH3是极性分子C.它的分子构型是平面三角形D.磷原子采纳sp3杂化方式【解析】PH3分子中含有3个σ键和一个孤电子对,故杂化轨道的数量为4,采取sp3杂化方式,分子构型为三角锥形,与NH3相似。
电石生产工艺技术的改进与优化

电石生产工艺技术的改进与优化摘要:在电石行业的发展过程中,需要涉及电石生产技术。
根据该技术的应用现状,提出有针对性的改进措施,确保技术运行效果的全面优化。
为实现电石行业的长远发展目标,在改进电石生产工艺时遵循节能减排的基本目标,综合利用其附加产品,满足电石生产的特定需求。
关键词:电石行业;生产技术;技术改进;优化对策引言电石炉运行过程中,为使其始终处于最佳状态,应全面改进电石生产工艺,以保证电石生产工艺应用的合理性和科学性,满足清洁新技术的应用要求,减轻对环境和资源的压力,促进电石行业经济效益和生态效益的同步提高。
我国电石行业发展相对落后,技术水平落后,经营管理粗放,经营管理水平低。
但随着中国经济的快速发展和行业内部结构的调整,20世纪80年代初,挪威王国埃肯工业公司引进了具有国际先进技术水平的大型全封闭电石炉技术。
目前,国内外电炉生产厂家大多使用KVA 25500埃肯肯密封电石炉。
埃肯电石炉是美国目前和现在最先进的电石炉生产技术,如:全密封电石炉、组合手柄高压电极控制系统、炉气干表面除尘组、计算机控制系统、环形物料输送控制系统等。
中国经济的快速发展,特别是世界油价的持续上涨,促进了电石法聚氯乙烯生产规模的扩大,对电石技术的需求日益增加。
我国电石炉的产量和生产技术也在不断提高,我国电石厂的技术也在不断创新和优化。
1电石生产工艺改进前的介绍传统的电石生产方法主要是用石灰窑直接煅烧石灰石为硅灰,然后用盘式上下辊机械输送到对辊破碎机完成破碎处理。
破碎后,用滚筒筛即可得到合格的硅灰颗粒,最后将硅灰颗粒垂直抛入硅灰仓[1]。
但煤焦油必须先在双辊破碎机中进行破碎,待破碎后,再用滚筒进行筛分,以获得符合产品要求的煤焦油粒度。
随后,为了保证生产出来的焦炭和干法洗精煤的分级,硅灰会通过储料罐直接释放出来,然后通过自动称重直接加工成炉料,再由转运设备输送到料斗,再由给料机定量投入电石炉。
至于35000V高压输电线路,经过电石炉变压器降低到低压后,继续穿过铜排,引入热电极之间。
电石渣在综合利用过程中对环境的影响

电石渣在综合利用过程中对环境的影响摘要:随着国家建材、化工领域的发展和技术的突破,电石渣在各行各业都得到了广泛的应用。
如今通过利用电石渣生成水泥、回收氧化钙等方式成为电石渣综合利用的主要方式,在综合利用电石渣的过程中,电石渣的处理、运输、储存、煅烧等过程对周围环境会造成污染或腐蚀。
因此电石渣在综合利用生产过程中对环境影响的研究就非常有必要,现在以电石渣为原料在水泥生产过程中对环境的影响进行分析研究。
关键词:电石渣;综合利用;环境;影响前言:电石渣是化工厂利用电石水解生产乙炔气后排出的以氢氧化钙为主要成分的工业废渣。
乙炔气是十分重要的化工原料,特别是PVC行业,每年消耗乙炔的量高达600~650万t。
工业上制取乙炔气体的方法主要有电石水解法、甲烷部分氧化裂解和烃裂解法。
我国煤炭资源、石灰石资源十分丰富,石油及天然气资源相对短缺,由于采用电石水解法制取乙炔的成本较低,同时,采用电石水解生产乙炔的装置简单,产生的乙炔气体纯度高,因此,国内PVC生产厂家采用的原料乙炔气中约有70%是利用电石水解法生产的。
电石渣的主要成分是Ca(OH)2,其化学成分CaO含量高达70%,还含有CaCO3、SiO2、硫化物、镁和铁等金属的氧化物、氢氧化物等无机物以及少量有机物。
从乙炔发生器中排出的电石渣浆水分高达90%以上,经沉降池浓缩后,水分仍有75%~80%,现场刚生产出的湿电石渣气味较大,含有硫化氢、磷化氢等有害气体,对在现场工作的人体健康不利,且不易改善。
1.电石渣应用研究进展随着工业发展与技术进步,电石渣的应用范围越来越广,归纳起来主要在3个领域,即建材、环保和化工。
1.1建材方面建材行业主要用于生产水泥、制砖和做路基材料。
用电石渣大比例替代石灰石原料生产水泥,能有效降低水泥生产成本,具有良好的经济效益。
具体生产工艺有机立窑工艺、湿法回转窑工艺、湿磨干烧工艺,新型干磨干烧工艺。
用电石渣、煤渣等为主要原料生产标准建筑砖,减少因粘土砖而毁坏良田的情况。
电石法乙炔生产中电石单耗的影响因素分析

电石法乙炔生产中电石单耗的影响因素分析摘要:电石法乙炔生产中电石单耗的高低水平取决于多种因素,影响因素主要包括电石质量、电炉操作状态、工艺参数、设备状态和环境治理等,这些因素综合作用影响着乙炔的产量和质量以及企业的可持续发展。
因此,生产企业需要采取相应的措施,优化生产过程,提高乙炔产量和质量,以及合理处理废料和排放物,以实现企业的可持续发展。
关键词:电石法;乙炔;电石单耗电石法乙炔生产中电石单耗的高低水平影响着整个生产过程的效率和质量。
常见的影响因素包括电石质量、电炉操作状态、工艺参数、设备状态和环境治理等。
生产企业需要针对不同的因素采取相应的措施,以优化生产过程,提高乙炔的产量和质量,同时实现企业的可持续发展。
一、电石法乙炔生产与电石单耗概述1.1电石法乙炔生产概述电石法乙炔生产是乙炔生产的一种传统方法,它是以钙石灰和焦炭为原料,利用电石炉产生高温反应,使钙石灰还原为氧化钙和二氧化碳,再利用焦炭与氧化钙反应生成电石,接着再将电石与水进行反应得到乙炔和氢氧化钙。
这种方法具有生产成本低、生产效率高等优点,已经成为了乙炔生产的重要方式之一。
1.2电石单耗概述电石单耗是指在电石法乙炔生产过程中,生产1吨乙炔所需的电石的重量。
它是评价电石法乙炔生产节能性和经济性的主要指标之一。
电石单耗的降低,不仅可以减少电石的消耗,降低生产成本,从而提高企业的收益,而且可以减少生产过程中的碳排放量,从而符合节能减排和环保的要求。
1.3国内外研究现状及存在的问题在国内外,关于电石法乙炔生产中的电石单耗的研究已经有了一定的成果。
国内外的研究表明,电石单耗受到原材料质量和配比、电石炉型和运行条件、煤气净化和利用方式等因素的影响。
然而,目前仍存在一些问题。
一方面,虽然已经有很多研究者尝试从不同的角度来降低电石单耗,但是从实践效果来看,降低幅度仍然有限。
另一方面,虽然电石法乙炔生产已经发展了几十年,但是在很多生产中,仍然存在着电石单耗过高、生产效率低下的问题,尤其是一些小型的企业。
硫化氢检测原理
硫化氢检测原理
硫化氢是一种无色、有毒、易燃的气体,常见于化工、石油、污水处理等行业。
因此,对硫化氢的检测显得尤为重要。
硫化氢检测的原理主要有以下几种:
1. 化学反应法:硫化氢与特定试剂发生化学反应,产生颜色变化或其他可观测的物理变化,从而检测硫化氢的存在。
例如,硫化氢可以与银离子反应生成黑色的硫化银沉淀,或者与碘液反应生成紫色的碘化氢。
2. 电化学法:利用硫化氢的氧化还原反应,通过电极的电势变化来检测硫化氢的存在。
例如,将硫化氢气体通入电解质溶液中,通过电极的电势变化来检测硫化氢的浓度。
3. 光学法:利用硫化氢对特定波长的光的吸收或散射来检测硫化氢的存在。
例如,利用紫外线或红外线光谱仪来检测硫化氢的吸收光谱。
4. 气敏法:利用硫化氢对特定材料的气敏性来检测硫化氢的存在。
例如,将硫化氢气体与氧化锌等敏感材料接触,通过材料电阻的变化来检测硫化氢的浓度。
总的来说,硫化氢检测的原理多种多样,不同的检测方法适用于不同的场合和要求。
在实际应用中,需要根据具体情况选择合适的检测方法,并严格按照操作规程进行操作,以确保检测结果的准确性和可靠性。
乙炔的制备和性质实验改进
54㊀中小学实验与装备2019年第1期第29卷实验改进乙炔的制备和性质实验改进江西师范大学化学化工学院(330022)㊀王霞琳㊀刘晓玲1㊀实验药品和仪器电石0.5g㊁饱和硫酸铜溶液5m L㊁0.1m o l/L 高锰酸钾溶液㊁溴的四氯化碳溶液㊁滤纸㊁酒精灯㊁50m L锥形瓶㊁单孔橡胶塞㊁直角尖嘴导气管㊁透明胶带(小号)㊁注射器(5m L)㊁镊子.2㊀实验装置图实验装置图如图1所示.图1㊀实验装置图3㊀实验步骤(1)按照图1连接实验装置并检查装置气密性.(2)向干燥的锥形瓶中加入0.5g的电石,在注射器中吸入5m L饱和硫酸铜溶液.将2片撕成小片的滤纸条用透明胶带分别固定直角尖嘴导气管的平口端附近位置,然后向2片滤纸条上分别滴加0.1m o l/L的高锰酸钾溶液和溴的四氯化碳溶液.(3)将注射器中的饱和硫酸铜溶液慢慢注入锥形瓶中,饱和硫酸铜中的水与电石缓慢反应,同时观察滤纸条上高锰酸钾溶液和溴的四氯化碳溶液的颜色变化情况,用酒精灯点燃直角尖嘴导气管口产生的气体,观察现象.4㊀实验现象及解释(1)锥形瓶中陆续有气泡产生且试管壁发烫.水与电石发生反应产生气体,放出热量.(2)蘸有溴的四氯化碳溶液的滤纸条褪色,乙炔与溴水发生反应.(3)蘸有0.1m o l/L高锰酸钾溶液的滤纸条褪色,乙炔与高锰酸钾发生氧化反应,使得高锰酸钾溶液褪色.(4)直角尖嘴导气管口产生的气体点燃后,火焰明亮并伴有浓烈的黑烟,乙炔与氧气在点燃条件下发生反应.(5)生成黑色沉淀.电石中含硫化物和磷化物,反应产生硫化氢和磷化氢等还原性杂质气体,硫酸铜与杂质反应生成C u S㊁C u3P㊁C u等沉淀.5㊀安全事项说明笔者多次用不同质量的电石做实验时发现,在实验过程中装入50m L锥形瓶中的电石质量应保持在0.5g左右.电石的质量过低(<0.35g),通过导气管气体的体积偏小,会造成气体无法被点燃;电石的质量过大(>0.58g),反应速率过快,锥形瓶中会充满白色的浓烟和气泡,干扰实验现象的观察,点燃产生的气体时伴随很大的浓烟,造成空气污染.6㊀改进后的优点(1)实验经过微型改进后,减少了不必要的药品浪费,简化了实验步骤,节约了反应时间,实验效果也较明显,符合绿色环保的理念,操作简单安全,适用于学生实验.(2)用饱和硫酸铜溶液代替饱和氯化钠溶液的优点如下:①硫酸铜不与电石反应,通过利用饱和硫酸铜溶液反应,可以很好的降低水与电石反应的速率,使反应趋于平稳;②硫酸铜不与乙炔发生反应,但是可以和电石反应中产生的硫化氢㊁砷化氢㊁磷化氢等发生反应,从而达到除杂的效果,硫酸铜的浓度越高,除杂能力越好.(3)利用注射器控制液体的流量,从而控制反应的开始与停止,通过调解推压的力度来控制乙炔气体的气流,使反应时间延长,从而保证乙炔的制备以及性质验证一体化实验的顺利完成.收稿日期:2019-01-19。
电石电耗偏高原因分析及优化解决方案研究
电石电耗偏高原因分析及优化解决方案研究摘要:电石炉借助高温熔化炉料,炉料经反应后生成电石,面对高达2000℃的高温,电石炉容积内应具有充足的反应空间,为迎合节能降耗时代主题,需针对电石炉电耗偏高问题展开应对处理。
基于此,本文从原料及操作两个方面展开电石电耗偏高原因分析,并有针对性地提出优化解决措施,旨在解决电石炉高电耗问题,促进电石生产行业可持续发展。
关键词:电石炉;电耗偏高;原因分析引言:《电石单位产品能源消耗限额(GB 21343-2015)》中指出,电石生产装置单位产品能耗先进值需≤3050kW·h/t,为确保电石生产活动满足限额规定,应对电耗偏高问题展开应对处理,而引发电石电耗偏高的因素较多,但主要分为两大类,即由原料、操作引起的电耗偏高问题,由于产生电耗偏高问题的原因不同,展开处理时,应根据具体原因展开专项处理。
一、电石电耗偏高原因分析(一)原料方面原因1.白灰生过烧白灰生烧量与碳酸钙含量成正比,当白灰生烧量增大时,需额外电耗对碳酸钙进行分解,以此可引发电耗偏高现象,此外,相较于正常白灰,生烧白灰偏重,可对炉料配比产生影响,过烧白灰偏轻,而过烧白灰结构致密、活性度较低,可影响电石炉内反应情况。
白灰生过烧≤8.5%时对电石电耗无影响,但在实际电石生产工作中,白灰生过烧控制情况仍有待提高。
2.杂质含量高石灰石内易存在氧化镁、氧化铝、氧化铁、氧化硅等杂质,杂质进入电石炉内将引起大量电耗,在高温条件下,杂质将与炉料内兰炭进行还原反应,生成单质镁、铝、铁、硅,在生产过程中,还原反应所生成的单质将损坏炉墙,在引起电石炉内料面板结问题,对电石生产造成阻碍。
3.白灰活性低白灰活性可影响电石炉内反应能力,白灰活性高则意味着炉料熔化速度快,缩短电石生成时间,使电石反应稳定连续进行,而低白灰活性则意味着,炉料进入电石炉后反应速度慢,电石炉内产生熔化不均衡现象,料层结构混乱,使电石炉内出现反复性操作,严重降低电石生产效率,并造成较高电耗。
电石在发生器中反应的影响因素分析与改进措施
费。 改变 后 的操作方 法是 , 要求 尽量 地将 小加 料斗 加 至料斗 的最 大容 积 ( 际可达 7 %一 0 , 而减 少 实 0 8 %)从 发 生器 的置换 空 间 。
2 电石在发生器中的反应
2 1 发 生器 的生产 工艺 .
乌海 化工公 司有 I、 Ⅱ期 2条 生产线 , 乙炔生产
22 几个 关键 环节 操作方 法 的改进 .
221 加 料 斗 的 置 换 . .
电石 的水 解是 液 固相 反应 ,电石与水 的接 触 面
积越 大 , 电石粒 度 越小 时 , 水解 速 度 越快 , 即 其 较低 温度 下 的水解 速度 如表 1 所示 。叫
表 】 不 同 粒 度 电 石 的水 解 时 间
平 衡作用 , 逆水 封在 正 常情况 下不起 作 用 。 电石 与水 反应 为放 热反 应 , 移走 反应 热 . 向 为 需
由于杂 质 的原 因 ,在 发生器 水相 中也 进行 一些 副反 应 , 成磷 化氢 、 化 氢等 , 生 硫 因此 , 发生 器排 出 的
发 生器 内连 续 加水 , 渣 浆经 溢 流 管进 人 渣 浆 高 位 稀 槽 。发 生 器 底 部 较 浓渣 浆 和矽 铁 渣定 期 由排 渣 阀 排 放 , 入 渣 浆 池 , 后 , 渣 浆 高 位 泵 打 到 渣 浆 进 然 用 高 位槽 , 渣浆 高位 槽下 来 的渣浆 用 渣浆 输 送泵 打至
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电石中硫化氢、磷化氢检测方法优化
技术背景:电石是生产乙炔的重要原料。
在生产乙炔的过程中,因电石中混有硫化钙(CaS)和磷化钙(Ca3P2),遇水分别反应生成H2S和PH3,反应式如下:
CaS+H2O——Ca(OH)2+H2S
Ca3P2+H2O——Ca(OH)2+ PH3
硫化氢和磷化氢均是有毒无色气体,其中硫化氢的活泼的化学性质不仅会对金属管道造成腐蚀,也会对工业反应中的金属催化剂产生影响,造成催化剂中毒。
在普通的湿法制乙炔中,硫化氢极易被水解的氢氧化钙吸附,所以检测的意义不大。
而精细化工采用的干法制乙炔,干法制乙炔是一种新型环保方法,但同时也会带来硫化氢和磷化氢的完全释放,对后续的处理要求严格,同时对管道和反应催化剂会有一定的影响。
为了降低乙炔发生气中的硫化氢、磷化氢,对原料电石的检测和把关十分重要。
原有的乙炔气体收集方法是在电石发生气装置中进行,其原理和湿法制乙炔一致,所以检测结果对精细化工的指导效果有很大的偏差。
为了更好的针对干法制乙炔工艺,特将乙炔收集方法改进为干法制乙炔,同时对原料电石进行把关,不合格的电石退回,降低乙炔发生气中硫化氢超标的风险。
该方法对原料电石的检测、降低硫化氢超标风险、提高装置管道及催化剂运行时间、提高生产效益有很大的意义。
改进方法:图一为原有的电石发生气装置,该装置操作复杂,收集
乙炔气体麻烦,气体排放量大,对分析工有一定的危害,且为湿法
制乙炔方法,对精细化工干法制乙炔工艺装置指导意义微乎其微。
改进后的装置,如图二。
极其简单,但实用性极大,操作方便,可
以有效控制乙炔发生气体的速率、体积,危害小,与干法制乙炔工
艺装置相似,对工艺生产有很强的指导意义。
操作方法:改进后的电石发生气装置如下:
操作步骤:
1.取30-50g破碎后的电石,放入锥形瓶内,用橡皮塞拧紧。
2.将气球套入乙炔收集口处。
3.通过长颈漏斗缓慢加入10%的硫酸水溶液,待气球充满后停
止加液。
置换一次即可。
加稀硫酸的目的是防止产生的硫化
氢被氢氧化钙吸附。
4.将收集的气体分别进乙炔气相色谱和硫磷气相色谱,测乙
炔的浓度C,硫化氢和磷化氢的浓度分别为C1和C2。
5.计算:
电石发生气中实际的硫化氢含量C H2S=C1/C,磷化氢含量为
C PH3=C2/C
数据验证:
通过数据验证:改进后的电石发生气装置可以有效的检测出电石发生气中的硫化氢的含量。
对硫化氢含量超过600ppm的原料电石,可以要求退回,有效的保证了精细化工原料的质量,降低硫化氢超标风险,延长了装置管道和催化剂的使用寿命。
综合效益:该装置通过对原料电石的检验,加强对原料电石的监管,具有以下综合效益:
1.安全效益:通过对原料电石的监控,对不合格的电石退回,降低
了乙炔发生气中硫化氢、磷化氢的含量,降低了有毒气体带来的安全事故风险。
2.环保效益:通过减少乙炔发生气中硫化氢、磷化氢的含量,降低
了乙炔清净单元酸碱的使用量和排放量,具有一定的环保效益,且带来一定的经济效益。
3.经济效益:通过对原料电石的有效监控,降低了乙炔发生气中硫
化氢、磷化氢的含量。
可有效的延长装置管道以及催化剂的使用寿命。
