丙肝病毒是怎么进入细胞的
丙型肝炎的传播途径与医院感染控制

丙型肝炎的传播途径与医院感染控制丙型肝炎是一种由丙型肝炎病毒(HCV)引起的肝脏疾病,其传播途径主要包括血液传播、性传播和母婴传播。
在医院环境中,感染控制是预防和控制丙型肝炎传播的关键措施之一。
1. 血液传播:血液传播是丙型肝炎最主要的传播途径。
这种传播方式主要发生在注射毒品者之间共用注射器、血液制品感染、输血或器官移植等情况下。
在医院中,血液传播主要发生在手术、血液透析、血液采集等操作过程中。
因此,医院应加强对医务人员的培训,提高操作技能,确保操作过程中的安全性。
2. 性传播:性传播是丙型肝炎的另一主要传播途径。
性行为中的血液接触、粘膜损伤等情况都可能导致病毒传播。
医院应加强对医务人员的性教育,提高他们对性传播疾病的认识,并积极推广安全性行为,如正确使用安全套等。
3. 母婴传播:丙型肝炎可以通过母婴传播,即孕妇将病毒传给胎儿。
这种传播途径主要发生在母亲怀孕期间和分娩过程中。
医院应加强对孕妇的筛查,及时发现并治疗感染者,同时提供科学的分娩方式,减少母婴传播的风险。
为了控制丙型肝炎在医院的感染传播,以下措施是必不可少的:1. 严格遵守无菌操作规范:医务人员在进行手术、血液采集等操作时,必须严格遵守无菌操作规范,使用一次性医疗器械,避免交叉感染的风险。
2. 加强医务人员的个人防护:医务人员在接触可能存在丙型肝炎病毒的患者时,应佩戴适当的个人防护用品,如手套、口罩等,以减少感染的风险。
3. 定期进行职业暴露监测:医务人员在工作中可能会发生意外的针刺伤等职业暴露情况,医院应建立健全的职业暴露监测制度,及时发现并处理职业暴露事件,减少感染的可能性。
4. 加强环境清洁与消毒:医院应加强环境清洁与消毒工作,特别是对手术室、血液透析室等高风险区域进行定期清洁和消毒,以减少病毒的存活和传播。
总之,丙型肝炎的传播途径主要包括血液传播、性传播和母婴传播。
在医院中,加强感染控制措施是预防和控制丙型肝炎传播的关键。
医务人员应加强自身防护意识,严格遵守操作规范,同时医院也应加强环境清洁和消毒工作,确保医疗环境的安全性。
丙肝病毒(HCV)的发病机制[推荐下载]
![丙肝病毒(HCV)的发病机制[推荐下载]](https://img.taocdn.com/s3/m/0756aaf63186bceb19e8bbb6.png)
丙肝病毒(HCV)的发病机制[推荐下载]
本文内容非常有参考的价值,如果对您有所帮助,请打赏,谢谢!
丙型病毒性肝炎是由丙肝病毒(HCV)所引起,是通过输血或血制品、血透析、单采血浆还输血球、肾移植、静脉注射毒品、性传播、母婴传播等传染引起的。
那么HCV是如何在血液中播散而致病的呢?丙肝的发病机制是什么呢?
丙肝HCV的致病机制
HCV进入体内之后,引起病毒血症。
血浆中HCV浓度约为100―100000000/ml。
病毒血症间断地出现于整个病程。
在第一周即可从血液或肝组织中用PCR法检出HCVRNA。
第2周开始,可检出抗HCV。
少部分病例感染3个月后才检测到抗HCV。
由于缺乏适当的细胞培养体系,HCV致病机制方面的研究受到一定限制。
目前研究认为HCV致肝细胞损伤有下列因素的参与,其中免疫应答起着更重要的作用。
(1)HCV直接杀伤作用:HCV在肝细胞内复制干扰细胞内大分子的合成,增加溶酶体膜的通透性而引起细胞病变;另外,HCV表达产物(蛋白)对肝细胞有毒性作用,在体外表达HCV某些蛋白(如包膜蛋白)时,发现它们对宿主菌或细胞有毒性作用。
(2)宿主免疫因素已证实肝组织内存在HCV特异细胞毒性淋巴细胞(CD8+T细胞),可攻击HCV感染的肝细胞。
另外,CD4+Th细胞被致敏后分泌的细胞因子,在协助清除HCV的同时,也导致了免疫损伤。
(3)自身免疫,HCV感染者常伴有自身免疫改变,如胆管病理损伤与自身免疫性肝炎相似;常合并自身免疫性疾病,血清中可检出多种自身抗体,如抗核抗体、抗平。
丙肝病毒

在上世纪70年代之前,认识到甲肝。之后不久, 认识到乙肝。
到70年代初,发现“非甲非乙”型肝炎病毒。
80年代末,丙肝病毒基因被成功克隆,并将 “非甲非乙”型肝炎病毒命名为丙型肝炎病毒。 直至90年代初,丙肝病毒定量检查开始出现。
HCV
1
形态结构
2
致病性
检测与防治
感染率高。
所致疾病:丙肝
பைடு நூலகம்
● 丙肝起病隐匿,是容易被忽视的疾病
● 疾病发展越后期,越难治愈
● 目前没有疫苗预防
揭秘丙肝的“隐形术”
●患者症状不明显
多数患者感染丙肝病毒后,缺乏明显症状,通常只是感到疲劳乏力。 因此有许多患者并不知道自已感染丙肝,未能及时就诊与治疗以至延 误了病情。 ● ALT水平变化不明显
3
丙型肝炎病毒 (HCV)
HCV是引起丙型肝炎(HepatitisC)的 病原体,是引起慢性肝炎、肝硬化以及 原发性肝细胞肝癌的重要原因之一。
根据世界卫生组织估计,全世界感染 HCV的病例数超过2亿。
形态
HCV病毒体呈球形,直径小于80nm, 为单股正链RNA病毒,在核衣壳外包绕 含脂质的囊膜,囊膜上有剌突。
其中1/3病人ALT正常,1/3病人ALT低水平升高;这不但影响了早期
发现早期诊断,也因多数人的误解,影响了早期治疗。以往认为上述 情况不需要治疗。
微生物学检测
抗-HCV为非保护性抗体,阳性为病毒感染标志。 放射免疫诊断(RIA)或酶联免疫试验(ELISA) 检测血清中抗HCV HDV cDNA/聚合酶链反应测定肝和血清中HCVRNA 免疫组化法检测肝组织中HCV抗原
基因结构
黄病毒科丙肝病毒属,基因组为单股正链RNA,约由 9600个核苷酸组成,分为编码区和非编码区(5'端和3' 端)。其编码区是一个开放阅读框(ORF),编码约含 3010个氨基酸的前体蛋白,包括结构区和非结构区:结 构区编码病毒的核心蛋白(C蛋白)和包膜蛋白
组成hcv的主要成分

组成hcv的主要成分HCV,即丙型肝炎病毒(Hepatitis C virus),是一种病毒性肝炎的主要原因,它属于RNA病毒,可以分为6个不同的血清型:1a、1b、2a、2b、3a和4。
这些血清型的致病性有所不同,其中1a和1b的传播最为广泛。
HCV由五种结构蛋白组成,包括外壳蛋白(envelope proteins)、内膜蛋白(membrane proteins)、核心蛋白(core proteins)、非结构蛋白(nonstructural proteins)和转录因子(transcription factors)。
外壳蛋白(envelope proteins)由两个结构单位E1和E2组成,它们在病毒膜上形成“锥形”结构,可以抑制宿主免疫系统对病毒的识别,从而使病毒能够感染宿主细胞。
它们可以帮助病毒进入宿主细胞,从而实现繁殖。
内膜蛋白(membrane proteins)由三个结构单位M1、M2和M3组成,它们与外壳蛋白相互作用,以促进病毒的复制。
M1蛋白结构单位可以抑制宿主的抗病毒免疫应答,并参与病毒的繁殖。
M2蛋白结构单位可以抑制宿主细胞的凋亡,M3蛋白结构单位能够增加病毒的传播速度。
核心蛋白(core proteins)由C和NS5A结构单位组成,它们主要负责病毒的繁殖,并参与病毒的复制和传播。
C蛋白结构单位可以帮助病毒进入宿主细胞,并参与病毒的复制。
NS5A结构单位可以抑制宿主细胞的凋亡,参与病毒的繁殖。
非结构蛋白(nonstructural proteins)是病毒的转录因子,可以调节病毒的繁殖和传播。
病毒的非结构蛋白有NS3、NS4A、NS4B、NS5B和NS5C等,它们可以调节病毒的繁殖和传播,从而实现病毒感染和复制。
转录因子(transcription factors)是病毒的转录因子,可以调节病毒的繁殖。
转录因子可以调节病毒的转录和复制,从而促进病毒的繁殖。
总之,HCV由外壳蛋白、内膜蛋白、核心蛋白、非结构蛋白和转录因子等五种结构蛋白组成,它们可以帮助病毒进入宿主细胞,从而实现繁殖。
丙型肝炎病毒

丙型肝炎由丙型肝炎病毒(HCV)感染所致,主要由血液/体液传播。
据世界卫生组织估计,全球有亿人感染HCV。
在我国健康人群抗HCV阳性率为%~%,约3800万人。
由于病毒生物学特点和宿主免疫功能等多方面因素,机体免疫往往难以有效清除病毒,致使约50%~80%HCV感染者发展为慢性肝炎,其中20%~30%将发展成肝硬化。
肝硬化患者中每年有1%~4%发展成为肝细胞癌症。
一、基因组特征:丙型肝炎病毒呈球形颗粒,直径约为50nm,有一脂质包膜。
基因组为单链正链RNA,链长月。
整个基因组只有一个ORF,编码一条由3010~3033个氨基酸组成的聚蛋白前体,该蛋白前体在病毒蛋白酶和宿主信号肽酶作用下,裂解为病毒的结构蛋白和非结构蛋白。
(如图所示)在HCV基因组中,5’端有一个长度和序列非常稳定的非编码区(UTR),由341个核苷酸组成,形成4个二级结构域,为病毒复制和翻译所必需。
此区是整个基因组中最保守的区域,所以常常选择该区域的基因序列作为基因扩增的靶序列,这样可以检测出目前已知的所有HCV基因型。
3’端UTR包括3个结构域:靠近5’端为基因型特异的多变区(不同基因型之间的核苷酸序列差异较大;相同基因型之间核苷酸序列比较保守);居中部分为一个多聚U区域(poly U),含有50~62个核苷酸,对病毒RNA复制至关重要,但不同基因型的HCV的多聚U区域长度不等;3’端尾部为高度保守的发夹样结构,称为X-tail。
通过定点突变破坏这一结构会导致RNA病毒复制的显著降低,说明该区域对RNA病毒有效复制同样重要。
5’端和3’端UTR之间是一个ORF并且分成9个区域:核心区→E1区→NS1/E2区→NS2区→NS3区→NS4a区→NS4b区→NS5a区→NS5b区。
其中NS5b区域在不同型HCV中同源性较低,可作为HCV分型依据。
二、分类急性丙型肝炎——成人急性丙型肝炎病情相对较轻,多数为急性无黄疸型肝炎,ALT升高为主,少数为急性黄疸型肝炎,黄疸为轻度或中度升高。
病毒性丙肝的传染途径

如对您有帮助,可购买打赏,谢谢
病毒性丙肝的传染途径
导语:病毒性丙肝是一种常见的肝病,如果治疗不及时,还会引起肝硬化或者是更严重的肝癌,其危害性不容小觑。
很多病毒性丙肝的患者都担心会把疾病
病毒性丙肝是一种常见的肝病,如果治疗不及时,还会引起肝硬化或者是更严重的肝癌,其危害性不容小觑。
很多病毒性丙肝的患者都担心会把疾病传染给别人,那么如何防止把病毒性丙肝传染给别人,就要先了解病毒性丙肝的传染途径,接下来小编就来跟大家讲讲病毒性丙肝都有哪些传染的途径吧。
1.母婴传播
抗-HCV阳性母亲将丙肝病毒传播给新生儿的危险性为2%,若母亲在分娩时丙肝RNA阳性,则传播的危险性可高达4-7%;合并HIV感染时,丙肝病毒高载量可能增加传播的危险性。
部分丙肝感染者的传播途径不明,接吻、拥抱、喷嚏、咳嗽、食物、饮水、共用餐具和水杯,无皮肤破损极其他血液暴露的一般接触不传播丙肝。
2.性传播
与丙肝感染者性交及有性乱行为者感染丙肝的危险性较高。
同时伴有其他性传播疾病者,特别是感染人类免疫缺陷病毒(HIV)的患者,感染丙肝的危险性更高。
3血液传播:
肝病专家徐主任指出血液传播是丙肝的主要传播途径,凡是容易接触到他人血液的行为都有可能导致感染。
感染最大的几率是医源性传播,比如输血、手术、打针等,如果消毒措施不到位的话,很容易传染丙肝。
预防疾病常识分享,对您有帮助可购买打赏。
丙肝的病因治疗与预防
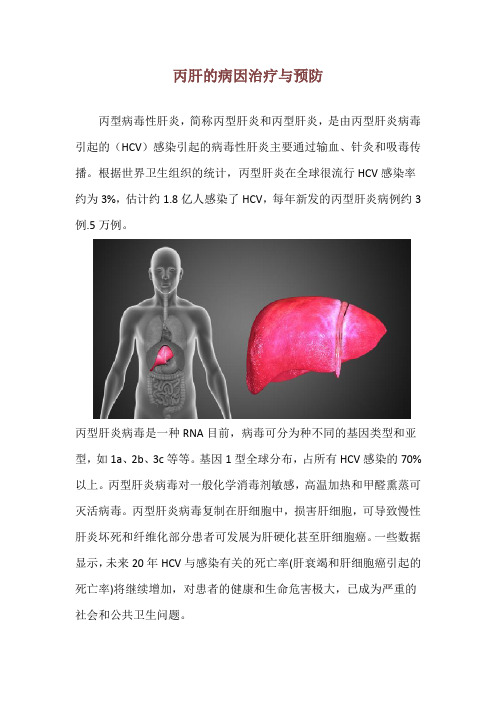
丙肝的病因治疗与预防丙型病毒性肝炎,简称丙型肝炎和丙型肝炎,是由丙型肝炎病毒引起的(HCV)感染引起的病毒性肝炎主要通过输血、针灸和吸毒传播。
根据世界卫生组织的统计,丙型肝炎在全球很流行HCV感染率约为3%,估计约1.8亿人感染了HCV,每年新发的丙型肝炎病例约3例.5万例。
丙型肝炎病毒是一种RNA目前,病毒可分为种不同的基因类型和亚型,如1a、2b、3c等等。
基因1型全球分布,占所有HCV感染的70%以上。
丙型肝炎病毒对一般化学消毒剂敏感,高温加热和甲醛熏蒸可灭活病毒。
丙型肝炎病毒复制在肝细胞中,损害肝细胞,可导致慢性肝炎坏死和纤维化部分患者可发展为肝硬化甚至肝细胞癌。
一些数据显示,未来20年HCV与感染有关的死亡率(肝衰竭和肝细胞癌引起的死亡率)将继续增加,对患者的健康和生命危害极大,已成为严重的社会和公共卫生问题。
丙型肝炎的临床表现与乙型肝炎相似,但对人类健康的威胁不亚于乙型肝炎。
目前还没有预防丙型肝炎的有效疫苗,但只要及时发现和规范治疗,大多数丙型肝炎患者都可以临床治愈。
丙型肝炎的根本原因是感染了丙型肝炎病毒。
在饮酒、疲劳、长期服用肝毒性药物等外部因素的影响下,可促进疾病的发展。
丙型肝炎病毒的传播主要有五种方式:1、输血传播:输入丙型肝炎病毒感染的血液和血液制品后,可引起输血后丙型肝炎的发生,这是传播的主要途径。
2、性传播:丙型肝炎患者可通过性传播,性传播也是一种体液传播。
此外,如果嘴唇粘膜损坏,接吻也可以传播。
目前,蚊虫叮咬尚未被确认为丙型肝炎的传染途径。
3、母婴传播:丙型肝炎的母婴传播包括两个方面,一个是垂直传播,另一个是水平传播。
子宫和胎儿在子宫和怀孕期间感染的概率不大。
主要是围产期和出生后密切接触水平的传播。
作为丙型肝炎母亲,孩子出生后很有可能被感染。
第四,医源性传播:在医院检查治疗过程中,因未经严格消毒反复使用而被重复使用HCV被污染的医疗器械被称为医源性传播,包括手术、牙科器械、采血针、针灸针和内镜。
对丙型肝炎病毒的病理生理学检测

对丙型肝炎病毒的病理生理学检测丙型肝炎病毒是一种影响全球范围内的重要病原体之一,其主要引起急性和慢性肝炎、肝硬化和肝细胞癌等严重的肝脏疾病。
因此,对丙型肝炎病毒的检测和诊断至关重要,早期发现和治疗可以显著降低相关疾病的发生率和死亡率。
本文将介绍一些关于丙型肝炎病毒病理生理学检测的基本知识。
一、丙型肝炎病毒概述丙肝病毒是一种RNA病毒,与埃博拉病毒、登革热病毒和肺炎军团菌等同属于菱形病毒科。
该病毒存在于全世界范围内,主要通过体液(如血液、精液和阴道分泌物等)传播。
感染后,丙肝病毒会引起急性或慢性肝炎,部分患者会发展成肝硬化和肝癌,其中肝癌是严重疾病的最终结果之一。
二、丙型肝炎病毒检测方法目前,常用的丙型肝炎病毒检测方法包括血清学检测、分子生物学检测、组织学检测和免疫组化检测等方法。
1. 血清学检测血清学检测是一种基于患者血清中的抗体或抗原对丙肝病毒的检测方法。
该方法包括ELISA、免疫荧光等检测方式,该方法能够快速、简单和经济地检测血清中的抗体或抗原。
但是,该方法对于急性感染的敏感性较低,而对于慢性感染和复发性感染的检测效果较好。
2. 分子生物学检测分子生物学检测是一种基于核酸技术的检测方法,能够直接检测丙肝病毒的RNA或DNA。
该技术包括PCR、实时PCR、荧光PCR等方法,其优点是灵敏度高、特异性好、快速等,特别是对于急性感染和复杂病例往往是首选方法。
3. 组织学检测组织学检测是一种直接检测丙肝病毒感染组织的方法,目前主要采用免疫组化技术。
通过检测组织中的病毒蛋白或核酸,能够发现存在于组织中的病毒感染情况,对病毒相关性肝细胞癌和肝移植的病情评估起到重要作用。
4. 免疫组化检测免疫组化检测也是一种通过检测组织样本中的特定抗原、抗体、或细胞分子来诊断疾病或病毒感染的方法。
该技术适用于病理学和临床医学领域,能够在组织级别上提供病毒感染的定量分析。
三、丙型肝炎病毒检测的意义丙肝病毒感染可分为急性和慢性两种。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
丙肝病毒是怎么进入细胞的?
丙型肝炎病毒(HCV)有着和人类免疫缺陷病毒(HIV)相同的传播途径,是引起输血后肝炎的最主要原因,据世界卫生组织估计,目前全世界将近有1.7亿人感染了HCV{[Anon], 1999 #75}。
其中绝大多数人(55-85%)因为病毒清除不干净而成为携带者,其血清中可以持久稳定的检测到病毒{Hoofnagle, 2002 #76},而有发展成慢性丙型肝炎的危险,包括轻微肝炎、纤维化、肝硬化和肝细胞癌。
这一过程并不是直接由病毒引起的,而是由于病毒和免疫系统得相互作用导致健康的肝脏组织被纤维疤痕组织取代。
大约有20%的慢性丙肝病人会在20年之内发展成肝硬化。
一旦肝硬化形成,发展成肝癌的速率就是1-4%/年{Moradpour, 2001 #77}。
长期以来,丙型肝炎的研究一直面临两大难题:即缺少有效的组织培养模型和小动物模型,阻碍了对HCV致病机理探讨、抗病毒药物筛选和疫苗研究等的研究进程。
虽然临床上分离的HCV能够感染体外培养的肝细胞,但效率很低,而且经常是不可重复的。
肝细胞一直被认为是该病毒复制的基本场所,而直到现在我们对HCV进入细胞的机制还知之甚少。
不过近三年来一些研究模型的出现大大推动了这方面的研究,其中最主要的是两个:1) .反转录病毒假颗粒体系,是用反转录病毒(如HIV)的核衣壳和HCV的包膜蛋白组装成的,叫作HCV pesudoparticle(HCVpp){Bartosch, 2003 #11;Hsu, 2003 #50}。
因为包膜蛋白全部都是HCV的成分,因此进入细胞的过程跟HCV肯定很像,是研究HCV进细胞机制很好的模型;2) .HCV 的JFH毒株,能
够在细胞培养的情况下释放出具有感染性的病毒粒{Lindenbach, 2005 #25; Wakita, 2005 #26; Zhong, 2005 #27}。
HCV介绍
HCV为单股正链RNA病毒,直径为40-60nm,有包膜,与经典的黄病毒(如黄热病毒、登革热病毒) 和虫媒病毒(pestivirus)如牛病毒性腹泻病毒(BVDV)同属黄病毒科(Flaviviridae),但HCV分属肝病毒(Hepacivirus)属。
HCV基因组全长约9600bp,于基因组5′末端和3′末端分别存在5′非翻译区(5′U TR) 和3′非翻译区(3′U TR) ,中心部存在1 条编码多蛋白前体的可译框(ORF) ,可编码约3010 个氨基酸。
5′U TR 中包涵内部核糖体进入位点(internal ribosome entry site : IRES)承担HCV 基因翻译起动结构的功能,3′U TR则在基因组复制过程具有负链生成的引物作用。
自然情况下突变形成HCV被分为6个基因型和多个亚型。
各基因型之间的核苷酸序列相差30%左右,各亚型之间则相差5-10%。
还有许多其它的突变体,叫作准种(quasispecies),是由于病毒在被感染者体内复制的时候病毒的RNA聚合酶错误率太高而引起的。
ORF 所翻译出的多蛋白前体于翻译同时和翻译后由宿主细胞的信号蛋白酶(signal peptidase)和HCV自身编码的蛋白酶加工成约10个成熟的HCV蛋白。
于N 末端一侧编码有结构蛋白Core , E1 、E2 和p7 ,其中Core形成病毒的核壳体,E1,E2则是包膜蛋白,它们被宿主内质网上的信号蛋白酶从多蛋白前体上剪切下来。
E1,E2的膜外结构域被高度糖基化,并且形成异二聚体滞留在内质网上。
结构蛋白在内
质网上不断积累,最后形成病毒的衣壳和包膜。
另一方面,由中心至C 末端则编码有非结构蛋白NS2 、NS3 、NS4A、NS4B、NS5A 和NS5B ,其加工由HCV自身编码的蛋白酶介导,其中NS2-3自身蛋白酶(autoprotease)切割NS2和NS3间的连接,而NS3丝氨酸蛋白酶负责下游NS3至NS5B间的加工成熟。
对于病毒的结构和形态知道的还不多。
从病人血清总分离道德病毒粒,其直径变化范围很大,从20-100nm,而且有证据证明有包膜病毒和无包膜病毒同时存在于血清中{Petit, 2005 #28; Andre, 2005 #29; Roingeard, 2004 #30}。
目前还不知道是否这些不同形式的HCV病毒都具有感染性,还是其中有些是无感染性的缺陷病毒。
HCV在血清中可以跟脂蛋白、免疫球蛋白等不同成分结合,其中大部分是跟脂蛋白结合。
通过密度梯度离心将病人血清分离,在VLDL、LDL、HDL 及不含脂蛋白的片断中都可以检测到HCV RNA,而且其中的相对含量因病人而异。
当然,这种变化也有可能是操作不当而造成的假象。
不过对于大多数含HCV的血清来说,HCV RNA主要还是存在于VLDL/LDL和不含脂蛋白的片断中{Petit, 2005 #83}。
此外,还有人发现HCV RNA与病人血清中的外来体(exosomes)相关联{Masciopinto, 2004 #8}。
通过将密度梯度离心得到的不同片断分离,以同样的稀释倍数注入黑猩猩体内,发现所有的片断中都具有感染性病毒粒{Bradley, 1991 #32},但通过PT-PCR对HCV-RNA的含量进行分析后发现感染性较高的血清中的HCV RNA主要存在于低密度片断中,而感染性较低的
血清中的HCV RNA则存在于较高密度的片断中{Hijikata, 1993 #31}。
也即跟脂蛋白结合的HCV具有较高的感染性,而存在于HDL或无脂蛋白片断中的HCV感染性较低。
包膜蛋白在病毒感染中的作用
HCV编码2个包膜蛋白E1和E2,均在翻译后水平修饰为糖基化蛋白,分子量分别为31kD和70kD。
E1和E2可形成非共价异二聚体(non-covalent heterodimers){Lanford, 1993 #50},后者被认为是HCV颗粒脂质包膜上的镶嵌结构。
但到目前为止,在现有的HCV研究模型中,尚未观察到HCV糖蛋白和病毒颗粒分泌和释放,因此,对该过程还知之甚少。
在脂蛋白相关的感染颗粒中到底有哪些病毒成分?病人血清密度梯度离心的VLDL/LDL片断中不断被检测到的是HCV RNA和核心蛋白,说明至少病毒的衣壳是存在于该感染颗粒中的。
但是包膜蛋白E1、E2却始终很难检测到。
有些研究表明用E2特异性抗体或E2结合蛋白CD81可以捕捉到病人血清中的E2及与之相联系的HCV RNA{Cerino, 2001 #90; Pileri, 1998 #91},但是并不能保证该HCV RNA就是与脂蛋白结合的那部分HCV RNA。
还有一些研究分别用抗E2和抗脂蛋白的抗体来沉淀HCV RNA,发现在VLDL/LDL片断中抗脂蛋白抗体捕获的HCVRNA〉90%,而抗E2抗体沉淀出来的HCVRNA=25%,说明绝大多数脂蛋白结合的HCVRNA并不能被抗E2抗体识别{Nielsen, 2006 #92}。
而有些研究小组则根本不能在包含HCVRNA的低密度颗粒中检测到E2
{Petit, 2005 #7}。
这是个令人非常困惑的问题,有几种可能的情况可以解释:1).用来检测E1、E2的方法灵敏度不够高。
2).抗体识别表位被覆盖了。
但是这不能解释为什么用westernblotting也检测不到病毒的包膜蛋白。
3).脂蛋白结合颗粒中的病毒包膜极不稳定,在纯化的过程中丢失了.但是Bradley等人却证明通过蔗糖密度梯度离心分离出来的病毒颗粒仍然具有感染性,说明跟病毒感染相关的主要结构并没有在离心过程中改变或者丢失{Bradley, 1991 #87}。
4).跟脂蛋白结合的病毒颗粒可能是无包膜结构的。
在含HCV的血清中用酶水解掉其中的脂蛋白后,HCVRNA变得对核酶非常敏感{Thomssen, 2002 #94},而有包膜的病毒RNA通常是被包膜和衣壳保护着的。
说明脂蛋白结合的病毒粒很可能跟经典的包膜病毒结构组成不一样。
无包膜的存在虽然可以很好的解释为什么很难检测到包膜蛋白,但还从来没有碰到过那个包膜病毒不利用包膜蛋白进入细胞的。
虽然临床上没有检测到,功能分析的数据表明E1、E2是存在于感染性颗粒中的。
E2特异性的抗体可以阻止血清中的HCV感染人的细胞{Zibert, 1995 #95}。
用重组的E1、E2作疫苗免疫黑猩猩后可以使他免受HCV感染,或者使已被感染的动物康复{Choo, 1994 #96}。
用HCV和抗E2的抗血清共同注射黑猩猩也可以使他免受感染{Farci, 1996 #89}。
因此抗E1、E2的抗体可以阻止HCV和宿主细胞的相互作用。
HCV和宿主的相互作用
CD-81SR-BI。
