现代有机合成第5章
第5章 第1节 合成高分子化合物的基本方法

(2)a
H OCH2CH2CH2CO OH
加聚反应和缩聚反应的比较 加聚反应 单体 结构 反应 机理 缩聚反应
单体必须是含有双键等不饱和键 单体为含有两个或两个以上的官 的化合物(如乙烯、氯乙烯、丙烯 能团(如—OH、—COOH、—NH2、 腈等) 反应发生在不饱和键上 —X 等)的化合物 反应发生在不同的官能团之间
B
[ 缩聚反应的单体至少有两个相互作用的官能团。
OH 不能发生
加聚反应;CH2= = = CHCOOH 和 HOCH2CH= = = CHCH2CH3 不能单独发生缩 聚反应。]
[合 作 探 究· 攻 重 难]
加聚反应和缩聚反应
[ 典例] 下列化合物中
a. b.HO(CH2)2OH d. c.CH3CH===CH—CN e.HOOC(CH2)4COOH
(4)无论是加聚反应还是缩聚反应,有机物的单体和高聚物的链节之间的关 系是组成相同,结构不同。( )
(5)
的名称为聚乙二酸乙二酯。(
)
【答案】 (1)× (2)× (3)√ (4)× (5)√
2.今有高聚物 , 有关它的下列叙述中正确的
是(
) 【导学号:40892212】 A.它的链节是 CH3—CH2—OOCCH3 B.它的聚合度 n=3 C.它的单体是 CH2===CH—COOCH3 D.它是一种线型高分子化合物
C [ 常见的缩聚反应主要有羟基和羧基的缩聚( 包括二元羧酸和二元醇的缩 聚、羟基酸的缩聚)、酚和醛的缩聚以及氨基和羧基的缩聚(包括二元羧酸和二元 胺的缩聚、氨基酸的缩聚)等。根据缩聚反应的特点,单体必须含有两个或两个 以上的官能团,③中含有—COOH 和—NH2;④中含有—COOH 和—OH;⑤中 含有—COOH 和—NH2。]
有机化学第五章答案
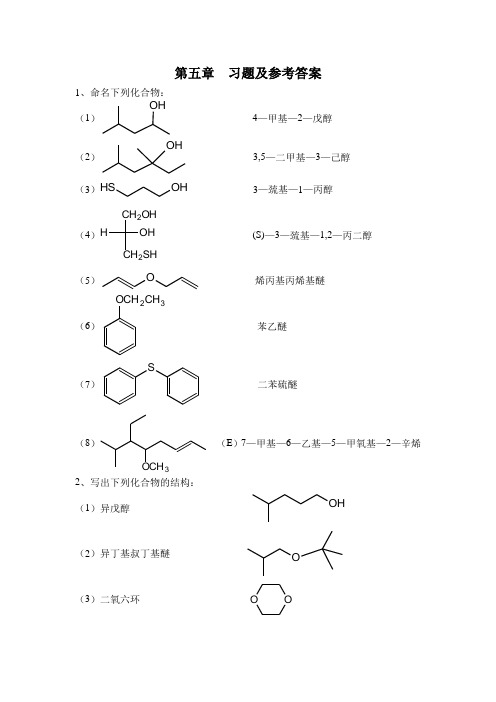
第五章 习题及参考答案1、命名下列化合物:(1)O H4—甲基—2—戊醇(2)O H3,5—二甲基—3—己醇(3)O H SH 3—巯基—1—丙醇(4)H O H CH 2OHCH 2SH(S)—3—巯基—1,2—丙二醇 (5)O烯丙基丙烯基醚(6)OCH 2CH3苯乙醚(7)S二苯硫醚(8)OCH3(E )7—甲基—6—乙基—5—甲氧基—2—辛烯2、写出下列化合物的结构:(1)异戊醇O H(2)异丁基叔丁基醚O(3)二氧六环 O O(4)DMSOC H 3SC H 3O(5)THFO(6)环氧丙烷 O3、按沸点从高到低顺序排列下列化合物:(1)正丁醇(2)正戊醇(3)异丁醇(4)叔丁醇(5)四氢呋喃 (2)﹥(1)﹥(3)﹥(4)﹥(5) 4、用化学方法区别下列各组化合物: (1)正丁醇、仲丁醇、叔丁醇取三支试管分别加入三种化合物少许,分别加入几滴Lucas 试剂,立即变浑浊的是叔丁醇,放置片刻变浑浊的是仲丁醇,室温下无变化,加热后变浑浊的是正丁醇。
(2)1,4—丁二醇、1,2—丁二醇取两支试管分别加入硫酸铜溶液少许,滴加氢氧化钠溶液至有氢氧化铜沉淀生成,一只试管中加1,4—丁二醇,另一只试管中加1,2—丁二醇,能生成将蓝色溶液的是1,2—丁二醇,则另一个是1,4—丁二醇 (3)苄醇和苄基溴高锰酸钾酸性溶液,步骤略 (4)O(CH2CH 2OH)2C H 2C H O HO HC H 3同(2)5(1)CH 2CH 3CH3O H H SOCC HC H 3C H(2)H 3CH2(3)(CH 3)3CCH 2OH+B r H H 3C C H 2C H 3B rC H(4)+OIH O H+CH 3I (Imol)(5)+IH +CH 3I OCH3O H(6)O33(7)O3+OO H(8)O HC C C H 3PhPh O HPh H 2SO4PhC C C H Ph O(9)O HO(CrO 3 /(C 5H 5N)2)或(CrO 3 /H 2SO 4/H 2O)或(MnO2/C 5H 12)6、将下列化合物按水溶解度由大到小排列成序:(1)丙三醇 (2)正丁醇 (3)甲乙醚 (4)甲硫醚 (1)﹥(2)﹥ (3)﹥ (4) 7、解释下列现象: (1)CH 2OHH 2SO4++(2)(CH 3)3C C H O HC H 334(CH 3)3C C HC H 2+(CH 3)2CH CC H 2C H 3+(CH 3)2C=C(CH 3)2(3)CH2OH24175℃(4)O HO HC H3C H3H2SO4OC H3C H3解释:(1)CH2OHH2SO4+C H2O+HH-H2OCH2+重排+++-H++(2)+(CH3)3C C HO HC H385%H3PO4(CH3)2CH C C H2C H3(CH3)2C=C(CH3)2(CH3)3C C HO+C H3H H-H2O(CH3)3C C H+C H3重排C H3C+C HC H3C H3C H3-H+(CH3)3C C H C H2-H+(3)+CH 2OHH 2SO4175℃CH 2O +H 2-H 2OCH2+-H +(4)+O H O HC H 3C H3H 2SO4OC H 3O H OH2+C H 3C H 3-H OO HC H 3C H 3重排3O +C H 3C H H-H +8、写出环氧丙烷与下列试剂反应的主要产物:(1)无水HBr (2)(CH 3CH 2)2NH (3)CH 3CH 2ONa/CH 3CH 2OH (4)CH 3CH 2MgBr (5)CH 3CH 2OH/H + (6)PhOH/OH -O(CH CH )NH3CH 2ONa/CH 3CH 2OHCH 3CH 2MgBrCH 3C H 3C B r C H 3O HC H 3COCH 2CH3C H 3O HC H 3C HC H 2O HC H 3C HC H 2OMgBrC H 2C H 3C H 3C HC H 2O HN(CH2CH 3)2C H 3C HC H 2O HOCH 2CH39、用指定原料合成:(1)由叔丁醇和乙醇合成乙基叔丁基醚C H 3C H 2O H H 3C H 2IC H 3CO HC H 3C H 3NaC H 3CO C H 3C H 3NaC H 3CO C H 3C H 3Na +C H 3C H 2IC H C H O HH 3COC H 3C H 3C 2H 5(2)由正丙醇和异丙醇合成2—甲基—2—戊醇C H 2C H 2O HC H 3C H 3C H O HC H 34C H 3C C H 3O+C H 2C H 2B C H 3Mg无水醚C H 2C H 2MgBrC H 3C H 3C C H 3O C H 2C H 2MgBrC H 3C H 3CC H 2C H 3C H 2C H 3OMgBr2C H 3C C H 2C H 3C H 2C H 3O H(3)由溴苯和异丙醇合成2—苯基—2—丙醇C H 3C H O HC H 34C H 3C C H 3O+Mg C H 3C C H 3O C H 3CC H 3OMgBr 2B rTHFMgBrMgBrC H 3CC H 3O H(4)由环己醇合成二环己醚+O HB rH B rO NaO N aB rO N aHO10、用高碘酸分别氧化四个邻二醇,得到的氧化产物如下: (1)只得到C H 3C C H 2C H 3O(2)得到CH3CHO 和CH3CH2CHO (3)得到HCHO 和C H 3C C H 3O(4)得到一个二羰基化合物C H 3C C H 2OC H 2C H 2CHO请根据氧化产物分别写出四个邻二醇的结构式。
第五章--第一节511-合成高分子化合物的基本方法

第五章第一节合成高分子化合物的基本方法县中学高二化学组编审班别姓名组别学习目标1.能举例说明合成高分子的组成与结构特点,能依据简单合成高分子的结构分析其链节和单体。
2.能说明加聚反应和缩聚反应的特点。
3.使学生感受到,掌握了有机高分子化合物的合成原理,人类是可以通过有机合成不断合成原自然界不存在的物质,从而为不断提高人类生活水平提供物质基础课前自学一、加成聚合反应回顾练习:写出制取聚乙烯的化学方程式,指出聚乙烯中的链节、聚合度以及它的单体。
1、几个基本概念:单体:链节:聚合度:.2、加聚反应:高分子化合物,简称高分子,又叫聚合物或高聚物。
3、聚合物的平均相对分子质量=链节的相对质量×n(聚合度)一块高分子材料是由若干n值不同的高分子材料组成的物。
思考与交流1:根据单体判断聚合产物。
第一组:CH2=CHCH3、CH2=CHCN、CH2=CHCOOH、HCHO、CH≡CCH3小结:此类化合物加聚将单体的不饱和键的碳链单独列一行,其他视为支链部分。
第二组:(1,3-丁二烯型)CH2=CH—CH=CH2、CH2=C(CH3)—CH=CH2小结:1,3-丁二烯型的单体聚合时,主链上的单双键相互替换即可。
第三组:(共聚反应)CH2=CH2和CH2=CHCN,CH2=CH—CH=CH2和CH2=CHCN小结:方法类似第一、二组,仅需将不饱和碳链进行连接即可,其他仍视为支链。
4.加聚反应具有的特点(1)单体必须是含有键、_____键等不饱和键的化合物;例如:烯、二烯、炔、醛等含不饱和键的化合物。
(2)发生加聚反应的过程中,没有副产物产生,聚合物链节的化学组成跟单体的化学组成相同。
聚合物相对分子质量为单体相对分子质量的整数倍。
学与问:通过聚合物的链节可以看出聚合物的单体,你知道下列聚合物的单体吗?补充:几种分子间脱水的情况1. 醇分子间脱水:以乙二醇为例2. 羧酸分子间脱水:以两分子乙酸、邻苯二甲酸为例3. 一元醇和一元羧酸分子间脱水:酯化反应4. 二元醇和二元羧酸分子间脱水:乙二酸和乙二醇反应5. 羟酸分子间脱水:以乳酸为例二、缩合聚合反应回顾:1乙酸与乙醇酯化反应2、两个甘氨酸分子形成二肽乙酸和乙醇分别是一元酸和一元醇,如果用二元酸和二元醇发生酯化反应,就会得到连接成链的聚合物(简称聚酯):1.缩聚反应_________________________________________________________________________2.缩聚反应的特点:(1)缩聚反应的单体往往是具有双官能团(如—OH、—COOH、—NH2、—X及活泼氢原子等)或多官能团的小分子;(2)缩聚反应生成聚合物的同时,还有小分子副产物(如H2O、NH3、HCl等)生成;(3)所得聚合物链节的化学组成与单体的化学组成不同;(4)缩聚物结构式要在方括号外侧写出链节余下的端基原子或原子团(这与加聚物不同,而加聚物的端基不确定,通常用横线“—”表示。
有机合成-5官能团的保护

CH2OH CHOCO(CH2)14CH3 CH2OH OCH3 HO HO O O OH OCH3 89% TsOH O O 少量 HCl 蒸镏
CH2OH CHOH CH2OOC(CH2)14CH3
1) mCPBA, 99% 2) (CH3)2CuLi, 乙醚, 94% HO O O
2、形成碳酸环酯
HOH2C
O
O O P OLi OLi OH
HO
二、羰基的保护
CH3OH, H+ R2C O 2 mol/L, H2SO4 O HN H C2H5 O p-TsOH, PhH HOCH2CH2OH 85% O O HS(CH2)3SH, BF3(C2H5)2O R2C O CH3I, H2O, CH3OH R2C S S HN H C2H5 O 1) LiAlH4, THF 2) NaOH aq 3) 1 mol/L HCl O HN H C2H5 R2C OCH3 OCH3
AcO
OAc O Ar, reflux Ph condition
O
H H OAc taxinine (1)
O
AcO
OAc +
AcO
OAc
AcO +
OAc
O H
H OAc
OH HO
N H
H OAc 29-a
OH
N HO
H
H OAc
OH
taxinineA (29)
29-b
Table 2: Selective Hydrolysis of Cinnamoyl Group at C-5 of taxinine (1) yields (%) entry Reagents (equiv) conditions 29 NH2OH. HCl (12) NaOAc (12) H2O 1,4-dioxane NH2OH. HCl (15) NaOAc (15) MeOH 1,4-dioxane NH2OH. HCl (15) NaOAc (10) H2O 1,4-dioxane NH2OH. HCl (10) NaOAc (15) H2O 1,4-dioxane NH2OH. HCl (5) NaOAc (10) EtOH, H2O 1,4-dioxane 70-75 oC, 64 h 29-a 29-b 1
第五章 第一节 合成高分子化合物的基本方法

第一节合成高分子化合物的基本方法[核心素养发展目标] 1.宏观辨识与微观探析:能根据单体的官能团差异理解加聚反应和缩聚反应的原理,从而认识高分子化合物的形成历程。
2.证据推理与模型认知:建立高聚物与单体间的相互推断的思维模型,能运用该思维模型进行高聚物与单体间的相互推断。
一、有机高分子化合物1.概念由许多小分子化合物通过共价键结合成的,相对分子质量很高(104~106)的一类化合物。
2.特点(1)相对分子质量很大,由于高分子化合物都是混合物,其相对分子质量只是一个平均值。
(2)合成原料都是低分子化合物。
(3)每个高分子都是由若干个重复结构单元组成的。
3.与高分子化合物有关的概念(1)单体:能够进行聚合反应形成高分子化合物的低分子化合物。
(2)链节:高分子化合物中化学组成相同、可重复的最小单位。
(3)聚合度:高分子链中含有链节的数目,通常用n表示。
催化剂如:――→(4)聚合物的平均相对分子质量=链节的相对质量×n。
1.下列关于高分子化合物的说法中正确的是()A.高分子化合物的相对分子质量一般在几千至几万B.高分子化合物一般都是混合物C.聚乙烯有固定的熔点和沸点D.高分子化合物分子中只含C、H、O三种元素答案 B解析高分子化合物的相对分子质量在104以上,A错误;高分子化合物一般都是混合物,没有固定的熔、沸点,B正确,C错误;蛋白质属于高分子化合物,除含有C、H、O外,还含有N、P等元素,D错误。
2.下列属于有机高分子化合物的有________。
①油脂②蔗糖③蛋白质④淀粉⑤碳纤维⑥甘油⑦聚氯乙烯(PVC)⑧DNA和RNA⑨汽油答案③④⑦⑧有机高分子化合物与低分子有机物的区别有机高分子化合物低分子有机物相对分子质量高达10 000以上 1 000以下分子的基本结构若干重复结构单元组成单一分子结构性质物理、化学性质有较大差别二、加成聚合反应1.概念一定条件下,由含有不饱和键的化合物分子以加成反应形式结合成高分子化合物的反应,简称加聚反应。
第5章硝化精细有机合成

(C)瞬间系统, 亦称快速传质型。
反应速度快速到使处于液相中的反应物不能
2019/9/27
15
4、非均相混酸硝化法
当被硝化物和硝化产物在反应温度下都是液态时,常 常采用非均相混酸硝化的方法。通过剧烈的搅拌,有 机相被分散到酸相中而完成硝化反应。这种硝化方法 有很多优点,是目前工业上最常用、最重要的硝化方 法.也是本章讨论的重点。
2019/9/27
16
5、有机溶剂中的硝化法
H2O + NO2+ H3O+ +HSO4-
活泼 质点
总的式子为:
2 H 2 S O 4 + H N O 3 N O 2 + + H 3 O + + 2 H S O 4 -
2019/9/27
8
硝酸 表3-1 由硝酸和硫酸配成的混酸中HNO3的转化率
混酸中的硝酸的 5 10 15 20 40 60 80 90 100 含量(%)
NO 3
CH 3
O3N
NO 3
(H 3C) 3C
CH 3 NO 3
人造麝香
3-叔丁基-2,4,6-三硝基二甲苯
2019/9/27
6
二、硝化剂及其硝化活泼质点 1、硝酸
1050㎝-1 NO31400㎝-1 NO2+
HNO3 + HNO3
H2+NO3 + NO3-
H2+NO3
有机化学教案第5章 第1节
第一节 合成高分子化合物的基本方法[目标定位] 1.知道并会应用有关概念:单体、高聚物、聚合度、链节、加聚反应和缩聚反应等。
2.熟知加聚反应和缩聚反应的原理,会写相应的化学方程式,学会高聚物与单体间的相互推断。
一 加成聚合反应1.写出乙烯分子间相互反应生成聚乙烯的化学方程式: n CH 2===CH 2――→催化剂CH 2—CH 2。
(1)像这种由含有不饱和键的化合物分子以加成反应形式结合成高分子化合物的反应叫加成聚合反应,简称加聚反应。
(2)能够进行聚合反应形成高分子化合物的低分子化合物称为单体;高分子化合物中化学组成相同、可重复的最小单位称为链节;含有链节的数目称为聚合度,通常用n 表示。
(3)聚合物的平均相对分子质量等于链节的相对质量×n 。
2.写出丙烯发生加聚反应的化学方程式,并注明高聚物的单体、链节、聚合度:。
3.写出下列物质发生加聚反应的化学方程式:(1)丙烯酸: 。
(2)苯乙烯:。
(3)1,3丁二烯:n CH 2===CH—CH===CH 2――→催化剂CH 2—CH===CH—CH 2。
(4)乙烯、丙烯(1∶1)共聚: n CH 2===CH 2+n CH 2===CH—CH 3 ――→催化剂(或 )。
(5)丙烯与1,3丁二烯(1∶1)共聚:n CH 2===CH—CH 3+n CH 2===CH—CH===CH 2――→催化剂(或)。
4.写出下列加聚产物的单体(1) :___________________________________________。
(2) :________________________________________________。
(3) :______________________________________________。
答案 (1)(2)CH 2===CH 2和CHCH 3CH 2(3)1.加聚反应的特点(1)单体必须是含有双键、三键等不饱和键的化合物。
有机合成课件5章(金属有机化合物)
H2O C2H5OH (CH3)2CO (CH3)2SO
16 28 20 23
第五章 金属有机化合物
3)金属盐与金属有机化合物的反应
M'X+R-M RM'+MX R2Cd+MgCl2 RCu RLi R2CuLi
如:
CdCl2+RMgX CuI+RLi
4)金属或非金属的化合物与烯烃等不饱和键的加成: 二异丁基铝氢与炔的加成: R
1,2
C
C C C O R' 1,4 RMgX
C C OMgX R'
C C C OMgX R R'
第五章 金属有机化合物
这两种加成是互相竞争的,究竟是哪一种占优势呢?要由R1 和R的相对空间体积大小决定。如:
O Ph C C H H
O Ph C C H H
H + PhMgBr 1,2
CH3 CH CH3
CH3 H3C C CH CH Ph H K CH2Ph
第五章 金属有机化合物
Ph2C CH3SOCH2Na Ph C H2 C CH2SOCH3 CH2 2 Na
因此,一般反应不选择烯烃和炔烃作溶剂。 3,有机锂: 一般为烷烃的溶液,反应溶剂可选择醚,THF等。试验证明,
乙醚中室温保存不久,会分解乙醚。它比RMgX稳定性差。制
OCH3
CO2C2H5
O C-CH3 THF + BrCH2CO2C2H5 + Zn reflux CO2H O H3C CH2CO2C2H5 O
第五章 金属有机化合物
O C CH3 + BrCH2CO2C2H5 + Zn THF reflux CO2C2H5 H3C CH2CO2C2H5 O O
有机合成课件第5章缩合反应
phCHO+C3 H C2 H C2 HCC3 H
O
浓 HClPhCCHCC3 H
C2 H C3 H
O
phCHO +
CH3
O
PhCH
CH3
NaOH,ROH
回流
O
HCl PhC2H
63%
CH3 略
CHO +
C3 H
H2C CO
Байду номын сангаас
EtONa
CHO H2C
C3 H
C3 H O
C3 H
ph C C ph
ph
a. 反应机理:碱催化
O
O
RCH 2 RCH 2 RCH 2
C
R' + B -
O
O
C + CH C R'
R'
R
OH
O
C C C R'
RCH
C R' + HB
O
O
H RCH 2 C C C R'
R' R
HB
OH
O
B-
H
RCH 2 C C C R'
R' R
O
R' R
HB RCH 2 C C C R' + H 2O + B -
第五章 缩合反应
一.概述 1.概念
凡两个或两个以上有机化合物分子之间相 互反应,形成一个新链,同时放出简单分 子 ;(H2O,ROH, 氨 , HX 等 ) 或 两 个 有 机 物 分 子通过加成形成较大分子的反应均称为缩 合反应(Condensation Reaction)
有机合成 第5章 重排反应
2019/9/20
第三章
3
反应机理:
2019/9/20
第三章
4
实例
OH Ph Me
OH H+ H+
O
Ph Ph Me
OH
Ph
Me
OH
-
H+
Ph
O
Me
O OH
H2SO4
HO
2019/9/20
第三章
5
补充:Wagner—Meerwein重排
例1
例2
2019/9/20
第三章
6
例3 例4
2019/9/20
• The Demjanov rearrangement (named after its discoverer Nikolai Demyanov) is the chemical reaction of primary amines with nitrous acid to give rearranged alcohols. Both ring enlargement or contraction can occur.
2019/9/20
第三章
23
八、氢过氧化物重排(氧正离子)
R
R
H+
R
OH
R
O
R
O + R OH
• 氢过氧化物中,烃基移位的次序: Ar>叔R>仲R>Pr=H>Et>>Me
2019/9/20
第三章
24
反应机理:
R R R
H+ OH
O
R R R
OH2+ O
R R
R
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
另外,一种称为“ate”complex的中间体的转化和重排也是合成烯烃的 重要方法。
使用消除反应的例子也是多种多样的,Conforth等设计了下列方法获 得角鲨烯 (squalene)。
在这些内容开始之前,我们还想分析一下合成策略中的“汇聚 式合成”(convergent synthesis)所带来的立体化学组合问题。将分 子M1和M2连接在一起时,有16种可能的组合。下表中:N为非手性 底物,反应发生在非手性位置;N*为手性底物,反应发生于非手性 位置;P为非手性底物,反应发生在潜手性位置;P*为手性底物,反 应发生在潜手性位置。
我们以带有一个手性的底物∑*和试剂E产生两个产物∑*—E和∑*—为例进 行自由能与选择性之间关系的讨论。如果∑*—E比∑*— 稳定,反应中一系 列物种的能量则可以用图5.1表示,反之,可以用图5.2表示。
现代有机合成化学
第五章 不对称合成
但是不论哪一种情况,过渡态[∑*—E]≠的能量比另一种过渡态[∑*— ]≠ 低是不可改变的。因此,如果反应由动力学控制,那么产物∑*—E的形成在a和 b两种情况下均是有利的。反应如果受热力学控制,两种情况就不一样了,第一 种情况下∑*—E仍为主要产物;第二种情况中∑*— 就成了优势产物。因此, 对于第二种情况,通过一定的实验条件控制是有可能分别得到两种非对映体中 的某一种。
对于一个结构较为复杂的目标分子来说,反应的选择性自然是相 当重要的。选择性的结果自然与底物结构有着重要的关系,如何引入 分子中的第一个手性中心则更是重要。近年来许许多多的策略和方法 被用来满足对映纯化合物的合成。从广义上,不对称合成包括对映体 拆分、手性源方法和立体选择性反应等,在本章中,我们将集中分析 通常指的狭义的不对称合成,即立体选择性反应。立体选择性反应又 可以分成三个主要大类:
O
+
RH
BG2*
OBG*2 R
OH R
OBG*2
>R H2O,NaOH
OH R
现代有机合成化学
第五章 不对称合成
这样的处理方法对催化反应也适应,例如由手性的Lewis酸碱催化的反应。 反应中某一个基态物种为试剂—催化剂或底物—催化剂的结合物,并且最初的 反应底物也包括催化剂。在过渡金属络合物催化的反应中,反应的瞬间中间体 也是非对映关系的结合物,同样这一原理也是适用的。下面我们讨论这种一步 反应的情况。 1.一步反应
应中就可能 发生动力学拆分效果。
接下来我们将分类具体讨论不对称合成反应。
5.2烯烃的立体控制合成
烯烃的立体控制合成除了炔烃的还原、炔烃的加成,还可以通过消除反应、 周环反 应和环裂解反应等实现。本教材的第二章中,我们已经叙及了炔烃的还 原法,在此将介绍一下后面的几种反应。
现代有机合成化学
第五章 不对称合成
现代有机合成化学
第五章 不对称合成
反应产物的立体选择性与相应的过渡态自由能差(△△G#) 及产物的自由能差(△△G°)密切相关。通过分子力学计算可 得到一个定量的参考数据来指导试剂和反应条件的选择等。下 面我们对过渡态理论在不对称诱导中的作用[3a]作一简要介绍。
现代有机合成化学
第五章 不对称合成
现代有机合成化学
第五章 不对称合成
·非对映选择性反应(diastereoselective reactions) ·对映选择性反应(enantioselective reactions) ·双立体差异反应(double stereodifferentiating reactions)或双不对称 反应(doubleasymmetric reactions) 本章的内容就是按照这一分类叙述的。
现代有机合成化学
第五章 不对称合成
假定底物中其他的手性中心对反应不产生影响而且反应物是对映纯的, 那么: 1.N1N2、N1N2*、N1*N2、N1*N2*没有新的手性中心产生。 2.N1P2、P1N2将产生一对消旋体。 3.P1P2将产生两对不等量的消旋体。 4.N1*P2、P1N2*、N1P2*、P1*N2将产生两个不等量的非对映异构体。 5.N1*P2*、P1*N2*将产生两个不等量的非对映异构体。 6.P1P2*、P1*P2产将产生四个非对映异构体。 7.P1*P2*将产生四个非对映异构体。 另外,如果汇聚式合成中一个底物是光学纯的,另一个是消旋体,在反
根据Curtin-Hammett规则,当k1'和k2'相对于速率常数k1、k-1、k2、 k-2很小时,那么I1*和I2*呈快速平衡状态,因此反应立体选择性还是 取决于过渡态的自由能差值,即:
[∑* - E]/[∑*-3] = e△△G≠/RT
现代有机合成化学
第五章 不对称合成
图5.4表示稳定的中间体Il*也是较活泼的中间体的情况,kl’> k2’;而图5.5则表示稳定的中间体Il*却是不活泼的情况。这种情况 下的动力学就比较复杂,并有前文提及的isoinversion现象,选择性 可能依赖于温度和压力。有证据[3c]表明Rh催化的碳碳双键的氢化就遵 循这种机理。
e [∑* - E]/[∑*-3] = △△G≠/RT
现代有机合成化学
第五章 不对称合成
从上式可以发现产物比例与温度相关,选择性与温度呈递减关系。 下表列出一些在25℃(298K)时,竞争性过渡态差值△△G≠与产物比例 的大致关系[3d]。
比率
de(%) △△G≠
比率 De(%) △△G≠
(kcal/mol)
AD BD
取代
AD BE
AE
加成
D
BD
现代有机合成化学
第五章 不对称合成
另一类反应则通过对meso化合物的去对称化(desymmetry)得以实现。
A
A
B
B
D
D
A
E
B
B
D
D
BA
A
B
E B
A B
D
D
EF
D
D
G A
D E
A B D
F
BA
A
G
D
D
EF
现代有机合成化学
第五章 不对称合成
另外,对双键几何异构体(E/Z,或trans/cis)的控制问题也是不对称合 成的一部分。这些都将在后文中详细叙述。
第五章 不对称合成
现代科学在分子层次的发展和要求,尤其是人们对复杂分子对映体 不同生理作用的深入了解,推动了现代有机合成化学领域中不对称合成 研究的迅速发展。对于含多个手性中心的有机分子的合成最关键的问题 常常是对立体化学的控制,这不仅需要良好的合成设计,而且还要选择 最佳的立体控制合成反应。从理论上讲,一个含n个手性中心的分子如 不含某些对称元素则应该存在2n个立体异构体。如果合成中不采取任何 立体控制办法,即使每步反应产率均为100%,实际每步有效产率也只 有50%,经多步反应后,总效率将急速下降,尤其在整个操作过程中对 立体异构体的分离简直是一种混沌状态。正因为这些因素,不对称合成 成为最近20年中发展最为迅速也最有成就的领域。
现代有机合成化学
第五章 不对称合成
多数动力学控制的反应选择性与其两种过渡态之间的自由能差密 切相关。
△△G≠ = (G≠∑*-E)-(G≠∑*-3)
而自由能则与熵(S)和焓(H)有如下关系:
△△G≠= △△H≠-T△△S≠
现代有机合成化学
第五章 不对称合成
多数情况下,两种非对映关系的过渡态之间的熵变相差是很小的,因此焓变 项成为决定因素。但是熵变项并不总是可以忽略不计,再某些条件下可能成为 主要因素[3c],这样选择性就与反应的温度变化密切相关,有可能通过温度的 改变而获得相反的选择性。当达到△△H≠=T△△S≠ 时,转折点的温度被称为 isokinetic temperature (isoinversion)。这种情况的发生不太频繁,但往 往在多步过程中被观察到。 动力学控制条件下非对映产物的比例可以用下式表述:
O
R
OG* + R' M
O
-O+M R
COOG* *GOOC
R'
R
O-M+ R'
∑*-E
>
∑*-3
H2O
HOH2C
HOH2C
OH LiAlH4 HO COOG* *GOOC OH
R R'
R R'
R R'
R R'
现代有机合成化学
第五章 不对称合成
同样,当反应试剂带有一个手性时,它与前手性的底物反应也产 生一样的效果。下面是一个手性硼试剂与醛的反应图解。
现代有机合成化学
第五章 不对称合成
目录
5.1
简介
5.2 烯烃的立体控制合成
5.3
非对映选择性合成
5.4
对映选择性合成
5.5
双立体差异反应
5.6 “绝对”不对称合成
现代有机合成化学
第五章 不对称合成
5.1 简 介
在底物中引入新的手性中心通常有两种方式:一种是通过对双键 (包括碳碳双键和碳杂双键)的面选择性加成;另一种则是对非手性化 合物的取代反应,包括对映选择性和非对映选择性反应。
(kcal/mol)
1.0
0.0
0.00
19.0 90.0
1.74
3.0
50.0
0.65
99.0 98.0
2.72
9.0
80.0
1.30
99.9 99.8
4.09
现代有机合成化学
Байду номын сангаас
第五章 不对称合成
2.多步反应[3e] 相对于一步反应的情形,多步反应的选择性与决速步骤没有绝对
