磷酸氢二钠柠檬酸缓冲液
常用缓冲溶液的配制方法

常用缓冲溶液的配制方法磷酸氢二钠–柠檬酸缓冲液24Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液含35.01克/升。
C 4H 2O 7·H 2O 分子量 = 210.14,0.1 mol/L 溶液为21.01克/升。
pH 4.0 20mL :Na2HPO4 0.219g + C4H2O7·H2O 0.258g柠檬酸–柠檬酸钠缓冲液(0.1 mol/L )6872柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升。
pH 4.0 20mL : C4H2O7·H2O 0.275g + Na3 C6H5O7·2H2O 0.203g乙酸–乙酸钠缓冲液(0.2 mol/L )Na 2Ac·3H 2O 分子量= 136.09,0.2 mol/L 溶液为27.22克/升。
pH 4.0 20mL :NaAc 0.098g + HAc 0.282mL甘氨酸–氢氧化钠缓冲液(0.05M )甘氨酸分子量=75.07; 0.2M溶液含15.01克/升。
pH 10.0 20mL :甘氨酸0.075g + NaOH 0.013g碳酸钠-碳酸氢钠缓冲液(0.1M ) 2+2+ 无水Na 2CO 2分子量=105.99;0.1M 溶液为10.60克/升。
Na 2CO 2·10H 2O 分子量=286.2;0.1M 溶液为28.62克/升。
Na 2HCO 3分子量=84.0;0.1M 溶液为8.40克/升。
pH 10.0 20mL :无水碳酸钠 0.127g +碳酸氢钠0.067g补注:pH 4.0 EDTA2-McIlvaine2O0. 05 mol/L EDTA(372.2)+ 0. 06 mol/L Na2HPO4·12HO(358.14)+ 0. 08 mol/L 柠檬酸(210.14)18. 61g/L EDTA + 21. 4884 g/L Na2HPO4·12HO + 16.8112 g/L 柠檬酸20mL 0. 372g EDTA + 0. 430 g Na2HPO4 ·12HO + 0.336 g 柠檬酸。
常用缓冲溶液配制方法

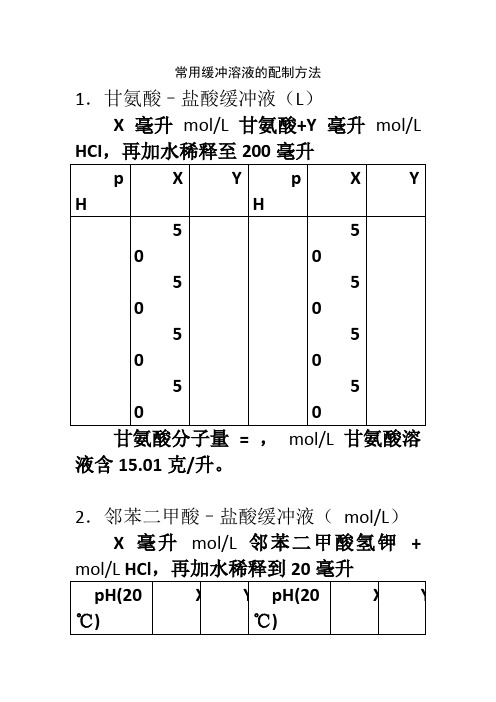
常用缓冲溶液配制方法 Prepared on 24 November 2020常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(L)X毫升 mol/L甘氨酸+Y毫升 mol/L HCI,再加水稀释至200毫升甘氨酸分子量 = , mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液( mol/L)X毫升 mol/L邻苯二甲酸氢钾 + mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量 = , mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na2HPO4分子量 = , mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量 = , mol/L溶液含35.01克/升。
C4H2O7·H2O分子量 = , mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液( mol/L)柠檬酸C6H8O7·H2O:分子量, mol/L溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O:分子量, mol/L溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液( mol/L)Na2Ac·3H2O分子量 = , mol/L溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液()Na2HPO4·2H2O分子量 = , mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量 = , mol/L溶液为克/升。
NaH2PO4·2H2O分子量 = , mol/L溶液为克/升。
磷酸盐是化学研究中使用最广泛的一种缓冲剂,由于它们是二级解离,有二个pKa 值,所以用它们配制的缓冲液,pH 范围最宽:NaH2PO4: pKa1=,pKa2=;Na2HPO4:pKa1=,pKa2=配酸性缓冲液:用NaH2PO4,pH=1~4,配中性缓冲液:用混合的两种磷酸盐,pH=6~8,配碱性缓冲液:用Na2HPO4,pH=10~12。
常用缓冲溶液配制方法

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(L)X毫升 mol/L甘氨酸+Y毫升 mol/L HCI,再加水稀释至200毫升)甘氨酸分子量 = , mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液( mol/L)邻苯二甲酸氢钾分子量 = , mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液Na 2HPO 4分子量 = , mol/L 溶液为28.40克/升。
-Na 2HPO 4·2H 2O 分子量 = , mol/L 溶液含35.01克/升。
C 4H 2O 7·H 2O 分子量 = , mol/L 溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液①使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液( mol/L )6872柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量, mol/L 溶液为29.41克/毫升。
;22#7.磷酸盐缓冲液242Na2HPO4·12H2O分子量 = , mol/L溶液为克/升。
NaH2PO4·2H2O分子量 = , mol/L溶液为克/升。
磷酸盐是生物化学研究中使用最广泛的一种缓冲剂,由于它们是二级解离,有二个pKa 值,所以用它们配制的缓冲液,pH 范围最宽:NaH2PO4: pKa1=,pKa2=;Na2HPO4:pKa1=,pKa2=配酸性缓冲液:用NaH2PO4,pH=1~4,配中性缓冲液:用混合的两种磷酸盐,pH=6~8,配碱性缓冲液:用Na2HPO4,pH=10~12。
《用钾盐比钠盐好,因为低温时钠盐难溶,钾盐易溶,但若配制SDS-聚丙烯酰胺凝胶电泳的缓冲液时,只能用磷酸钠而不能用磷酸钾,因为SDS(十二烷基硫酸钠)会与钾盐生成难溶的十二烷基硫酸钾。
磷酸盐缓冲液的优点为:①容易配制成各种浓度的缓冲液;②适用的pH 范围宽;③pH 受温度的影响小;④缓冲液稀释后pH 变化小,如稀释10倍后pH 的变化小于。
常用缓冲溶液的配制方法

常用缓冲溶液的配制方法1. 磷酸氢二钠–柠檬酸缓冲液 (2)2.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L) (2)3.甘氨酸–盐酸缓冲液(0.05 mol/L) (3)4.邻苯二甲酸–盐酸缓冲液(0.05 mol/L) (3)5.乙酸–乙酸钠缓冲液(0.2 mol/L) (3)6.磷酸盐缓冲液 (3)7.磷酸二氢钾–氢氧化钠缓冲液(0.05M) (4)8.巴比妥钠-盐酸缓冲液(18℃) (4)9.硼酸–硼砂缓冲液(0.2M硼酸根) (5)10.甘氨酸–氢氧化钠缓冲液(0.05M) (5)11.碳酸钠-碳酸氢钠缓冲液(0.1M) (5)12.Tris–盐酸缓冲液(0.05M,25℃) (6)13.硼砂-氢氧化钠缓冲液(0.05M硼酸根) (6)14.PBS缓冲液 (6)15. B-R缓冲溶液配制 (7)16. 常用pH缓冲溶液的配制和pH值 (7)1. 磷酸氢二钠–柠檬酸缓冲液pH0.2mol/LNa2HPO4(mL)0.1mol/L 柠檬酸(mL)pH0.2mol/LNa2HPO4 (mL)0.1mol/L柠檬酸(mL)2.2 2.4 2.62.83.0 3.2 3.4 3.63.84.0 4.2 4.4 4.64.85.0 0.401.242.183.174.114.945.706.447.107.718.288.829.359.8610.3019.6018.7617.8216.8315.8915.0614.3013.5612.9012.2911.7211.1810.6510.149.705.25.45.65.86.06.26.46.66.87.07.27.47.67.88.010.7211.1511.6012.0912.6313.2213.8514.5515.4516.4717.3918.1718.7319.1519.459.288.858.407.917.376.786.155.454.553.532.611.831.270.850.55Na2HPO4分子量= 14.98,0.2 mol/L溶液为28.40克/升。
常用缓冲溶液配制方法
常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(L)X毫升mol/L甘氨酸+Y毫升mol/L甘氨酸分子量= ,mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(mol/L)X毫升mol/L邻苯二甲酸氢钾+邻苯二甲酸氢钾分子量= ,mol/L 邻苯二甲酸氢溶液含40.85克/升Na2HPO4分子量= ,mol/L溶液为28.40克/升。
Na2HPO4·2H2O分子量= ,mol/L 溶液含35.01克/升。
C4H2O7·H2O分子量= ,mol/L溶液为21.01克/升。
①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存。
柠檬酸C 6H 8O 7·H 2O :分子量, mol/L 溶液为21.01克/升。
柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量, mol/L 溶液为29.41克/毫升。
Na2Ac·3H2O分子量= ,mol/L溶液为27.22克/升。
7.磷酸盐缓冲液(1)磷酸氢二钠–磷酸二氢钠缓冲液()Na2HPO4·2H2O分子量= ,mol/L溶液为85.61克/升。
Na2HPO4·12H2O分子量= ,mol/L 溶液为克/升。
NaH2PO4·2H2O分子量= ,mol/L溶液为克/升。
磷酸盐是生物化学研究中使用最广泛的一种缓冲剂,由于它们是二级解离,有二个pKa 值,所以用它们配制的缓冲液,pH 范围最宽:NaH2PO4:pKa1=,pKa2=;Na2HPO4:pKa1=,pKa2=配酸性缓冲液:用NaH2PO4,pH=1~4,配中性缓冲液:用混合的两种磷酸盐,pH=6~8,配碱性缓冲液:用Na2HPO4,pH=10~12。
用钾盐比钠盐好,因为低温时钠盐难溶,钾盐易溶,但若配制SDS-聚丙烯酰胺凝胶电泳的缓冲液时,只能用磷酸钠而不能用磷酸钾,因为SDS(十二烷基硫酸钠)会与钾盐生成难溶的十二烷基硫酸钾。
各种缓冲液的缓冲范围

缓冲液名称及常用浓度缓冲pH范围MES (2吗啉代乙磺酸) 5.5-6.7 Bis-Tris 5.8-7.2 HEPES 6.8-8.2 PIPES 6.1-7.5 MOPS 6.5-7.9 Tricine7.4-8.8 TEA (三乙醇胺)7.4-8.3甘氨酸-盐酸缓冲液(0.05mol/L) 2.2-5.0邻苯二甲酸-盐酸缓冲液(0.05mol/L) 2.2-3.8磷酸氢二钠-柠檬酸缓冲液 2.2-8.0柠檬酸-氢氧化钠-盐酸缓冲液 2.2-6.5柠檬酸-柠檬酸钠缓冲液(0.1mol/L) 3.0-6.6乙酸-乙酸钠缓冲液(0.2mol/L) 3.6-5.8邻苯二甲酸氢钾-氢氧化钠缓冲液 4.1-5.9磷酸氢二钠-磷酸二氢钠缓冲液 5.8-8.0磷酸氢二钠-磷酸二氢钾缓冲液(1/154.92-8.18 mol/L)磷酸二氢钾-氢氧化钠缓冲液(0.05mol/L) 5.8-8.0巴比妥钠-盐酸缓冲液(18℃) 6.8-9.6 Tris-盐酸缓冲液(0.05mol/L 25℃)7.10-9.00甘氨酸-氢氧化钠缓冲液(0.05mol/L)8.6-10.6硼砂-氢氧化钠缓冲液(0.05mol/L)9.3-10.1碳酸钠-碳酸氢钠缓冲液(0.1mol/L)9.16-10.83碳酸钠-氢氧化钠缓冲液(0.025mol/L)9.6-11.0磷酸氢二钠-氢氧化钠缓冲液10.9-12.0氯化钾-盐酸缓冲液(0.2mol/L) 1.0-2.2氯化钾-氢氧化钠缓冲液(0.2mol/L)12.0-13.0主要物质分子量195.2209.2238.3302.4209.3179.2149.2甘氨酸Mr=75.07邻苯二甲酸氢钾Mr=204.23磷酸氢二钠Mr=141.98柠檬酸Mr=192.06柠檬酸Mr=192.06 柠檬酸钠Mr=257.96乙酸钠Mr=81.76 乙酸Mr=60.05邻苯二甲酸氢钾Mr=204.23磷酸氢二钠Mr=141.96 g/mol磷酸二氢钠Mr=119.98 g/mol巴比妥钠Mr=206.18三羟甲基氨基甲烷(Tris)Mr=121.14甘氨酸Mr=75.07硼砂Na2B4O7?10H2O Mr=381.43碳酸钠Mr=286.2 碳酸氢钠Mr=84.0氯化钾Mr=74.55氯化钾Mr=74.55。
各种缓冲液配制方法

各种缓冲液配制方法不同缓冲液的缓冲范围pH缓冲液是化学实验室中常用的一种试剂,可以帮助维持溶液的酸碱度。
下面介绍三种常用缓冲液的配制方法和缓冲范围。
一、甘氨酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L甘氨酸和Y毫升0.2 mol/L 盐酸,加入适量的水稀释至200毫升。
缓冲范围:pH值在2.2至3.6之间,X和Y的取值见上表。
二、邻苯二甲酸-盐酸缓冲液(0.05 mol/L)配制方法:取X毫升0.2 mol/L邻苯二甲酸氢钾和Y毫升0.2 mol/L盐酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至3.8之间,X和Y的取值见上表。
三、磷酸氢二钠-柠檬酸缓冲液配制方法:根据上表中的数据,取相应的0.2 mol/L和0.1 mol/L的Na2HPO4和柠檬酸,加入适量的水稀释至20毫升。
缓冲范围:pH值在2.2至8.0之间,具体取值见上表。
以上缓冲液的配制方法和缓冲范围可根据实验需要进行调整和改变。
在实验过程中,正确选择缓冲液可以提高实验的成功率和准确性。
以下是已经修改好的文章:柠檬酸的浓度可以用毫升表示,其浓度数据如下:9.28 mL8.85 mL8.40 mL7.91 mL7.37 mL6.78 mL6.15 mL5.45 mL4.55 mL3.53 mL2.61 mL1.83 mL1.27 mL0.85 mL0.55 mL对于Na2HPO4,其分子量为141.98,0.2 mol/L的溶液需要28.40 g/L。
而Na2HPO4·2H2O的分子量为178.05,0.2 mol/L的溶液需要35.61 g/L。
最后,Na2HPO4·12H2O的分子量为358.22,0.2 mol/L的溶液需要71.64 g/L。
对于C6H8O7·H2O,其分子量为210.14,0.1 mol/L的溶液需要21.01 g/L。
以下是柠檬酸-氢氧化钠-盐酸缓冲液的相关数据:pH: 2.2.3.1.3.3.4.3.5.3.5.8.6.5钠离子浓度(mol/L): 0.20.0.20.0.20.0.20.0.35.0.45.0.38柠檬酸(g) 氢氧化钠(g) 盐酸(mL)C6H8O7·H2O NaOH 97% HCl (浓)210 210 210210 245 285266 84 8383 144 186156 160 116106 45 68105 126最终体积(L):10使用时可以每升中加入1克酚。
柠檬酸盐缓冲液配制方法

柠檬酸盐缓冲液配制方法柠檬酸盐缓冲液配制方法 1我们经常使用的缓冲溶液,其pH值随温度变化略有变化,要知晓这一点,常用标准缓冲溶液pH值与温度对照表如下:标准缓冲液pH值与温度对照表温度℃四草酸氢钾0.05M邻苯二甲酸氢钾0.05M混合磷酸盐0.025M硼砂0.01M5 1.67 4.00 6.959.3910 1.67 4.00 6.029.3315 1.67 4.00 6.909.2820 1.68 4.00 6.889.2325 1.68 4.00 6.869.1830 1.68 4.01 6.859.1435 1.69 4.02 6.849.11再配制缓冲溶液,不用到处查阅了!柠檬酸盐缓冲液配制方法1,表格展示,轻松一览,赶快收藏吧……柠檬酸盐缓冲液配制方法 11.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2mol/L甘氨酸+Y毫升0.2mol/LHCI,再加水稀释至200毫升pH X Y pH X Y2.05044.03.05011.42.4 2.6 2.850505032.424.216.83.23.43.65050508.26.45.0甘氨酸分子量= 75.07,0.2mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2mol/L邻苯二甲酸氢钾+ 0.2mol/LHCl,再加水稀释到20毫升pH(20℃)X Y pH(20℃)X Y2.2 2.4 2.62.83.0555554.0703.9603.2952.6422.0223.23.43.63.855551.4700.9900.5970.263邻苯二甲酸氢钾分子量= 204.23,0.2mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液pH0.2mol/LNa2HPO4(毫升)0.1mol/L柠檬酸(毫升)pH0.2mol/LNa2HPO4(毫升)0.1mol/L柠檬酸(毫升)2.20.4010.60 5.210.729.282.4 2.62.83.0 3.2 3.4 3.63.84.0 4.2 4.4 4.64.85.01.242.183.174.114.945.706.447.107.718.288.829.359.8610.3018.7617.8216.8315.8915.0614.3013.5612.9012.2911.7211.1810.6510.149.705.45.65.86.06.26.46.66.87.07.27.47.67.88.011.1511.6012.0912.6313.2213.8514.5515.4516.4717.3918.1718.7319.1519.458.858.407.917.376.786.155.454.553.532.611.831.270.850.55Na2HPO4分子量= 14.98,0.2mol/L溶液为28.40克/升。
