有机化合物 甲烷PPT课件
合集下载
甲烷完整PPT课件

甲烷完整PPT课件
目录
• 甲烷基本概念与性质 • 甲烷制备方法与工艺流程 • 甲烷燃烧反应与能量转换原理 • 甲烷储存运输技术发展现状与挑战 • 甲烷在工业生产和生活中应用案例 • 实验操作注意事项与安全防护措施
01
甲烷基本概念与性质
甲烷定义及分子式
甲烷定义
最简单的有机化合物,由碳和氢 元素组成。
燃烧反应方程式及条件
甲烷燃烧反应方程式
CH4 + 2O2 → CO2 + 2H2O
燃烧条件
需要足够的氧气供应和一定的点燃温度。
能量转换原理及效率分析
能量转换原理
甲烷燃烧时,化学能转化为热能和光 能。
效率分析
燃烧效率受氧气供应、燃烧温度、燃 烧室设计等因素影响,高效燃烧技术 可提高能量转换效率。
环保性能评估及排放标准
与卤素单质发生取代反应,生成卤代 烃。
甲烷在自然界中存在形式
天然气
甲烷是天然气的主要成分,广泛存在于地下 岩石储层中。
沼气
在沼泽地带、污水沟、动物粪便等环境中, 由微生物发酵产生。
煤层气
赋存在煤层中的甲烷,以吸附状态存在于煤 基质颗粒表面。
重要性及应用领域
能源领域
作为燃料,广泛应用于 民用、工业、交通等领
Байду номын сангаас域。
化工原料
用于生产合成氨、甲醇 、甲醛等化工产品。
温室气体
甲烷是一种重要的温室 气体,对全球气候变化
有重要影响。
其他应用
用作制冷剂、发泡剂等 。
02
甲烷制备方法与工艺流程
天然气分离法
01
02
03
天然气成分及性质
天然气主要由甲烷组成, 同时含有少量乙烷、丙烷 等烃类以及硫化氢、二氧 化碳等非烃类成分。
目录
• 甲烷基本概念与性质 • 甲烷制备方法与工艺流程 • 甲烷燃烧反应与能量转换原理 • 甲烷储存运输技术发展现状与挑战 • 甲烷在工业生产和生活中应用案例 • 实验操作注意事项与安全防护措施
01
甲烷基本概念与性质
甲烷定义及分子式
甲烷定义
最简单的有机化合物,由碳和氢 元素组成。
燃烧反应方程式及条件
甲烷燃烧反应方程式
CH4 + 2O2 → CO2 + 2H2O
燃烧条件
需要足够的氧气供应和一定的点燃温度。
能量转换原理及效率分析
能量转换原理
甲烷燃烧时,化学能转化为热能和光 能。
效率分析
燃烧效率受氧气供应、燃烧温度、燃 烧室设计等因素影响,高效燃烧技术 可提高能量转换效率。
环保性能评估及排放标准
与卤素单质发生取代反应,生成卤代 烃。
甲烷在自然界中存在形式
天然气
甲烷是天然气的主要成分,广泛存在于地下 岩石储层中。
沼气
在沼泽地带、污水沟、动物粪便等环境中, 由微生物发酵产生。
煤层气
赋存在煤层中的甲烷,以吸附状态存在于煤 基质颗粒表面。
重要性及应用领域
能源领域
作为燃料,广泛应用于 民用、工业、交通等领
Байду номын сангаас域。
化工原料
用于生产合成氨、甲醇 、甲醛等化工产品。
温室气体
甲烷是一种重要的温室 气体,对全球气候变化
有重要影响。
其他应用
用作制冷剂、发泡剂等 。
02
甲烷制备方法与工艺流程
天然气分离法
01
02
03
天然气成分及性质
天然气主要由甲烷组成, 同时含有少量乙烷、丙烷 等烃类以及硫化氢、二氧 化碳等非烃类成分。
初三化学上学期甲烷-课件

来源和用途
甲烷广泛存在于地球上的矿物、化石燃料和生物体内,被广泛用于化工、生产和能源领域。
甲烷的组成和结构
分子组成和结构
甲烷分子由一个碳原子和四个氢原子构成,采 用正四面体构型。
化学键结构分析
甲烷的化学键分量包括共价键和σ键,这些键构 成了甲烷分子的基本结构。
甲烷的制备和检验
制备方法
甲烷可以通过天然气解析或碳氢化合物热解等方 法来制备。
总结
甲烷的重要性
综合应用实例
甲烷是一种非常重要、广泛应用的有机物化合物, 是化工和能源领域的重要组成部分。
针对甲烷的特定需求和的创新应用,如基于甲烷 的新型合成材料的研究。
课程回顾和问题答疑
初三化学上学期甲烷-PPT 课件
本PPT课件将详细介绍甲烷的概念、性质、组成、结构、制备、检验、反应 特性和应用技术。带您深入了解这种重要的有机化合物。
甲烷的概述
基本概念
甲烷是一种无色、无味、易燃的气体,化学式为CH4。是天然气的主要成分之一,具有低密度、不溶于水、易燃爆炸等特点。
质量检验方法
可以使用检验器具或质量分析仪来检测甲烷的纯 度和品质。
甲烷的反应特性
1
卤素取代反应
2
甲烷可以和氯气或溴气反应生成卤代 烷。
燃烧反应
甲烷可以在氧气存在下发生剧烈燃烧, 作为一种重要的燃料。
甲烷的应用技术
生产中的应用
甲烷广泛应用于工业加热、电力和烟气除尘等领域。
能源领域的应用
甲烷作为一种清洁、高效、低成本的能源媒介,具有广泛的应用前景。
甲烷广泛存在于地球上的矿物、化石燃料和生物体内,被广泛用于化工、生产和能源领域。
甲烷的组成和结构
分子组成和结构
甲烷分子由一个碳原子和四个氢原子构成,采 用正四面体构型。
化学键结构分析
甲烷的化学键分量包括共价键和σ键,这些键构 成了甲烷分子的基本结构。
甲烷的制备和检验
制备方法
甲烷可以通过天然气解析或碳氢化合物热解等方 法来制备。
总结
甲烷的重要性
综合应用实例
甲烷是一种非常重要、广泛应用的有机物化合物, 是化工和能源领域的重要组成部分。
针对甲烷的特定需求和的创新应用,如基于甲烷 的新型合成材料的研究。
课程回顾和问题答疑
初三化学上学期甲烷-PPT 课件
本PPT课件将详细介绍甲烷的概念、性质、组成、结构、制备、检验、反应 特性和应用技术。带您深入了解这种重要的有机化合物。
甲烷的概述
基本概念
甲烷是一种无色、无味、易燃的气体,化学式为CH4。是天然气的主要成分之一,具有低密度、不溶于水、易燃爆炸等特点。
质量检验方法
可以使用检验器具或质量分析仪来检测甲烷的纯 度和品质。
甲烷的反应特性
1
卤素取代反应
2
甲烷可以和氯气或溴气反应生成卤代 烷。
燃烧反应
甲烷可以在氧气存在下发生剧烈燃烧, 作为一种重要的燃料。
甲烷的应用技术
生产中的应用
甲烷广泛应用于工业加热、电力和烟气除尘等领域。
能源领域的应用
甲烷作为一种清洁、高效、低成本的能源媒介,具有广泛的应用前景。
甲烷ppt

※取代反应与置换反应的比较:
取代反应 可与化合物发生取 代,生成物中不一定 有单质 反应能否进行受外界 条件(温度、光照、催 化剂等)影响较大 逐步取代,很多反应 是可逆的 置换反应 反应物、生成物中一 定有单质 在水溶液中进行的置 换反应遵循金属活动 性顺序 反应一般单方向进行
1、下列关于烃的说法中,正确的是( D ) A.烃是指分子里含有碳、氢元素的化合物 B.烃是指分子里含碳元素的化合物 C.烃是指燃烧反应后生成二氧化碳和水的有 机物 D.烃是指仅由碳和氢两种元素组成的化合物
注:
(1)甲烷与氯气反应可能有五种产物,其
中有两种气体产物。 (2)有机反应很复杂,产物较多。
(3)多数有机物都难溶于水,易溶于
有机溶剂。
3.分解反应:
CH4 C 2H2
高温
其产物:
H2 是合成氨及合成汽油等工业的原料。
C 是橡胶工业的原料,可以用于制造颜料、 油墨、油漆等
注:多数有机物熔点低,受热易分解。
3.然后再写少两个碳原子的直链:把剩下的两个碳原子当作一个支链 加在主链上:
显然,与 相同。 4. 然后再将两个碳原子分成两个支链加在第二个碳上,就得到: C(CH3)4
C6H14的同分异构体有几种?
二、最简单的有机பைடு நூலகம்——甲烷
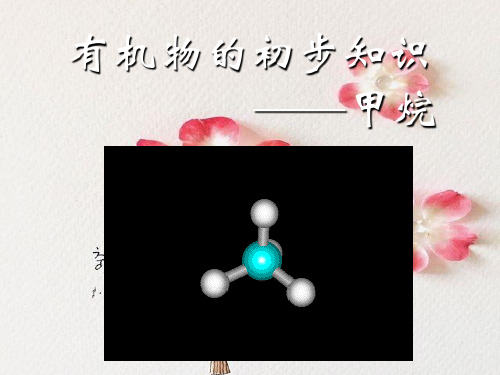
(一)甲烷的分子结构(化学式:CH4)
结构式:用一条短线表示一对共用电子对 的图式。
甲烷分子 的 比例模型
甲烷分子的立体结构(球棍模型)
※甲烷结构特点 ( 以碳原子为中心, 四个氢原子为顶点) 1、正四面体、 2、原子不共面、 3、键角:109度28 分
(二)形成: 甲烷俗称沼气,是在隔绝
第一节 最简单的有机化合物 --- 甲烷
《最简单的有机化合物-甲烷》ppt课件

最简单的有机化合物-甲烷ppt课 件
目 录
• 甲烷基本概念与性质 • 甲烷合成方法与途径 • 甲烷应用领域及价值体现 • 甲烷对环境影响及治理措施 • 实验室制备和检测技术方法论述 • 总结回顾与拓展延伸思考
01 甲烷基本概念与性质
甲烷定义及结构特点
甲烷定义
最简单的有机化合物,化学式为 CH4,由一个碳原子和四个氢原子 组成。
发生火灾时,应使用干粉灭火 器或二氧化碳灭火器进行灭火
,禁止用水灭火。
发生人身伤害时,应立即进行 急救处理,并及时就医治疗。
06 总结回顾与拓展延伸思考
关键知识点总结回顾
01
甲烷的分子结构和性质
甲烷是最简单的有机化合物,分子式为CH4,具有正四面体结构,性质
稳定,不易发生化学反应。
02 03
甲烷的制备和用途
氯甲烷等衍生物
甲烷还可以与氯气等反应,生成氯甲烷等一系列 有机氯化物,用于生产塑料、橡胶等。
环保领域应用(如垃圾填埋气回收)
垃圾填埋气回收
在垃圾填埋场中,有机物在厌氧条件下分解产生甲烷,通过收集和利用这些甲 烷,可以减少温室气体排放并回收能源。
生物质能源
利用农作物秸秆、畜禽粪便等生物质资源发酵产生甲烷,进而生产生物质燃气 或发电,实现资源的循环利用。
04 甲烷对环境影响及治理措 施
温室气体效应分析
甲烷的温室效应
甲烷是一种强效温室气体,其温室效应潜力值远高于二氧化碳, 对全球气候变化具有重要影响。
甲烷排放源
甲烷排放主要来源于能源、农业、废弃物处理等领域,其中能源领 域的排放占比较大。
甲烷浓度变化
随着人类活动的不断增加,大气中甲烷浓度不断上升,加剧了全球 气候变化。
目 录
• 甲烷基本概念与性质 • 甲烷合成方法与途径 • 甲烷应用领域及价值体现 • 甲烷对环境影响及治理措施 • 实验室制备和检测技术方法论述 • 总结回顾与拓展延伸思考
01 甲烷基本概念与性质
甲烷定义及结构特点
甲烷定义
最简单的有机化合物,化学式为 CH4,由一个碳原子和四个氢原子 组成。
发生火灾时,应使用干粉灭火 器或二氧化碳灭火器进行灭火
,禁止用水灭火。
发生人身伤害时,应立即进行 急救处理,并及时就医治疗。
06 总结回顾与拓展延伸思考
关键知识点总结回顾
01
甲烷的分子结构和性质
甲烷是最简单的有机化合物,分子式为CH4,具有正四面体结构,性质
稳定,不易发生化学反应。
02 03
甲烷的制备和用途
氯甲烷等衍生物
甲烷还可以与氯气等反应,生成氯甲烷等一系列 有机氯化物,用于生产塑料、橡胶等。
环保领域应用(如垃圾填埋气回收)
垃圾填埋气回收
在垃圾填埋场中,有机物在厌氧条件下分解产生甲烷,通过收集和利用这些甲 烷,可以减少温室气体排放并回收能源。
生物质能源
利用农作物秸秆、畜禽粪便等生物质资源发酵产生甲烷,进而生产生物质燃气 或发电,实现资源的循环利用。
04 甲烷对环境影响及治理措 施
温室气体效应分析
甲烷的温室效应
甲烷是一种强效温室气体,其温室效应潜力值远高于二氧化碳, 对全球气候变化具有重要影响。
甲烷排放源
甲烷排放主要来源于能源、农业、废弃物处理等领域,其中能源领 域的排放占比较大。
甲烷浓度变化
随着人类活动的不断增加,大气中甲烷浓度不断上升,加剧了全球 气候变化。
甲烷PPT精品课件
我也要象他一 样,做一个出
名的商人
第一个◎通过 了解姓氏文化, 提高文化认同 感。
第二个◎通过饮 食文化、服饰文 化和书法艺术, 感受民族文化的 魅力。
我们聪明勤劳的祖先是怎样赋 予龙的形象?
这些动物的部位与龙的个性 特征和本领有什么联系?
龙,作为中华民族的图
腾,婆娑了浩渺的美丽传说之树,澎 湃了浩瀚的神话故事之海洋,绘制了 夺目的锦绣画卷,演驿了动魄的撼世 乐章,缔造了傲世的缤纷历史,造就 了英雄的精彩人生,形成了我中华民 族所特有的龙文化。龙女拜观音,东 海龙王塌东京,杯弓蛇影,叶公好 龙…
龙文化的久远,龙文化的深厚, 不仅在东方永远闪光,在世界历史上 也永远闪光!
多姿多彩龙的 形象给我们带 来的不同感受
从一个个龙的故事到一个个龙的形象,从一篇篇
龙的传说到一种种龙的精神,神话中,我们领略到了
龙的威武与高大,神话中,我们感受到了龙的神圣与
伟大,神话中,我们了解了龙的传统与历史,神话中,
活动感受
通过“民间文化——我们身 边的文化宝藏”这一活动, 了解和认识身边的文化现象, 领略文化的魅力,增强文化 认同感。
贾路娄危 江童颜郭 梅盛林刁 钟徐邱骆 高夏蔡田 樊胡凌霍 虞万支柯 咎管卢莫 经房裘缪 干解应宗 丁宣贲邓 郁单杭洪 包诸左石 崔吉钮龚 程嵇邢滑 裴陆荣翁 荀羊於惠 甄魏家封 芮羿储靳 汲邴糜松 井段富巫 乌焦巴弓 牧隗山谷 车侯宓蓬 全郗班仰 秋仲伊宫 宁仇栾暴 甘钭厉戎 祖武符刘 景詹束龙 叶幸司韶 郜黎蓟薄 印宿白怀 蒲台从鄂
万俟司马 上官欧阳 夏侯诸葛 闻人东方 赫连皇甫 尉迟公羊 澹台公冶 宗政濮阳 淳于单于 太叔申屠 公孙仲孙 轩辕令狐 钟离宇文 长孙慕容 鲜于闾丘 司徒司空 亓官司寇 仉督子车 颛孙端木 巫马公西 漆雕乐正 壤驷公良 拓拔夹谷 宰父谷粱 晋楚闫法 汝鄢涂钦 段干百里 东郭南门 呼延归海 羊舌微生 岳帅缑亢 况后有琴 梁丘左丘 东门西门
甲烷 ppt课件

活动探究三 甲烷能与氯气反应吗?
CH4与Cl2的反应
现象: 试管内气体颜色变浅,液面上升,内
壁出现油状液滴,试管中出现少量白雾。
学一学
H
· · H C × H + Cl Cl
H
H
·Байду номын сангаас· H C Cl + H × Cl
H
H
· H C × H
H
Cl ··Cl
学一学
H
H
H C H + Cl Cl 光 H C Cl + H Cl
NaOH溶液
稀硫酸
(滴有石蕊溶液)(滴有石蕊溶液)
活动探究二 甲烷能与高锰酸钾、强酸和强碱反应吗?
通常情况下,甲烷比较稳定,不与 高锰酸钾、强酸和强碱反应。
化学性质
一、甲烷的燃烧
产生淡蓝色火焰, 并放出大量的热
点燃
CH4+2O2
CO2+2H2O
活动探究三 甲烷能与氯气反应吗?
注意:观察实验现象并记录
第三章 有机化合物
最简单的有机化合物 甲烷
观察甲烷——物理性质
自无色无味的气体沼) 密度比空气小(标况 下0.717g/L)) 极难溶于水
温故知新 甲烷的分子结构 电子式: 结构式:
甲烷的分子结构模型
球棍模型
比例模型
验证实验——CH4的稳定性
CH4
验证实验——CH4的稳定性
尾气 收集
酸性KMnO4溶液
H
H
CH4+Cl2 光 CH3Cl+HCl
一氯甲烷(难溶于水的气体)
写一写
H
H
Cl C H + Cl Cl 光 Cl C Cl + H Cl
甲烷PPT教学课件

微粒数为:8×1/8 + 6×1/2 = 4
(3)体心立方:在立方体顶点的微粒 为8个晶胞共享,处于体心的金属原 子全部属于该晶胞。
微粒数为:8×1/8 + 1 = 2 长方体晶胞中不同位置的粒子对晶胞的贡献:
3、甲烷的 分子结 构:
分子式:CH4 电子式: 结构式:
空间构型: 正四面体
4、甲烷的物理性质
甲烷是无色、无 臭的气体,密度是 0.717g/L(标准状 况),极难溶于水。
5、甲烷的化学性质
1、氧化反应:
点燃
CH4+ 2O2
CO2+2H2O
CH4在空气中的爆炸极限:5%~15.4%(V/V)
2、取代反应:分析
• 你知道固体有晶体和非晶体之分吗? • 晶体:具有规则几何外形的固体 • 非晶体:没有规则几何外形的固体 • 能否举例说明?
雪花晶体
食糖晶体 明矾晶体
食盐晶体
单质硫
祖母绿
绿宝石
猫眼石
紫水晶
黄黄水水晶晶
NaCl晶体结构示意图:
ClNa+
金刚石晶体 结构示意图
干 冰 晶 体 结 构
非晶态又称玻璃态
玻璃结构示意图
B M
O
Si
晶体的原子呈周期性排列 非晶体的原子不呈周期性排列
宏观晶体的形貌
立方
1.从外形看,晶体与非晶体有何不同? 2.构成晶体的微粒在空间的排列有何特点?
晶体与非晶体比较
自范性
微观结构
晶体 有(能自发呈现多期性有序排列
非晶 没有(不能自发呈现 粒子排列相对无序 体 多面体外形)
B.晶体有自范性但排列无序
C.非晶体无自范性而且排列无序
(3)体心立方:在立方体顶点的微粒 为8个晶胞共享,处于体心的金属原 子全部属于该晶胞。
微粒数为:8×1/8 + 1 = 2 长方体晶胞中不同位置的粒子对晶胞的贡献:
3、甲烷的 分子结 构:
分子式:CH4 电子式: 结构式:
空间构型: 正四面体
4、甲烷的物理性质
甲烷是无色、无 臭的气体,密度是 0.717g/L(标准状 况),极难溶于水。
5、甲烷的化学性质
1、氧化反应:
点燃
CH4+ 2O2
CO2+2H2O
CH4在空气中的爆炸极限:5%~15.4%(V/V)
2、取代反应:分析
• 你知道固体有晶体和非晶体之分吗? • 晶体:具有规则几何外形的固体 • 非晶体:没有规则几何外形的固体 • 能否举例说明?
雪花晶体
食糖晶体 明矾晶体
食盐晶体
单质硫
祖母绿
绿宝石
猫眼石
紫水晶
黄黄水水晶晶
NaCl晶体结构示意图:
ClNa+
金刚石晶体 结构示意图
干 冰 晶 体 结 构
非晶态又称玻璃态
玻璃结构示意图
B M
O
Si
晶体的原子呈周期性排列 非晶体的原子不呈周期性排列
宏观晶体的形貌
立方
1.从外形看,晶体与非晶体有何不同? 2.构成晶体的微粒在空间的排列有何特点?
晶体与非晶体比较
自范性
微观结构
晶体 有(能自发呈现多期性有序排列
非晶 没有(不能自发呈现 粒子排列相对无序 体 多面体外形)
B.晶体有自范性但排列无序
C.非晶体无自范性而且排列无序
《最简单的有机化合物-甲烷》课件

1804年,法国化学家弗朗索瓦·马丁·安托万·克洛斯发现了甲烷的生成与活火山有关 。
甲烷的物理性质
甲烷是一种无色、无 味的气体。
甲烷在标准状况下是 无色透明的,沸点为 -161.5°C,熔点为182.5°C。
甲烷的分子式为CH4 ,分子量为16.043。
甲烷的化学性质
甲烷是一种非常稳定的化合物, 在常温常压下很难与其他物质发
高效开采技术
随着科技的发展,甲烷的开采技 术也在不断进步,提高开采效率 和安全性是未来的重要发展方向 。
高效利用技术
甲烷作为能源的利用方式多样, 包括直接燃烧、发电、燃料电池 等,未来需要进一步研发高效利 用技术,提高能源利用效率。
甲烷与其他新能源的比较
与太阳能的比较
太阳能是一种可再生能源,但受地理位置和天气影响较大,而甲烷 的分布更广泛,使用更方便。
生物质能源
甲烷可用于生产生物质能 源,如生物柴油和生物质 发电等。
01
甲烷对环境的影响
温室效应
01
甲烷是一种温室气体,能够吸收 和重新辐射热量,从而导致温室 效应。
02
Hale Waihona Puke 甲烷在大气中的浓度增加会导致 全球变暖加剧,进而引发一系列 环境问题,如冰川融化、海平面 上升、气候变化等。
甲烷排放与全球气候变化
沼气中的甲烷
沼气是由有机废弃物在厌氧条件 下发酵产生的气体,主要成分是
甲烷。
沼气可用于家庭和工业燃料,同 时也可用于发电和生产有机肥料
。
沼气的产生和利用有助于减少环 境污染和废弃物处理问题。
生物分解中的甲烷
在生物分解过程中,有机物质在厌氧 条件下被微生物分解产生甲烷。
生物分解技术的研究和应用对于解决 能源和环境问题具有重要意义。
甲烷的物理性质
甲烷是一种无色、无 味的气体。
甲烷在标准状况下是 无色透明的,沸点为 -161.5°C,熔点为182.5°C。
甲烷的分子式为CH4 ,分子量为16.043。
甲烷的化学性质
甲烷是一种非常稳定的化合物, 在常温常压下很难与其他物质发
高效开采技术
随着科技的发展,甲烷的开采技 术也在不断进步,提高开采效率 和安全性是未来的重要发展方向 。
高效利用技术
甲烷作为能源的利用方式多样, 包括直接燃烧、发电、燃料电池 等,未来需要进一步研发高效利 用技术,提高能源利用效率。
甲烷与其他新能源的比较
与太阳能的比较
太阳能是一种可再生能源,但受地理位置和天气影响较大,而甲烷 的分布更广泛,使用更方便。
生物质能源
甲烷可用于生产生物质能 源,如生物柴油和生物质 发电等。
01
甲烷对环境的影响
温室效应
01
甲烷是一种温室气体,能够吸收 和重新辐射热量,从而导致温室 效应。
02
Hale Waihona Puke 甲烷在大气中的浓度增加会导致 全球变暖加剧,进而引发一系列 环境问题,如冰川融化、海平面 上升、气候变化等。
甲烷排放与全球气候变化
沼气中的甲烷
沼气是由有机废弃物在厌氧条件 下发酵产生的气体,主要成分是
甲烷。
沼气可用于家庭和工业燃料,同 时也可用于发电和生产有机肥料
。
沼气的产生和利用有助于减少环 境污染和废弃物处理问题。
生物分解中的甲烷
在生物分解过程中,有机物质在厌氧 条件下被微生物分解产生甲烷。
生物分解技术的研究和应用对于解决 能源和环境问题具有重要意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
光
(一氯甲烷)
(2)
CH 3Cl Cl 2 CH 2Cl 2 HCl
光
(二氯甲烷)
(3) CH 2Cl 2 Cl 2 光 CHCl 3 HCl
(三氯甲烷)
(4)
CHCl 3 Cl 2 CCl 4 HCl
光
(四氯甲烷)
取代反应与置换反应的比较:
取代反应 置换反应 可与化合物发生 反应物、生成物 取代,生成物中不一 中一定有单质 定有单质 在水溶液中进行 反应能否进行受外界 的置换反应遵循金 条件影响较大 属活动性顺序 逐步取代,很多 反应是可逆的 反应一般单方向进行
M=22.4 (标准状况)
2、甲烷在自然界中的存在:
甲烷是池沼底部产生的沼气和煤矿的坑 道所产生的坑道气气体的主要成分。这些 气体中的甲烷都是在隔绝空气的条件下, 由植物残体经过某些微生物发酵的作用而 生成的。此外,在有些地方的地下深处蕴 藏着大量叫做天然气的可燃性气体,它的 主要成分也是甲烷(按体积计,天然气里 一般约含有甲烷80%~97%)。
A、一氯甲烷
C、氯仿
B、二氯甲烷 D、HCl
5、下列关于甲烷的叙述不正确的是( D ) A.甲烷是沼气、坑道气的主要成分 B.通常情况下,甲烷性质较稳定,与 强酸、强碱、强氧化剂均不反应 C.甲烷在空气中燃烧时,火焰不明亮 且无烟 D.甲烷在空气中加热到 1000℃时,分 解成炭黑和氢气
(2000年会考题)下列事实能证明 甲烷分子中是以C 原子为中心的正 四面体结构的是( B ) A CH3Cl只代表一种物质 B CH2Cl2只代表一种物质 C CHCl3只代表一种物质 D CCl4只代表一种物质
H
+ Cl—Cl
光
H
C H
Cl
+H
Cl
分子式 状态 (S T P)
CH3Cl 气态 (g)
取
代
反
应
的
进
程
二氯甲烷的形成 H Cl C H H H
+ Cl—Cl
光
Cl
C H
Cl + H
Cl
分子式 状态 (S T P)
CH2Cl2
液态 (l)
三氯甲烷的形成 Cl
Cl H + Cl—Cl
光
H
C Cl
有机物
1、有机物的涵义: 含碳元素的化合物(CO、CO2、 H2CO3及其盐除外)
2、无机物能转变为有机物的实例:
二氧化碳和氨气在一定条件下可 以转化为尿素和水
3、有机物的种类多 截止20世纪末已经超过了2000 万种,而无机物只有10万种左右。
4、常见的有机化合物: 食物中的淀粉、脂肪、蛋白质、 衣物、各种塑料用具、橡胶制品、 油漆等都是典型的有机物。
成为主要能源之一,是因为它具有不可比拟的 特点,特别是在我国的广大农村,这些特点就 更为显著了。 我国地广人多,生物能资源丰 富。研究表明,在21世纪无论在农村还是城镇, 都可以根据本地的实际情况,就地利用粪便、 桔杆、杂草、废渣、废料等生产的沼气来发电。
例题:把1体积CH4和4体积Cl2组成的 混合气体充入大试管中,将此试管倒 立在盛Na2SiO3的水溶液中,放在光 亮处,片刻后,发现试管中的气体颜 色变 浅 ,试管中的液面上升 ,试 管壁上有油状液滴 出现,水槽中还观 察到 白色的胶状沉淀 。 2H+ + SiO32- = H2SiO3
甲烷的性质与氢气的 性质有何区别???
练习: 1。某气体的燃烧产物是CO2和H2O,且CO2和H2O的质 量比是11:9,此气体是(A ) A..CH4 B.C2H2 C.C2H4 D.C3H6
2.有4mL甲烷和一氧化碳的混合气体,完全燃烧时 恰好用去了3mL的氧气,则此混合气体中甲烷和一 氧化碳的体积比为( B ) A.1:1 C.5:1 B.1:5 D.任意比
b.我国天然气资源十分丰富,NG(天 然气)及LPG(液化石油气)汽车已 进入实施阶,1987年已有5000辆NG 汽车;1988年,中国石油天然气总 公司进行CNG汽车试运行,至今运行 情况良好;上海、广州、深圳、哈 尔滨、成都、西安等地代用燃料车 等都已驶上街头。
c.专家们认为,21世纪沼气在农村之所以能够
2、下列气体的主要成份不是甲烷的是( C ) A 沼气 B 天然气 C 水煤气 D 坑道所产生的气体 3、下列叙述正确的是( B ) A、 有机物一定来自有机体内 B、 有机物与无机物可以相互转化 C、 CO属于有机物 D、 A-B + C-D A-C +B-D 一定属于复 分解反应
4、 在光照条件下,将等物质的量 的甲烷和氯气充分反应得到的产物 的物质的量最多的是( D )
4、受热分解
隔绝空气加热到1000℃以上,甲烷会分 解为炭黑和氢气。
CH4
高温
C+2H2
生成物 H2 是合成氨工业的原料
C 是橡胶工业的原料
取代反应与置换反应的比较:
取代反应 实例 定义 反应物 生成物 电子转移
CH4+Cl2 CH3Cl+HCl
置换反应
Zn+H2SO4=ZnSO4+H2↑
有机物分子里的某些原子 一种单质跟一种化合物反 或原子团被其他原子或原 应,生成另一种化合物和 子团所代替的反应。 另一种单质的反应。 一种化合物和一种单质 或化合物 一般生成两种化合物 发生电子对的偏移 一种单质和一种化合物 另一种化合物和另一种单质 一定发生电子的得失
有机物的特点
1、种类繁多
原 因: 1、碳原子含有4个价 电子,可以跟其它原子形成4个 共价键(碳四价); 2、碳原子相互之间能以共价键结合形成 长的碳链。
C C C C C C C C C C
C
C
烃:仅含碳和氢两种元素 的有机物
第一节
甲烷
一、甲烷的物理性质
1、 甲烷是无色、无味的气体,密 度是0.717g/L(标准状况S.T.P ),极 难溶于水。 密度 –摩尔质量公式:
注意:点燃前必须验纯,否则会发生爆炸!
思考:如何用实验验证甲烷中
含有碳元素和氢元素?
3、取代反应(特征反应)
有机物分子里的某些原子或原子团被 其他原子或原子团所代替的反应
实验现象:量筒内Cl2 的黄绿色逐渐消失,量 筒内壁出现油状液滴, 量筒内水面上升
甲烷的结构式形成卤代物的历程 一氯甲烷的形成
三、甲烷的化学性质: 一般条件下,甲烷与强酸、强 碱或强氧化剂等不起反应,说 明什么问题???
1、稳定性:通常情况下,甲烷比较稳 定,与强酸、强碱和强氧化剂等一般不 发生化学反应。
甲烷与酸性高锰酸钾溶 液、溴水等不反应。
2.氧化反应:
CH 4 2O2 CO 2 2H 2O
点燃
二、甲烷的结构
分子式:CH4,试着写出甲烷的电子式、结构式
结构式:用短线表示一对共用电子对的图式
C-H键角:109028·
空间结构
[思考]上述结构式是否说明甲烷分子的真 实构型是以碳原子为中心,四个氢原子 为顶点的平面正方形? 经过科学实验证明甲烷分子的结构是 正四面体结构,碳原子位于正四面体的 中心,4个氢原子分别位于正四面体的4 个顶点上(键角是10928 )。甲烷的分子 结构比较稳定。
H
C Cl
Cl + H
ClΒιβλιοθήκη 俗称 分子式 状态 (S T P)
氯仿 CHCl3 液态 (l)
四氯甲烷的形成 Cl Cl
C Cl H Cl
+ Cl—Cl
光
Cl
C Cl
Cl + H
Cl
别名 分子式 状态 (S T P)
四氯化碳 CCl4
液态 (l)
甲烷取代反应机理
(1)
CH 4 Cl 2 CH 3Cl HCl
练习:将1mol甲烷和4mol的氯气发生 取代反应,待反应完全后,测得四种 有机取代物的物质的量相等,则消耗 氯气为:
A.0.5mol C.2.5mol
B.2mol D.4mol
1、烃是( C ) A 含有C、H元素的有机物 B 含有C元素的化合物 C 仅由C、H两种元素组成的有机物 D 完全燃烧只生成CO2和H2O的化合 物
是否可逆 有不少是可逆反应
一般是不可逆反应
五、甲烷的用途及前景
1、用途
①甲烷的取代反应产物都是很 好的有机溶剂。 ②热分解产物炭黑是橡胶工 业的重要原料,也可用于制 造颜料、油墨、和油漆等。 ③做气体燃料。
2、前景
a.国内外推广代用燃料(主要成 分是 CH4 )的情况美国、日本、 欧洲是当今世界3个代用燃料开发 、研究、使用的主体,而且都制 订了相应的法规政策,以确保代 用燃料的推广使用。
(一氯甲烷)
(2)
CH 3Cl Cl 2 CH 2Cl 2 HCl
光
(二氯甲烷)
(3) CH 2Cl 2 Cl 2 光 CHCl 3 HCl
(三氯甲烷)
(4)
CHCl 3 Cl 2 CCl 4 HCl
光
(四氯甲烷)
取代反应与置换反应的比较:
取代反应 置换反应 可与化合物发生 反应物、生成物 取代,生成物中不一 中一定有单质 定有单质 在水溶液中进行 反应能否进行受外界 的置换反应遵循金 条件影响较大 属活动性顺序 逐步取代,很多 反应是可逆的 反应一般单方向进行
M=22.4 (标准状况)
2、甲烷在自然界中的存在:
甲烷是池沼底部产生的沼气和煤矿的坑 道所产生的坑道气气体的主要成分。这些 气体中的甲烷都是在隔绝空气的条件下, 由植物残体经过某些微生物发酵的作用而 生成的。此外,在有些地方的地下深处蕴 藏着大量叫做天然气的可燃性气体,它的 主要成分也是甲烷(按体积计,天然气里 一般约含有甲烷80%~97%)。
A、一氯甲烷
C、氯仿
B、二氯甲烷 D、HCl
5、下列关于甲烷的叙述不正确的是( D ) A.甲烷是沼气、坑道气的主要成分 B.通常情况下,甲烷性质较稳定,与 强酸、强碱、强氧化剂均不反应 C.甲烷在空气中燃烧时,火焰不明亮 且无烟 D.甲烷在空气中加热到 1000℃时,分 解成炭黑和氢气
(2000年会考题)下列事实能证明 甲烷分子中是以C 原子为中心的正 四面体结构的是( B ) A CH3Cl只代表一种物质 B CH2Cl2只代表一种物质 C CHCl3只代表一种物质 D CCl4只代表一种物质
H
+ Cl—Cl
光
H
C H
Cl
+H
Cl
分子式 状态 (S T P)
CH3Cl 气态 (g)
取
代
反
应
的
进
程
二氯甲烷的形成 H Cl C H H H
+ Cl—Cl
光
Cl
C H
Cl + H
Cl
分子式 状态 (S T P)
CH2Cl2
液态 (l)
三氯甲烷的形成 Cl
Cl H + Cl—Cl
光
H
C Cl
有机物
1、有机物的涵义: 含碳元素的化合物(CO、CO2、 H2CO3及其盐除外)
2、无机物能转变为有机物的实例:
二氧化碳和氨气在一定条件下可 以转化为尿素和水
3、有机物的种类多 截止20世纪末已经超过了2000 万种,而无机物只有10万种左右。
4、常见的有机化合物: 食物中的淀粉、脂肪、蛋白质、 衣物、各种塑料用具、橡胶制品、 油漆等都是典型的有机物。
成为主要能源之一,是因为它具有不可比拟的 特点,特别是在我国的广大农村,这些特点就 更为显著了。 我国地广人多,生物能资源丰 富。研究表明,在21世纪无论在农村还是城镇, 都可以根据本地的实际情况,就地利用粪便、 桔杆、杂草、废渣、废料等生产的沼气来发电。
例题:把1体积CH4和4体积Cl2组成的 混合气体充入大试管中,将此试管倒 立在盛Na2SiO3的水溶液中,放在光 亮处,片刻后,发现试管中的气体颜 色变 浅 ,试管中的液面上升 ,试 管壁上有油状液滴 出现,水槽中还观 察到 白色的胶状沉淀 。 2H+ + SiO32- = H2SiO3
甲烷的性质与氢气的 性质有何区别???
练习: 1。某气体的燃烧产物是CO2和H2O,且CO2和H2O的质 量比是11:9,此气体是(A ) A..CH4 B.C2H2 C.C2H4 D.C3H6
2.有4mL甲烷和一氧化碳的混合气体,完全燃烧时 恰好用去了3mL的氧气,则此混合气体中甲烷和一 氧化碳的体积比为( B ) A.1:1 C.5:1 B.1:5 D.任意比
b.我国天然气资源十分丰富,NG(天 然气)及LPG(液化石油气)汽车已 进入实施阶,1987年已有5000辆NG 汽车;1988年,中国石油天然气总 公司进行CNG汽车试运行,至今运行 情况良好;上海、广州、深圳、哈 尔滨、成都、西安等地代用燃料车 等都已驶上街头。
c.专家们认为,21世纪沼气在农村之所以能够
2、下列气体的主要成份不是甲烷的是( C ) A 沼气 B 天然气 C 水煤气 D 坑道所产生的气体 3、下列叙述正确的是( B ) A、 有机物一定来自有机体内 B、 有机物与无机物可以相互转化 C、 CO属于有机物 D、 A-B + C-D A-C +B-D 一定属于复 分解反应
4、 在光照条件下,将等物质的量 的甲烷和氯气充分反应得到的产物 的物质的量最多的是( D )
4、受热分解
隔绝空气加热到1000℃以上,甲烷会分 解为炭黑和氢气。
CH4
高温
C+2H2
生成物 H2 是合成氨工业的原料
C 是橡胶工业的原料
取代反应与置换反应的比较:
取代反应 实例 定义 反应物 生成物 电子转移
CH4+Cl2 CH3Cl+HCl
置换反应
Zn+H2SO4=ZnSO4+H2↑
有机物分子里的某些原子 一种单质跟一种化合物反 或原子团被其他原子或原 应,生成另一种化合物和 子团所代替的反应。 另一种单质的反应。 一种化合物和一种单质 或化合物 一般生成两种化合物 发生电子对的偏移 一种单质和一种化合物 另一种化合物和另一种单质 一定发生电子的得失
有机物的特点
1、种类繁多
原 因: 1、碳原子含有4个价 电子,可以跟其它原子形成4个 共价键(碳四价); 2、碳原子相互之间能以共价键结合形成 长的碳链。
C C C C C C C C C C
C
C
烃:仅含碳和氢两种元素 的有机物
第一节
甲烷
一、甲烷的物理性质
1、 甲烷是无色、无味的气体,密 度是0.717g/L(标准状况S.T.P ),极 难溶于水。 密度 –摩尔质量公式:
注意:点燃前必须验纯,否则会发生爆炸!
思考:如何用实验验证甲烷中
含有碳元素和氢元素?
3、取代反应(特征反应)
有机物分子里的某些原子或原子团被 其他原子或原子团所代替的反应
实验现象:量筒内Cl2 的黄绿色逐渐消失,量 筒内壁出现油状液滴, 量筒内水面上升
甲烷的结构式形成卤代物的历程 一氯甲烷的形成
三、甲烷的化学性质: 一般条件下,甲烷与强酸、强 碱或强氧化剂等不起反应,说 明什么问题???
1、稳定性:通常情况下,甲烷比较稳 定,与强酸、强碱和强氧化剂等一般不 发生化学反应。
甲烷与酸性高锰酸钾溶 液、溴水等不反应。
2.氧化反应:
CH 4 2O2 CO 2 2H 2O
点燃
二、甲烷的结构
分子式:CH4,试着写出甲烷的电子式、结构式
结构式:用短线表示一对共用电子对的图式
C-H键角:109028·
空间结构
[思考]上述结构式是否说明甲烷分子的真 实构型是以碳原子为中心,四个氢原子 为顶点的平面正方形? 经过科学实验证明甲烷分子的结构是 正四面体结构,碳原子位于正四面体的 中心,4个氢原子分别位于正四面体的4 个顶点上(键角是10928 )。甲烷的分子 结构比较稳定。
H
C Cl
Cl + H
ClΒιβλιοθήκη 俗称 分子式 状态 (S T P)
氯仿 CHCl3 液态 (l)
四氯甲烷的形成 Cl Cl
C Cl H Cl
+ Cl—Cl
光
Cl
C Cl
Cl + H
Cl
别名 分子式 状态 (S T P)
四氯化碳 CCl4
液态 (l)
甲烷取代反应机理
(1)
CH 4 Cl 2 CH 3Cl HCl
练习:将1mol甲烷和4mol的氯气发生 取代反应,待反应完全后,测得四种 有机取代物的物质的量相等,则消耗 氯气为:
A.0.5mol C.2.5mol
B.2mol D.4mol
1、烃是( C ) A 含有C、H元素的有机物 B 含有C元素的化合物 C 仅由C、H两种元素组成的有机物 D 完全燃烧只生成CO2和H2O的化合 物
是否可逆 有不少是可逆反应
一般是不可逆反应
五、甲烷的用途及前景
1、用途
①甲烷的取代反应产物都是很 好的有机溶剂。 ②热分解产物炭黑是橡胶工 业的重要原料,也可用于制 造颜料、油墨、和油漆等。 ③做气体燃料。
2、前景
a.国内外推广代用燃料(主要成 分是 CH4 )的情况美国、日本、 欧洲是当今世界3个代用燃料开发 、研究、使用的主体,而且都制 订了相应的法规政策,以确保代 用燃料的推广使用。
