山东大学网络教育学院-药物化学1试题及答案
山东大学网络教育学院-药物化学1试题及答案汇编
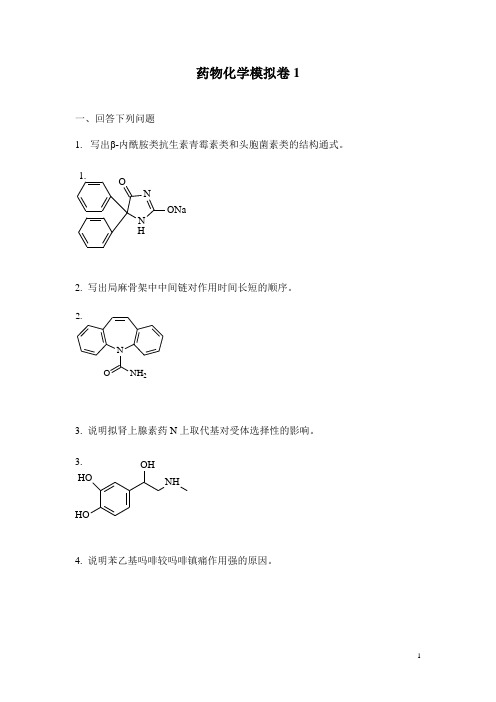
药物化学模拟卷1一、回答下列问题1. 写出 -内酰胺类抗生素青霉素类和头胞菌素类的结构通式。
N NOONa H1.2. 写出局麻骨架中中间链对作用时间长短的顺序。
N NH 2O2.3. 说明拟肾上腺素药N 上取代基对受体选择性的影响。
NHHOHOOH3.4. 说明苯乙基吗啡较吗啡镇痛作用强的原因。
N OOO O NO 2H4.5. 氮芥类抗肿瘤药毒性较大,如何通过结构修饰降低其毒性?N N O NH 2HCl5.6. 在肾上腺皮质激素的C-1、C-6、C-9、C-16和C-21位如何进行结构修饰及结构修饰的目的。
ONHCH 3Cl7. 在雌二醇和睾丸素的C-17α位引入乙炔基的到的化合物各有什么样的生物活性?NNOCH 3Cl8. 比较阿莫西林和氨苄西林聚合速度的快慢并说明原因。
ON PO N ClCH 2CH 2ClCH 2CH 2H二、写出下列结构药物的名称和一种代谢产物N NOONa H1.N NOONa HOH苯妥英钠N NH 2O2.NNH 2OONNH 2OHON H或或卡马西平NHHOHOOH3.CHOHOHOOH NHH 3CO HOOH或肾上腺素N OOO O NO 2H4.N CH 2OHOH OO ONO 2H N OOO ONO 2H 或硝苯地平N N ONH 2HCl5.N N O OH HCl盐酸阿糖胞苷 6.ONHCH 3ClO NHCH 3ClOHONH 2Cl或氯胺酮 7.NNOCH 3ClNNO CH 3ClOHNNO ClOHH 或地西泮 8.ON PO N ClCH 2CH 2ClCH 2CH 2H ON PO N ClCH 2CH 2ClCH 2CH 2OHH N ClCH 2CH 2ClCH 2CH 2H 等环磷酰胺三、写出下列药物的化学结构及主要药理作用 1. 氟尿嘧啶 2. 吡哌酸HN N O OFHN NN ON COOHC 2H 5HN抗癌药 抗菌药3. 布洛芬4. 吗啡OHO非甾体抗炎药 麻醉性镇痛药5. 氢化可的松6. 维生素D 3C OCH 2OH HOOHOCH 2甾体抗炎药 抗佝偻病四 出下列结构的药物名称及主要药理作用NOOH1.米非司酮 抗孕激素OO SOCCH 3O2.螺内酯 保钾利尿药N N NH 2H 2NOCH 3OCH 3OCH 33.甲氧苄啶 二氢叶酸还原酶抑制剂CHCONH NH 2N SO4.头孢来星(头孢氨苄)抗菌药NNOCNH 5.米力农 强心药NS(H 2N)2C=NSNH 2NSO 2NH 26.法莫替丁 抗溃疡药NS 2CH 2CH 2NN CH 2CH 2OHCl7.奋乃静 抗精神病药。
山东大学网络教育学院-药物分析1试题与答案

药物分析模拟题1一、A型题(最佳选择题)每题的备选答案中只有一个最佳答案。
E 1. 我国现行的中国药典为A.1995版B.1990版C.1985版D.2000版E.2005版B 2. 中国药典的英文缩写为A. BPB. CPC. JPD. ChPE. USPC 3. 相对标准差表示的应是A.准确度B.回收率C.精密度D.纯精度E.限度C 4. 滴定液的浓度系指A.%(g/g)B.%(ml/ml)C.mol/LD.g/100mlE.g/100gC 5. 用20ml移液管量取的20ml溶液,应记为A.20mlB.20.0mlC.20.00mlD.20.000mlE.20±1mlA 6. 注射液含量测定结果的表示方法A.主要的%B.相当于标示量的%C.相当于重量的%D.g/100mlE.g/100g E 7. 恒重系指供试品连续两次干燥或炽灼后的重量差为A.0.6mgB.0.5mgC.0.4mgD.0.3mgE.0.2mgC 8. 阿斯匹林中检查的特殊杂质是A.水杨醛B.砷盐C.水杨酸D.苯甲酸E.苯酚E 9. 以下哪种药物中检查对氨基苯甲酸A.盐酸普鲁卡因B.盐酸普鲁卡因胺C.盐酸普鲁卡因片D.注射用盐酸普鲁卡因E.盐酸普鲁卡因注射液E 10. 药品检验工作的基本程序A.鉴别、检查、写出报告B.鉴别、检查、含量测定、写出报告C.检查、含量测定、写出报告D.取样、检查、含量测定、写出报告E.取样、鉴别、检查、含量测定、写出报告C 11.含锑药物的砷盐检查方法为A.古蔡法B.碘量法C.白田道夫法D.Ag-DDCE.契列夫法E 12. 药物中杂质的限量是指A.杂质是否存在B.杂质的合适含量C.杂质的最低量D.杂质检查量E.杂质的最大允许量C 13. 维生素C注射液测定常加哪种试剂消除抗氧剂干扰A.NaClB.NaHCO3C.丙酮D.苯甲酸E.苯酚C 14. 旋光法测定的药物应是A.对氨基水杨酸钠B.盐酸普鲁卡因胺C.葡萄糖注射液D.注射用盐酸普鲁卡因E.盐酸利多卡因A 15. 用来描述TCL板上色斑位置的数值是A.比移值B.比较值C.测量值D.展开距离E.分离度二、B型题(配伍选择题)备选答案在前面,试题在后。
《药物化学》习题总答案【精选文档】

第一章绪论一、单项选择题(1)下面哪个药物的作用与受体无关 (B)(A)氯沙坦(B)奥美拉唑(C)降钙素(D)普仑司 (E)氯贝胆碱(2)下列哪一项不属于药物的功能 (D) (A)预防脑血栓 (B)避孕(C)缓解胃痛(D)去除脸上皱纹(E)碱化尿液,避免乙酰磺胺在尿中结晶.(3)肾上腺素(如下图)的a碳上,四个连接部分按立体化学顺序的次序为 (D)(A)羟基〉苯基〉甲氨甲基〉氢(B)苯基>羟基>甲氨甲基>氢(C)甲氨甲基〉羟基〉氢〉苯基(D)羟基〉甲氨甲基>苯基>氢(E)苯基>甲氨甲基〉羟基>氢(4)凡具有治疗、预防、缓解和诊断疾病或调节生理功能、符合药品质量标准并经政府有关部门批准的化合物,称为(E)(A)化学药物 (B)无机药物(C)合成有机药物(D)天然药物(E)药物(5)硝苯地平的作用靶点为 (C)(A)受体(B)酶(C)离子通道(D)核酸 (E)细胞壁(6)下列哪一项不是药物化学的任务(C)(A)为合理利用已知的化学药物提供理论基础、知识技术。
(B)研究药物的理化性质。
(C)确定药物的剂量和使用方法。
(D)为生产化学药物提供先进的工艺和方法。
(E)探索新药的途径和方法.二、配比选择题(1)(A)药品通用名 (B)INN名称(C)化学名(D)商品名(E)俗名1、对乙酰氨基酚(A)2、泰诺(D)3、Paracetamol (B)4、N—(4—羟基苯基)乙酰胺 (C)5.醋氨酚(E)三、比较选择题(1) (A)商品名 (B)通用名(C)两者都是(D)两者都不是1、药品说明书上采用的名称 (B)2、可以申请知识产权保护的名称 (A)3、根据名称,药师可知其作用类型 (B)4、医生处方采用的名称 (A)5、根据名称,就可以写出化学结构式。
(D)四、多项选择题(1)下列属于“药物化学”研究范畴的是(A,B,C,D)(A)发现与发明新药(B)合成化学药物(C)阐明药物的化学性质(D)研究药物分子与机体细胞(生物大分子)之间的相互作用(E)剂型对生物利用度的影响(2)已发现的药物的作用靶点包括 (A,C,D,E)(A)受体 (B)细胞核 (C)酶(D)离子通道 (E)核酸(3)下列哪些药物以酶为作用靶点 (A,B,E) (A)卡托普利(B)溴新斯的明(C)降钙素(D)吗啡(E)青霉素(4)药物之所以可以预防、治疗、诊断疾病是由于(A,C,D)(A)药物可以补充体内的必需物质的不足(B)药物可以产生新的生理作用(C)药物对受体、酶、离子通道等有激动作用(D)药物对受体、酶、离子通道等有抑制作用(E)药物没有毒副作用(5)下列哪些是天然药物 (B,C,E)(A)基因工程药物 (B)植物药(C)抗生素(D)合成药物 (E)生化药物(6) 按照中国新药审批办法的规定,药物的命名包括(A,C,E)(A)通用名(B)俗名(C)化学名(中文和英文)(D)常用名 (E)商品名(7)下列药物是受体拮抗剂的为 (B,C,D)(A)可乐定 (B)普萘洛尔(C)氟哌啶醇 (D)雷洛昔芬(E)吗啡(8)全世界科学家用于肿瘤药物治疗研究可以说是开发规模最大,投资最多的项目,下列药物为抗肿瘤药的是…………(A,D) (A)紫杉醇(B)苯海拉明(C)西咪替丁 (D)氮芥(E)甲氧苄啶(9)下列哪些技术已被用于药物化学的研究 (A,B,D,E)(A)计算机技术(B)PCR技术(C)超导技术(D)基因芯片 (E)固相合成(10)下列药物作用于肾上腺素的β受体有(A,C,D)(A)阿替洛尔(B)可乐定(C)沙丁胺醇 (D)普萘洛尔(E)雷尼替丁五、问答题(1)为什么说“药物化学”是药学领域的带头学科?(2)药物的化学命名能否把英文化学名直译过来?为什么?(3)为什么说抗生素的发现是个划时代的成就?(4)简述现代新药开发与研究的内容。
最新药物化学网课测试题及答案

药物化学尔雅网课测试题及答案1【单选题】以受体作为药物的作用靶点()A氯贝胆碱B洛伐他汀C硝苯地平D卡托普利2【单选题】阿司匹林以()作为药物的作用靶点A受体B酶C核酸D离子通道3【单选题】硝苯地平以()离子通道作为药物作用靶点,用于治疗高血压A钾B钙C钠D镁4【单选题】国际非专有名,又叫()A化学名B商品名C通用名,D俗名5【单选题】1.40年代是()的时代。
A霉素类抗生素B胺类药物C合成抗生素D素类药物1-1:ABBCA1【单选题】药物化学成为连接()与生命科学并使其融合为一体的交叉学科A物理B化学C数学D生物2【单选题】40年代是()的时代。
A青霉素类抗生素B磺胺类药物C半合成抗生素D激素类药物3【单选题】从()中提纯了吗啡A可卡因B阿片C古柯叶D青蒿4【单选题】阿司匹林是以()药作为上市。
A解热镇痛药B镇静催眠药C抗精神失常D中枢兴奋药5【单选题】口服避孕药是()年代开发的A30B 40C 50D 60BABAD6【单选题】药物的作用靶点究竟有()A受体酶核酸B受体核酸C受体酶核酸离子通道D酶核酸离子通道7【单选题】以受体作为药物的作用靶点()A氯贝胆碱B洛伐他汀C硝苯地平D卡托普利8【单选题】阿司匹林以()作为药物的作用靶点A受体B酶C核酸D离子通道9【单选题】硝苯地平以()离子通道作为药物作用靶点,用于治疗高血压A钾B钙C钠D镁10【单选题】国际非专有名,又叫()A化学名B商品名C通用名,D俗名1-2:BABAD CABBC1【单选题】新药的发现通常分为四个阶段,以下选项不属于四个阶段的内容的是( )A靶分子的确定和选择B先导化合物的发现C先导化合物的优化D药物开发2【单选题】以下用于先导物优化的方法,不正确的是( )A前药设计B软药设计C硬药设计D生物电子等排体替换3【单选题】哪一期的临床试验是在患者身上进行的( )A I期B II期C III期D 都是4【单选题】新药研究开始到上市总共需要多长时间( )A 3到6年B 8到10年C 2到5年D 10到12年5【单选题】以下对新药研发的观点,错误的是()A周期长B回报高C风险低D投资大2-1:DCBBC1【单选题】,下列说法有误的是( )A脂水分配系数呢?它是指药物在正辛醇中和水中分配达到平衡时浓度之比值。
山东大学--网络教育--药物化学1-3答案
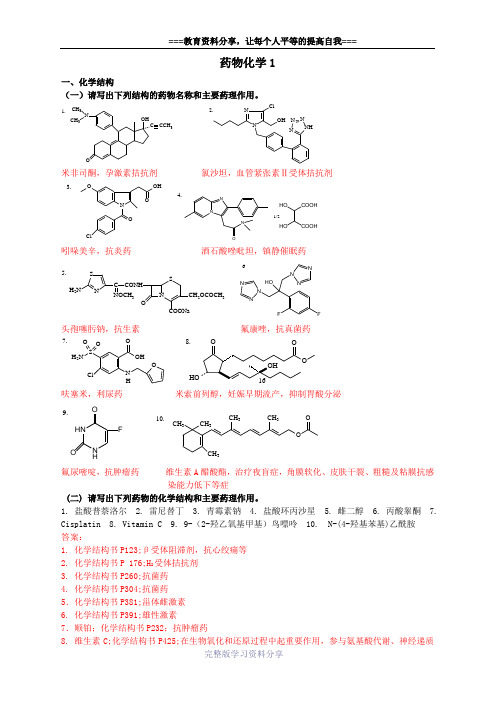
药物化学1一、化学结构(一)请写出下列结构的药物名称和主要药理作用。
OOHCCCH 3NCH 3CH 31.N NNHNN NClOH 2.米非司酮,孕激素拮抗剂 氯沙坦,血管紧张素Ⅱ受体拮抗剂ON OHO OCl 3.NNNO 1/2COOHHOHO 4.吲哚美辛,抗炎药 酒石酸唑吡坦,镇静催眠药S NH 2NC CONH N SONOCH 3COONaCH 2OCOCH 35.NNNHON NNFF 6.头孢噻肟钠,抗生素 氟康唑,抗真菌药OHN SH 2NClO OO OH7.O8.呋塞米,利尿药 米索前列醇,妊娠早期流产,抑制胃酸分泌HN N HFOO9.CH 3CH 3CH 3CH 3CH 3OO10.氟尿嘧啶,抗肿瘤药 维生素A 醋酸酯,治疗夜盲症,角膜软化、皮肤干裂、粗糙及粘膜抗感染能力低下等症(二) 请写出下列药物的化学结构和主要药理作用。
1. 盐酸普萘洛尔2. 雷尼替丁3. 青霉素钠4. 盐酸环丙沙星5. 雌二醇6. 丙酸睾酮7. Cisplatin8. Vitamin C9. 9-(2-羟乙氧基甲基)鸟嘌呤 10. N-(4-羟基苯基)乙酰胺 答案:1. 化学结构书P123;β受体阻滞剂,抗心绞痛等2. 化学结构书P 176;H 2受体拮抗剂3. 化学结构书P260;抗菌药4. 化学结构书P304;抗菌药 5.化学结构书P381;甾体雌激素 6. 化学结构书P391;雄性激素7.顺铂;化学结构书P232;抗肿瘤药8. 维生素C;化学结构书P425;在生物氧化和还原过程中起重要作用,参与氨基酸代谢、神经递质的合成、胶原蛋白和组织细胞间质的合成。
9. 更昔洛韦;化学结构书P334;抗病毒药 ;化学结构书P202;解热镇痛药 二、药物的作用机制(一)请写出下列药物的作用靶点,指出是该靶点的激动剂还是拮抗剂(或阻滞剂或抑制剂)。
1. 他莫昔芬 2. 氯贝胆碱 3. 吗啡抗雌激素 乙酰胆碱受体激动剂 阿片受体激动剂O CH 3O NO 2NCH 3H 3C O H 3COH 4.NNNH 2H 2N CH 2OCH 3OCH 3OCH 35.钙通道阻滞剂 二氢叶酸还原酶抑制剂(二)请写出对下列酶有抑制作用的一种药物名称,及其化学结构和主要药理作用。
药物化学试题及答案大题

药物化学试题及答案大题一、选择题(每题2分,共20分)1. 下列哪项不是药物化学的研究内容?A. 药物的合成B. 药物的分析C. 药物的临床试验D. 药物的代谢答案:C2. 药物化学中,药物的生物等效性指的是:A. 药物的化学结构B. 药物的生物活性C. 药物的药效学性质D. 药物在体内的吸收、分布、代谢和排泄过程答案:D3. 下列哪种化合物不属于抗生素?A. 青霉素B. 头孢菌素C. 阿司匹林D. 红霉素答案:C4. 药物化学中,药物的稳定性研究主要关注:A. 药物的物理性质B. 药物的化学性质C. 药物的生物活性D. 药物的临床效果答案:B5. 下列哪种方法不是药物的合成方法?A. 化学合成B. 生物合成C. 物理合成D. 半合成答案:C6. 药物的溶解度对其药效的影响是:A. 无关紧要B. 影响药物的吸收C. 影响药物的分布D. 影响药物的排泄答案:B7. 下列哪种药物属于非甾体抗炎药?A. 阿司匹林B. 地塞米松C. 胰岛素D. 利血平答案:A8. 药物的半衰期是指:A. 药物在体内的总时间B. 药物在体内的有效时间C. 药物浓度下降一半所需的时间D. 药物的代谢时间答案:C9. 药物化学中,药物的靶向性是指:A. 药物对特定细胞的选择性B. 药物对特定组织的分布C. 药物对特定器官的作用D. 药物对特定疾病的治疗答案:A10. 下列哪种药物属于抗高血压药?A. 阿司匹林B. 利血平C. 胰岛素D. 地塞米松答案:B二、填空题(每题2分,共10分)1. 药物的______是指药物在体内浓度下降到一半所需的时间。
答案:半衰期2. 药物的______是指药物在体内达到最大效应所需的时间。
答案:起效时间3. 药物的______是指药物在体内达到稳态浓度所需的时间。
答案:稳态时间4. 药物的______是指药物在体内被代谢或排泄的速率。
答案:清除率5. 药物的______是指药物在体内达到最大效应的浓度。
山东大学网络教育天然药物化学模拟题(三套、本科)

天然药物化学模拟试题 (一)一、选择题B/B/A/D/D, A/C/D/B/A, B/D/A/C/B,1、下列溶剂中,不能用于与水进行萃取的是( B )A、乙醚B、正丁醇C、乙腈D、苯2、下列化合物中,含有不饱和内酯环的是( B )A、黄酮B、强心苷C、甾体皂苷元D、糖类3、二倍半萜结构母核中含有的碳原子数目为( A )A、25个B、20个C、28个D、23个4、凝胶过滤的洗脱顺序是(D)A、极性小的先出柱B、极性大的先出柱C、分子量小的先出柱D、分子量大的先出柱5、生物碱的沉淀反应中,常有一些化学成分干扰,常与生物碱沉淀试剂发生沉淀反应的成分是( D )A、粘液质、果胶B、单糖、氨基酸C 、树胶、无机盐 D、蛋白质、鞣质6、从水溶液中萃取游离的亲脂性生物碱的最常用溶剂是(A )A、氯仿B、甲醇C、乙酸乙酯D、石油醚7、下列化合物由甲戊二羟酸途径生成的是(C )A、鬼臼毒素B、水飞蓟素C、甘草酸D、肝素8、下列哪项不是甾体皂苷的性质( D )A、溶血性B、表面活性C、挥发性D、与胆甾烷发生沉淀9、具有抗老年性痴呆活性的天然产物是( B )A、水飞蓟素B、穿心莲内酯C、长春碱D、石杉碱甲10、最容易酸水解的是苷类是( A )A、-羟基糖苷B、-氨基糖苷C、6-去氧糖苷D、2,6-二去氧糖苷11、糖和苷之联结位置的获知有( B )A、乙酰解B、酸水解C、碱水解D、全甲基化后醇解12、环烯醚萜类的结构特点是( D )A、具有C6-C3-C6的结构B、具有半缩醛和环戊烷C、具有不饱和内酯环D、具有环戊烷骈多氢菲结构13、区别甲型强心苷和乙型强心苷的依据是( A )A、甾体母核的取代情况B、甾体母核的氧化情况C、侧链内酯环的差别D、苷元与糖连接位置的差别14、下列哪一项不是挥发油中的组成成分( C )A、小分子萜类B、高级脂肪酸或酯C、苯丙素衍生物D、小分子脂肪族化合物15、具有抗肿瘤活性的天然化合物是( B )A、五味子素B、长春碱C、银杏内酯D、青蒿素二、用适当的化学方法鉴别下列各组化合物(标明反应所需化学试剂以及所产生的现象 )1、用Fehling试剂,A(葡萄糖)没有明显变化,B(果糖)呈现砖红色沉淀2、运用Molish反应,A(苷类)反应呈阳性在液面交界处出现紫红色环,B无变化3、先用Feigl反应,A、B(醌类)出现紫色,C无变化,然后用Borntragers反应(加入NaOH)→A(羟基蒽醌)出现红色,B无变化4、用FeCl3试剂,A无变化,B中酚羟基使其显紫色三、分离下列各组化合物(化学法指明所用试剂、现象和结果;层析法指明吸附剂或固定相,展开剂或流动相,Rf值大小或出柱先后顺序)1、2、3、参考答案:1、采用聚酰胺柱层析分离,以含有聚酰胺作为固定相,以乙醇-水混合溶剂作为洗脱剂,R f大小顺序为:C>A>B。
药学《有机化学》山东大学网络教育考试模拟题及答案
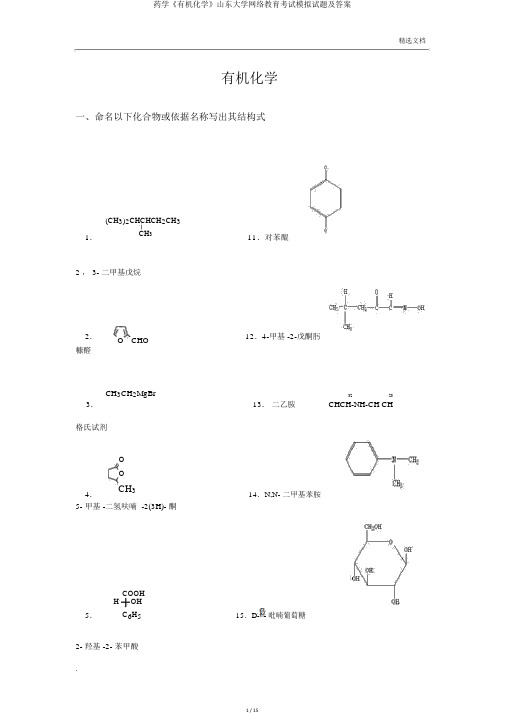
精选文档有机化学一、命名以下化合物或依据名称写出其结构式(CH3)2CHCHCH2CH31.CH3 11 .对苯醌2 , 3- 二甲基戊烷2.O CHO 12.4-甲基-2-戊酮肟糠醛3.CH3CH2MgBr13.二乙胺32 23CHCH-NH-CH CH格氏试剂OO4.CH314.N,N-二甲基苯胺5- 甲基 -二氢呋喃 -2(3H)- 酮COOHH OH5.C6H5 15.D- -吡喃葡萄糖2- 羟基 -2- 苯甲酸CH 3 6.CH 3顺 -1,2- 二甲基环己烷+-N 2 Cl7.苯基重氮盐酸盐CHCH 3 8.OH1- 苯 -1- 乙醇9.Cl CH 3 CH 3CH 2C CCl反 -2,3- 二氯 -2- 戊烯OC O C10.O邻苯二甲酸酐二、用结构式表示以下名词术语1. 季铵碱R 4N + OH -精选文档16.邻苯二甲酰亚胺17. 二苯醚18. 4-氨基吡啶NHNH NH2219. 2,4 二硝基苯肼20 . 水杨酸2. 对映异构体ClClClCl3.结构异构体CH3CH3H3 C CH3H3C三、达成以下反响式1.NaNH 2 CH3I H 2CH3C CH Pd - BaSO4CH3 CH3C CCH3 C C CH3 H H 2.OO OO ⑴ C H ONa ⑴H O/OH-2 5 2⑵+ +H ⑵ H3O /△+CH3 ①KMnO4/H+ C2H 5OH NH 33.② SOCl 2NaOBrOH-OC Cl+ C2H5OH .4.△C2H5OHCH3CHCH2CH2COOH+HOH四、用化学方法鉴识以下各组化合物1.O OH取少许三种试剂分别置于试管中, 加入氨的衍生物, 若反响产生的物质有特别颜色, 则为O OH; 再取少许节余试剂, 分别置于试管中, 加入Na, 有气泡产生, 则为, 其余一个为.2.取少许三种试剂分别置于试管中, 分别滴入适当的氯化亚铜的氨溶液, 产生棕色的积淀物为, 取其余两种试剂置于两支不一样的试管中, 滴家少许溴水, 若溴水退色为ChemPaster, 剩下的即为ChemPaster.五、推断结构化合物A(C9H10 O2), 能溶于氢氧化钠, 易使溴水退色, 可与羟胺作用, 能发生碘仿反响, 但不发生托伦反响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药物化学模拟卷1
一、回答下列问题
1. 写出 -内酰胺类抗生素青霉素类和头胞菌素类的结构通式。
N N
O
ONa H
1.
2. 写出局麻骨架中中间链对作用时间长短的顺序。
N NH 2
O
2.
3. 说明拟肾上腺素药N 上取代基对受体选择性的影响。
NH
HO
HO
OH
3.
4. 说明苯乙基吗啡较吗啡镇痛作用强的原因。
N O
O
O O NO 2H
4.
5. 氮芥类抗肿瘤药毒性较大,如何通过结构修饰降低其毒性?
N N O NH 2
HCl
5.
6. 在肾上腺皮质激素的C-1、C-6、C-9、C-16和C-21位如何进行结构修饰及结构修饰的目的。
O
NHCH 3
Cl
7. 在雌二醇和睾丸素的C-17α位引入乙炔基的到的化合物各有什么样的生物活性?
N
N
O
CH 3Cl
8. 比较阿莫西林和氨苄西林聚合速度的快慢并说明原因。
O
N P
O N ClCH 2CH 2ClCH 2CH 2
H
二、写出下列结构药物的名称和一种代谢产物
N N
O
ONa H
1.
N N
O
ONa HO
H
苯妥英钠
N NH 2
O
2.
N
NH 2
O
O
N
NH 2
O
HO
N H
或
或
卡马西平
NH
HO
HO
OH
3.CHO
HO
HO
OH NH
H 3CO HO
OH
或
肾上腺素
N O
O
O O NO 2H
4.
N CH 2OH
OH O
O O
NO 2H N O
O
O O
NO 2H 或
硝苯地平
N N O
NH 2
HCl
5.
N N O OH HCl
盐酸阿糖胞苷 6.
O
NHCH 3
Cl
O NHCH 3
Cl
OH
O
NH 2
Cl
或
氯胺酮 7.
N
N
O
CH 3Cl
N
N
O CH 3
Cl
OH
N
N
O Cl
OH
H 或
地西泮 8.
O
N P
O N ClCH 2CH 2ClCH 2CH 2
H O
N P
O N ClCH 2CH 2ClCH 2CH 2
OH
H N ClCH 2CH 2ClCH 2CH 2
H 等
环磷酰胺
三、写出下列药物的化学结构及主要药理作用 1. 氟尿嘧啶 2. 吡哌酸
HN N O O
F
H
N N
N O
N COOH
C 2H 5
HN
抗癌药 抗菌药
3. 布洛芬
4. 吗啡
OH
O
非甾体抗炎药 麻醉性镇痛药
5. 氢化可的松
6. 维生素D 3
C O
CH 2OH HO
O
HO
CH 2
甾体抗炎药 抗佝偻病
四 出下列结构的药物名称及主要药理作用
N
O
OH
1.
米非司酮 抗孕激素
O
O SOCCH 3
O
2.
螺内酯 保钾利尿药
N N NH 2
H 2N
OCH 3OCH 3OCH 3
3.
甲氧苄啶 二氢叶酸还原酶抑制剂
CHCONH NH 2
N S
COOH O
4.
头孢来星(头孢氨苄)抗菌药
N
N
O
CN
H 5.
米力农 强心药
N
S
(H 2N)2C=N
S
NH 2NSO 2NH 2
6.
法莫替丁 抗溃疡药
N
S CH 2CH 2CH 2N
N CH 2CH 2OH
Cl
7.
奋乃静 抗精神病药。
