物质的分类导学案
物质的分类(导)学案 (124)

第一节 物质的分类第1课时 简单分类法及其应用学习目标核心素养建构1.认识物质的分类方法和依据。
2.学会对常见物质进行分类。
3.感受分类在科研和学习中的重要作用。
[知 识 梳 理]一、常见的分类方法 1.交叉分类法(1)含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法。
即对事物以不同的标准进行分类。
(2)举例:①Na 2CO 3⎩⎨⎧按其组成的阳离子来分类,属于钠盐按其组成的阴离子来分类,属于碳酸盐按其溶解性来分类,属于易溶盐②将不同的物质与它所属的类别进行连线。
2.树状分类法(1)含义:对同类事物按照某些属性进行再分类的分类方法。
即对同类事物进行再分类。
(2)举例:【自主思考】1.(1)交叉分类法中所涉及的类别之间是什么关系?试用数学集合关系举例说明。
(2)树状分类法中所涉及的类别之间是什么关系?用数学集合关系举例说明。
提示 (1)交叉关系,如对Na 2SO 4进行的交叉分类:(2)有并列和从属关系二种,如物质的分类中: ①并列关系:金属单质 非金属单质②从属关系:二、分类方法的应用分类可以帮助我们更好地认识物质的性质,找出各类物质之间的关系: Ca ――→①CaO ――→②Ca (OH )2――→③CaCO 3 C ――→④CO 2――→⑤H 2CO 3――→⑥CaCO 3 写出有关序号的化学方程式并注明反应类型。
化学方程式反应类型①2Ca +O 2===2CaO; 化合反应。
②CaO +H 2O===Ca(OH)2;化合反应。
③Ca(OH)2+Na 2CO 3===CaCO 3↓+2NaOH; 复分解反应。
④C +O 2=====点燃CO 2;__ 化合反应。
⑤CO 2+H 2O===H 2CO 3;__化合反应。
⑥H 2CO 3+Ca(OH)2===CaCO 3↓+2H 2O ;复分解反应。
【自主思考】2.硫和碳均为非金属单质,在性质上有一定的相似性,你能写出下列转化的化学方程式吗?S ―→SO 2―→H 2SO 3―→Na 2SO 3 提示 ①S +O 2=====点燃SO 2 ②SO 2+H 2O===H 2SO 3③H 2SO 3+2NaOH===Na 2SO 3+2H 2O[效 果 自 测]1.判断正误,正确的打“√”,错误的打“×”。
《物质的分类》导学案3.doc

《物质的分类》学案第一课时物质的简单分类方法与应用学习目标1.了解常见化学物质及其变化的分类方法与应用2.良好的习惯对我们的学习生活有着本质的影响。
自主学习一1•对于自然界中的物质,从状态上可以分为,,三态。
2.初中学习中将元素分为元素和元素;其中Na、Mg、Al、Fe、Cu、Zn等属于元素,O> S、N、P、Cl等属于元素。
3.对于化合物,我们可以根据组成特点,把它们分为:、、、四大类,是否还可以对它们继续分类?常见的强酸有,强碱有4.对于化学反应,在初屮我们把它们分为四种基本反应类型,分别、、、°5.把大量事物按照事先设定的“ ”进行分类,是人们最熟悉、也是最方便的一种工作方法。
数以千万计的化学物质和为数更多的化学反应,的作用几乎是无可替代的。
人们可以分类进行学习,从而认识他们的性质。
同类事物可以使人的认识举一反三, 不同类的事物可以使人的认识由此及彼。
分类法是一种行之有效简单易行的科学方法。
练习一:根据物质的组成和性质,对下列物质进行分类:%1海水②蒸镭水③稀盐酸④食盐水⑤汞⑥液氧⑦硝酸溶液⑧硝酸银⑨纯碱⑩烧碱⑴)乙醇02)生石灰英中属于混合物的是(填写编号,下同),属于纯净物是,属于单质的是,属于化合物的是,属于盐的是属于氧化物的是,属于有机物的是。
自主学习二交叉分类法定刈同一种物质按不同的标准分类。
义:例:①某些盐的交叉分类按阴离子分类,按阳离子分类Na2CO3既是盐,又是盐;还属于盐。
钠盐Na2CO3顿盐NaHCO3碳酸盐Na2 SO4BaSO4(酸碱 化合物 I盐Na2 S04既是 盐, 又是 盐; 还属于 盐。
K2SO4既是 盐,又是 盐; 还属于 盐。
K2CO3既是 盐,又是盐;还属于盐。
练习二(1) 对下列碱进行交叉分类(连线)NaOH强碱KOH 一元碱Mg(OH)2弱碱 Ba(OH)2 二元碱(2) 根据下图屮物质及其类型Z 间的关系分别作出有关连线可溶性盐难溶性盐正盐 酸式盐 白主学习三. 树状分类法含义:对同类事物按某种标准再进行分类。
《物质的分类核心素养目标教学设计、教材分析与教学反思-2023-2024学年科学浙教版2013》

《物质的分类》导学案一、进修目标1. 了解物质的分类标准和方法;2. 掌握物质的分类方法和特点;3. 能够根据物质的性质进行分类。
二、进修重点1. 物质的分类标准;2. 物质的分类方法。
三、进修难点1. 掌握物质分类的特点;2. 能够灵活运用物质分类的方法。
四、进修内容1. 物质的分类标准根据物质的组成和性质,可以将物质分为纯物质和混合物两大类。
纯物质又可分为元素和化合物。
元素是由同一种原子组成的物质,化合物是由不同种元素经化学反应组成的物质。
混合物是由两种或两种以上的物质混合而成的物质。
2. 物质的分类方法根据物质的物理性质和化学性质,可以将物质进行分类。
物质的物理性质包括颜色、形状、状态等;化学性质包括燃烧性、溶解性等。
通过观察物质的性质,可以将其分类为固体、液体和气体等。
五、进修方法1. 利用实验观察物质的性质,进行分类;2. 阅读相关资料,了解物质的分类方法;3. 参与讨论,探讨物质分类的特点和方法。
六、教室练习1. 请根据物质的性质,将以下物质进行分类:水、铁、氧气、盐、糖、二氧化碳;2. 选择题:下列属于纯物质的是()。
A. 水B. 空气C. 砂糖D. 海水七、课后作业1. 阅读相关教材,了解更多关于物质分类的知识;2. 完成教室练习中的题目,并进行订正;3. 思考:物质的分类对我们的生活有何意义?如何运用物质分类的知识解决实际问题?八、拓展延伸1. 了解元素周期表中元素的分类方法;2. 探究不同物质的燃烧性质和溶解性质对其分类的影响;3. 开展实验,验证物质分类的准确性和实用性。
通过本节课的进修,置信同砚们对物质的分类有了更深入的了解,能够灵活运用物质分类的知识解决实际问题,为未来的进修打下坚实的基础。
希望同砚们能够在课后多加练习,加深对物质分类的理解,不息提升自己的进修能力和实践能力。
八年级科学上册 6.3 物质的分类导学案 (新版)华东师大

物质的分类一、要点梳理1. 单质是指由组成的一种物质,如、都是单质;2. 化合物是指由的一种物质,如、都是化合物;3. 单质分为单质(如:、等)和单质(如:、等);4. 金属单质由组成,除外,一般为固态;非金属单质由组成,通常条件下除外,一般都是气态(如:、等)或固态(如:、等);5. 单质和化合物都有的组成,并可用符号表示;6. 氧气用符号表示;O2可表示;也可表示;7. 仅有物质组成的为物(如等);由或的物质而成的为物(如等)。
8. 纯净物有确定的,所以有确定的;而混合物则没有,但是混合物中的各种成分仍然保持性质,彼此只是相互混合,并没有发生;9. 混合物可用一定的方法将各成分分离,常用的分离混合物的方法有和等;10. 过滤适用于不同的物质的分离;基本操作有、与。
而纸上层析则适用于不同的分离。
二、温馨提示1. 混合物分离的方法有:过滤、纸上层析、吸附、蒸馏、沉降、消毒等众多方法,但蒸馏是净化程度最高的方法。
2. 过滤要注意“一贴二低三靠”,实验操作的正确与否关系到实验的成败及实验者的安全。
3.层析技术是利用混合物中各组成成分的物理化学性质(分子形状大小、吸附力、亲和力等)的不同,使各组分经不同的速度移动,而达到分离的目的。
这种技术可用于化学性质相近的混合物的分离,特别适合于微量物质的分离和鉴别。
三、解题指导[例题1]下列的“水”属于纯净物的是()[解析] 雨水中含有水、溶解在水中的多种物质,属于混合物;海水中含有水、氯化钠等多种物质,属于混合物;食盐水中含有水、氯化钠等物质属于混合物;蒸馏水中只含的水,属于纯净物。
[答案] D[例题2] 下列不属于净化水的措施是()A.吸附 B.过滤 C.蒸馏 D.电解[解析]吸附主要是利用活性炭的吸附性,可除有色、有异味等杂质,过滤可除去水中不溶固体杂质,蒸馏是通过蒸发、冷凝等操作而获得纯净的水;电解是在通电条件下不分解的方法,不是净化水的方法。
[答案]D四、巩固练习1.下列物质中,属于纯净物的是()A.汽水 B.干冰 C.加铁酱油 D.新鲜空气2. 下列物质属于混合物的是:()A.矿泉水 B.高锰酸钾 C.过氧化氢 D.液氧3. 下列物质属于单质的是()A.金刚石 B.空气 C.水 D.煤4. 下列物质中属于金属单质的是()A.不锈钢 B.水银 C.铁锈 D.冰5.下列物质中一定有两种元素的是()A.氧化物 B.化合物 C.混合物 D.单质6.下列物质中,可能由一种元素组成的是()A.单质 B.溶液 C.化合物 D.混合物7. 下列物质中不可能含有两种元素的是()A.单质 B.氧化物 C.化合物 D.混合物8. 进行过滤操作时,一定要用到的仪器是()A.酒精灯 B.量筒 C.漏斗 D.水槽9. 除去水中的泥沙需用的方法是()A.过滤 B.蒸馏 C.吸附 D.加肥皂水10. 下列净化水操作中,主要涉及到化学变化的是()A.过滤 B.纸上层析 C.消毒 D.沉降要点梳理答案:1.同种元素氧气氢气(合理即可)2. 不同种元素水二氧化碳(合理即可)3. 金属铁铜(合理即可)非金属碳硫(合理即可)5. 确定元素6. O2氧气由氧元素组成一个氧分子由2个氧原子构成7. 一种纯净氧气水(合理即可)两种两种以上混合混合空气溶液(合理即可)8. 成分性质原来的反应9. 过滤纸上层析同步训练参考答案:1.B2.B3.A4.B5.A6.A7.A8.C9.A 10.C。
高中化学必修一第二章第一节《物质的分类》导学案

第二章第一节物质的分类【导】(3分钟)为什么你能从超市很快的挑出自己所需要的商品呢?图书馆里有那么多的书,为什么你能够很快的找到你所需要的那本书呢?你浏览网页时,为什么能够快速进入你所想要进入的网站呢?这一切都是分类的强大功能给我们带来的方便,今天就让我们一起来学习一下分类吧。
【学习目标】1.掌握分类的方法2.能够对酸碱盐氧化物准确分类【思、议】(15+6分钟)1、自读教材24-25页,回答什么是交叉分类和树状分类法?请分别应用这两种分类方法对你们班的学生进行分类。
2、酸:请把下列的酸按照不同的分类进行填空。
❶HCl ❷H2SO4 ❸ HNO3❹H2SO3❺ H2CO3❻CH3COOH ❼HCN ❽H3PO4❾HNO2一元酸____________ 二元酸______________________三元酸_____________强酸_______________ 弱酸__________________________ 含氧酸______________ 无氧酸_________________________ 3、碱:请把下列的碱按照不同的分类进行填空。
❶NaOH ❷Mg(OH)2❸Fe(OH)3❹Cu(OH)2❺Ba(OH)2❻Fe(OH)2❼KOH ❽NH3·H2O一元碱___________,二元碱___________,三元碱________________ 强碱_________________ 弱碱_____________________ 4、盐:请把下列的盐按照不同的分类进行填空。
❶NaCl ❷AgCl ❸Na2CO3❹NaHCO3❺KAl(SO4)2·12H2O ❻(NH4)2Fe(SO4)2❼Cu2(OH)2CO3❽BaSO4❾NaHSO4正盐_______________酸式盐_______________碱式盐__________________难溶盐_____________可溶盐_____________复盐_____________5、氧化物:请把下列的氧化物按照不同的分类进行填空。
21物质的分类导学案.doc

21物质的分类导学案.doc第二章化学物质及其变化第一节物质的分类导学案三维目标知识与技能:1.学会从多角度,依据不同标准对物质分类2.知道“交叉分类法”和“树状分类法”这两种常用的分类法3.能根据反应物,生成物的种类和类别对化学反应分类过程与方法:通过思考,讨论和交流等学习方式对信息进行加工处理情感态度与价值观:感悟分类是一种行之有效的科学方法重点:物质的分类难点:物质间的转化关系第一课时教学环节(自主学习)1.分类的含义:分类是_______________________________________________________ 的一■种常用的科学方法。
2.分类的意义:运用分类的方法不仅能使有关____________________ 的知识系统化,还可以通过_____________ 的研究,发现_____________ 的规律。
分类法是一种__________ , __________ 的科学方法。
3.分类的标准:正确分类的前提是选择_________________ 的标准。
4.交叉分类法:根据—的分类标准,对同一事物进行—分类的一种方法。
5.树状分类法:根据研究对象的 _________ 性和______ 性,对事物进行再分类,形成一定从属关系的不同等级系统的一种分类方法。
(小组互学)分析书中21页图2-2和2-3的分类方法,进行下列分类:1如果根据酸的分子里是否含有氧原子,可以把酸分为含氧酸和无氧酸两类;根据酸分子电离时所能生成的氢离子的个数,可以把酸分成一元酸、二元酸、三元酸等。
请用盐酸、硝酸、氢硫酸、硫酸制作一张交义分类图。
盐酸含氧酸硝酸无氧酸氢硫酸一元酸硫酸二元酸2按照物质的组成和性质,对纯净物进行分类,作出数状分类图。
然后选择下列合适的物质填在物质类别上。
2、Cu、H2SO4、Ba(0H)2、KNO3、CO2、空气、含镁60%的MgO(交流展示)(点拨释疑)(训练反馈)1、给物质分类时由于标准不同往往会出现()A、树状分类法B、环状分类法C、球状分类法D、交叉分类法2、人们把球分成篮球、排球、羽毛球等属于()A、树状分类法B、环状分类法C、球状分类法D、交叉分类法3、通常使用的分类方法是________ 、______________ 。
物质的分类导学案
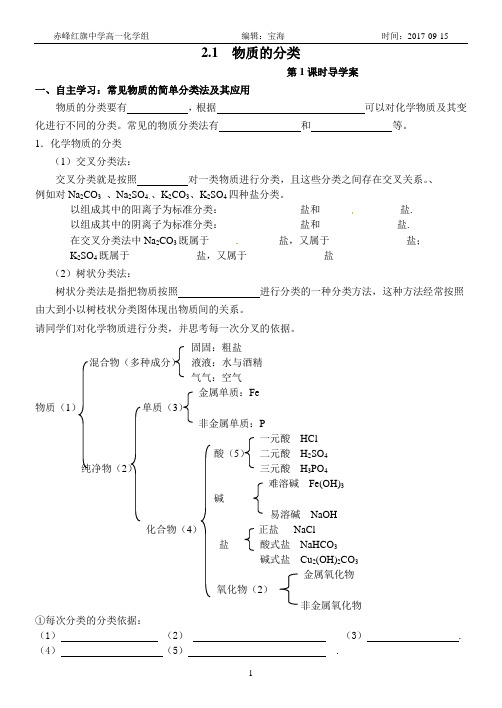
2.1 物质的分类第1课时导学案一、自主学习:常见物质的简单分类法及其应用物质的分类要有,根据可以对化学物质及其变化进行不同的分类。
常见的物质分类法有和等。
1.化学物质的分类(1)交叉分类法:交叉分类就是按照对一类物质进行分类,且这些分类之间存在交叉关系。
、例如对Na2CO3、Na2SO4、、K2CO3、K2SO4四种盐分类。
以组成其中的阳离子为标准分类:_______________盐和_______________盐.以组成其中的阴离子为标准分类:_______________盐和_______________盐.在交叉分类法中Na2CO3既属于_____________盐,又属于_______________盐;K2SO4既属于_____________盐,又属于_______________盐(2)树状分类法:树状分类法是指把物质按照进行分类的一种分类方法,这种方法经常按照由大到小以树枝状分类图体现出物质间的关系。
请同学们对化学物质进行分类,并思考每一次分叉的依据。
固固:粗盐混合物(多种成分)液液:水与酒精气气:空气金属单质:Fe _______物质(1)单质(3)非金属单质:P ________一元酸HCl ________酸(5)二元酸H2SO4 _____________纯净物(2)三元酸H3PO4 ______________难溶碱Fe(OH)3 _________碱易溶碱NaOH _________化合物(4)正盐NaCl ________盐酸式盐NaHCO3 ______________碱式盐Cu2(OH)2CO3 ______________金属氧化物_______氧化物(2)非金属氧化物______①每次分类的分类依据:(1)(2)(3) . (4)(5) .②将下列物质填进上表的横线上,O2,Cu,H2CO3,Ba(OH)2,KNO3,CO2,空气,含镁60%的MgO2.化学反应的分类反应类型分类依据① H2+Cl2=== 2HCl↑ ( )高温②CaCO3===CaO+CO2↑ ( )③Zn + 稀H2SO4 ===H2↑ + ZnSO4 ( ) ____________________④HCl + NaOH === NaCl + H2O ( )⑤CuO+H2 ===Cu+H2O( )⑥C+O2 === CO2↑ ( ) ______________________⑦Ca2+ + CO32- =CaCO3↓ ( )⑧H+ + OH- = H2O ( ) _________________________⑨NaOH + HCl=NaCl + H2O ( )⑩C + H2O === CO + H2 ( ) ___________________________练习1:每组中都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种物质找出来。
《物质的分类》 导学案

《物质的分类》导学案一、学习目标1、了解物质分类的方法和依据。
2、掌握常见物质的分类类别,如纯净物、混合物、单质、化合物、氧化物、酸、碱、盐等。
3、能够根据物质的组成和性质对物质进行正确分类。
二、学习重难点1、重点(1)物质分类的依据和常见物质类别的概念。
(2)单质、化合物、氧化物、酸、碱、盐的概念及相互关系。
2、难点(1)根据物质的组成和性质准确判断物质的类别。
(2)各类物质之间的转化关系。
三、知识梳理(一)物质分类的方法1、交叉分类法根据不同的分类标准,对同一物质进行多种分类的方法。
例如,对于碳酸钠(Na₂CO₃),从其组成的阳离子来看,属于钠盐;从其组成的阴离子来看,属于碳酸盐。
2、树状分类法对同类事物按照某种属性进行再分类的方法。
例如,物质可以分为纯净物和混合物,纯净物又可以分为单质和化合物,化合物可以进一步分为氧化物、酸、碱、盐等。
(二)常见物质的分类1、纯净物由一种物质组成,具有固定的组成和性质。
(1)单质由同种元素组成的纯净物。
包括金属单质(如铁、铜等)、非金属单质(如氧气、氮气等)和稀有气体单质(如氦气、氖气等)。
(2)化合物由不同种元素组成的纯净物。
包括氧化物、酸、碱、盐等。
2、混合物由两种或两种以上的物质混合而成,各成分保持原有的性质。
例如空气、溶液、合金等。
3、氧化物由两种元素组成,其中一种是氧元素的化合物。
分为金属氧化物(如氧化铜、氧化铁等)和非金属氧化物(如二氧化碳、二氧化硫等)。
4、酸在水溶液中电离出的阳离子全部是氢离子(H⁺)的化合物。
根据酸分子中可电离的氢原子个数,分为一元酸(如盐酸、硝酸等)、二元酸(如硫酸、碳酸等)和多元酸(如磷酸等)。
5、碱在水溶液中电离出的阴离子全部是氢氧根离子(OH⁻)的化合物。
根据碱在水中的溶解性,分为可溶性碱(如氢氧化钠、氢氧化钾等)和难溶性碱(如氢氧化铜、氢氧化铁等)。
6、盐由金属离子(或铵根离子)和酸根离子组成的化合物。
根据盐的组成和性质,分为正盐(如氯化钠、碳酸钠等)、酸式盐(如碳酸氢钠、硫酸氢钠等)和碱式盐(如碱式碳酸铜等)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2014年高考一轮资料
化学 必修一复习:第二章第一节 物质的分类 编制人: 审核人:高三化学组 编号:04 领导签字
第1页,共4页
第2页,共4页
《物质的分类》 学案
最新考纲: 1.了解分子、原子、离子等概念的含义,了解原子团的定义。
2.理解物理变化与化学变化的区别与联系。
3.理解混合物和纯净物、单质和化合物、金属和非金属的概念。
4.理解酸、碱、盐、氧化物的概念及相互联系。
5.了解胶体是一种常见的分散系。
知识点一 物质的组成和性质
1.元素、物质及微粒间的关系
(1)宏观上物质是由元素组成的,微观上物质是由__________、________或__________构成的。
(2)元素在物质中的存在形态
①游离态:元素以________形式存在的状态。
②化合态:元素以________形式存在的状态。
2.同素异形体
(1)______________________________叫同素异形体。
同素异形体的形成有两种方式:①构成分子的原子个数不同,如O 2和O 3;②原子排列方式不同,如金刚石和石墨。
(2)同素异形体之间的变化属于________变化。
3.电解质:_________________________________________________________
强电解质:____________________举例___________________________________ 弱电解质:____________________举例___________________________________
非电解质:______________________________________________________
【判断】
(1)原子与该原子形成的离子相对质量几乎相等。
( )
(2)由一种元素组成的物质一定是同一种物质。
( )
(3)由同一种元素组成的物质一定是纯净物,冰水混合物是混合物。
( )
(4)NH 3、SO 2、O 2为电解质。
( )
知识点二 物质的分类 1.分类法:常用的两种是__________法和____________法。
2.概念:酸性氧化物:
碱性氧化物:
【判断】 ①非金属氧化物一定是酸性氧化物。
( )
②酸性氧化物一定是非金属氧化物。
( )
③金属氧化物一定是碱性氧化物。
( )
④碱性氧化物一定是金属氧化物。
( )
⑤Na 2O 和Na 2O 2均能与H 2O 反应生成NaOH ,故二者都是碱性氧化物。
( ) ⑥酸酐一定是氧化物。
( )
3、a 、无机化合物的交叉分类法 ①某些盐的交叉分类
按阴离子分类 按阳离子分类 Na 2CO 3 碳酸盐 Na 2SO 4 钠盐 K 2SO 4 硫酸盐 K 2CO 3 钾盐
②某些碱的交叉分类 弱碱 NaOH KOH 可溶性碱
强碱 Mg(OH)2 一元碱 NH 3·H 2O 不溶性碱 二元碱 Ba(OH)2 ③某些氧化物的交叉分类
CO 2 非金属氧化物 酸性氧化物 SiO 2 气体氧化物 SO 2 固体氧化物
两性氧化物 Al 2O 3
碱性氧化物 CuO 金属氧化物 b 、 无机化合物的树状分类法 单质 纯净物 氧化物
化合物 酸 物质 碱 盐
混合物
2严谨的人,方方面面表现的都是严谨;乐观的人,时时处处看到的都是阳光
第3页,共4页第4页,共4页将落实进行到底
知识点三分散系、胶体
1.分散系
(1)概念:______________________________________________________所得到的体系。
(2)分类:
分类标准:______________________________________________________。
根据分类标准在数轴上填写分散系名称。
2.胶体
(1)定义:分散质粒子直径介于____________之间的分散系。
(2)分类:按分散剂划分
⎩⎪
⎨
⎪⎧
①:如AgI胶体
②:如烟水晶
③:如烟、雾、云
(3)胶体的性质
①丁达尔效应:用一束光通过盛有Fe(OH)3胶体的烧杯时,在与光束垂直的方向上进行观察,可以看到__________________,这个现象称作____________,这是由于胶体微粒对可见光的________而形成的。
丁达尔效应可用于区别________和________。
②布朗运动:胶粒在胶体中不停的做无规则运动。
③电泳:在________的作用下,胶体微粒作________移动,这种现象称为电泳,电泳现象说明________带电荷。
带正电的胶粒有, 带负电的胶粒有。
④聚沉:使胶体发生聚沉的方法有:、和。
(4)Fe(OH)3胶体的制备
向沸水中逐滴加入____________,继续煮沸至液体呈____________,停止加热,即制得Fe(OH)3胶体,化学方程式________________________________________________________。
(5) 胶体、溶液、浊液三种常见分散系的比较
知识点四分类法的应用:
分别以钙和碳为例,用化学方程式表示下列转化关系。
Ca CaO Ca(OH)2CaCO3 C CO2H2CO3CaCO3。
