食品化学 水和冰的结构
食品化学:水分

第二节 水和冰的性质和结构
一、水和冰的物理性质
部分氢化物的物理性质 氢化物 CH4 NH3 H2S H2O HF 熔点(℃) -184 -78 -86 0 -92 沸点(℃) -161 -33 -61 100 19 蒸发热( J/mol) 9210960 23027400 18673128 40821300 30144960
92
90 87 87
香蕉
鸡 肉 面包
75
70 65 35
奶油
稻米、面 粉 奶粉 酥油
16
12 4 0
表1 食 奶油 乳酪 鲜奶油 乳粉 液体乳制品 冰淇淋和冰糕 鳄梨 豆(青刀豆) 浆果 柑橘 黄瓜 干水果 新鲜水果(可食部分) 豆类(干) 马铃薯 红薯 芹菜、萝卜 品 水分含量 (%) 15 40~75 60~70 4 87~91 65 65 67 81~90 86~89 96 ≤ 25 90 10~12 78 69 79
在大多数新鲜食品中,水是最重要的成分,若希望 长期贮藏这类食品,只要采取有效的贮藏方法控制 水分就能够延长保藏期。 无论采用普通方法脱水或是低温冷冻干燥脱水,食 品和生物材料的固有特性都会发生很大的变化, 都无法使脱水食品恢复到它原来状态(复水或解 冻)。 因此研究水和食品的关系是食品科学的重要内容之 一,对食品的储藏有重要的意义。
三、水的缔合作用
水分子中的氧原子电负性大, O—H键的 电子对强烈的偏向氧原子一边,使氢原子 带有部分正电荷。 氢原子无内层电子,几乎是一个裸露的质 子,极易与另一个水分子中的氧原子的孤 对电子通过静电引力形成氢键。
温 0℃ 0.99984 1.793×10-3 75.64×10-3 0.6113 4.2176 0.5610 1.3×10-7 87.90
第一讲水对食品品质的影响解析

第一讲
水 与 冰 的 结 构 与 性 质
2.2.3 水、冰的物理特性及与食品质量关系 水是一种特殊的溶剂,其物理性质和热行为
有与其它溶剂显著不同的方面:
a.水的熔点、沸点、介电常数、表面张力、热 容和相变热均比质量和组成相近的分子高得 多。如甲烷的b.p:-162℃ ,m.p:-183℃ , 而水在0.1MPa下b.p:100℃ ,m.p:0℃ ;这 些特性将对食品加工中的冷冻和干燥过程产 生很大的影响;
SP3
O
H H 104.50
1.84D
2.2.2 水分子的缔合与水的三态
由于水分子的极性及两种组成原子的电负性差别, 导致水分子之间可以通过形成氢键而呈现缔合状态:
O
H
H
O
H
HO
H
H
第一讲
水 与 冰 的 结 构 与 性 质
由于每个水分子上有四个形成氢键的位点,因此每 个水分子的可以通过氢键结合4个水分子。
会
更
精
彩
Welcome to Join!
Starts here!
研究生 课程
《高 级 食 品 化 学》
主 讲 人:刘延奇 所在单位:食品与生物工程学院 日 期:2011.06.01
第 第一讲 水 分
一 讲
2.1 概述 2.2 水、冰的结构
水
2.3 水与非水组分之间的相互作用
2.4 水分活度
分
2.5 水与食品的稳定性
第一讲
水 与 溶 质 的 相 互 作 用
2.3.1.3 与非极性物质的相互作用 非极性的分子通常包括烃类、脂类、甾萜类等,
通过化学的手段也可在一些含极性基团的分子 (如蛋白质等)中引入非极性部分(基团)。当 水中存在非极性物质,即疏水性物质时,由于它 们与水分子产生斥力,可以导致疏水分子附近的 水分子之间的氢键键合增强。由于在这些不相容 的非极性实体邻近的水形成了特殊的结构,使得 熵下降,此过程称为疏水水合作用。
食品化学:第二章 水和冰

4.食品中水分存在形式-2(P13)
结合水分类:构成水、邻近水和多层水
➢ 构成水(constitutional water):结合最强的水, 已成为非水物质的一部分
➢ 邻近水(vicinal water):占据着非水成分大多数亲 水基团的第一层位置
➢ 多层水(multilayer water):占有第一层中剩下的 位置以及邻近水外侧的几层
水分吸附等温线(吸湿等温线)
➢ 在等温条件下,以食品含水量为纵坐标、以Aw为横 坐标作图。
➢ 不同食品,因其化学组成和组织结构不同,对水束 缚能力不一样,有不同的吸湿等温线,但都为S型。
7.食品中水分变化过程:水分吸附等温线-2
水分吸附等温线的意义:
➢ 表示食品的Aw与含水量对应关系; ➢ 浓缩、干燥等除去水的难易程度与Aw有关; ➢ 配制食品混合应注意水在配料间的转移; ➢ 测定包装材料的阻湿性质; ➢ 测定一定水分含量与微生物生长的关系; ➢ 预测食品稳定性与水分含量的关系。
➢ 冰点测定法:
✓ 先测定样品的冰点降低和含水量,利用 ✓ Aw = n1/(n1+n2) ;n2 = (G∆Tf ) /1860 ✓ G:样品中溶剂的量(g);∆Tf:冰点降低(℃)
6.水对食品稳定性的影响:水分活度-10
冷冻食品中Aw的测定:
➢ 冷冻食品中,水的蒸汽压与同一温度下冰的蒸汽压 相等,能准确计算冷冻食品水Aw;
➢ Aw与非酶褐变
✓ Aw < 0.2 : V 最小,褐变难于发生 ✓ Aw < 0.6 : V 升高 ✓ Aw > 0.7 : V 降低(因为水稀释了反应物浓度) ✓ Aw 0.6-0.7 :V 最大(羰氨反应达到最大值)
➢ Aw与脂肪的氧化
食品化学_水分

第一章 水分
水和冰的结构 水和溶质的相互作用 食品中水的存在状态 水分活度与食品稳定性 等温吸湿曲线及其应用
主要内容
食品中水的存在
水和冰的结构与性质 水和溶质的相互作用 食品中水的存在状态 水分活度与食品稳定性 等温吸湿曲线及其应用 冻结与食品稳定性
1.1 食品中的水
肉类含水量在
70%左右。
水分含量与食品特性 4
面包和馒头含
水量在40%左 右。
水分含量与食品特性 5
米和面含水量
在12%左右。
水分含量与食品特性 6
饼干、糖果、
奶粉等食品的 含水量在8% 以下。
1.2 水的特性
水的物理性质和其他小分子有显著差异。
高熔点 高沸点 高热容量 高相变热 高表面张力 高介电常数 结冰时体积增大
毛细水
流动水
自由水
自由水
水分活度和水分含量
图:不同食品的等温吸湿曲线
等温吸湿曲线因食品 不同而性状各异。但 只有低水分食品才看 得出曲线的形状。
图:不同温度的等温吸湿曲线
因为水分活度随着
温度而变化,等温 吸湿曲线也随温度 变化。
等温吸湿曲线中的滞后效应
等温吸湿曲线可以用两种方法绘制:
水首先冷却成为过冷状态,然后围绕晶核结
冰,冰晶不断长大。快速冻结可以形成较多 晶核和较小冰晶,有利保持食品品质。
3 水和溶质的相互作用
纯水以氢键结合成连续结构,而如果在水中
加入其他物质,水的原有结构将受到打扰, 发生水-溶质相互作用。
其中包括几种情况:
离子与水的相互作用 亲水极性化合物与水的相互作用 疏水物质与水的相互作用
食品化学知识点
食品化学知识点第一章水1、在冷冻食品中存在4中主要的冰晶体结构:六方形、不规则树枝状、粗糙的球形和易消失的球晶以及各种中间状态的晶体。
2、冰的特性—过冷A】食品中水的蒸汽压和该温度下纯水的饱和蒸汽压的比值。
3、【水分活度W4、水在食品中以游离水和结合水两种状态存在的。
5、结合水的特性:①在-40℃不会结冰;②不能作为所加入溶质的溶剂;③在质子核磁共振试验中使氢的谱线变宽。
6、各种有机分子与水之间的作用以氢键为主要方式。
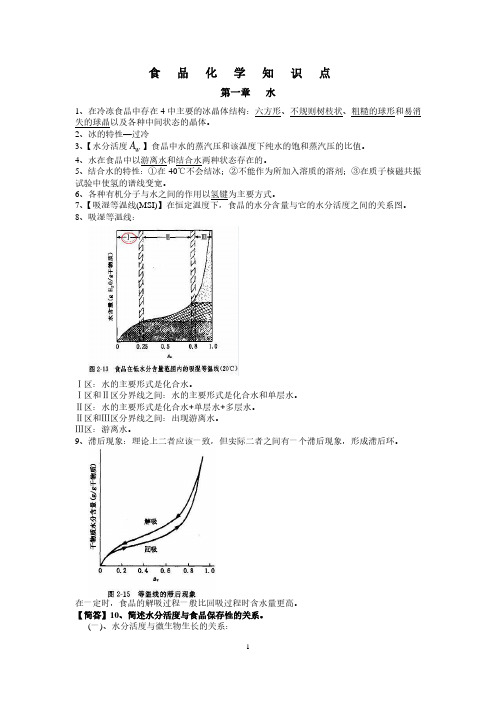
7、【吸湿等温线(MSI)】在恒定温度下,食品的水分含量与它的水分活度之间的关系图。
8、吸湿等温线:Ⅰ区:水的主要形式是化合水。
Ⅰ区和Ⅱ区分界线之间:水的主要形式是化合水和单层水。
Ⅱ区:水的主要形式是化合水+单层水+多层水。
Ⅱ区和Ⅲ区分界线之间:出现游离水。
Ⅲ区:游离水。
9、滞后现象:理论上二者应该一致,但实际二者之间有一个滞后现象,形成滞后环。
在一定时,食品的解吸过程一般比回吸过程时含水量更高。
【简答】10、简述水分活度与食品保存性的关系。
(一)、水分活度与微生物生长的关系:不同类群微生物生长繁殖的W A 最低范围是:大多数细菌为0.94~0.99,大多数霉菌为0.80~0.94,大多数耐盐细菌为0.75,耐干燥霉菌和耐高渗透压酵母为0.60~0.65。
在低于0.60时。
绝大多数微生物就无法生长。
细菌形成芽孢时的W A 阈值比繁殖生长时要高。
(二)、水分活度与酶水解的关系:当降低到0.25~0.30的范围,就能有效地减慢或阻止酶促褐变的进行。
(三)、水分活度与化学反应的关系:① 大多数化学反应都必须在水溶液中才能进行。
降低水分活度,食品中许多化学反应受到抑制,反应速率下降。
② 发生离子化学反应的条件是反应物首先必须进行离子的水合作用,所以要有足够的游离水。
③ 化学反应和生物反应都必须有水分子参与。
降低水分活度,减少了参加反应的水的有效数量,反应速率下降。
④ 当W A <0.8时,大多数酶活力受抑制;当W A 在0.25~0.30之间时,淀粉酶、多酚氧化酶和过氧化物酶就会丧失活力或受到强烈的抑制。
固态冰的立体结构

固态冰的结构与其分子的排列方式有关,冰的基本结构是由水分子(H₂O)构成的。
在冰的结构中,水分子通过氢键形成稳定的晶格,这导致冰在低温下凝固成为固态。
普通冰的结构:
1. 冰的分子结构:水分子是由一个氧原子和两个氢原子组成的。
在普通冰中,水分子呈六角形的环状结构排列。
2. 氢键:水分子之间通过氢键相互连接。
每个水分子通过氢键与其他四个水分子相连,形成一个均匀的晶格。
3. 晶格形状:水分子的六角形排列形成冰的晶格结构。
这种六角形排列的晶格结构使得冰的结构相对有序,而这也是冰在固态时呈现出透明和结晶质感的原因。
4. 密度增加:当水冷却至冰点以下,水分子的热运动减缓,氢键的形成使得水分子更加有序。
这导致水的密度增加,使得固态冰比液态水密度更大。
需要注意的是,虽然普通冰是最常见的冰相,但还存在其他形态的冰,例如压力下形成的冰₂、冰₂等,它们具有不同的晶体结构。
这些冰的结构差异通常是由于不同的温度和压力条件下,水分子之间的相互作用发生变化。
水和冰的结构

体相水可被微生物所利用,结合水则不能。
水和冰的结构
▪ 水分子由2个氢原子与 1个氧原子所组成。
▪ 水分子的结构见右图
冰的结构和性质
冰是水分子通过氢键相互结合、有序排列形成的低密度、具有一定刚 性的六方形晶体结构。普通冰的晶胞和基础平面可如下图所示:
水分吸湿等温线在食品加工中的作用
▪ 看出食品的浓缩与脱水何时较难,何时较 易.
▪ 预测食品保持多大的含水量时方才稳定, ▪ 直接看出不同食品中非水成分与水结合能力
的强弱.
吸湿等温线的测定方法
测定方法:在恒定温度下,改变食品中的水分 含量,测定相应的活度,以水分含量为纵轴、 Aw为横轴画出曲线。
滞后现象
水
▪ 食品的含水量直接影响到食品的贮藏性能和消费者 接受程度。
▪ 食品的含水量和水在食品中的存在形式,是直接引 起食品化学和微生物变质的原因之一。
▪ 食品的含水量直接影响食品的加工工艺和贮藏性能。 ▪ 水分含量的检测是食品分析的重要指标之一。
食品 中水 的存 在形 式
结合水
构成水
定义:与非水物质呈紧密结合状态的水 特点:非水物质必要的组分,-40度部结冰,
无溶剂能力,不能被微生物利用; 单分子层
定义:处于非水物质外围,与非水物质
邻近水
呈缔合状态的水;
水,0.5%
特点:-40度不结冰,无溶剂能力,不
能被微生物利用;
定义:处于邻近水外极力结合的水;
5%
特点:有一定厚度(多层),-40度基本不结
冰,溶剂能力下降,可被蒸发;
自由水
水分活度对微生物的影响
▪ 当食品的水分活度降低到一定的限度以下时, 就会抑制要求水分活度阈值高于此值的微生 物的生长、繁殖或产生毒素,使食品加工和 贮藏得以顺利进行。当然发酵技术中要求所 用微生物能正常快速增殖,此时则要给予合 适的、必要高的水分活度;另外,利用水分 活度控制食品质量或加工工艺时还要考虑pH、 营养成分、氧气等因素对于微生物的影响。
食品化学 第二章 水分

18种同位素变体 量极少
水分子的缔合作用
一个水分子可以和周围四个水分子缔合, 形成三维空间网络结构。
2015年10月25日
第二章 水分
水分子缔合的原因:
H-O键间电荷的非对称分布使H-O键具
有极性,这种极性使分子之间产生引力. 由于每个水分子具有数目相等的氢键 供体和受体,因此可以在三维空间形成 多重氢键. 静电效应.
R(水合的)+R(水合的)→R2(水合 偶极-疏水性物质 疏水相互作用ΔG<0 的)+水
2015年10月25日
疏水水合ΔG>0
第二章 水分
1、水与离子和离子基团的相互作用
类 型 实 例 作用强度 (与水-水氢键比)
偶极-离子
水-游离离子 较大 水-有机分子上的带电基团 (离子水合作用)
水-蛋白质NH 水-蛋白质CO 水-侧链OH 水+R→R(水合的) R(水合的)+R(水合的)→R2 (水合的)+水
水分含量不是一个腐败性的可靠指标
水分活度Aw 水与非水成分缔合强度上的差别 比水分含量更可靠,也并非完全可靠
与微生物生长和许多降解反应具有相关性
第二章 水分
2015年10月25日
第四节
f Aw f0 f p f 0 po
差别1%
2015年10月25日
水分活度
f ——溶剂(水)的逸度 f0——纯溶剂(水)的逸度 逸度:溶剂从溶液逃脱的趋势
p Aw po
严格
p Aw po
第二章 水分
仅适合理想溶液
RVP,相对蒸汽
第四节
水分活度
一、定义: 指食品中水的蒸汽压和该温度下纯水 的饱和蒸汽压的比值
Aw=P/P0
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
I区
0-0.2 1-6.5 不能冻结 无 单分子层水 不可利用
II区
0.2-0.85 6.5-27.5 不能冻结 轻微-适度 多分子层水 部分可利用
III区 >0.85 >27.5 正常 正常 体相水 可利用
MSI与温度的关系
❖ 水分含量一定 T↑,Aw↑
❖ Aw一定 T↑,水分含量↓
在不同温度下马铃薯的水分吸着等温线
疏水水合作用(hydrophobic hydration)
向水中添加疏水物质时,由于它们与水分子产生斥力,从而使疏
水基团附近的水分子之间的氢键键合增强,使得熵减小,此过程称为
疏水水合。
H2O+R
R(水合)
疏水相互作用(hydrophobic interaction)
当水与非极性基团接触时,为减少水与非极性实体的界面面积,
2 、要想长时间地储存一种含脂肪的食品,希望其微观水分处于 什么状态为好?
A 高于多分子层吸附水状态 B 处于多分子层吸附水状态 C 处于单分子层吸附水状态 D 低于单分子层吸附水状态
产品
水分/%
产品
水分/%
产品
水分/%
番茄
85
牛奶
87
果酱
28
莴苣
95
马铃薯
78
蜂蜜
20
卷心菜
92
香蕉
75
奶油
16
啤酒
90
鸡
70
稻米、面粉
12
柑橘
87
肉
65
奶粉
4
苹果汁
87
面包
35
酥油
0
第一节 概述
Introduction
二、水和冰的物理特性
水的熔点、沸点比较高,介电常数、表面张力、热容和相 变热等物理常数也较高,水的这些热学性质对于食品加工冷冻 和干燥过程有重大影响。
二、对淀粉老化的影响
食品在较高Aw的(30%-60%)的情况下,淀粉老化速度最快;如 果降低Aw ,则老化速度减慢,若含水量降至10%-15%,则食品中水分 多呈结合态,淀粉几乎不发生老化。
三、对蛋白质变性的影响
水分能使蛋白质膨润,体积增大,暴露出长链中可氧化的基团, Aw 的增大会加速蛋白质的氧化,破坏蛋白质结构,导致其变性。
思考题
1、葡萄中的汁可以用压榨法挤出来,而鸡肉中的水不能挤出来 A这说明葡萄中的水是自由水,而鸡肉中的水是结合水。 B这说明葡萄中的水大部分是自由水,而鸡肉中的水大部分是结合水。 C从以上事实中可以判断,葡萄中自由水的比例比鸡肉中更高。 D从以上事实尚不能判断葡萄和鸡肉中哪一种的自由水比例更高。
思考题
MSI的实际意义:
1、由于水的转移程度与Aw有关,从MSI 图可以看出食品脱水的难易程度,也可以看 出如何组合食品才能避免水分在不同物料间 的转移。
2、据MSI可预测含水量对食品稳定性的 影响。
3、从MSI还可看出食品中非水组分与水 结合能力的强弱。
MSI上不同区水分特性
区
Aw 含水量% 冷冻能力 溶剂能力 水分状态 微生物利用
解,阻止氧化进行。 2、这部分水能与金属离子形成水合物,降低了其催化性。
在Aw=0.33-0.73范围内,随Aw↑,反应速度↑的原因 1、水中溶解氧增加 2、大分子物质肿胀,活性位点暴露,加速脂类氧化 3、催化剂和氧的流动性增加
当Aw>0.73时,随Aw↑,反应速度增加很缓慢的原因 催化剂和反应物被稀释
相互作用的强度 与水-水氢键比较
较强
近乎相等
远低(△G>0) 不可比较(△G<0)
二、水与离子和离子基团的相互作用
Interaction of water with Ionic groups 净结构形成效应 (Net structure forming effect)
➢小离子或多价离子产生强电场
➢Li+, Na+, H3O+, Ca2+, Ba2+, Mg2+, Al3+, F-, OH➢具有比纯水较低的流动性和较紧密的堆积
高蛋白食品
冷冻干燥熟猪肉 Aw<0.85开始出现滞后 滞后不严重 回吸和解吸等温线均保持S形
淀粉质食品
冷冻干燥大米 存在大的滞后环 Aw=0.70时最严重
2、滞后现象产生的原因
(1)解吸过程中一些水分与非水溶液成分作用而无法放出水 分。 (2)不规则形状产生毛细管现象的部位,欲填满或抽空水分 需不同的蒸汽压(要抽出需P内>P外, 要填满则需P外> P内)。 (3)解吸作用时,因组织改变,当再吸水时无法紧密结合水, 由此可导致回吸相同水分含量时处于较高的aw。
食品化学
主讲人:
第二章 水与冰
第一节 概述 第二节 水与冰的结构 第三节 食品中水的存在形式 第四节 水分活度与吸着等温线 第五节 分子的移动性与食品的稳定性
第一节 概述
Introduction
一、水在食品中的作用
水是食品的主要组成成分,食品中水的含量、分布和状态对食品
的结构、外观、质地、风味、新鲜程度产生极大的影响。 某些代表性食品的典型水分含量
第二节 水与溶质的相互作用
Water-solute ineractions
一、水与溶质相互作用的分类
种类 偶极-离子
偶极-偶极H2O-游离离子 H2O-有机分子上的带电基团 H2O-蛋白质 NH H2O-蛋白质 CO H2O-侧链 OH H2O + RR(水合) R(水合)+R(水合)R2(水合)+H2O
疏水基团之间进行缔合,这种作用称为疏水相互作用。
R(水合)+R(水合)
R2(水合)+H2O
球 状 蛋 白 质 的 疏 水 相 互 作 用
第三节 水分吸着等温线
Moisture Sorption Isotherms(MSI)
一、定义 Definition
在恒定温度下,食品水分含量(每克干物质中水的质量)与Aw的关 系曲线。
净结构破坏效应 (Net structure breaking effect)
➢大离子和单价离子产生较弱电场
➢K+, Cs+, NH4+ , Cl-, Br-, I-, NO3- , BrO3- , IO3- , ClO4➢流动性比纯水强
三、水与具有氢键形成能力的中性基团的相互作用
Interaction of water with neutral groups processing hydrogen-bonding capabilities
水与溶质之间的氢键键合比水与离子之间的相互作用弱 能与水形成氢键的基团主要有:羟基、氨基、羰基、酰氨基等 可与一些生物大分子构成“水桥”
木 瓜 蛋 白 酶 中 的 三 分 子 水 桥
四、水与非极性物质的相互作用
Interaction of water with nonpolar substance
第四节 水分活度与食品的稳定性
Water activity and food stability
几
类
重
要
除非酶氧化在Aw<
的 反
0.3时有较高反应速
应
度外,其它反应均
速 度
是逾小反应速度愈
与
小。也就是说愈小
有利于食品的稳定
的 关
性。
系
Aw
一、对脂肪氧化酸败的影响
在Aw=0-0.33范围内,随Aw↑,反应速度↓的原因 1、水与脂类氧化生成的氢过氧化物以氢键结合,保护氢过氧化物的分
四、对化学及生物化学反应速度的影响
大多数化学反应在水溶液中进行, Aw愈大,自由水增多,有利于 反应进行:许多酶促反应需要水的介入和活化。
第五节 分子的移动性与食品的稳定性
Molecular mobility and food stability
本节自学
分子淌度(Mn) 玻璃态(Glass state) 玻璃化温度(Glass transition temperature,Tg) 无定形(Amorphous) 大分子缠结(Macromolecular entanglement)
二、滞后现象
Hysteresis
1、定义:采用回吸(resorption)的方法绘制的MSI和按解吸 (desorption)的方法绘制的MSI并不互相重叠的现象称为滞后现象。
在一指定的Aw时,解 吸过程中试样的水分含量大于 回吸过程中的水分含量
高糖-高果胶食品
空气干燥苹果 总的滞后现象明显 滞后出现在真实单层水区域 Aw>0.65时,不存在滞后
