食品化学 第三章食品中的水和冰 第三节 水分活度与吸湿等温曲线
食品化学名词解释

食品化学:Food Chemistry,是一门研究食品(包括食品原料)的化学组成、结构、性质、营养与安全性以及它们在食品贮藏加工运输中产生的化学变化、应用或控制这些变化的科学。
第2章水1 结合水:指食品中那些与非水组分通过氢键结合的水。
2 自由水:又称“体相水”除开束缚水外,剩余的那部分水都称为自由水,是与非水组分相距很远的水。
3 毛细管水:食品中的组织含有天然的毛细管,其内部保留的水称为毛细管水,实际上主要存在于细胞间隙中。
4 水分活度:指溶液(食品)中水的蒸汽压与同一温度下纯水饱和蒸汽压之比。
5 “滞后”现象:对于食品体系,采用向干燥样品中添加水(回吸作用)的方法绘制水分吸着等温线和按解吸过程绘制的等温线并不相互重叠,这种不重叠性称为滞后现象。
6 食品的吸湿等温线:moisture sorption isotherms,MSI,在恒定的温度下,将食品的Aw值作横坐标,此时达到平衡的食品含水量为纵坐标所描绘的曲线就称为吸湿等温线。
8 单分子层水:指与强极性基团(如-COOH、-NH2等)直接以氢键结合的第一个水分子层的水称单分子层水,亦称“邻近水”。
~第3章碳水化合物1吸湿性;指糖在空气湿度较高时吸收环境中水分的性质。
2保湿性;指糖在较低空气湿度环境下保持水分的性质。
3转化糖;指蔗糖的水解产物。
4糖化:是利用葡萄糖淀粉酶进一步将液化产物水解成葡萄糖。
5糊化;淀粉粒在适当温度下(一般60-80℃)的水中,吸水溶胀、分裂、形成均匀糊状溶液的变化过程称为糊化。
6液化:是指利用酸或淀粉液化酶使糊化淀粉水解成糊精和低聚糖等,由于在此过程中淀粉黏度大为降低,流动性增加,所以工业上称为液化。
7β-淀粉;未糊化的淀粉称为β-淀粉(20%直+80%支的结晶态),或生淀粉8α-淀粉;糊化后的淀粉又称α-化淀粉{9 DE:表示淀粉水解生成葡萄糖的程度,也称淀粉糖化值、葡萄糖当量(Dextrose Equivalency),定义为还原糖(以葡萄糖计)在淀粉糖浆中所占的百分数(按干物质计)。
食品化学知识点
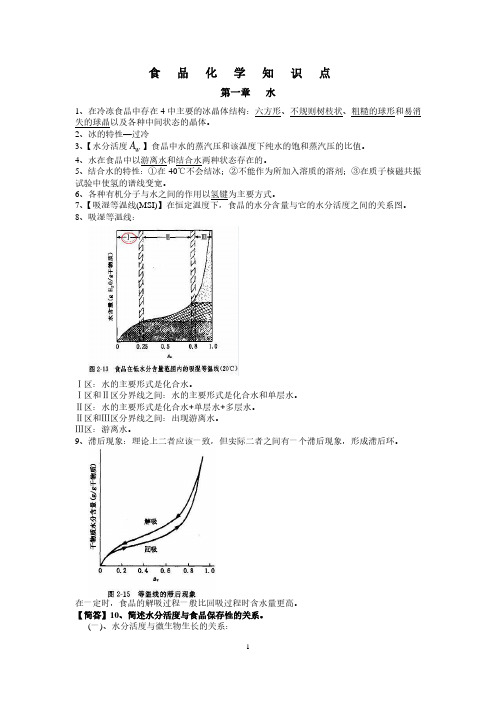
食品化学知识点第一章水1、在冷冻食品中存在4中主要的冰晶体结构:六方形、不规则树枝状、粗糙的球形和易消失的球晶以及各种中间状态的晶体。
2、冰的特性—过冷A】食品中水的蒸汽压和该温度下纯水的饱和蒸汽压的比值。
3、【水分活度W4、水在食品中以游离水和结合水两种状态存在的。
5、结合水的特性:①在-40℃不会结冰;②不能作为所加入溶质的溶剂;③在质子核磁共振试验中使氢的谱线变宽。
6、各种有机分子与水之间的作用以氢键为主要方式。
7、【吸湿等温线(MSI)】在恒定温度下,食品的水分含量与它的水分活度之间的关系图。
8、吸湿等温线:Ⅰ区:水的主要形式是化合水。
Ⅰ区和Ⅱ区分界线之间:水的主要形式是化合水和单层水。
Ⅱ区:水的主要形式是化合水+单层水+多层水。
Ⅱ区和Ⅲ区分界线之间:出现游离水。
Ⅲ区:游离水。
9、滞后现象:理论上二者应该一致,但实际二者之间有一个滞后现象,形成滞后环。
在一定时,食品的解吸过程一般比回吸过程时含水量更高。
【简答】10、简述水分活度与食品保存性的关系。
(一)、水分活度与微生物生长的关系:不同类群微生物生长繁殖的W A 最低范围是:大多数细菌为0.94~0.99,大多数霉菌为0.80~0.94,大多数耐盐细菌为0.75,耐干燥霉菌和耐高渗透压酵母为0.60~0.65。
在低于0.60时。
绝大多数微生物就无法生长。
细菌形成芽孢时的W A 阈值比繁殖生长时要高。
(二)、水分活度与酶水解的关系:当降低到0.25~0.30的范围,就能有效地减慢或阻止酶促褐变的进行。
(三)、水分活度与化学反应的关系:① 大多数化学反应都必须在水溶液中才能进行。
降低水分活度,食品中许多化学反应受到抑制,反应速率下降。
② 发生离子化学反应的条件是反应物首先必须进行离子的水合作用,所以要有足够的游离水。
③ 化学反应和生物反应都必须有水分子参与。
降低水分活度,减少了参加反应的水的有效数量,反应速率下降。
④ 当W A <0.8时,大多数酶活力受抑制;当W A 在0.25~0.30之间时,淀粉酶、多酚氧化酶和过氧化物酶就会丧失活力或受到强烈的抑制。
食品化学重点部分总结

水分活度(water activity)是指食品中水的蒸汽压与该温度下纯水的饱和蒸汽压的比值,可用下式表示:水分吸附等温线 (Moisture sorption isotherms,MSI),在恒定温度下,使食品吸湿或干燥,所得到的食品水分含量(每克干物质中水的质量)与Aw的关系曲线。
意义:吸湿等温线表示了食品的Aw与含水量对应关系,除去水(浓意义缩、干燥)的难易程度与Aw有关,配制食品混合应注意水在配料间的转移,测定包装材料的阻湿性质,测定一定水分含量与微生物生长的关系,预测食品稳定性与水分含量的关系区Ⅰ的水的性质:构成水和邻近水,最强烈地吸附,最少流动,水-离子或水-偶极相互作用,在-40℃不结冰,不能作为溶剂,看作固体的一部分,占总水量极小部分BET单层:区Ⅰ和Ⅱ接界,0.07g H2O/ g干物质,Aw =0.2 ,相当于一个干制品能呈现最高的稳定性时含有的最大水分含量区Ⅱ的水的性质:多层水通过氢键与相邻的水分子和溶质分子缔合,流动性比体相水稍差,大部分在-40℃不结冰,导致固体基质的初步肿胀,区Ⅰ和区Ⅱ的水占总水分的5%以下真实单层:区Ⅱ和Ⅲ接界, 0.38g H2O/ g干物质,Aw =0.85完全水合所需的水分含量,即占据所有的第一层部位所需的水分含量区Ⅲ的水的性质:体相水,被物理截留或自由的,宏观运动受阻,性质与稀盐溶液中的水类似,占总水分的95%以上回吸:把水加到干的样品中解吸:先使样品吸水饱和,再干燥滞后现象(Hysteresis):回吸与解吸所得的等温线不重叠现象即为“滞后现象”(Hysteresis)。
糖苷:是由单糖的半缩醛羟基和非糖化合物缩合形成的化合物。
凝胶:三维网络结构 ,氢键、疏水相互作用、范德华引力、离子桥连、缠结或共价键,网孔中液相,凝胶特性——二重性,固体性质和液体性质 ,粘弹性的半固体。
淀粉的糊化:淀粉粒在适当温度下,破坏结晶区弱的氢键,在水中溶胀,分裂,胶束则全部 崩溃形成匀的糊状溶液的过程被称为糊化。
食品化学水课件

重点 结合水及其分类;水分活度的定义及与温 度的关系;吸着等温线的含义。 难点 水分活度与微生物、化学反应、食品质构、 食品稳定性的关系;笼形水合物。
2016/10/8
3
水是以各种形态展现在人们面 前的丰富大自然的景象。
提起水的变化,真可说 是多彩多姿。
2016/10/8 4
2016/10/8
26
5 食品中水与非水成分的相互作用
结合水是样品在一定温度和低相对湿度下 的平衡水分含量; 高频电场对介电常数没有影响; 低温(-40℃或更低)下不能冻结; 不能作为外加溶质的溶剂; 在质子核磁共振实验中产生宽带; 处在溶质和其它非水物质的邻近位置。
2016/10/8 27
Chapter Two Water
2016/10/8
1
本章内容
水的功能 水和冰的物理性质 水分子和水分子的缔合; 冰和水的结构; 食品中水与非水成分的相互作用; Water activity and food stability (bilingual teaching)
水分活度与食品稳定性
5 食品中水与非水成分的相互作用
构成水(constitutional water)
结合最强的水,已成为非水物质的整体部分
邻近水(vicinal water)
占据着非水成分的大多数亲水基团的第一层位 置
多层水(multilayer water)
占有第一层中剩下位置及形成了邻近水外的几 层
5.5 水与能形成氢键的中性基团的相互作用 一般认为能形成氢键的溶质会促进(至少 不会破坏)纯水的正常结构。 溶质氢键部位的分布和定向在几何上与水 不相容时对水结构具有破坏作用,如尿 素——显著破坏效应。
食品化学课后题答案

食品化学课后复习题答案第一章绪论一、名词解释1、食品《食品工业基本术语》对食品的定义:可供人类食用或饮用的物质,包括加工食品、半成品和未加工食品,不包括烟草或只作药品用的物质。
《食品卫生法》对“食品”的法律定义:各种供人食用或者饮用的成品和原料以及按照传统既是食品又是药品的物品,但是不包括以治疗为目的的物品。
2、食品化学研究食品的种类、组成、营养、变质、分析技术及食品成分在加工和贮藏过程中所发生的化学反应的一门学科。
或者也可定义为是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产加工、贮存和运销过程中的化学变化及其对食品品质和食品安全性影响的科学。
3、基本营养素营养素是指那些能维持人体正常生长发育和新陈代谢所必需的物质。
基本营养素一般包括六大类,即蛋白质、脂肪、碳水化合物、矿物质、维生素和水。
二、简答题1、食品化学家与生物化学家的研究对象和兴趣有何不一样。
答:生物化学家的研究对象是具有生命的生物物质,他们的兴趣包括在与生命相适应或几乎相适应的环境条件下,生物物质所进行的繁殖、生长和变化。
而食品化学加则研究的是死的或将死的生物物质,其主要研究兴趣在于暴露在环境变化很大、不适宜生存的环境中热处理、冷冻、浓缩、脱水、辐照等加工和保藏条件下食品中各个组分可能发生的物理、化学和生物化学变化。
2、简述食品化学的主要研究内容。
首先是对食品中的营养成分、呈色、呈香、呈味成分和激素、有毒成分的化学组成、性质、结构和功能进行研究。
其次研究食品成分之间在生产、加工、贮存、运输、销售过程中的变化,即化学反应历程、研究反应过程中的中间产物和最终产物的结构及其对食品的品质和卫生安全性的影响。
最后是对食品贮藏加工的新技术、开发新的产品和新的食品资源以及新的食品添加剂等进行研究。
这三大部分构成了食品化学的主要研究内容。
3、简述食品化学的研究方法。
任何一门学科的发展都是通过理论-实践-理论不断循环的体系中发展的,食品化学是一门实践性很强的学科,在食品化学的研究中,要采用理论和实验相结合的方法,实验主要通过感官实验和理化实验两条途径来实现,将实验结果与查证的资料相结合从而得出新的结论或者观点,然后将理论知识再反馈到实践中,又可以指导实践,不断循环,使得食品化学的理论只是不断推向新的阶段。
食品化学笔记1

第二章 水分第一节 水和冰的结构和性质一、食品中的水分含量及功能 12、水的功能(1) 水在生物体内的功能稳定生物大分子的构象,使表现特异的生物活性 体内化学介质,使生物化学反应顺利进行 营养物质,代谢载体 热容量大,调节体温 润滑作用 (2) 水的食品功能组成成分显示色、香、味、形、质构特征 分散蛋白质、淀粉、形成溶胶 影响鲜度、硬度影响加工,起浸透、膨胀作用 影响储藏性 二 水的结构和性质 1 水的物理性质水的熔点、沸点较高;介电常数、表面张力、热容和相变等物理常数也较高; 密度较低,热导率较大;冰的热扩散速度是水的9倍。
2 水的结构H原子的单键结合成的非线性极性共价化合物。
氧原子外层电子构型为2s22p2---2s22p x22p y12p z1,两个与H原子之间靠近氧原子,由于孤对电子同性相斥,排斥力大于共价键的两对电子,使O—H键角度压缩为104.5º,(如果是正四面体中心原子与四对电子互成109º28’),水分子中共同电子对强烈地偏向氧原子一边,使H原子带有部分正电荷,H原子无内层电子因而不受排斥,只能和另一个水分子的氧原子的孤对电子相吸引,因此水分子之间形成H键,使2个,3个……水分子缔合。
水分子的缔合作用造成水具有低蒸气压、高沸点、高熔化热、高蒸发热的特点。
▲水的结构:四面体结构(不是正四面体)▲缔合作用:水分子中的氧原子的点负性大,O-H键的电子云强烈地偏向氧原子一边,使得氧原子带有部分正电荷,因为氢电子无内层电子,不受其他原子排斥,而只能和另一个水分子的孤对电子相吸引,结果,水分子间便形成缔合。
▲缔合作用的特点:①水具有溶剂性,也能溶解非离子有机分子,包括含羟基的糖和醇以及含羰基的醛和酮。
(原因:水的偶极性使其能以氢键与这些极性分子或功能基团相互作用)②水能作为两亲分子的分散介质。
(两亲分子的特点是同时具有亲水基和疏水基)三冰的结构和性质1、六方冰晶形成条件①在最适度的低温冷却剂中缓慢冷冻;②溶质的性质及浓度均不严重干扰水分子的迁移。
(完整版)食品化学答案整理
食品化学第二章水分1、名词解释:(1) 水分活度:指食品的水分蒸汽压与相同温度下纯水的饱和蒸汽压的比值。
(2) 水分的吸湿等温线:在恒定温度下,以食品中水分含量为纵坐标,以水分活度为横坐标绘制而成的曲线称为吸附等温线(MSI)。
(3) 等温线的滞后现象:一种食物一般有两条吸附等温线。
一条是水分回吸等温线,是食品在吸湿时的吸附等温线;一条是水分解吸等温线,是食品在干燥时的吸附等温线;往往这两条曲线并不完全重叠,在中低水分含量部分张开了一细长的眼孔,把这种现象称为“滞后”现象。
2、I可答题(1) 水分活度与食品稳定性的关系。
①食品aw与微生物生长[的关系:从微生物活动与食物水分活度的关系来看,各类微生物生长都需要一定的水分活度,一般说来:细菌为Aw>0.9; 酵母为Aw>0.87; 霉菌为Aw>0.&②食品aw与酶促反应的关系:一方面影响酶促反应的底物的可移动性,另一方面影响酶的构象。
食品体系中大多数的酶类物质在Aw<0.85时,活性大幅度降低,如淀粉酶、酚氧化酶和多酚氧化酶等。
但也有一些酶例外,如酯酶在Aw为0.3甚至0.1时也能引起甘油三酯或甘油二酯的水解。
③食品aw与非酶化学反应的关系:降低食品的Aw,可以延缓酶促反应和非酶反应的进行,减少食品营养成分的破坏,防止水溶性色素的分解。
但Aw过低,则会加速脂肪的氧化酸败,还能引起非酶褐变。
④食品aw与质地的关系:当水分活度从0.2 ~0.3增加到0.65时,大多数半干或干燥食品的硬度及黏着性增加。
水分活度为0.4〜0.5时,肉干的硬度及耐嚼性最大。
(2) 水分的吸附等温线的定义,以及3个区段的水分特性。
在恒定温度下,以食品中水分含量为纵坐标,以水分活度为横坐标绘制而成的曲线称为吸附等温线。
I区:为化合水和临近水区。
这部分水是食品中与非水物质结合最为紧密的水,为化合水和构成水,吸湿时最先吸入,干燥时最后排除;这部分水不能使干物质膨润,不能作为溶剂,在-40 C不结冰。
食品中水分和水分活
第Hale Waihona Puke 章第一节 概述食品中水分和水分活 度的测定
一、水分测定的意义 水分测定意义 水分是影响食品质量的因素, 控制水分是保障食品不变质的手段。
b. 固体样品要磨碎(粉碎),谷类达18 目,其他30~40目。 c. 液态样品要在水浴上先浓缩,然后进干 燥箱,不然烘箱受不了。 d.浓稠液体(糖浆、炼乳等):加水稀释, 最后要把加入的水除去。加入海砂,海 砂与玻璃棒在水浴上干燥后入干燥箱, 两者要知重量。 e.含水量﹥16%的谷类食品,采用两步干 燥法。如面包,切成薄片,自然风干 15~20h,再称量,磨碎,过筛,烘干。
不同的食品水分含量相差较多(见表5-1)
3、水分活度 Water Activity
从食品保藏的角度出发,食品的含水量不 用绝对含量(%)表示,而用活度表示 AW。 AW 指食品所显示的水蒸气压P对在同一湿 度下最大水蒸气压PO之比。 AW=P /P0=RH/100 P ——食品中水蒸气分压 P0——纯水的蒸气压 RH——平衡相对湿度
2.测定意义:水分活度表示食品中水分存 在的状态,反应水与食品的结合或游离 程度,Aw↓结合程度↑,Aw↑结合程度 ↓。 Aw影响色、香、味保存期。一般, 同种食品水分含量↑,Aw值↑。 3.水分活度值的测定方法 (1)Aw测定仪法; (2)扩散法; (3)溶剂萃取法。
(1)样品必须具备的条件: (2)称量皿的使用: (3)称样量: ⑷ 干燥条件 (5)干燥时间:
2. 蒸馏法 共沸蒸馏法:水与甲苯或二甲苯形成共 沸物。适用:易氧化、分解、热敏性及 易挥发组分。 [原理]:两种互不相溶的液体,二元体系 的沸点低于其中各组份分沸点,将食品 中的水分与有机溶剂如甲苯、苯、二甲 苯等,共沸蒸出,冷凝并收集馏出液, 由于水与其他组分密度不同,馏出液在 有刻度的接收管中分层,根据水的体积计 算水分含量。
食品化学
原因 :
水分能使蛋白质膨润,体积增大,暴露出长链中可氧化 的基团,Aw的增大会加速蛋白质的氧化,破坏蛋白质的 结构,导致其变性.
36
6. Starch Staling —Aw
Starch staling occur rapidly in water content of 30%-60%.
Starch staling does not occur when water content decrease to 10%-15%. 食品在较高Aw(30-60%)的情况下,淀粉老化速度最快;
如果降低Aw,则老化速度减慢,若含水量降至于10%-15%, 则食品中水分多呈结合态,淀粉几乎不发生老化.
37
低水分活度能抑制食品化学变化的 机理
第一, 大多数化学反应都必须在水溶液中才 能进行, 降低食品的水分活度, 则食品中结 合水的比例增加, 自由水的比例减少, 而结 合水是不能作为反应物的溶剂的, 所以降低 水分活度, 能使食品中许多可能发生的化学 反应、酶促反应受到抑制。 第二 , 很多化学反应是属于离子反应, 该 反应发生的条件是反应物首先必须进行离 子化或水化作用, 而发生离子化或水化作用 的条件必须有足够的自由水才能进行。
18
一般来说,当Aw一定时, 解吸过程中食品的水分 含量大于回吸过程中水 分含量。 解吸线在上方 滞后环形状取决于 食品品种 温度
滞后环
19
滞后环的形状—食品品种
高糖-高果胶食品
空气干燥苹果
总的滞后现象明显 滞后出现在真实单层水 区域 Aw>0.65时,不存在滞 后
20
滞后环的形状—食品品种
多层水
BET
食品化学简化大概重点课件
第2章 水分 2.3.2 水的存在状态: 自由水、结合水 结合水:指通过化学键结合的水。根据被结合的牢固程度,有几种不同的形式:(1) 化合水 (2) 邻近水 (3) 多层水 食品中大部分的结合水是和蛋白质、碳水化合物等相结合的。 自由水:就是指没有被非水物质化学结合的水。它又可分为三类:1)滞化水 (2)毛细管水 (3)自由流动水 2.4.1 水分活度的定义 水分活度是指食品中水的蒸气压和该温度下纯水的饱和蒸气压的比值。
水分活度是从0——1之间的数值,纯水时AW = 1,完全无水时AW = 0。食品中结合水的含量越高,食品的水分活度就越低 水分活度与水分含量的关系:食品中的含水量愈高,水分活度也愈大。但两者之间并没有完全确定的对应关系。 2.5 吸湿等温线 2.5.1定义和区域 定义:在恒定温度下,食品的水分含量与它的水分活度之间的关系图称为吸湿(着)等温线(MSI)。 区域:分三区域分析 等温吸湿线三区域 Ⅰ区:是低湿度范围,水分子和食品成分中的羧基和氨基等离子基团牢固结合,结合水最强,所以Aw也最低,一般在0~0.25之间,相当于物料含水量0~0.065g/g的干物质。它可以简单地看作为固体的一部分。这部分水可看成是在干物质可接近的强极性基团周围形成一个单分子层所需水的近似量。 Ⅱ区:水分占据固形物表面第一层的剩余位置和亲水基团周围的另外几层位置,形成多分子层结合水或称为半结合水,主要靠水—水和水—溶质的氢键键合作用与邻近的分子缔合,同时还包括直径<1μm的毛细管中的水。Aw在0.25~0.8之间,相当于物料含水量在0.07g至0.14~0.33g/g干物质。加速了大多数反应的速度。 Ⅲ区:是毛细管凝聚的自由水。Aw在0.8~0.99之间,物料含水量最低为0.14~0.33g/g的干物质,最高为20g/g的干物质。这部分水是食品中结合最不牢固和最容易流动的水。其蒸发焓基本上与纯水相同,既可以结冰也可作为溶剂,并且还有利于化学反应的进行和微生物的生长。 表2-4 吸着等温线上不同区水分特性(自己画图) 2.5.2 滞后现象* 如果向干燥样品中添加水(回吸作用)的方法绘制水分吸着等温线和按解吸过程绘制的等温线并不相互重叠,这种不重叠性称为滞后现象。在一定Aw时,食品的解吸过程一般比回吸过程时含水量更高。 2.6 水分活度与食品的稳定性 2.6.1 食品水分与微生物生命活动的关系 不同类群微生物生长繁殖的最低水分活度范围是: 大多数细菌为0.99~0.94 大多数霉菌为0.94~0.80 大多数耐盐细菌为0.75 耐干燥霉菌和耐高渗透压酵母为0.65~0.60 在水分活度低于0.60时,绝大多数微生物就无法生长。 2.6.2 食品水分与食品化学变化的关系 降低食品的Aw,可以延缓褐变,减少食品营养成分的破坏,防止水溶性色素的分解。 但Aw过低,则会加速脂肪的氧化酸败,又能引起非酶褐变。要使食品具有最高的稳定性所必需的水分含量, 最好将Aw保持在结合水范围内。这样,使化学变化难于发生,同时又不会使食品丧失吸水性和复原性。 第3章碳水化合物(Carbohydrates) 3.2.3 化学反应 3.2.3.1 美拉德反应 Maillard reaction(结构式不用记,但生成产物要记住) 定义——指羰基与氨基经缩合、聚合反应生成类黑色素物质的反应。胺、氨基酸、蛋白质与糖、醛、酮之间的这类反应统称之为。 1. 机理——大体上分为: 1)初始阶段: ① 羰氨缩合 ② 环化为N-葡基胺 ③阿姆德瑞(Amadori)重排——经分子重排生成氨基脱氧酮糖(果糖胺) 2)中期阶段:分两方向进一步降解:方向一 脱氨脱水生成羟甲基糠醛 方向二 脱氨基重排生成还原酮 氨基酸与二羰基化合物的作用,也称为斯特勒克(Strecker)降解作用 3)未期阶段:包括醇醛缩合和聚合作用;参加的底物包括上几步所产生的所有醇、醛、糠醛、二羰基化合物、还原酮类等; 生成黑色素。 3. 美拉德反应与食品工业 非酶褐变对食品质量的影响(列出几个大框,每个大框要举个列子) 1、对营养质量的影响 2. 对感官质量的影响 3.对口味的影响 2、斯特勒克降解作用是褐变中产生嗅感物质的主要过程。这也是人工生产味感物质的主要原理。 3、亚硫酸盐的影响P112 碳基可以和亚硫酸根形成加成化合物,其加成物能与氨基化合物缩合,但缩合产物不能再进一步生成Schiff碱和N-葡萄糖基胺,因此,可用二氧化硫和亚硫酸盐来抑制羰氨反应褐变。 4、3.2.3.2 焦糖化褐变P55 定义——糖类在没有含氨基化合物存在的情况下加热到其熔点以上时发生的褐变反应。 机理:受强热情况下,糖类生成两类物质:一类是糖的脱水产物,即焦糖或称酱色;一类是裂解产物,是一些挥发性的醛酮类,可进一步缩合、聚合形成粘稠状的黑色物质。 影响焦糖化褐变的因素 1、 不同糖的种类因熔点不同而反应速度不同。 2、 糖液pH =8时要比pH=5.9时快10倍。 (一)吸潮性和保潮性 吸潮性——在较高的空气湿度下吸收水分的性质。 保潮性——较高湿度下吸收水分和在较低湿度下散失水分的性质。 比较吸潮保潮性:果糖73.4%>高转化糖>低转化糖>蔗18.4%>葡萄糖 14.5% 3.4.2 淀粉P74 1、淀粉粒结构:淀粉颗粒的大小与形状随植物的品种而改变。所有的淀粉颗粒皆显示出一个裂口,称为脐点。淀粉分子从脐点伸向边缘。大多数淀粉颗粒在脐点的周围显示出生长环。 2、直链淀粉结构:线性的。a-1,4苷键相连接,聚合度为200~980,在溶液中,可取螺旋结构、部分断开结构和不规则的卷曲结构P75 3.4.2.2 糊化(α-化)和老化 (1)淀粉的糊化(starch dextrinization) 1、糊化的概念 糊化--b-淀粉在水中经加热后出现膨润现象,继续加热,成为溶液状态,这种现象称为糊化,处于这种状态的淀粉称为a-淀粉。 膨润现象--在水中经加热后,一部分胶束被溶解,空隙逐渐扩大,淀粉粒因吸水而膨胀,胶束消失,这种现象称为膨润现象。 3、影响糊化的因素: 1)淀粉粒结构(分子间缔合程度,支直链比例,颗粒大小)。 2)温度高低(见P76图3-4) 3)共存的其它组分 :脂类、盐会不利糊化。 (2)淀粉的老化 1、淀粉老化的定义——经过糊化的淀粉在较低温度下放置后,会变得不透明甚至凝结而沉淀,这种现象为淀粉的老化。 老化后的淀粉失去与水的亲和力,难以被淀粉酶水解,因此不易被人体消化吸收,遇碘不变蓝色。 3、影响老化的因素: ① 淀粉种类: 直链易 , 支链难 。链长适中的易,过长过短都 难 。 ② 含水量: 30~60% 易 , <10%或大量水中 难 。 ③ 温度: 2~4℃ 易 , >60或<-20℃ 难;冷却速度慢加重老化。 ④ pH :<7或>10 难 。 ⑤ 脂类物质可使直链淀粉的老化变 难 。 4、淀粉老化原理及应用实例 1)防止淀粉老化:将糊化后的α-淀粉,在80 ℃以下的高温迅速去除水分或冷却到0 ℃以下迅速脱水,成为固定的α-淀粉. 2)油炸方便面加工: 配料混合—搅烂成面团—压延、切条折花、成型—蒸熟—油炸—冷却—成品。 3)速煮米饭加工: 蒸煮—突然降温至-10~-30℃然后升华干燥(或高温热风干燥) 。 果葡糖浆 用高果糖浆配制的汽水、饮料入口后给人一种爽神的清凉感。 对加工果脯、果酱等 不仅能保留果品的风味本色,鲜艳而透亮,还可防止其表面干涸翻砂。 糕点加工,质地松软,久贮不干,保鲜性能优良,可明显提高产品延长货架保存期。 用于冰淇淋等冷饮加工时,可克服经常出现冰晶的缺点,使产品质地柔软、细腻可口。 在营养和代谢方面尚有特殊的功能 。 3.4.3 果胶 :果酱与果冻的胶凝剂。软糖原料,在食品添加剂中是重要的增稠剂。(重点) 影响果胶的胶凝的因素:糖分,ph,甲氧基的比例 果胶的应用 果胶结构 主链 是α-半乳糖醛酸的1,4相连的聚合衍生物. 衍生: 甲酯化, 成盐 侧链 在主链中相隔一段距离含有鼠李糖基侧链 果胶的主要用途 作为果酱与果冻的胶凝剂。 慢凝胶的HM和LM果胶用于制造凝胶软糖; LM果胶在生产酸奶时用于水果基质; HM果胶使用于高温和巴氏消毒的乳制品; 果酱、果汁、饮料、冰淇淋,添加量<1% 第四章 脂质 4.1 概述 4.1.1 脂质的定义及作用 定义:用油溶性溶剂如乙醚、石油醚、氯仿等从动物、 植物、微生物的组织和细胞中提取出的物质的统称。 脂质(lipid):脂肪(fat) 类脂( lipoid) 作用 :1、是人类重要的能源和营养源: •参与体内机体的构成,如构成细胞膜。 •供能,产热是碳水化物、蛋白质的两倍。 •提供人体需要的多不饱和脂肪酸(PUFs) (1) 系统命名 饱和脂肪酸:以直链碳原子数来命名 eg:CH3-(CH2)9-CH2-COOH 称为“十二(烷)酸”(习用名为“月桂酸”) 不饱和脂肪酸: 链长、不饱和中心的位置与构型 (顺-式用“c”、反-式用“t”)、取代基的位置和性质 CH3-(CH2)4-CH=CH-CH2-CH=CH-(CH2)7-COOH (习用名为“亚油酸”) 称为: 顺-9-顺-12-十八碳二烯酸 或: 十八碳-顺-9-顺-12-二烯酸 或: 十八碳-9c,12c-二烯酸(简便) (2)数字命名 (3)俗名或普通名(看书) 4.2.2.1 油脂的结构 1、结构(采用立体定向编号Sn-系统)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
N:稀溶液中溶质的mol分数; n2:稀溶液中溶质的mol数。
n1:稀溶液中水的mol数;
3.3.2 水分活度和温度的关系
上边对于水分活度定义及测定方法的叙述中,均强调了在一定的温度 下。也就是说温度对于水分活度的值有较大的影响。
物理化学中的克劳修斯-克拉贝龙方程精确表示了水分活度与绝对温度 (T)之间的关系:
m 1=Y轴 截 距 1 +斜 率
Ⅱ区:多层水区,即食品中与酰胺基、羧基等基团和结合水、邻近水 以水-溶质、水-水以氢键和缔合作用被相对固定的水,也包括直径小于 1μm的毛细管的水;这部分水的aw一般在0.25~0.8之间,相当于物料含 水量在0.07g/g干物质至0.14~0.33g/g干物质。当食品中的水分含量相当 于Ⅱ区和Ⅲ区的边界时,水将引起溶解过程,它还起了增塑剂的作用并且 促使固体骨架开始溶胀。溶解过程的开始将促使反应物质流动,因此加速 了大多数的食品化学反应。
由b可以得出结论:在比较冰点以上或冰点以下的水分活度值时应该注 意到以下两个重要的区别。第一,在冰点以上,水分活度是样品组成和温 度的函数,并且样品组成对于水分活度值有明显的影响;而在冰点以下时, 水分活度与样品的组成无关,仅与温度有关。因此不能根据冰点以上水分 活度值来预测体系中溶质种类和含量对冰点以下体系发生变化的影响。第 二,冰点以上和以下时,就食品而言,水分活度的意义是不一样的。例如: 在水分活度为0.86的-15℃的食品中,微生物不再生长,其它化学反应的速 度也很慢;但在同样的水分活度而温度是20℃情况下,一些化学反应将快 速进行,一些微生物也将中等速度生长。
定样品水分活度的对数在不太宽的温度范围内随绝对温度的升高而正比例 升高。
b.但在较大的温度范围内, lnaw与-1/T之间并非始终为一直线关系;当 冰开始形成时,lnaw与-1/T曲线中出现明显的折点,冰点以下lnaw与-1/T的变 化率明显加大了,并且不再受样品中非水物质的影响;这是因为此时水的 汽化潜热应由冰的升华热代替,也就是说前述的aw与温度的关系方程中的 △H值大大增加了。要解释冰点以下aw与样品的组成无关,现在的观点认为, 在冰点以下样品的蒸气分压等于相同温度下冰的蒸气压,并且水分活度的 定义式中的p0此时应采用过冷纯水的蒸气压。
dlnaw/d(1/T)=-△H/R……………….(1) 其中R为气体常数,△H为样品中水分的等量净吸附热。
整理此式可得: lnaw=-kΔH/R(1/T)………………(2) 其中:此处的ΔH 可用纯水的汽化潜热表示,是常数,其值为40537.2J/mol;
样 品 的 绝 对 温 度 - 纯 水 的 蒸 气 压 为 样 品 蒸 气 压 ( p ) 时 的 绝 对 温 度
3.3.3 吸湿等温曲线
一、定义及测定方法
定义:在恒定温度下,食品的水含量(以g水/g干物质表示)对其活度 形成的曲线称为等温吸湿曲线(MSI)。
大多数食品或食品原料的吸湿等温线为S型,而水果、糖制品、含有大 量糖和其他可溶性小分子的咖啡提取物等食品的吸湿等温线为J型。如图:
测定方法:在恒定温度下,改变食品中的水分含量,测定相应的活度, 以水分含量为纵轴、Aw为横轴画出曲线。
不同种类的食品即使水分含量相同,其腐败变质的难易程度也有明 显的差异。食品的品质和贮藏性能与水分活度有密切的关系。
3.3.1 水分活度的定义及测定方法
一、定义:一定温度下样品水分蒸气压与纯水蒸气压的比值;
用公式表示即为:aw=p/p0=ERH/100=N=n1/(n1+n2)
其中:aw:水份活度; p:样品中水的蒸气分压 p0:同温纯水蒸气压; ERH:样品周围空气不与样品换湿时的平均相对湿度;
食品单分子层水含量的意义及计算:
意义:由于一般食品当其含水量接近单层值时,有最大的稳定性,因而根据具体对象确 定其单层值,对于食品的有效保存是非常重要的。
计算:a..公式法:BET方程式:
m (A 1-w A w )=m 1 1C+m C1 -C 1A w
其中:m:水分含量(g水/g干物质) m1:单层值 C:常数 b.作图法:以Aw/[m(1-Aw)]~Aw作BET图,在一定范围内有较好的 线性关系。由图上可 以直接测量出Y轴截距及斜率;通过下式求出M1值。
c.结合水不易结冰,由于这种性质使得植物的种子和微生物的孢子 得以在很低的温度下保持其生命力;而多汁的组织在冰冻后细胞结构往 往被体相水的冰晶所破坏,解冻后组织不同程度的崩溃;
d.结合水不能作为可溶性成分的溶剂,也就是说丧失了溶剂能力;
e.体相水可被微生物所利用,结合水则不能。
3.3 水分活度与吸湿等温曲线
二、MSI中的分区
一般的MSI均可分为三个区,如下图所示:
Ⅰ区:为构成水和邻近水区,即与食 品成分中的羧基、氨基等基团通过氢 键或静电引力相互结合的那部分水。 由于这部分水比较牢固的与非水成分 结合,因此aw较低,一般在0~0.25之 间,相当于物料含水量0~0.07g/g干 物质。这种水不能作为溶剂而且在40℃不结冰,对固体没有显著的增塑 作用,可以简单的看作固体的一部分。 要注意的是,一般把Ⅰ区和Ⅱ区交界 处的水分含量称为食品的“单分子层” 水含量,这部分水可看成是在干物质 可接近的强极性基团周围形成一个单 分子层所需水量的近似值。
Ⅲ区:自由水区,aw在0.8~0.99之间,物料最低含水量在0.14~0.33 g/g干物质,最高为20g/g干物质。这部分水是食品中与非水物质结合最不 牢固、最容易流动的水,也称为体相水。其蒸发焓基本上与纯水相同,既 可以结冰也可作为溶剂,并且还有利于化学反应的进行和微生物的生长。 在凝胶和细胞体系中,体相水以物理的方式被截留,其宏观流动性受到影 响,但它与稀盐溶液中水的性质相似。
k =
纯 水 的 蒸 气 压 为 样 品 蒸 气 压 ( p ) 时 的 绝 对 温 度
K的直观意义是在达到同样水蒸气压时,食品的温度比纯水温度高出的比值, 本质反映了食品中非水成分对水活性的影响。食品中非水成分越多并且与水的结
合能力越强,k值越大,相同温度时aw值越小;反之亦然。 讨论:a.由公式(2)可知, lnaw与-1/T之间为一直线关系,其意义在于:一
