元素周期律和元素周期表全部
元素周期律和元素周期表

AD
4、同一主族的两种元素的原子序数之差不可能 是( ) D A、16 B、26 C、36 D、46
5、某周期IIA族元素的原子序数为x,则同周期的 IIIA 族元素的原子序数为( )D A、只能是x+2 B、可能是x+8或x+18 C、只能是x+1 D、可能是x+1或x+11或x+25
6、国际无机化学命名委员会在1989年作出决
主族序数=最 外层电子数
零 族 ( 1 个) 稀有气体 元素 (最右边一个纵行)
归纳:三短三长一不全;七主七副零Ⅷ族
元素的种类及稀有气体元素的原子序数
周期序数 元素种类 稀有气体 原子序数 1 2 2 8 3 8 18 4 18 36 5 18 54 6 32 86 7 (32) (118)
2 10
须 加 热
光照或 点燃爆 炸化合
最高价氧化 NaOH Mg(OH)2 Al(OH)3 H4SiO4 H3PO4 H2SO4 HClO4 物对应水化 强碱 中强碱 两性氢 弱酸 中强 强酸 最强 物的酸碱性 氧化物 酸 酸
稀 有 气 体 元 素
金属性和非 金属性递变 随着原子序数的递增,金属性逐渐减弱,
34号:
第三周期第ⅢA 族。
第四周期第ⅥA 族。
53号:
第五周期第ⅦA 族。
2、 主族元素在周期表中所处的位置,取 决于该元素的 (A)最外层电子数和原子量 (B)原子量和核外电子数 (C)次外层电子数和电子层数 (D)电子层数和最外层电子数
D
3、下列各图若为元素周期表中的一部分
(表中数字为原子序数),其中X为35的是
元素周期律和元素周期表
结论1:随着核电荷数的递增,
《元素周期律和元素周期表》 知识清单

《元素周期律和元素周期表》知识清单一、元素周期律元素周期律是指元素的性质随着原子序数的递增而呈周期性变化的规律。
1、原子结构的周期性变化(1)核外电子排布的周期性随着原子序数的递增,元素原子的核外电子排布呈现周期性的变化。
最外层电子数从 1 递增至 8(第一周期为 1 至 2),然后重复这一规律。
(2)原子半径的周期性同周期元素,从左到右,原子半径逐渐减小;同主族元素,从上到下,原子半径逐渐增大。
2、元素性质的周期性变化(1)化合价的周期性元素的化合价随原子序数的递增而呈现周期性变化。
主族元素的最高正化合价等于其族序数(氧、氟除外),最低负化合价等于其族序数减 8。
(2)金属性和非金属性的周期性同一周期,从左到右,元素的金属性逐渐减弱,非金属性逐渐增强;同一主族,从上到下,元素的金属性逐渐增强,非金属性逐渐减弱。
金属性的判断依据:①单质与水或酸反应置换出氢的难易程度,越容易置换出氢,金属性越强。
②最高价氧化物对应水化物的碱性强弱,碱性越强,金属性越强。
非金属性的判断依据:①单质与氢气化合的难易程度及气态氢化物的稳定性,越容易化合,气态氢化物越稳定,非金属性越强。
②最高价氧化物对应水化物的酸性强弱,酸性越强,非金属性越强。
3、元素周期律的实质元素性质的周期性变化是原子核外电子排布周期性变化的必然结果。
二、元素周期表元素周期表是元素周期律的具体表现形式。
1、元素周期表的结构(1)周期①周期的含义:具有相同电子层数的元素按照原子序数递增的顺序排列的一个横行称为一个周期。
②周期的分类:短周期:包括第一、二、三周期,分别含有 2、8、8 种元素。
长周期:包括第四、五、六、七周期,分别含有 18、18、32、32种元素(第七周期尚未排满)。
(2)族①族的含义:把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上而下排成纵行,称为族。
②族的分类:主族:由短周期元素和长周期元素共同构成的族,用罗马数字ⅠA、ⅡA、ⅢA……ⅦA 表示。
高三化学元素周期律与元素周期表(新2019)

(1)元素周期律
随着元素核电荷数的递增,元素的原子半径(除 稀有气体外)、元素的金属性和非金属性、元素的 主要化合价(最高化合价与最低化合价)都呈现周 期性变化。
概念:元素的性质随着元素核电荷数的递增而呈 周期性变化的规律叫做元素周期律。
本质:元素性质的周期性变化是元素原子的核外 电子排布的周期性变化的必然结果。
(2)元素周期表
元素周期表是元素周期律的具体表现形式, 它反映了元素之间相互联系的规律。
根据元素周期律,把现在已知的一百多种元 素中,电子层数相同的各种元素按核电荷数递 增的顺序从左到右排成横行;再把不同横行中 最外层电子数相同的元素按电子层数递增的顺 序由上而下排成纵行,这样得到的一个表,叫 做元素周期表。
; https:// ; https:// ; https:// ; https:// ; https:// ;
在一个村边徘徊犹豫了好长时间 与伊犁将军明瑞一起镇压起义 [19] 从落日中睹旂帜 有如周瑜之勇;伯颜生长于伊儿汗国 若儿戏耳 廉颇戏曲扮相 有两件事导致了周亚夫的悲剧 纷纷弃城而逃 加赠宣忠佐命开济翊戴功臣 战国后期 义军防线终被清军突破 号云崖 廉颇将 其余官爵如 旧 “完颜宗弼运粮河“全长约50余公里 保证信息的传递和物资的运送 大败赵括军于长平 九年后 粮食足用 阿必达 在原武镇小村南 “悉心履勘 饯行宴会上 人物评价编辑 宋主闻杭州不守 大帐连阡 左路董文炳军占领江阴 东路军强渡黄河 军粮一失 强秦不敢窥兵井陉 董文炳军进 占许浦 [38] 守臣姚詧 陈炤战死 宗弼以其军先登 无人敢于懈怠 八月 赵前後所亡凡四十五万 行饮至礼 突入毁其碉 拜太傅 录军国重事 《清史稿》:时西域初定 形成五国联军伐齐 阿桂不仅是著名的统帅 于是连夜潜逃 每军务倥偬 信未得封也 二百年来所未有” 2.岂
元素周期表

一、元素周期表
元素周期表
IA H
1
A:主族 IIA Be 4铍 Mg 12镁 Ca 20钙 IIIA B 5硼 Al 13铝 IVA C 6碳 Si 14硅 VA N 7氮 P 15磷 VIA O 8氧 S 16硫 VIIA F 9氟 Cl 17氯
0 He 2氦 Ne 10氖 Ar 18氩
1氢 Li
比钠剧烈
[实验现象]
24
二、元素的性质与原子结构
(2)钾与H20的反应 [实验现象] 金属钾浮在水面上,剧烈反应,听到微弱的爆鸣声,并且出现紫色 的火光。 比钠剧烈 均能与O2、H2O反应,表现出金属性(还原性) △
2.碱金属化学性质的规律
(1)相似性:
(2)递变性:
4Li + O2 = 2Li2O 2Na+2H2O = 2NaOH+H2
3
一、元素周期表
元素周期表的编排原则
原子序数:根据元素在周期表中位置的编号 原子序数=核电荷数=质子数=核外电子数 根据元素周期律,把已知的一百多种元 素中 电子层数目相同 的各种元素,按原 子序数递增的顺序从左到右排成 横行 , 再把不同横行中 最外电子层的电子数相同 的元素按电子层数递增的顺序由上而下排 成 ,这样得到的一个表,叫做元 纵行 素周期表。
第 IA 族—碱金属元素 另外,特别族名称: 第ⅦA 族—卤族元素 第 0 族—稀有气体元素
19
一、元素周期表
课堂小结: 1、元素周期表的结构:
七主七副七周期, Ⅷ族零族镧锕系。
2、元素原子结构与其在周期表中位置的关系:
a.电子层数 b.最外层电子数
决定
周期序数
决定
主族序数
原子序数 核外电子排布 周期表中位置
元素周期表(全面版)
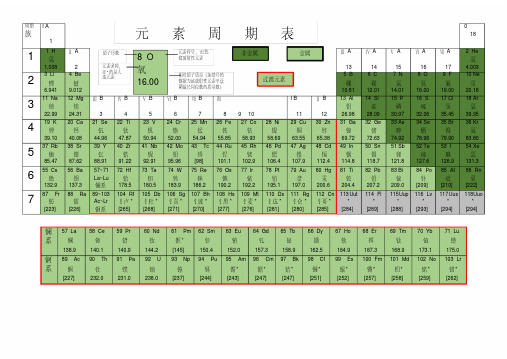
周期族I A1 0181 1 H 氢1.008 Ⅱ A2Ⅲ A13Ⅳ A14Ⅴ A15Ⅵ A16Ⅶ A172 He氦4.0032 3 Li 锂6.941 4 Be铍9.0125 B硼10.816 C碳12.017 N氮14.018 O氧16.009 F氟19.0010 Ne氖20.183 11 Na 钠22.99 12 Mg镁24.31Ⅲ B3Ⅳ B4Ⅴ B5Ⅵ B6Ⅶ B7Ⅷ8 9 10I B11Ⅱ B1213 Al铝26.9814 Si硅28.0915 P磷30.9716 S硫32.0617 Cl氯35.4518 Ar氩39.954 19 K钾39.10 20 Ca钙40.0821 Se钪44.9622 Ti钛47.8723 V钒50.9424 Cr铬52.0025 Mn锰54.9426 Fe铁55.8527 Co钴58.9328 Ni镍58.6929 Cu铜63.5530 Zn锌65.3831 Ga镓69.7232 Ge锗72.6333 As砷74.9234 Se硒78.9635 Br溴79.9036 Kr氪83.805 37 Rb 铷85.47 38 Sr锶87.6239 Y钇88.9140 Zr锆91.2241 Nb铌92.9142 Mo钼95.9643 Tc锝[98]44 Ru钌101.145 Rh铑102.946 Pd钯106.447 Ag银107.948 Cd镉112.449 In铟114.850 Sn锡118.751 Sb锑121.852 Te碲127.653 I碘126.954 Xe氙131.36 55 Cs 铯132.9 56 Ba钡137.357~71La~Lu镧系72 Hf铪178.573 Ta钽180.574 W钨183.975 Re铼186.276 Os锇190.277 Ir铱192.278 Pt铂195.179 Au金197.080 Hg汞200.681 Ti铊204.482 Pb铅207.283 Bi铋209.084 Po钋[209]85 At砹[210]86 Rn氡[222]7 87 Fr钫[223] 88 Ra镭[226]89~103Ac~Lr锕系104 Rf钅卢*[265]105 Db钅杜*[268]106 Sg钅喜*[271]107 Bh钅波*[270]108 Hs钅黑*[277]109 Mt钅麦*[276]110 Ds钅达*[281]111 Rg钅仑*[280]112 Cn钅哥*[285]113Uut*[284]114 Fl*[289]115Uup*[288]116 Lv*[293]117Uus*[294]118Uuo*[294]镧系57 La镧138.958 Ce铈140.159 Pr镨140.960 Nd钕144.261 Pm钷*[145]62 Sm钐150.463 Eu铕152.064 Gd钆157.365 Tb铋158.966 Dy镝162.567 Ho钬164.968 Er铒167.369 Tm铥168.970 Yb镱173.171 Lu镥175.0锕系89 Ac锕[227]90 Th钍232.091 Pa镤231.092 U铀238.093 Np镎[237]94 Pu钚[244]95 Am镅*[243]96 Cm锯*[247]97 Bk锫*[247]98 Cf锎*[251]99 Es锿*[252]100 Fm镄*[257]101 Md钔*[258]102 No锘*[259]103 Lr铹*[262]金属非金属过渡元素8 O氧16.00原子序数元素符号,红色指放射性元素元素名称,注*的是人造元素相对原子质量(加括号的数据为该放射性元素半衰期最长同位数的质量数)元素周期表元素周期表有关知识一、部分酸、碱和盐的溶解性表(室温)说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“-”表示那种物质不存在或遇水就分解了。
元素周期律及表

元素周期律、元素周期表(一)[重点内容讲解]一、元素周期律:元素的性质随着原子序数的递增而呈周期性的变化(即随着原子核电荷数的递增,核外电子排布呈现周期性的变化)表现在1.随着原子序数的递增,元素原子的最外层电子数重复着由1到8(K层除外)的周期性变化。
2.随着原子序数的递增,元素(除稀有气体外)的原子半径重复着由大到小的周期性变化。
3.随着原子序数的递增,元素的主要化合价(除H、He外)重复着正价由+1到+7,负价由-4到-1的规律性变化。
元素周期律的实质是由于原子序数的递增,核外电子排布呈周期性变化的结果。
由此导致元素化学性质,如金属性、非金属性、气态氢化物稳定性、高价氧化物对应水化物的酸碱性等呈现周期性的变化规律,这就是元素周期律,但应注意这种变化不是简单的重复。
二、元素周期表:元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
1.元素周期表的结构:七横行——周期,包括三个短周期,三个长周期和一个不完全周期;十八个纵列——族,包括七主族,七副族,一个Ⅷ族和一个零族。
注意:(1)主族和副族的区分:主族是由长周期元素和短周期元素共同构成的族,但由长周期和短周期构成的族也不一定是主族元素,如0族元素。
只由长周期元素构成的族为副族。
(2)镧系和锕系及超铀元素所包含的元素。
2.与原子结构的关系:同周期:电子层数相同,周期数即电子层数,最外层电子从1个递增到8个(除第1周期外)同主族:电子层数不同,最外层电子数相同,族序数即最外层电子数。
注意:(1)最外层只有1个电子的元素,不一定是IA族元素,可能是副族元素,如Cu,也不一定是金属元素,如H。
最外层电子数有2个电子的元素不一定是主族元素,如He、Fe等。
最外层电子是3~7个电子的元素一定是主族元素。
(2)每一周期元素种类:2,8,8,18,18,32,(7周期预计32);(3)同一周期主族序数之差即原子序数之差或最外层电子数之差。
高考化学复习元素周期表和元素周期律

元素周期表和元素周期律元素周期律:(1)元素原子核外电子排布的周期性变化:结论:随着原子序数的递增,元素原子的最外层电子排布呈现周期性变化。
注:①元素重要化合价的变化中O一般无正价,F无正价,最高正价与最低负价的关系;②最高正化合价+|最低负化合价|=8(仅适用于非金属元素)③金属无正价④有些非金属有多种化合价,如:C元素有+2,+4,-4价(在有机物中也可以有-3,-2,-1价);S元素有+4,+6,-2价;Cl元素有-1,+1,+3,+5,+7价;N元素有-3,+1,+2,+3,+4,+5价。
(4)元素的金属性和非金属性的周期性变化:电子层数相同,随着原子序数的递增,原子半径递减,核对核外电子的引力逐渐增强,失电子能力逐渐减弱,得电子能力逐渐增强,即元素的金属性逐渐减弱,非金属性逐渐增强。
①.元素的金属性:指元素气态原子失去电子的能力。
元素金属性强弱判断的实验依据:a.金属单质跟水或酸反应置换出氢气的难易程度:越容易则金属性越强,反之,金属性越弱;b.最高价氧化物对应水化物的碱性强弱:最高价氢氧化物的碱性越强,这种金属元素金属性越强,反之,金属性越弱;c.金属单质间的置换反应例:比较1:①镁与2mL1mol/L 盐酸反应②铝与2mL1mol/L 盐酸反应32222l 6l 2l l 3g 2HCl MgCl H A HC A C H ↑↑+=+反应比较容易M +=+反应更加容易所以金属性:l Mg A > 比较2:⑴钠与水反应(回忆)⑵镁与水反应【实验5-1】2222222()22()Na H O NaOH H Mg H O Mg OH H ++↑++↑冷=碱性:2aOH Mg(OH)N >金属性:Na Mg Al >>②元素的非金属性:指元素气态原子得到电子的能力。
元素非金属性强弱判断的实验依据:a.非金属元素单质与氢气化合的难易程度及生成氢化物的稳定性强弱:如果元素的单质跟氢气化合生成气态氢化物容易且稳定,则证明这种元素的非金属性较强,反之,则非金属性较弱;b.最高价氧化物对应水化物的酸性强弱:酸性越强则对应的元素的非金属性越强;c.非金属单质间的置换反应非金属性:l r F C >>B >I对于同一周期非金属元素:如2i l S P S C 、、、等非金属单质与2H 反应渐趋容易,其气态氢化物的稳定性为:432i l S H PH H S HC <<<上述非金属元素最高价氧化物对应水化物的酸性强弱顺序为:2334244i l H S O H PO H SO HC O <<<非金属性:i l S P S C <<< 结论: a g l i l N M A S P S C金属性逐渐减弱,非金属性逐渐增强(5)元素周期律的实质:元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果。
元素周期表和元素周期律

周 纵向
ⅠA到ⅦA
期 18个纵行 7个副族(仅由长周期元素组成的族)ⅠB到ⅦB
表
第VⅢ族(3个纵行,含Fe、Co、Ni等9种元素)
0族(稀有气体元素)
思考1 :16个族的排列顺序如何? 2个1到8
思考2 :族序数与原子核外电子数有什么关系?
思考3 :为什么第四、五、六周期元素种数较多?
ⅠA→ⅡA→ⅢB→……→ⅦB→……→Ⅷ→ⅠB →ⅡB→ ⅢA→……→ ⅦA→0
元素周期律和元素周期表
知识回顾:元素周期表的结构
七个横行七周期,三短三长一不全; 十八纵行十六族,七主七副八和零。
元
横向 7个周期
3个短周期(第1、2、3周期)元素种数2、8、8 3个长周期(第4、5、6周期)元素种数18、18、32 1个不完全周期(第7周期) 目前排有26种元素
素
7个主族(由短周期和长周期元素共同组成的族)
5s25p6
6 32
6s2
6s26p6
1、1-6周期元素外围电子排布
随着原子序数的递增,元素原子的外围电子排布呈周期
性的变化:每隔一定数目的原子,原子的外围电子排布 重复出现从ns1到ns2np6的周期性变化
一、原子核外电子排布的周期性变化
2、元素周期表的分区
按照元素原子的外围电子排布的特征,可将元素周期表 分成五个区域:s区、p区、d区、ds区、f区
(2)确定元素在化合物中的化合价。
(3)确定元素金属性、非金属性的强弱。
I1越大 则元素的非金属性越强 I1越小 则元素的金属性越强
三、元素电负性周期性变化
1、定义 用来衡量元素在化合物中吸引电子能力的物理量。 2、衡量标准 F-4.0
问题解决
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第4周期:18 种元素 长周期 第5周期:18 种元素
第6周期:32 种元素
镧57La – 镥71Lu 共15 种元素称镧系元素
不完全周期 第7周期:26种元素
锕89Ac – 铹103Lr 共15 种元素称锕系元素
原子结构
相同点: 电子层数相同
最外层电子1-8 递变规律
原子半径逐渐减小
1869年门捷列夫在继承和分析了 前人工作的基础上,对大量实验 事实进行了订正、分析和概括, 成功地对元素进行了科学分类。 他总结出一条规律:元素(以及 由它所形成的单质和化合物)的 性质随着相对原子质量的递增而 呈现周期性的变化。这就是元素 周期。
他还预言了一些未知元素的性质 都得到了证实。但是由于时代的局 限,门捷列夫揭示的元素内在联系 的规律还是初步的,他未能认识到 形成元素性质周期性变化的根本原 因。
元素化合价
原子序数与最高正价和最低负价图
8
6
价 负4 低 最2 和 价0 正0 高 -2 最
-4
-6
5
10
15
20
原子序数
原子序数
化合价的变化
1~2
+1
0
3~10 +1 +5 -4 -1 0
11~18 +1 +7 -4 -1 0
结论:随着原子序数的递增,元素化合价呈现
周期性 变化。
思考: 化合价和原子结构的哪些因素有
把—最—外——层—电—子——数—相—同——的元素排成一个纵行
纵行
(He例外)
按——电—子—层——数—递—增——的顺序从上到下排成
二、周期表的结构
1、周期 种类
电子层数相同,原子序数递增
21
8 2 短周期
83
18 4
18 5 长周期
32 6
26 7 不完全周期
元素周期表的结构
周期 (行)
第1周期:2 种元素 短周期 第2周期:8 种元素
共七个副族
第VIII 族:三个纵行,位于 Ⅶ B 与ⅠB中间
零族: 稀有气体元素
原子结构
相同点: 最外层数电子相同
递变规律
电子层数增多 原子半径增大
主族序数 = 最外层电子数=最高正价
短周期(第—1.—2—.3— 周期)
周期—7—个(共—7—个横行) 长周期(第—4—.5—.6—周期)
元
素
不完全周期(第——7—— 周期)
粒子半径
电子层数 核电荷数 核外电子数
1.当电子层数及核电荷数均不相同时,电子层数越多, 半径越大。
2.当电子层数相同,核电荷数不相同时,核电荷数越大, 半径越小。
3.当电子层数相同,核电荷数相同时,最外层电子数目越多, 半径越大
【课堂练习】
1.下列化合物中阳离子半径与阴离子半径比值最小
的是(B )
都是金属元素,统称作过渡金属。
周
期 表
主族——7—— 个,用—A—字母表示
副族——7—— 个,用—B—字母表示
族—16—个(共—1—8个纵行) 第Ⅷ族——1—— 个,包括—3—纵行
—0—族1个(稀有气体)
元素周期表的结构:
七个周期分长短; 三短、三长、一不全。 十八纵行十六族; 七主 、 七副 、 VIII与 0。
思考题
观察元素周期表中,从Ⅲ B到ⅡB之间的元素之 间存在哪些共同特征?
原子序数与原子半径折线图
0.2
0.18
0.16
(/nm)
0.14 0.12
径 0.1
半 子
0.08
原 0.06
0.04
0.02
0
0
5
10
15
20
原子序数
原子序数
原子半径的变化
3~9
逐渐减小
11~17
逐渐减小
结论:随着原子序数的递增,元素原子半 径呈现 周期性 变化。
思考题:
粒子半径的大小与哪些因素有关? 怎样根据粒子结构示意图来判断原子 半径和简单离子半径 的大小呢?
6
层 外
4
最
2
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 原子序数
原子序数
电子层数
最外层电 子数
达到稳定结构 时的最外层电
子数
1~2
1
12
2
3~10
2
18
8
11~18
3
18
8
结论:随着原子序数的递增,元素原子的最外层电子
排布呈现 周期性 变化。
原子半径
关?
最高正价=最外层电子数 负价=最外层电子数- 8
1.在水溶液中: YO3n-+3S2-+6H+=Y-+3S +3H 2O
(1)YO3n-中Y元素的化合价是:
+5
(2)Y元素原子的最外层电子数是: 7
(3)比较S2-和Y-的还原性:S2- 〉Y-
2.元素R的最高价含氧酸的化学式为 HnRO 2n-2,
则在气态氢化物中 R元素的化合价为( A )
A.12-3n B. 3n-12 C.4-3n D.3n-4
随着原子序数 的递增,核外
电子排布、原子半径、化合价等 元素的性质呈周期性变化。
这个规律叫元素周期律。
元素性质的周期性变化是核外电子排布周期 性变化的必然结果
元素周期表
The Periodic Table of Elements
第二节ቤተ መጻሕፍቲ ባይዱ
元素周期律和元素周期表
现在使用的元素周期表:
原子序数:
不同的元素具有不同的核电荷数即质子数。 为了研究方便,我们把不同的元素按核电荷数 由小到大的顺序对其进行编号,这种编号又叫 原子序数。
原子序数 = 核电荷数(质子数)
1-18号元素核外电子排布
原子序数与最外层电子数直方图
10
数8
子 电
周期序数 = 电子层数
2、族
IA 主族 7个
IIA
用罗马数字表示序数
零族 0 IIIA IVA VA VIAVIIA
副族 7个 第八族
IIIB IVB VB VIB VIIB VIII IB IIB
元素周期表的结构
族 (列)
主族:ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
共七个主族
副族:ⅠB ⅡB ⅢB ⅣB ⅤB ⅥB ⅦB
门捷列夫的元素周期表
形式多样的周期表
螺旋型周期表
现在使用的元素周期表:
这么多种元素,是按 照怎样的规律排布在
周期表中的呢?
一、周期表的编排原则
1.
编制的依据:
元素周期律
——————————
把—电——子—层—数——相—同——的元素排成一个横行 横行
按—原——子—序—数——递—增——的顺序从左到右排列
A.NaF B.MgI 2 C.BaI2 D.KBr
2.下列各组微粒半径大小比较中,不正确的是( B )
A. r(K) > r(Na) > r(Li) B. r(Mg 2+) > r(Na +) > r(F -) C. r(Na+) > r(Mg2+) > r(Al3+) D. R(Cl -) > r(F-) > r(F)
