实验室中用过氧化氢溶液制取氧气的化学方程式
锰酸钾制取氧气的化学方程式

锰酸钾不能制取氧气,所以没有化学方程式。
实验室制取氧气通常是加热高锰酸钾制取,也可以通过氯酸钾的分解制取,还可以通过过氧化氢溶液的催化分解制取。
加热高锰酸钾制取氧气的化学方程式为:2KMnO4=(加热)=K2MnO4+MnO2+O2↑,即在加热条件下得到锰酸钾、二氧化锰和氧气;加热氯酸钾制取氧气的化学方程式为:2KClO3=(加热,二氧化锰)=2KCl+3O2↑,即在二氧化锰的催化作用,并加热的条件下得到氯酸钾和氧气;用过氧化氢制取氧气的化学方程式为:2H2O2=(MnO2)=2H2O+O2↑,即在二氧化锰的催化作用下得到水和氧气。
过氧化氢制氧气化学方程

过氧化氢制氧气化学方程全文共四篇示例,供读者参考第一篇示例:过氧化氢是一种常见的化学物质,也称为双氧水,其分子式为H2O2。
过氧化氢在生活中有着广泛的应用,比如护发、消毒等。
而在化学实验中,过氧化氢还可以被用来制取氧气,即过氧化氢制氧气的反应。
下面我们就来了解一下过氧化氢制氧气的化学方程式及反应过程。
让我们看一下过氧化氢的化学式:H2O2。
过氧化氢分子由两个氧原子连在一起,并且氧气的含量很高。
这使得过氧化氢在分解时可以释放出氧气分子。
而氧气是一种气体,它存在于空气中,并且对人类和动植物的生长发育有着至关重要的作用。
过氧化氢制氧气的化学方程式如下:2H2O2 → 2H2O + O2从上面的方程式可以看出,过氧化氢在受热或受光照射的条件下会发生分解反应,产生水和氧气。
具体的反应过程如下:过氧化氢分子在适当的条件下受到激发,分解成水分子和氧气分子。
这个反应是一个放热反应,需要一定的温度或能量来促进反应发生。
过氧化氢在分解的过程中会释放出大量的能量,这也是为什么它在护发产品和消毒剂中被广泛使用的原因之一。
在实验室中,我们可以通过加热过氧化氢的方法来制取氧气。
我们需要一个装有过氧化氢的试管,然后在试管中加入一些催化剂,如铁粉或二氧化锰。
这些催化剂可以加速过氧化氢的分解反应,从而更快地产生氧气。
当试管中的过氧化氢受到加热或光照射时,它会开始分解,释放出氧气气体。
通过在试管口放置一个吸管或导管,我们可以将生成的氧气收集起来。
收集到的氧气可以用于实验室中的各种化学实验,也可以用于其他需要氧气气体的场合。
过氧化氢制氧气是一个简单而又有趣的化学实验。
通过这个实验,我们可以更好地了解过氧化氢的性质,同时也可以得到纯净的氧气气体。
希望大家在实验室中能够安全地进行这项实验,同时也要保护好自己和他人的安全。
【本文共688字】过氧化氢除了可以制取氧气外,还可以被用于其他领域。
在医疗领域中,过氧化氢被用作一种消毒剂,可以有效地杀灭细菌和病毒。
实验室用氧化氢溶液制取氧气的化学方程式

实验室用氧化氢溶液制取氧气的化学方程式1. 引言:氧气的重要性大家好,今天咱们要聊的可不是小打小闹,而是科学实验中一个非常重要的环节——制取氧气。
你知道吗,氧气是我们生活中不可或缺的“空气之王”,没有它,我们可就像没了盐的菜,味道大打折扣。
无论是我们呼吸的空气,还是植物光合作用中不可缺少的成分,氧气总是默默地为我们的生活保驾护航。
今天我们就来聊聊如何在实验室里,用氧化氢溶液来制取氧气,这可是个很有意思的话题哦!1.1 氧化氢是什么?说到氧化氢,很多人可能会想,嘿,这不就是水吗?没错,氧化氢的化学式是H₂O,简单来说,就是两个氢原子和一个氧原子结合在一起的。
可是,在实验室里,我们用的是氧化氢溶液,也就是浓度较高的氢氧化物,这种东西可不是随便就能找到的。
用它来制氧气,就像做一道美味的菜,得有好的食材嘛!1.2 制氧气的化学反应那么,如何用氧化氢溶液来制取氧气呢?这里就得用到一个经典的化学反应了。
简单说,就是把氧化氢溶液和一些催化剂混合,催化剂就像个神奇的调味品,它能加速反应,帮助我们更快地得到氧气。
这个反应的化学方程式是:2H₂O₂→ 2H₂O + O₂。
听起来是不是很简单?实际上,这其中的学问可不少哦!2. 实验步骤:准备工作接下来,咱们进入实验的环节。
首先,你得准备好氧化氢溶液、催化剂(一般用的是二氧化锰),还有一个可以收集氧气的装置,比如倒置的试管或气球。
别小看这些材料,它们就像厨师的调料,缺一不可哦!在准备好之后,首先把催化剂放入氧化氢溶液中,哇,这时就像打开了魔法箱,反应开始了!2.1 观察反应过程随着反应的进行,你会看到溶液冒出气泡,哇,这可真是个“泡泡秀”啊!这些气泡正是生成的氧气,仿佛在跟你说:“嘿,快来收我吧!”在这个过程中,反应是相当迅速的,可能还会伴随着一点点的热量释放,像是小火焰在为我们欢呼。
别忘了,这些氧气可不是白来的,背后可是有化学反应在默默支持呢!2.2 收集氧气当你看到气泡越来越多,就可以准备收集氧气了。
实验07过氧化氢制取氧气实验(原卷版)-2024-2025学年九年级化学上册同步学与练(人教版)

【同步实验课】过氧化氢制取氧气实验【实验目的】1.学习实验室用过氧化氢制取氧气的方法。
2.了解化学反应需要一定的条件,知道催化剂对化学反应的重要作用。
【实验仪器】锥形瓶、分液漏斗、双孔橡胶塞、胶皮管、玻璃导管、集气瓶、水槽、玻璃片、弹簧夹、火柴【实验试剂】过氧化氢溶液、二氧化锰【实验步骤】(1)连接装置并。
(2)向锥形瓶中加入。
(3)塞好带有分液漏斗和导管的双孔塞。
(4)向分液漏斗中加入。
(5)滴加液体:打开分液漏斗活塞,慢慢滴加过氧化氢溶液。
(6)用排水集气法收集。
1. 反应原理(1)文字表达式:(2)符号表达式:2. 催化剂(1)定义:在化学反应中能其他物质的化学反应速率,而本身的和在反应前后都没有发生变化的物质。
(2)特点:“一变两不变”①一变:;(可以加快也可以减慢)①两不变:。
(物理性质可以改变)01实验梳理02实验点拨03典例分析04对点训练05真题感悟【注意】①催化剂(填“能”或“不能”)改变生成物的质量;①催化剂(填“能”或“不能”)控制反应的发生与停止;①同一化学反应(填“一定”或“不一定”)只有一种催化剂;同一物质可以在的化学反应中起催化作用。
(3)验证某物质是催化剂的方法①改变反应速率:设计实验,观察加入该物质前后化学反应速率是否改变。
①反应前后质量不变:称量该物质在的质量是否发生变化。
①化学性质不变:一般进行实验,观察重新加入反应物的现象和原来的现象是否相同。
3. 分液漏斗检查装置气密性的方法方法①:连接装置后,先关闭分液漏斗活塞,再将导管的末端放入水中,双手紧握锥形瓶,若,松开手后导管中形成一段水柱,说明装置气密性良好。
方法①:连接装置后,夹紧止水夹,关闭分液漏斗活塞,向分液漏斗中加水,打开活塞,一段时间后,,说明装置气密性良好。
4.发生装置的评价D.可用向下排空气法收集氧气【典例03】过氧化氢在催化剂作用下可迅速分解成水和氧气,量筒中涌出柱状的泡沫,可形象地称为“大象牙膏”,下列说法正确的是()A.反应产生的氧气支持燃烧,可以作燃料B.加发泡剂和催化剂后反应减缓了C.反应前后催化剂的质量不变D.没有催化剂过氧化氢不会分解【典例04】某小组用过氧化氢制取氧气,下图是实验室中常用仪器,回答下列问题。
2017-2019年天津市九年级上学期化学期中考试试题分类——实验探究题(解析版)
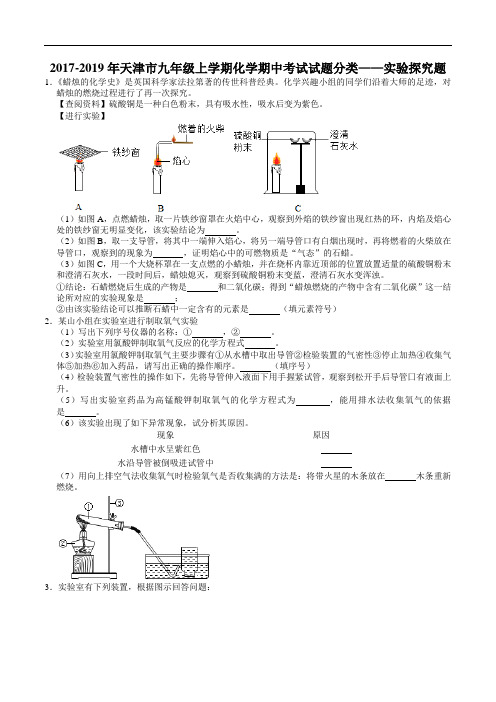
2017-2019年天津市九年级上学期化学期中考试试题分类——实验探究题1.《蜡烛的化学史》是英国科学家法拉第著的传世科普经典。
化学兴趣小组的同学们沿着大师的足迹,对蜡烛的燃烧过程进行了再一次探究。
【查阅资料】硫酸铜是一种白色粉末,具有吸水性,吸水后变为紫色。
【进行实验】(1)如图A,点燃蜡烛,取一片铁纱窗罩在火焰中心,观察到外焰的铁纱窗出现红热的环,内焰及焰心处的铁纱窗无明显变化,该实验结论为。
(2)如图B,取一支导管,将其中一端伸入焰心,将另一端导管口有白烟出现时,再将燃着的火柴放在导管口,观察到的现象为,证明焰心中的可燃物质是“气态”的石蜡。
(3)如图C,用一个大烧杯罩在一支点燃的小蜡烛,并在烧杯内靠近顶部的位置放置适量的硫酸铜粉末和澄清石灰水,一段时间后,蜡烛熄灭,观察到硫酸铜粉末变蓝,澄清石灰水变浑浊。
①结论:石蜡燃烧后生成的产物是和二氧化碳;得到“蜡烛燃烧的产物中含有二氧化碳”这一结论所对应的实验现象是;②由该实验结论可以推断石蜡中一定含有的元素是(填元素符号)2.某山小组在实验室进行制取氧气实验(1)写出下列序号仪器的名称:①,②。
(2)实验室用氯酸钾制取氧气反应的化学方程式。
(3)实验室用氯酸钾制取氧气主要步骤有①从水槽中取出导管②检验装置的气密性③停止加热④收集气体⑤加热⑥加入药品,请写出正确的操作顺序。
(填序号)(4)检验装置气密性的操作如下,先将导管伸入液面下用手握紧试管,观察到松开手后导管囗有液面上升。
(5)写出实验室药品为高锰酸钾制取氧气的化学方程式为,能用排水法收集氧气的依据是。
(6)该实验出现了如下异常现象,试分析其原因。
现象原因水槽中水呈紫红色水沿导管被倒吸进试管中(7)用向上排空气法收集氧气时检验氧气是否收集满的方法是:将带火星的木条放在木条重新燃烧。
3.实验室有下列装置,根据图示回答问题:(1)写出仪器a和b的名称:a,b。
(2)用过氧化氢溶液和二氧化锰的混合物制取并收集氧气,应选用的装置为(填字母)。
过氧化氢溶液制取氧气的化学方程式

过氧化氢溶液制取氧气的化学方程式
过氧化氢溶液制取氧气的化学方程式为2H2O2 → O2 + 2H2O,即
将过氧化氢溶液(H2O2)通过反应转化为氧气(O2)和水(H2O)。
过氧化氢为双氢氧化物,其结构式为H-O-O-H,它以混合液体或气
体形式存在,其分子内产生一种有效而持久的催化作用,使该物质以
激烈的氧化性而发生相应的化学反应。
在一般情况下,过氧化氢溶液中H2O2 会发生自由基反应,即•OH+ H2O2 → HO2• + H2O,此反应为水溶液中过氧化氢自由基反应
的基本步骤,可在其水溶液中反复发生。
然后,HO2•的氧原子会和另一个水分子的氢原子结合,形成H2O2,即•OH + H2O → HO2• + H。
此外,过氧化氢中另一种自由基反应是
H2O2 + •OH → HO• + H2O,此反应同样可在水溶液中反复发生。
最后,氧自由基HO•会和另一水分子H原子结合,形成氧气和水。
HO•+ H → O2 + H2O,即过氧化氢溶液发生细分解,最终产生氧气和水,因此,过氧化氢溶液制取氧气的化学方程式为2H2O2 → O2 +
2H2O。
h2o2制氧气的化学方程式

过氧化氢(H2O2)制取氧气的化学方程式为2H2O2=2H2O+O2 (MNO2是催化剂,不用加热)知识拓展:如图所示是过氧化氢(H2O2)分子的空间结构示意图。
(1)写出过氧化氢分子的电子式________。
(2)下列关于过氧化氢的说法中正确的是(填序号)____。
①分子中有极性键②分子中有非极性键③氧原子的轨道发生了sp2杂化④O—O共价键是p—pσ键⑤分子是非极性分子(3)过氧化氢分子之间易形成氢键,该氢键的表示式是____________。
(4)过氧化氢难溶于二硫化碳,主要原因是______________________;过氧化氢易溶于水,主要原因是________________________。
(5)过氧乙酸也是一种过氧化物,它可以看作是过氧化氢分子中的一个氢原子被乙酰基(CH3CO)取代的产物,是一种常用的杀菌消毒剂。
在酸性条件下过氧乙酸易发生水解反应生成过氧化氢。
①写出过氧乙酸发生水解反应的化学方程式(有机物用结构简式表示):____________。
②过氧乙酸用作杀菌消毒剂的原因是________________________________________。
答案:(1)过氧化氢的电子式为;(2)①H-O为极性键,故①正确;②O-O 为非极性键,故②正确;③由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,故③错误;④O的s轨道电子和O 的s轨道电子成键,故是s-sσ键,故④错误;⑤过氧化氢中的键的极性不能相互抵消,是极性分子,⑤错误;答案选①②;(3)O元素的电负性很强,O原子与H原子之间可以形成氢键,该氢键的表示式为O-H…O;(4)H2O2是极性分子,CS2是非极性分子,依据相似相溶的原理可知,H2O2难溶于CS2;H2O2中氧元素的电负性很强,H2O2分子H2O 分子之间形成氢键,使H2O2与水任意比互溶;(5)①过氧乙酸发生水解反应的化学方程式为:+H2O→CH3COOH+H2O2;②过氧乙酸用作杀菌消毒剂的原因是过氧乙酸分子中有O-O键,有强氧化性。
2020年初中学业水平考试 化学(云南专版) 02 万能解题模板(二) 气体的制取、净化和干燥

万能解题模板(二) 气体的制取、净化与干燥实验室制取气体的常见装置如下,据图回答下列问题:考向1 填写仪器名称 写出仪器①~⑧的名称。
①__试管__;②__酒精灯__;③__铁架台__;④__长颈漏斗__;⑤__锥形瓶__;⑥__分液漏斗__;⑦__集气瓶__;⑧__水槽__。
考向2 发生装置的选择及反应原理(化学方程式)的书写选择发生装置的依据:__反应物状态__(固固型或固液型)和__反应条件__(是否需要加热)。
1.常见气体的制取(O 2、CO 2、H 2)(1)实验室用高锰酸钾加热制取氧气,发生装置为__B__(填字母,下同),反应的化学方程式为__2KMnO 4=====△K 2MnO 4+MnO 2+O 2↑__。
(2)实验室用氯酸钾和二氧化锰固体混合物加热制取氧气,发生装置为__A__,反应的化学方程式为__2KClO 3=====MnO 2△2KCl +3O 2↑__。
(3)实验室分解过氧化氢制取氧气,发生装置为__D(或E)__,反应的化学方程式为__2H 2O 2=====MnO 22H 2O +O 2↑__。
(4)实验室用大理石(或石灰石)和稀盐酸制取二氧化碳,发生装置为__D(或E)__,反应的化学方程式为__CaCO 3+2HCl===CaCl 2+H 2O +CO 2↑__。
(5)实验室用锌粒和稀硫酸制取氢气,发生装置为__D(或E)__,反应的化学方程式为__Zn +H 2SO 4===ZnSO 4+H 2↑__。
2.其他气体的制取(N 2、NH 3、CH 4、H 2S)(1)实验室用NaNO 2和NH 4Cl 的浓溶液加热制取氮气,发生装置为__C__。
(2)实验室用硫化亚铁固体与稀盐酸反应制取硫化氢气体,发生装置为__D(或E)__。
(3)实验室用氯化铵和熟石灰的固体混合物加热制取氨气,发生装置为__A__。
(4)实验室用无水醋酸钠和碱石灰固体加热制取甲烷,发生装置为__A__。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验室中用过氧化氢溶液制取氧气的化学方程式
过氧化氢是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。
过氧化氢制取氧气的化学方程式为2H2O2=2H2O+O2↑。
实验药品:3%过氧化氢溶液、小木条、二氧化锰固体。
实验步骤
(1)在试管中加入少量过氧化氢溶液,把带火星的小木条放在试管口,观察现象(无明显现象)。
(2)在试管中加入少量二氧化锰,观察现象(出现大量气泡,木条复燃)。
(3)当停止生成气泡时,继续加入过氧化氢溶液,观察现象(出现大量气泡,木条复燃)。
(4)化学方程式:2H2O2=2H2O+O2↑。
