中考化学溶解度图像
中考化学一轮专题复习专题溶解度曲线及溶解度表

命题点4 物质结晶或提纯方法的判断(5考) (1)若甲中混有少量乙(或丙)时,提纯甲所用的方法为_降__温__结__晶__。 (2)若乙中混有少量甲时,提纯乙的方法为_蒸__发__结__晶__。 (3)若丙中混有少量甲(或乙)时, 提纯丙的方法为_升__温__结__晶__。
命题点5 饱和溶液与不饱和溶液的判断及转化(3考)
(4)下列说法正确的是__b_(填序号)。
a.40 ℃时,甲、乙、丙三种溶液的溶质质量分数的大小关系为甲<乙<
丙 (3)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是_________;实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,所
(2)甲、乙两物质中溶解度受 ,曲线为水平直线,以此判断题中各项。
5.对于Zn(s)+H2SO4(aq)===ZnSO4(aq)+H2(g) ΔH<0的化学反应下列叙述不正确的是 【解析】A、由于Ca(OH)2和BaCl2相互混合时,没有水、沉淀或气体生成,不符合复分解反应的条件,碱与盐1不能反应,故A错误;B、由于Ca(OH)2和BaCl2相互混合时,没 有水、沉淀或气体生成,不符合复分解反应的条件,碱与盐2不能反应,故B错误;C、NaOH和Na2CO3相互混合时,没有水、沉淀或气体生成,不符合复分解反应的条件,碱与盐1
D. 所得溶液中溶质质量分数约为26.5%
7. KCl和KNO3在不同温度下的溶解度数据如表所示,下列说法中正确 的是( A ) A. 60 ℃时,100 g水中最多溶解45.5 g KCl
B. 随着温度的升高,某饱和KCl溶液中会有固体析出
C. KNO3的溶解度始终大于KCl
D.
60
2024年中考化学专题强化训练溶解度曲线
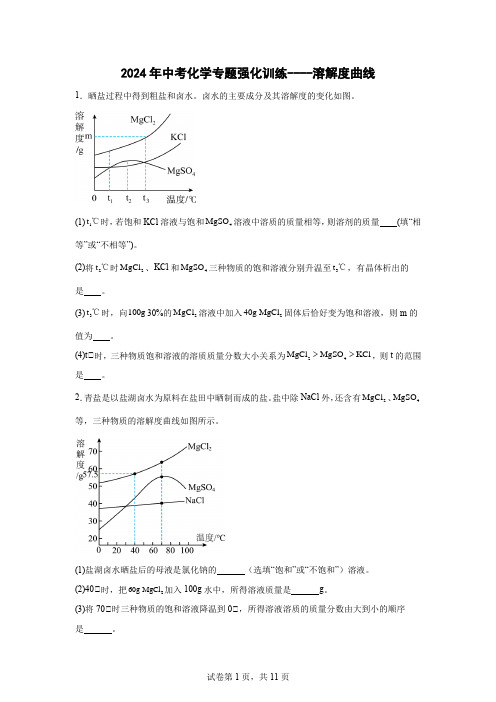
2024年中考化学专题强化训练----溶解度曲线1.晒盐过程中得到粗盐和卤水。
卤水的主要成分及其溶解度的变化如图。
(1)1t ℃时,若饱和KCl 溶液与饱和4MgSO 溶液中溶质的质量相等,则溶剂的质量 (填“相等”或“不相等”)。
(2)将2t ℃时2MgCl 、KCl 和4MgSO 三种物质的饱和溶液分别升温至3t ℃,有晶体析出的是 。
(3)3t ℃时,向100g 30%的2MgCl 溶液中加入240g MgCl 固体后恰好变为饱和溶液,则m 的值为 。
(4)t℃时,三种物质饱和溶液的溶质质量分数大小关系为24MgCl MgSO KCl >>,则t 的范围是 。
2.青盐是以盐湖卤水为原料在盐田中晒制而成的盐。
盐中除NaCl 外,还含有2MgCl 、4MgSO 等,三种物质的溶解度曲线如图所示。
(1)盐湖卤水晒盐后的母液是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)40℃时,把260g MgCl 加入100g 水中,所得溶液质量是 g 。
(3)将70℃时三种物质的饱和溶液降温到0℃,所得溶液溶质的质量分数由大到小的顺序是 。
(4)氯化钠中含有少量硫酸镁,若要提纯氯化钠,可采用的方法是。
3.某同学进行了如图1所示实验,结合硝酸钾和氯化钠的溶解度曲线回答下列问题。
(1)20℃时,氯化钠的溶解度是g;(2)若氯化钠中混有少量硝酸钾,可采用的方法提纯氯化钠;(3)图1中烧杯℃为硝酸钾的(填“饱和”或“不饱和”)溶液;若通过升高温度使℃中固体继续溶解,则其溶液中溶质的质量分数(填“增大”“减小”或“不变”)。
4.如图是A、B、C三种固体物质的溶解度曲线,据图作答:(1)P点的意义是。
(2)A、B、C三种物质中,溶解度随着温度上升而减小的物质是。
(3)t2℃时,将30g A物质加入50g水中可形成g溶液。
5.如图是某苏打气泡水的标签。
(1)该气泡水中溶剂的化学式是。
C H O。
从赤藓糖醇的化学式中能获得与其有关的(2)赤藓糖醇是一种甜味剂,其化学式为4104信息是(任写一条)。
初三化学中考专题(5)溶解度曲线练习及答案

初三化学中考专题(5)溶解度曲线练习及答案1.a、b两种物质的溶解度曲线如图所示。
下列说法不正确的是A.将t1℃时b的饱和溶液加水可变为不饱和溶液B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变C.t2℃时,两种物质的饱和溶液中溶质质量分数a>bD.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.t2℃时,甲、乙两种物质的溶解度相等B.甲的溶解度随温度的升高而增大C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t1℃时,丙的饱和溶液中溶质的质量分数为40%3.下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系正确的是A.甲>乙>丙B.甲=乙=丙C.甲=乙>丙D.丙>甲=乙4.(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是A.t1℃时,甲物质的溶解度为20gB.t1℃时,30g甲加入到50g水中最多可得70g溶液C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液D.t2℃时,甲乙两物质的饱和溶液分别降温到t1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5.(多选)甲、乙两种固体物质的溶解度曲线如图所示。
20℃时,进行了如下图所示的实验,下列叙述正确的是A.甲的溶解度大于乙的溶解度B.实验过程中,属于不饱和溶液的是A溶液和C溶液C.实验过程中,只有B溶液和D溶液属于饱和溶液D.实验过程中,B溶液与E溶液中溶质的质量分数相同6.(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C.分别将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线如下图所示。
2021年中考化学专题复习:溶解度曲线
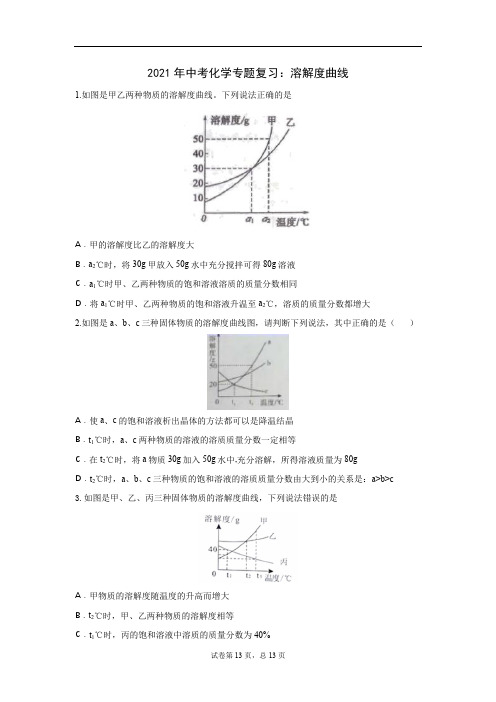
2021年中考化学专题复习:溶解度曲线1.如图是甲乙两种物质的溶解度曲线。
下列说法正确的是A.甲的溶解度比乙的溶解度大B.a2℃时,将30g甲放入50g水中充分搅拌可得80g溶液C.a1℃时甲、乙两种物质的饱和溶液溶质的质量分数相同D.将a1℃时甲、乙两种物质的饱和溶液升温至a2℃,溶质的质量分数都增大2.如图是a、b、c三种固体物质的溶解度曲线图,请判断下列说法,其中正确的是()A.使a、c的饱和溶液析出晶体的方法都可以是降温结晶B.t1℃时,a、c两种物质的溶液的溶质质量分数一定相等C.在t2℃时,将a物质30g加入50g水中,充分溶解,所得溶液质量为80gD.t2℃时,a、b、c三种物质的饱和溶液的溶质质量分数由大到小的关系是:a>b>c3.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.甲物质的溶解度随温度的升高而增大B.t2℃时,甲、乙两种物质的溶解度相等C.t1℃时,丙的饱和溶液中溶质的质量分数为40%D.当甲中混有少量丙时,可采用降温结晶的方法提纯4.如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是()A.a的溶解度大于b的溶解度B.P点表示t1℃时a、c两物质溶解度相等C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质最分数由大到小的顺序为:b>a=c5.甲、乙两种固体的溶解度曲线如右图所示,下列说法正确的是A.甲的溶解度大于乙的溶解度B. t1°C时,甲乙饱和溶液中溶质的质量分数相等C. t2°C时,60g 甲的饱和溶液稀释到20%需加水10gD.将t1°C时相等质量的甲、乙的饱和溶液升温到t2°C,溶液中溶质的质量甲大于乙6.A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是()A.阴影区域中,A、C均处于不饱和状态B.除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯BC.将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>BD.t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7% 7.甲、乙两种物质溶解度曲线如图所示。
中考化学1轮复习专题06 溶液、溶解度和溶质的质量分数(解析版)

专题06溶液、溶解度和溶质的质量分数【知识网络】定义:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物组成:溶质和溶剂定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量固体大多数固体物质的溶解度随温度的升高而增大,如KNO3溶解度变化规律:少数固体物质的溶解度受温度的影响很小,如NaCl溶解度极少数固体物质的溶解度随温度的升高而减小,如C a(O H)2常用溶解度曲线表示气体溶解度:随温度升高而减小,随压强增大而增大溶液溶质的质量分数= ×100%配制溶质的质量分数一定的溶液的步骤:计算、称量、溶解定义:固体溶质从饱和溶液中析出的过程方蒸发溶剂,适于溶解度受温度的影响不大的物质结晶法冷却热的饱和溶液,适于溶解度受温度的影响变化大的物质放热,如:NaOH 浓H2SO4溶解现象吸热,如NH4NO3变化不明显,如NaCl乳化现象:洗洁精洗衣物和餐具上油污是发生了乳化现象【考点梳理】考点一、溶液、溶解现象、饱和溶液和不饱和溶液1.溶液(1)定义:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物。
(2)组成:溶质和溶剂。
(3)特征:溶液具有均一性和稳定性。
均一性指溶液各部分密度、浓度、性质都相同。
稳定性指外界条件不改变,溶液久置不出现沉淀,不分层。
2.溶解现象(1)影响溶解快慢的因素①溶剂的温度:温度越高,溶解越快。
②固体溶质的颗粒大小:颗粒越小,溶解越快。
③搅拌加速溶解。
(2)溶解时的吸热和放热现象物质溶解时,往往会引起温度的改变。
溶解的过程发生两个变化:①溶质的分子或离子向水中扩散的过程,要吸收热量;②溶质的分子或离子与水分子作用形成水合分子或水合离子过程,要放出热量。
当吸热大于放热时,溶液温度降低,反之升高。
(3)溶于水温度升高的物质:氢氧化钠、浓硫酸等,溶于水温度降低的物质:硝酸铵等。
3.正确区分乳化现象和溶解现象(1)乳化是使用乳化剂将植物油(的油珠)分散成无数细小的液滴存在于水中而不能聚集。
【化学】溶解度曲线

【化学】溶解度曲线溶解度及溶解度曲线七嘴⼋⾆说考情溶解度及溶解度曲线是全国各地市的中考重点,也是同学们学习的难点。
陕西说:近10年必考,从2011年开始均在填空及简答题中考查,有曲线、表格、实物图、表格结合实物图、表格结合曲线、实物图结合曲线、实物图结合表格和曲线多种考查形式。
安徽说:近10年必考,除2018年在填空和简答题中考查⼀空外,其余均在选择题第10题考查表格或曲线。
考查曲线⾛向有⼀升、⼀条先升后降、两升、⼀升⼀降、两降多种形式。
河南说:近10年必考,选择题和填空题中均有考查。
除2015年考查溶解度表外其余均考查溶解度曲线,且考查的曲线除2010年是1条曲线外,其余均为2条曲线。
曲线⾛向有⼀升、两升、⼀升⼀降、⼀升⼀平缓多种形式。
江西说:近10年必考,近5年在选择题或选择填充题中考查,2009~2013年在填空与说明题中考查。
以单纯考查曲线为主,偶尔考查曲线结合表格、曲线结合实物图。
曲线⾛向有⼀升、两升、⼀升⼀降、两升⼀降多种形式。
云南说:近5年必考,在选择题、填空与简答中均有涉及。
以三条或两条曲线为主,偶尔也考查⼀条或四条曲线。
⼭西说:近10年仅2017年未考,其余在选择题和⾮选择题中均有考查。
考查形式有曲线、表格、曲线结合实物图等形式。
曲线⾛向有⼀升、两升、⼀升⼀平缓、⼀升⼀降多种形式。
河北说:近10年考查5次,除2018年在实验探究题的⼀空考查外,其余均在选择题的6题或7题考查。
考查形式除2013年考查溶解度表外,其余均考查曲线。
曲线⾛向有⼀升、两升、⼀升⼀降、两升⼀降多种形式。
说来说去还得练1.(推荐河南、江西、河北)甲物质的溶解度曲线如图所⽰,下列有关说法不正确...的是()A.甲的溶解度随温度升⾼⽽增⼤B.图中P点表⽰甲的饱和溶液C.将甲溶液从t2℃降⾄t1℃,⼀定有晶体析出D.t2℃时,将60g甲加⼊50g⽔中最多形成105g溶液2.(推荐安徽、云南)某固体物质的溶解度曲线如图所⽰,下列有关说法不正确...的是()A.该物质85℃时的溶解度⽐45℃时的溶解度⼩B.50℃和70℃时,该物质的溶解度均为50gC.降低温度,⼀定能使其接近饱和的溶液变为饱和溶液D.10℃时,该物质饱和溶液的溶质质量分数约为16.7%3.(推荐河北、河南、安徽、⼭西、云南、江西)如图是A、B两种固体物质的溶解度曲线,下列有关说法正确的是()A.物质A的溶解度⼤于物质B的溶解度B.t1℃时,A、B两种物质的溶解度均为25gC.降低温度可从B的饱和溶液中析出晶体D.t2℃时,分别将相同质量的A、B配制成饱和溶液,所需溶剂的质量:A>B4.(推荐云南、河北、⼭西、江西)如图是a、b、c 三种固体物质的溶解度曲线,下列有关说法正确的是()A.三种物质的溶解度⼤⼩为a>b>cB.物质a中混有少量b时,可⽤降温结晶的⽅法提纯aC.t1℃时,a、b、c三种物质的饱和溶液中所含溶质质量a=c<bD.分别将a、b、c三种物质的饱和溶液从t1℃升温⾄t2℃,所得溶液的溶质质量分数a>b>c5.(推荐陕西)下表是NaCl、KNO3两种固体物质在不同温度时的溶解度,回答问题。
(全国版)中考化学复习 主题一 身边的化学物质 专项(一)溶解度曲线课件

两条曲线
4.[2018·泸州] 氯化钾(KCl)和氯酸钾(KClO3)的溶解度随温度变化曲线如图G14所示,下列说法正确的是
(
)
A.30 ℃时,KCl饱和溶液的溶质质量分数为35%
B.60 ℃时,a点对应KCl溶液恒温加水可变饱和
C.KCl的溶解度随温度变化的趋势比KClO3大
D.90 ℃ 150 g KClO3饱和溶液降温到10 ℃可析出(xīchū)45 g晶体
KClO3饱和溶液中含有氯酸钾质量为50 g,降温到10 ℃,氯酸钾的溶解度为5 g,析出晶体质量为50 g-5 g=45 g。
第八页,共23页。
类型(lèixíng)二
两条曲线
5.[2018·娄底] 如图G1-5是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是(
)
A.20 ℃时,甲、乙两种物质的溶解度相同(xiānɡ tónɡ)
)
A.烧杯(shāobēi)②中的上层溶液是饱和溶液
B.烧杯(shāobēi)①中溶液的溶质是硝酸钾
C.烧杯(shāobēi)①中溶液质量比烧杯(shāobēi)②中溶液质量大
D.将温度升高到t2 ℃,烧杯(shāobēi)②中的固体全部溶解
图G1-10
第十九页,共23页。
类型(lèixíng)四
. +
(只列计算式)
。
(3)将a点对应的溶液升温到70 ℃,其质量分数
不变
(填“变大”“变小”或“不变”)。
(4)欲使KNO3溶液的状态从b点转化为c点,可采取的措施是
第五页,共23页。
增加溶剂
。
类型一
一条(yī tiáo)曲线
[解析] (1)a点位于曲线(qūxiàn)上,对应的溶液是饱和溶液。(2)a点对应的溶解度为45.8 g,则溶质的质量分数
中考化学:溶解度曲线

中考化学:溶解度曲线近年来,全国各地中考中,“溶解度”以海水中的物质、侯氏制碱法、氨碱法制纯碱等初中课本中的工业流程作为背景,考察同学们对溶解度曲线上升下降、交点等特征的了解,分值通常在3-5分。
什么是溶解度曲线?溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行各物质溶解度的比较、混合物的分离与提纯、以及进行物质结晶或溶解的计算。
从溶解度曲线中能获得哪些信息?1、点① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a表示A物质在t1℃时溶解度为m1g。
② 曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。
如:图中b表示在t1℃时,A的饱和溶液中有(m2-m1)g未溶解的溶质。
③ 曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中c表示在t1℃时,A的不饱和溶液中,还需要加入(m1-m3)g A物质才达到饱和。
④ 曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d表示在t2℃,A、B两物质的溶解度都为m4g。
2、线溶解度曲线大致可以分为下面三类:①如图中A物质的溶解度随温度升高而明显增大,A曲线为“陡升型”。
如KNO3等大多数固体物质;②图中B物质的溶解度随温度变化不大,B曲线为“缓升型”,如NaCl等少数固体物质;③图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
溶解度曲线怎么考?1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2.可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
溶解度
1、小明同学绘制了如右图所示A、B两种固体物质的溶液度曲线:
(1)当温度为℃时,A物质与B物质的溶解度相等。
(2)若将B物质从溶液中结晶析出,宜采用的方法是。
(3)我国有许多盐碱湖,湖中溶有大量的NaCl和Na2CO3,那
里的人们“冬天捞碱,夏天晒盐。
”据此你认为图中 (填
“A”或“B”)物质的溶解度曲线与纯碱的相似。
2、(8分)下表列出了固体物质A在不同温度时的溶解度:
(1)70℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解形成的是
(填“饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂
的质量比为(填最简整数比);
(2)通过对上表数据的分析,物质A的溶解度曲线
应是右图中的(填“甲”或“乙”);
(3)80℃时,配制一定量甲物质的溶液,将其降温
到60℃,是否有固体析出?(填“有”、
“没有”或“不确定”)。
3、根据右图所示的KNO3和NaCl的溶解度曲线回答下列问题。
(1)10℃时,KNO3的溶解度约为g;
(2)温度升高时溶解度明显增大的是;
(3)在温度不变的情况下,将NaCl的不饱和溶液变成
饱和溶液,可采用恒温蒸发水和的方法
4、甲、乙两种固体的溶解度曲线如右图所示。
(1)℃时,甲和乙的溶解度相等;
(2)40℃时,若将40g乙(不含结晶水)放入160g水中充分溶解,
所得溶液的溶质质量分数为,该溶液是溶液(填
“饱和”或“不饱和”);
(3)40℃时,将甲、乙两物质的饱和溶液各100g降温至20℃,析
出晶体(均不含结晶水)的质量关系是:
m(甲)m(乙)(填“﹥”、“﹦”或“﹤”)。
5、右图是a、b两种固体物质的溶解度曲线。
从图中可获得的信息是()
A. 固体物质的溶解度均随温度升高而增大
B.t℃,相同质量的a、b溶解时放出热量相同
C.升高温度,可使a或b的饱和溶液变为不饱和溶液
D.将相同质量的a、b分别加入100g水中,所得溶
液质量分数相同
6、如图是甲、乙两种物质的溶解度曲线,回答下列问
题:
(1)从甲物质的溶解度曲线可以得到哪些信息(请写出其中的一条)___________________________。
(2)t1℃时,甲、乙两种物质的溶解度较大的是___________。
(3)t1℃时,将20g甲物质放入50g水中,充分搅拌能否全部溶解____________(填“能”、“不能”或“无法判断”)。
(4)将一定量t2℃时甲物质的饱和溶液降温到t1℃时,该过程中没有发生改变的是___________(填序号)
A.溶质质量
B.溶液质量
C.溶剂质量
D.溶质的质量分数
7、甲、乙两物质的溶解度曲线如图所示,下列说法正确的是
A甲和乙的饱和溶液,从t1℃升温到t2℃,仍是饱和溶液
B.t1℃时,甲和乙的溶解度相等
C.t1℃时,甲和乙各30g分别加入80g水中,均能恰好完全溶解
D.t2℃时,在100g水中放入60g甲,形成不饱和溶液
8、如图是A、B、C三种固体物质的溶解度曲线。
⑴随着温度的升高,溶解度减小的是();
⑵t1℃时,B、C的()相等;
⑶从B的饱和溶液中提取B晶体应采用的方法是()
⑷t2℃时,要使接近饱和的A溶液变为饱和溶液,可采用的一种
方法是()
9、下图甲是A、B 二种固体物质的溶解度曲线图。
(1)在t 2℃时,P 点表示A 物质的溶液(填“饱合”或“不饱和”)。
(2)t 1℃时,A 、B 各Wg 分别加入到两只盛有100g 水的烧杯中,充分搅拌得到A 溶液和B 溶液,然后分别放入盛有同样冰块的小烧杯。
一段时间后,有晶体析出的是 溶液,变成不饱和溶液的是 溶液,溶质质量分数保持不变的是溶液。
10、甲、乙两种固体的溶解度曲线如右下图。
将①②两试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里。
升高温度后,下列有关说法正确的是()
A. ①②两溶液的质量一定相等
B. ①②两溶液均变为不饱和溶液
C. ①溶液质量增加,②溶液质量减少
D. ①溶液中溶质的质量分数一定大于②溶液
11、右图是甲、乙两种固体物质的溶解度曲线,
下列说法正确的是
A .甲的溶解度大于乙的溶解度
B .乙的不饱和溶液降温可变成饱和溶液
C .20oC 时,甲、乙两种物质的溶解度相等
D .50oC 时,甲的饱和溶液中溶质的质量分数为40%
12、右图是NaCl 、MgSO 4的溶解度曲线。
下列说法正确的是
A .只有在t 1℃时,NaCl 和MgSO 4的溶解度才相等
B .t 1℃~t 3℃,MgSO 4的溶解度随温度升高而增大
C .在t 2℃时,MgSO 4饱和溶液的溶质质量分数最大
D .把MgSO 4饱和溶液的温度从t 3℃降至t 2℃时,有晶体析出
13、右下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是 …………………………( )
A .t 2℃时,甲、乙两种物质的溶解度相等
B .甲的溶解度随温度的升高而增大
C .分别将t 3℃时甲、乙、丙的饱和溶液降温至t 1℃,则
所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙
D .t 1℃时,丙的饱和溶液中溶质的质量分数为40%
14、A 、B 、C 三种固体物质的溶解度曲线如右图所示。
0 t 1 t 2 t 3 温度/℃
(1)t
℃时,A、B、C的溶解度大小关系是(用“>”、“<”或
“=”表示),它们的饱和溶液中,溶质质量分数最大的物质是。
(2)t2℃时,将A、B、C各25 g分别放入100g水中,能形成饱
和溶液的物质是,将其转化为不饱和溶液的两种方法有、。
15、右图是a、b两种固体物质(不含结晶水)的溶解度曲线。
下列说法
正确的是()
A.b的溶解度大于a的溶解度
B.t1℃时,将a、b两种物质的饱和溶液分别恒温蒸发等质量的水,析
出晶体的质量一定相等
C.将t2℃时的b的不饱和溶液降温至t1℃,一定能得到b的饱和溶液
D.t2℃时,a溶液的溶质质量分数一定小于b溶液的溶质质量分数
16、右图是甲、乙两种固体物质的溶解度曲线。
据此判断
下列说法不正确的是:
A.t2℃时,甲、乙的溶解度相等
B. t3℃时,将60g乙加入100g水中可得l60g溶液
C.乙的溶解度受温度影响很小
D.t l℃时,乙的溶解度大于甲的溶解度
17、右图是某实验小组的同学绘制的两种固体物质的溶解度曲线图。
请你根据图示回答问题: (1)t1℃时,a物质的溶解度 b 物质的溶解度
(填“>”、“<”或“=”)。
(2)将t2℃时a、b两种物质相同质量的饱和溶液,分别
冷却到t1℃,析出晶体最多的是物质。
(3)溶解度曲线图中的任何一点都表示溶液的一种特定状
态。
图中A、B两个状态中,溶液属于不饱和状态的
是,状态最不稳定的是。
