高一化学苏教版物质的分类资料
新教材 苏教版高中化学必修第一册 专题一 物质的分类及计量 知识点考点重点难点提炼汇总

专题一物质的分类及计量第一单元物质及其反应的分类............................................................................................ - 1 - 第1课时物质的分类.................................................................................................. - 1 - 第2课时物质的转化化学反应的分类.................................................................... - 4 - 第二单元物质的化学计量.................................................................................................... - 8 - 第1课时物质的量...................................................................................................... - 8 - 第2课时气体摩尔体积............................................................................................ - 11 - 第三单元物质的分散系.................................................................................................... - 15 -第一单元物质及其反应的分类第1课时物质的分类1.分类的概念分类是指按照种类、等级或性质分别归类。
苏教版化学必修一专题1-3第2单元知识点总结
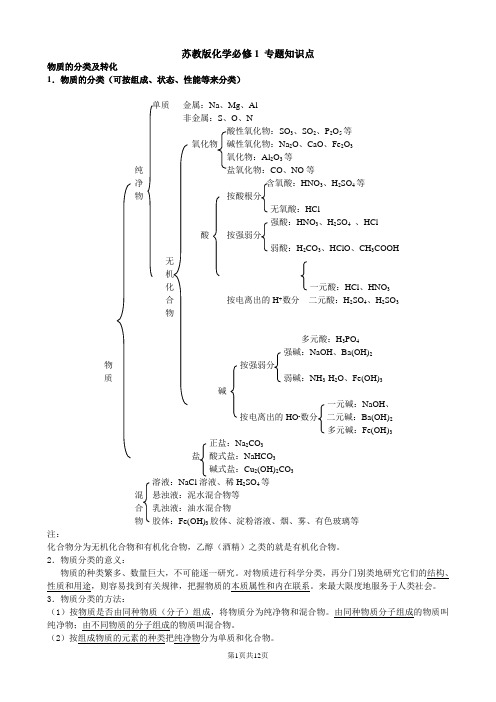
苏教版化学必修1 专题知识点物质的分类及转化1.物质的分类(可按组成、状态、性能等来分类)单质金属:Na、Mg、Al非金属:S、O、NSO3、SO2、P2O5等氧化物碱性氧化物:Na2O、CaO、Fe2O3氧化物:Al2O3等纯CO、NO等净含氧酸:HNO3、H2SO4等物按酸根分无氧酸:HCl强酸:HNO3、H2SO4、HCl酸按强弱分弱酸:H2CO3、HClO、CH3COOH无机化一元酸:HCl、HNO3合按电离出的H+数分二元酸:H2SO4、H2SO3物多元酸:H3PO4强碱:NaOH、Ba(OH)2物按强弱分质弱碱:NH3·H2O、Fe(OH)3碱一元碱:NaOH、按电离出的HO-数分二元碱:Ba(OH)2多元碱:Fe(OH)3正盐:Na2CO3盐酸式盐:NaHCO3碱式盐:Cu2(OH)2CO3溶液:NaCl溶液、稀H2SO4等混悬浊液:泥水混合物等合乳浊液:油水混合物物胶体:Fe(OH)3胶体、淀粉溶液、烟、雾、有色玻璃等注:化合物分为无机化合物和有机化合物,乙醇(酒精)之类的就是有机化合物。
2.物质分类的意义:物质的种类繁多、数量巨大,不可能逐一研究。
对物质进行科学分类,再分门别类地研究它们的结构、性质和用途,则容易找到有关规律,把握物质的本质属性和内在联系。
来最大限度地服务于人类社会。
3.物质分类的方法:(1)按物质是否由同种物质(分子)组成,将物质分为纯净物和混合物。
由同种物质分子组成的物质叫纯净物;由不同物质的分子组成的物质叫混合物。
(2)按组成物质的元素的种类把纯净物分为单质和化合物。
(3)化合物的分类方法很多,如按化合物的性质分类,又把化合物分为酸、碱、盐、氧化物等;若按化合物在水溶液或在融化状态下是否导电,则可以分为电解质和非电解质;若按在化学反应中的表现,则分为氧化剂和还原剂。
(4)按混合物中分散质微粒的直径大小可将混合物分类,分为溶液、胶体和浊液等。
4.单质、氧化物、酸、碱和盐之间的相互关系(1)相互关系的研究方法:先选定一类物质,预测它可能和哪些类别的物质发生反应;然后选出各类物质的代表物,探究它们之间是否发生反应。
高中化学新苏教版必修一:专题1 物质的分类及计量 章末共享 课件(19张)

2.某化学兴趣小组欲研究H2SO4、BaCl2、Na2CO3、NaCl、NaOH的 性质,对于如何研究,他们设计了两种研究方案:
方案Ⅰ:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液, 进行实验;
方案Ⅱ:将它们按照钠盐和其他化合物分类,然后分别溶于水得到 溶液,进行实验。
_在_两__支__试__管_中__分__别__加_入__少__许__H_2S_O__4溶__液__,_分__别__加__入_稍__过__量__的__两_种__未__知__溶_液__,__充_ _分_混__合__后_,__再__向__混_合__溶__液_中__分__别__滴_加__N_a_2_C_O_3_溶_液__,__若_有__气__泡__生_成__,__则_加__入__的__未_知_ _溶_液__为__N_a_C_l溶__液__;_若__无__气__泡_生__成__,_则__加__入__的_未__知__溶_液__为__N_a_O_H_溶__液______。
的关系进行求解。
答案:A
2.如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、 乙两室;标准状况下,在乙室中充入0.4 mol HCl,甲室中充入NH3、 H2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的 质量差为7.0 g。
(1)甲室中气体的质量为__7_._6_g___。 (2)甲室中NH3、H2的物质的量之比为__1_∶__1___。 (3)将隔板a去掉,当HCl与NH3充分反应生成NH4Cl固体后,隔板b将位于刻度 “_____2___”处(填数字,不考虑固体物质产生的压强)。
3 . 一 定 量 的 液 态 化 合 物 XY2 与 一 定 量 O2 恰 好 完 全 反 应 , XY2(l) + 3O2(g)===XO2(g)+2YO2(g),冷却后在标准状况下,测得生成物的体 积为672 mL,密度为2.56 g·L-1。
高中化学专题:物质的分类及计量-高一化学上学期单元复习知识清单(苏教版2019必修第一册)
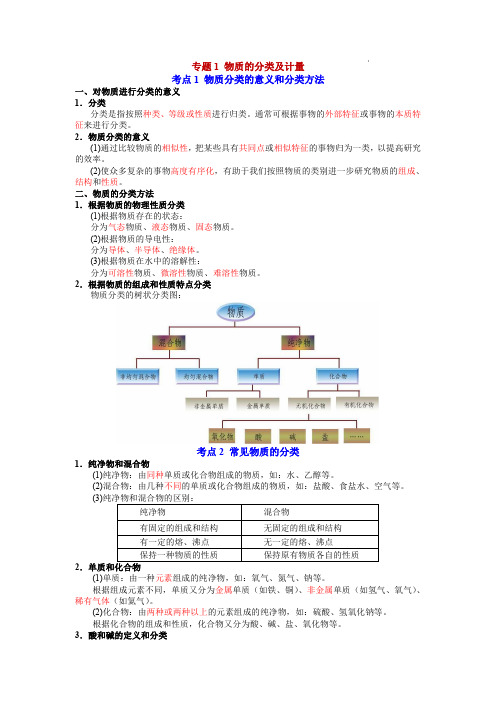
专题1物质的分类及计量考点1物质分类的意义和分类方法一、对物质进行分类的意义1.分类分类是指按照种类、等级或性质进行归类。
通常可根据事物的外部特征或事物的本质特征来进行分类。
2.物质分类的意义(1)通过比较物质的相似性,把某些具有共同点或相似特征的事物归为一类,以提高研究的效率。
(2)使众多复杂的事物高度有序化,有助于我们按照物质的类别进一步研究物质的组成、结构和性质。
二、物质的分类方法1.根据物质的物理性质分类(1)根据物质存在的状态:分为气态物质、液态物质、固态物质。
(2)根据物质的导电性:分为导体、半导体、绝缘体。
(3)根据物质在水中的溶解性:分为可溶性物质、微溶性物质、难溶性物质。
2.根据物质的组成和性质特点分类物质分类的树状分类图:考点2常见物质的分类1.纯净物和混合物(1)纯净物:由同种单质或化合物组成的物质,如:水、乙醇等。
(2)混合物:由几种不同的单质或化合物组成的物质,如:盐酸、食盐水、空气等。
(3)纯净物和混合物的区别:纯净物混合物有固定的组成和结构无固定的组成和结构有一定的熔、沸点无一定的熔、沸点保持一种物质的性质保持原有物质各自的性质2.单质和化合物(1)单质:由一种元素组成的纯净物,如:氧气、氮气、钠等。
根据组成元素不同,单质又分为金属单质(如铁、铜)、非金属单质(如氢气、氧气)、稀有气体(如氦气)。
(2)化合物:由两种或两种以上的元素组成的纯净物,如:硫酸、氢氧化钠等。
根据化合物的组成和性质,化合物又分为酸、碱、盐、氧化物等。
3.酸和碱的定义和分类(1)酸和碱的定义酸是指电离出来的阳离子全部是氢离子的化合物,如硫酸、HCl、硝酸等碱是指离出来的阴离子全部是氢氧根离子的化合物,如氢氧化钾、氢氧化钙等。
(2)酸的分类①根据组成,将酸分为无氧酸和含氧酸无氧酸:不含氧元素的酸,如HCl等。
含氧酸:含氧元素的酸,如H2SO4、HNO3等。
②根据在水溶液中电离出的H+个数,分为一元酸(如HCl、HNO3)、二元酸(如H2SO4、H2CO3)和三元酸(如H3PO4)。
苏教版化学必修一1.1 丰富多彩的化学物质-物质的分类 课件 (共18张PPT)

有机化合物 化合物
无机化合物
青县一中化学组座!
钠(Na)、氯气(Cl2)、 氯化铁(FeCl3 )溶液、硫酸(H2SO4)、 碳酸钙(CaCO3)、氧化钙(CaO)、 氢氧化钠(NaOH)、葡萄糖(C6H12O6)。
青县一中化学组
混合物
物质
纯净物
单质
金属单质 非金属单质
气态:空气、氧气 液态:乙醇、水、食盐水、碘酒 固态:硫酸铵、铜、碘、石墨
2.根据溶解性
易溶:乙醇、食盐(水)、硫酸铵 微溶:碘 难溶:空气、氧气、铜、石墨
3.根据导电性
导体为:铜、石墨、食盐水 半导体:
绝缘体:空气、乙醇、碘、氧气
青县一中化学组
4.根据物质的组成和性质特点 混合物
物质
纯净物
单质
金属单质 非金属单质
物质的分类
青县一中化学组
专题一化学家眼中的物质世界
青县一中化学组
青县一中化学组
分类!
(一)、物质的分类
分组交流与讨论(P3)
在日常生活中,常会接触到下列物质:
空气、乙醇、水、硫酸铵、铜、碘酒、 碘(I2)、氧气、石墨、食盐水 青县请一将中上化述学物组质进行分类,并说明分类的依据?
1.根据物质存在的状态
学工作者经常要根据物质的组成对物质进行分类
研究。近年来发现,在金星大气层中存在三氧化
二碳。下列物质与它属于同类的是( C )
A.H2、O3 C.SO2、NO
B.H2SO4、H2CO3 D.Na2SO3、KClO3
青县一中化学组
例4
将下列各组物质,按酸、碱、盐顺序排列 正确的是( B ) A.硫酸、纯碱、食盐 B.氢硫酸、烧碱、硫酸铜 C.碳酸、氧化铜、碳酸钠 D.醋酸、熟石灰、苛性钠
苏教版高一化学知识点总结电子版

苏教版高一化学知识点总结电子版化学是一门研究物质的性质、组成、结构、变化和反应规律的科学,一直以来都是高中学习中的重点科目之一。
随着教育的发展,苏教版高一化学教材已经成为许多学校的教学教材,提供了丰富的化学知识点和相关实验。
本文旨在对苏教版高一化学知识点进行总结,并提供电子版供学生参考。
1. 物质的分类物质是构成我们周围世界的基本要素,根据其性质和组成,可以将物质分为元素和化合物两大类。
其中,元素是由原子组成的,它们不能被化学方法分解;化合物是由不同元素的原子按照一定比例结合而成,它们可以通过化学方法进行分解。
2. 原子结构原子是构成物质的最小单位,由原子核和电子组成。
原子核由质子和中子组成,质子带有正电荷,中子没有电荷。
电子带有负电荷,围绕原子核的轨道上运动。
原子的质子数和电子数相等,原子的质量主要由原子核质量决定。
3. 元素周期表元素周期表是按照原子序数排列的一种表格,它将元素按照一定的规律进行分类。
元素周期表分为周期和族两个方向,周期表示元素的电子层次增加,族表示元素的化学性质相似。
元素周期表的组织形式为8个主族和10个副族。
4. 化学键原子通过化学键相互结合形成化合物。
常见的化学键有离子键、共价键和金属键。
离子键是通过正负离子之间的吸引力结合的,共价键是通过相互共享电子结合的,金属键是金属中的离子间的相互吸引力。
5. 反应物与生成物化学反应是物质发生变化的过程,通常由反应物和生成物组成。
反应物是参与反应的物质,生成物是在反应中生成的物质。
化学反应可以分为合成反应、分解反应、置换反应和化合反应等类型。
6. 化学方程式化学方程式是用化学式表达化学反应的过程,反应物和生成物用化学式表示,并在方程式的左右两侧用符号表示反应过程中的能量变化和反应条件。
化学方程式需要满足质量守恒和电荷守恒的原则。
7. 酸碱中和反应酸碱反应是指酸和碱在一定条件下发生中和反应产生盐和水。
其中,酸是可以释放出H+离子的物质,碱是可以释放出OH-离子的物质。
高一化学知识点大全苏教版

高一化学知识点大全苏教版高一化学知识点大全(苏教版)一、化学的基本概念化学是自然科学的一个分支,研究物质的性质、组成、结构、以及物质之间的相互作用。
二、物质的分类1. 纯物质和混合物- 纯物质指组成相同的物质,如金属、非金属等。
- 混合物指由两种或多种不同物质按一定比例混合而成的物质,如空气、海水等。
2. 元素和化合物- 元素是由相同类型原子组成的纯物质,如氧气、碳等。
- 化合物是由两种或多种不同类型元素按一定比例化学结合而成的物质,如水、二氧化碳等。
三、化学符号与化学式1. 元素符号- 元素符号用于表示元素,一般由拉丁字母组成,如氢的符号为H,氧的符号为O。
2. 化学式- 化学式用于表示化合物的组成,如水的化学式为H2O,二氧化碳的化学式为CO2。
四、原子结构原子由电子、质子和中子组成。
1. 质子和中子位于原子核中,质子带正电,质量为1,中子不带电,质量也为1。
2. 电子位于原子核外轨道上,带负电,质量极轻。
五、元素周期表元素周期表是按照元素的原子序数由小到大排列的表格,它反映了元素的周期性变化规律。
1. 元素周期表的结构- 元素周期表分为横行(周期)和竖列(族)。
- 横行称为周期,周期数代表元素的能级。
- 竖列称为族,族数代表元素的化学性质。
2. 元素的周期性变化规律- 原子半径:随着周期数增加,原子半径逐渐减小。
- 电离能:随着周期数增加,电离能逐渐增大。
- 电负性:随着周期数增加,电负性逐渐增大。
六、化学方程式化学方程式用化学符号和化学式表示化学反应。
1. 反应物和生成物- 反应物是在反应中参与变化的物质。
- 生成物是由反应物变化而成的物质。
2. 反应类型- 合成反应:两个或多个物质合成为一个新物质。
- 分解反应:一个物质分解为两个或多个物质。
- 置换反应:一个化合物中的原子或根离子被另一种原子或根离子取代。
- 双替反应:两种化合物中的阳离子和阴离子交换位置。
七、物质的性质物质的性质可以分为物理性质和化学性质。
高一化学_物质的分类

解析:只有一种元素不可能是化合物,可能由同素异 形体构成的混合物.
3、【实践活动】
下列10种物质:①Fe ②KNO3 溶液 ③
CuSO4
④ CuSO4· 5H2O ⑤ CO
⑥ CuO ⑦ HNO3
⑧ Ba(OH)2
⑨ 乙醇 ⑩ NaHCO3 中,
属于混合物的是_②___;属于单质的是__①__;
高中化学(苏教版)必修一
第一单元
第一节 物质的分类
(第1课时)
授课人:牛文丽
简单分类法及其应用
Na2CO3 Na2SO4 K2SO4 K2CO3
钠盐 钾盐 硫酸盐 碳酸盐
交叉分类法:对一种事物以多种
标准进行分类 物质所属类别有交叉部分
想一想
这是交叉分类么?为什么?
树状分类法:对同类事物进行再分类的一种
按电离出H+ 二元酸 H2SO4、H2CO3
多元酸 H3PO4
难挥发酸 H2SO4、 H3PO4
按挥发性
易挥发酸
HCl、HNO3、 CH3COOH
酸的分类
不溶 H2SiO3 按Байду номын сангаас解性
酸
溶 H2SO4、HCl
按稳定性
不稳定 H2CO3、HNO3、
H2SO3、HClO
稳定
H2SO4
碱的分类 按电离能力
1、下列关于氧化物的叙述正确的是:
1、酸性氧化物都是非金属氧化物
×
2、不能与酸反应的氧化物一定能和碱反应 ×
3、水也是氧化物,且是含氧量最高的氧化物 ×
4、金属氧化物都是碱性氧化物 ×
5、碱性氧化物都是金属氧化物
6、非金属氧化物都是酸性氧化物 ×
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
③_________3_C__O_+_F__e_2O__3_=_=_=_=_2_F__e_+_3_C__O_2______。
◆课堂互动探究 重点1:物质的分类 ⒈物质常见的分类方法(P3)
混合物(如:_食__盐__水__、_白_酒____等)
金属单质(如:F_e__、C__u__等) 单质
物质
CaO+H2O==Ca(OH)2
盐→酸性氧化物
碱→盐
Ca(OH)2+2HCl=CaCl2+H2O
盐+盐→两种新盐
三、化学反应的几种类型 ⒈根据反应物和生成物的类别及反应前后物质种类的 变化,将反应分为__化__合_____反应、_分__解____反应、 __置__换 ___反应和___复_分_解___反应。 ⒉根据反应前后元素的化合价是否发生变化,将化学 反应分为_氧__化__还__原_反应__和___非__氧__化__还__原__反__应_____。 其中元素化合价升高的反应称为氧化反应,元素化合 价降低的反应称为还原反应。
②举例:____N_O__2__、__ CO2_____、___S_O__2 ____等。 (2)碱性氧化物 ①概念:能和__酸___反应生成_盐__和__水______的氧化物。 ②举例:__ C_a__O__、__Na2O_____、__M_g_O_____等。 通常,酸性氧化物属于非金属氧化物,碱性氧化物属 于金属氧化物
CO2
高温
②
高温
CO
③
铁
(1)在上述框图中填写有关反应生成物的化学式。 (2)写出上述反应的化学方程式。
高温
①_________C_+__O_2_=_=_=_=__C_O__2 _____________;
高温
②_________C_+__C_O__2=__=_=_=_2_C__O____________;
纯净物:只有一种物质 混合物:有多种物质 单质:只有一种元素的某种物质 化合物:有多种元素的某种物质 氧化物:只有两种元素且含有氧元素的化合物
关键概念辨析: 1、物质分为纯净物、混合的分类标准是什么?
有多少种物质组成
2、纯净物分为单质和化合物的分类标准是什么? 这种纯净物有多少种元素组成
3、在课本P3问题解决中,找出哪些是混合物,哪些 是单质
请判断下列哪些是酸性氧化物,哪些是碱性氧化物: Na2O CaCO3 CO2 HCl Fe2O3
二、物质的转化 以右图钙及其化合物的转化 为例,填写下表(合理即可):
物质的转化类型 化学方程式
单质→化合物 化合物→单质 碱性氧化物→碱 酸性氧化物→酸
2Ca+O2==2CaO Ca+Cl2==CaCl2 CaCl2==Ca+Cl2↑
数以千万计的化学物质,需要分类吗?
学习目标: ⒈学会从不同角度对常见物质进行分类。掌握化学物 质的分类方法,认识比较和分类等科学方法对化学研 究的作用。 2、理解单质、氧化物、酸、碱、盐等物质之间的相互 转化关系。初步了解通过化学反应实现物质相互转化 的重要意义。
课前自主学与练 一⒈、根物据质物的 质分 常类 温下的存在状态,可将物质分为_气__态____ 物质、__液__态___物质和_固__态____物质。 ⒉根据物质的导电性,可将物质分为_导__体______、 _半__导__体____和__绝__缘__体_____。 ⒊根据物质在水中的溶解性可将物质分为_可__溶__性____物 质、__微__溶__性___物质和_难__溶__性___物质。
......
⒉常见的氧化物(P4) (1)SO2属于酸性氧化物,请写出SO2与足量KOH溶液 反应的化学方程式。
_________S_O__2_+_2_K_O__H_=_K__2_S_O__3+_H__2_O_________ MgO属于碱性氧化物,请写出MgO与硫酸反应的化学方 程式。 _________M_g_O__+_2_H__C_l_=_M__g_C_l_2_+_H_2_O_
※自主体验:
⒈下列各组物质的分类中,前者从属于后者的一组是
( B)
A.纯净物、混合物
B.氧化物、化合物
C.盐、钠盐
D.金属氧化物、碱性氧化物
⒉某市环保部门为了使城市生活垃圾得到合理利用,近
年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、
废纸、旧橡胶制品等属于( A )
A.有机物 B.盐类 C.无机物 D.单质
非金属单质(如:C___、_O_2__等)
纯净物
_有__机___化合物(如:甲__烷__、葡_萄__糖__等)
氧化物(如:C_u_O_、_C_O__等)
化合物
酸(如:_H_C__l_、_H__2_S_O_等4 ) 碱(如:N__a_O__H_、C_a_(_O_H_等)2)
__无__机__化合物 盐(如:N_a_C_、l K__N_O_等3 )
思考:看这三种分类,都有“根据...分类”,这 说明分类必须具有分_类__的_标__准_____。
思考:上述三种对物质的分类分类的标准是否一样? 不一样
有没有可能一个物质既是固体又是可溶性物质? 有可能,例如:NaCl
你能得到什么结论?
按照不同标准,同一种物质可以属于不同种类
⒋根据物质的性质 (1)酸性氧化物 ①概念:能和__碱___反应生成_盐__和__水____的氧化物。
例1:同学们吃的零食的包装袋中经常有一个小纸袋,
上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质: _______________碱__性__氧__化__物质世界 第一单元 丰富多彩的化学物质
第1课时 物质的分类与转化
新马高级中学高一化学备课组
图书馆中排列整齐的书本
超市中整齐的商品
[思考] 1.当你置身于图书馆或书店中,是怎样找 到你想要的书的?
2.当你去商店买东西时,你是如何挑选到 自己想买的东西的?
按照一定标准分好类,让我们方便快捷
4、根据实例,你能看出酸碱盐有什么特点,如 何判断吗?
酸:除水外,H在最前的化合物是酸 碱:OH—在最后的化合物是碱 盐:除金属氧化物外,有金属元素也有非金属元素的 化合物
⒊某炼铁厂用于炼铁的主要原料是赤铁矿石(Fe2O3)、
焦炭、空气等,主要反应过程如图所示。
过量空气、
焦炭、
赤铁矿石、
焦炭 高温 ①
