蛋白质和核酸
组成细胞的分子:蛋白质和核酸(知识梳理)

组成细胞的分子:蛋白质和核酸【学习目标】1、说出氨基酸的结构特点以及氨基酸形成蛋白质的过程2、概述蛋白质的结构和功能3、理解核酸的基本结构,掌握核酸的结构和功能。
4、以特定的染色剂染色,观察并区分DNA和RNA在细胞中的分布。
5、氨基酸的结构特点以及氨基酸形成蛋白质的过程、蛋白质的结构和功能(重点)。
6、氨基酸形成蛋白质的过程、蛋白质结构多样性的形成原因(难点)【要点梳理】要点一、蛋白质1、氨基酸及其种类(1)氨基酸的组成元素:C、H、O、N,有的含有S(2)氨基酸是组成蛋白质的基本单位。
含有氨基和羧基的有机化合物都叫做氨基酸。
天然氨基酸现已发现的有300多种,但作为构成蛋白质的氨基酸大约有20种。
(3)组成蛋白质的氨基酸的结构:①构成蛋白质的氨基酸分子,可用氨基酸的结构通式表示如下:②构成蛋白质的氨基酸的结构特点是:每种氨基酸分子至少含有一个氨基(-NH2)和一个羧基(-COOH),并且都有一个氨基和一个羧基连接在同一个碳原子上;不同的氨基酸分子,具有不同的R基。
可以根据R基的不同,将氨基酸区别为不同的种类。
2、蛋白质的形成及其相关计算(1)氨基酸缩合成蛋白质的示意图:(2)蛋白质的分子结构氨基酸分子互相结合的方式是:一个氨基酸分子的羧基(-COOH)和另一个氨基酸分子的氨基(-NH2),脱去一分子水而连接起来,这种结合方式叫做脱水缩合。
通过缩合反应,在羧基和氨基之间形成的连接两个氨基酸分子的那个键叫做肽键,由肽键连结形成的化合物称为肽。
肽键结构如图:由两个氨基酸缩合,形成一个肽键,产生一分子水和一分子二肽;由三个氨基酸缩合,形成两个肽键,脱掉两分子水,产生一个三肽;由n个氨基酸缩合成一条肽链,脱掉(n一1)个水分子,形成(n一1)个肽键,产生一个多肽。
若n个氨基酸缩合形成m条肽链,则形成(n-m)个肽键,脱掉(n-m)个水分子(m<n/2m)。
由三个或三个以上的氨基酸分子连结成的肽叫做多肽,多肽通常呈链状结构,叫多肽链。
高中化学选修五第四章蛋白质和核酸知识点

第三节蛋白质和核酸一、氨基酸1、氨基酸的分子结构氨基酸是羧酸分子烃基上的氢原子被氨基(—NH2)取代后的产物。
氨基酸的命名是以羧基为母体,氨基为取代基,碳原子的编号通常把离羧基最近的碳原子称为α碳原子,离羧基次近碳原子称为β碳原子,依次类推。
2、氨基酸的物理性质常温下状态:无色晶体;熔、沸点:较高;溶解性:能溶于水,难溶于有机溶剂。
3、氨基酸的化学性质(1)甘氨酸与盐酸反应的化学方程式:;(2)甘氨酸与氢氧化钠反应的化学方程式:氨基酸是两性化合物,基中—COOH为酸性基团,—NH2为碱性基团。
(3)成肽反应两个氨基酸分子(可以相同也可以不同)在酸或碱存在下加热,通过一分子的氨基和另一分子的羧基脱去一分子水,缩合形成含有肽键的化合物,称为成肽反应。
【习题一】下列对氨基酸和蛋白质的描述正确的是()A.氨基酸和蛋白质遇重金属离子均会变性B.蛋白质水解的最终产物是氨基酸C.α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,只生成2种二肽D.氨基酸溶于过量氢氧化钠溶液中生成的离子,在电场作用下向负极移动【分析】A.重金属盐能使蛋白质发生变性;B.氨基酸是组成蛋白质的基本单位,蛋白质水解的最终产物是氨基酸;α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,生成4种二肽;D.氨基酸中-COOH和NaOH反应生成羧酸根离子,应该向正极移动。
【解答】解:A.重金属盐能使蛋白质发生变性,但不能使氨基酸发生变性,故A错误;B.氨基酸通过发生水解反应生成蛋白质,所以蛋白质最终水解产物是氨基酸,故B正确;C.氨基酸生成二肽,是两个氨基酸分子脱去一个水分子,当同种氨基酸脱水,生成2种二肽;是异种氨基酸脱水:可以是α-氨基丙酸脱羟基、α-氨基苯丙酸脱氢;也可以α-氨基丙酸脱氢、α-氨基苯丙酸脱羟基,生成2种二肽。
所以共有4种,故C错误;D.氨基酸中-COOH和NaOH反应生成羧酸根离子,带负电荷,该向正极移动,故D错误;故选:B。
【习题二】下列叙述错误的是()A.氨基酸在一定条件下可发生缩聚反应B.氨基酸具有两性C.天然蛋白蛋水解的最终产物均为α-氨基酸D.饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析【分析】A.氨基酸在一定条件下可发生缩聚反应形成多肽;B.氨基酸中有氨基和羧基,氨基能与酸反应,羧基能与碱反应;C.天然蛋白质是α-氨基酸形成的;D.硫酸铜是重金属盐.【解答】解:A.氨基酸可发生缩聚反应形成多肽,故A正确;B.氨基酸分子中有氨基(-NH2)和羧基(-COOH),既能够和与酸反应,又能与碱反应,故B正确;C.天然蛋白质水解的最终产物是α-氨基酸,故C正确;D.硫酸铜是重金属盐,蛋白质遇硫酸铜发生变性,故D错误。
蛋白质跟核酸

基因表达的调控
核酸通过与蛋白质的相互作用, 调控基因的表达,影响细胞功能 和发育。
细胞信号转导
某些核酸可以作为信号分子,参 与细胞信号转导过程,影响细胞 生长、分化和凋亡。
03
蛋白质与核酸的比较
组成上的比较
01
蛋白质是由氨基酸组成的生物大 分子,具有复杂的空间结构和功 能,是生命活动中不可或缺的物 质。
核酸分子通常以单链形式存在, 但在特定情况下可以形成双链结
构。
双螺旋结构
DNA通常以双螺旋结构存在,这 种结构由两条反向平行的链和碱基 之间的氢键形成。
三螺旋结构
某些情况下,DNA可以形成三螺旋 结构,这种结构由三条链和碱基之 间的氢键形成。
核酸的功能
遗传信息的载体
核酸是遗传信息的载体,通过 DNA的复制、转录和翻译过程, 将遗传信息传递给下一代或合成 蛋白质。
蛋白质跟核酸
• 蛋白质 • 核酸 • 蛋白质与核酸的比较 • 蛋白质与核酸的相互关系 • 蛋白质的组成
01
02
03
氨基酸
蛋白质是由氨基酸组成的 大分子化合物,常见的有 20种氨基酸,通过肽键连 接成肽链。
肽键
连接氨基酸的化学键,具 有极性,是蛋白质一级结 构的主要化学键。
生物检测
蛋白质和核酸具有高度的特异性和灵敏度,可以用于生物 检测中的标记和识别,为食品安全、环境监测等领域提供 技术支持。
THANKS
感谢观看
04
蛋白质与核酸的相互关系
蛋白质对核酸的影响
蛋白质是核酸的合成和复制过程中的 重要调节因子,可以影响核酸的转录 和复制过程,从而影响基因的表达。
蛋白质可以与核酸结合,形成复合物 ,对核酸的结构和稳定性产生影响, 从而影响核酸的功能。
高中化学第四章第3节 蛋白质和核酸知识点

第三节蛋白质和核酸蛋白质是生物体内一类极为重要的功能高分子化合物,是生命活动的主要物质基础。
它不仅是细胞、组织、肌肉、毛发等的重要组成成分,而且具有多种生物学功能。
一、氨基酸1、氨基酸的分子结构氨基酸是羧酸分子烃基上的氢原子被氨基(—NH2)取代后的产物。
氨基酸的命名是以羧基为母体,氨基为取代基,碳原子的编号通常把离羧基最近的碳原子称为α碳原子,离羧基次近碳原子称为β碳原子,依次类推。
2、氨基酸的物理性质常温下状态:无色晶体;熔、沸点:较高;溶解性:能溶于水,难溶于有机溶剂。
3、氨基酸的化学性质(1)甘氨酸与盐酸反应的化学方程式:;(2)甘氨酸与氢氧化钠反应的化学方程式:氨基酸是两性化合物,基中—COOH为酸性基团,—NH2为碱性基团。
(3)成肽反应两个氨基酸分子(可以相同也可以不同)在酸或碱存在下加热,通过一分子的氨基和另一分子的羧基脱去一分子水,缩合形成含有肽键的化合物,称为成肽反应。
二、蛋白质的结构与性质1、蛋白质的结构蛋白质是一类高分子化合物,主要由C、H、O、N、S等元素组成。
蛋白质分子结构的显著特征是:具有独特而稳定的结构。
蛋白质的特殊功能和活性与多肽链的氨基酸种类、数目及排列顺序、特定空间结构相关。
2、蛋白质的性质(1)水解蛋白质在酸、碱或酶的作用下,水解成相对分子质量较小的肽类化合物,最终水解得到各种氨基酸。
(2)盐析少量的盐能促进蛋白质溶解。
当向蛋白质溶液中加入的盐溶液达到一定浓度时,反而使蛋白质的溶解度降低而从溶液中析出,这种作用称为盐析。
盐析是一个可逆过程,不影响蛋白质的活性。
因此可用盐析的方法来分离提纯蛋白质。
(3)变性影响蛋白质变性的因素有:物理因素:加热、加压、搅拌、振荡、紫外线照射、超声波等。
化学因素:强酸、强碱、重金属盐、三氧乙酸、乙醇、丙酮等。
变性是一个不可逆(填“可逆”或“不可逆”)的过程,变性后的蛋白质生理活性也同时失去。
(4颜色反应颜色反应一般是指浓硝酸与含有苯基的蛋白质反应,这属于蛋白质的特征反应。
蛋白质和核酸的化学结构和功能

蛋白质和核酸的化学结构和功能蛋白质和核酸是细胞中两类重要的生物大分子,它们在生命起源和演化中发挥着重要的作用。
蛋白质和核酸的化学结构和功能是生命科学的重要研究领域,在本文中,我们将探讨蛋白质和核酸的化学结构和功能。
一、蛋白质的化学结构与功能1.1 蛋白质的化学结构蛋白质是由氨基酸通过肽键链接而成的线性多肽,其中每个氨基酸分子有自己的化学结构,包括α-氨基酸、β-氨基酸等等。
常见的α-氨基酸有20种,在不同的蛋白质中按照不同的顺序排列,可以形成不同的蛋白质。
蛋白质的化学结构可以分为四个层次:一级、二级、三级、四级结构。
一级结构即氨基酸序列,二级结构是氢键作用下的螺旋状或β-折叠状分子链,三级结构是由氢键、离子键、氢结合、疏水作用等多种非共价力相互作用所维持的三维结构,而四级结构是由两个或多个具有独立生物活性的多肽链相互作用而形成的复合物。
1.2 蛋白质的功能蛋白质是细胞和生命体系的基础组成部分,在生命体系中扮演着非常重要的角色。
蛋白质的功能多种多样,可以通过控制基因表达、构建细胞骨架、调节代谢和能量代谢等多种机制发挥作用。
蛋白质作为酶可以在细胞代谢、免疫反应和信号传导中发挥重要作用,如谷氨酸脱氢酶、葡萄糖氧化酶等酶就是在控制代谢反应中发挥主导作用的蛋白质。
蛋白质还可以作为携带物质得到利用,如血红蛋白携带氧分子,白蛋白携带脂溶性物质等。
此外还可以构建细胞骨架、参与免疫反应等。
二、核酸的化学结构与功能2.1 核酸的化学结构核酸是由核苷酸单元组成,是基因信息的储存、复制、转录和翻译的重要分子。
核苷酸由五碳糖、硫酸基和核苷酸碱基组成。
在DNA中,五碳糖为脱氧核糖,硫酸基为磷酸,碱基包括腺嘌呤、胞嘧啶、鸟嘌呤、脱氧胸腺嘧啶四种;在RNA中,五碳糖为核糖,硫酸基为磷酸,碱基包括腺嘌呤、尿嘧啶、鸟嘌呤、胸腺嘧啶。
核酸分为DNA和RNA两种,它们的分子结构有所不同。
DNA是双螺旋结构,由两个互补的链通过氢键相互配对而形成的,其中腺嘌呤与胸腺嘧啶通过两条氢键相连,鸟嘌呤与胞嘧啶则通过三条氢键相连。
1-3 蛋白质和核酸
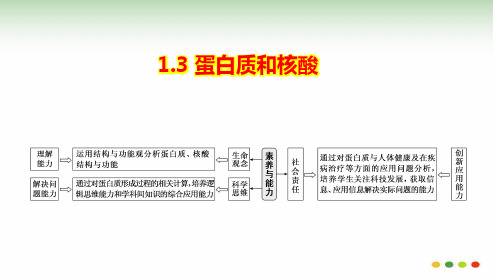
6.经测定,某多肽链的分子式是 C21HxOyN4S2,其中含有一个二硫键(—S—S—)。已知
该多肽是由下列氨基酸中的其中几种作为原料合成的:苯丙氨酸(C9H11O2N)、天冬
氨酸(C4H7O4N)、丙氨酸(C3H7O2N)、亮氨酸(C6H13O2N)、半胱氨酸(C3H7O2NS)。下
列关于该多肽的叙述,错误的是
1.3 蛋白质和核酸
考点一 蛋白质的结构和功能
1.组成蛋白质的氨基酸的结构和种类 (1)氨基酸的结构
C、H、O、N
羧基 同一个
(2)氨基酸的种类 种类基 必非酸 需必氨需特 种氨点 类基: : 酸必种 特8须类 点从 种: :外人13界体种环细境胞中能获够取合成
2.蛋白质的合成 (1)多肽的形成过程
2.(2021·石家庄模拟)下图中甲是组成乙或丙的基本单位(单体)。下列相关叙述不正确的
是
()
A.如果甲中的 m 是 U,则甲一定是丙的基本单位 B.如果甲中的 m 是 G,则甲一定是乙的基本单位 C.如果甲中的 a 是脱氧核糖,则甲物质聚合成的大分子物质可以分布于线粒体和
2.(2021·山东潍坊统考)下面是三种化合物的结构简式,下列有关这三种化合物的叙述,
错误的是
()
A.三种化合物可以用一个结构通式表示 B.三种化合物的共同点之一是都含有一个氨基、一个羧基 C.三种化合物都不能与双缩脲试剂发生紫色反应 D.三种化合物两两结合形成的物质的游离氨基数相同 解析:三种物质都是构成生物体中蛋白质的氨基酸,都可用氨基酸的结构通式表示,A 正确;图中三种氨基酸的共同点应为“至少都含有一个氨基、一个羧基”,B 错误;双 缩脲试剂鉴定蛋白质产生紫色反应,是由于蛋白质中有肽键,氨基酸中无肽键,故不能 与双缩脲试剂发生紫色反应,C 正确;三种化合物两两结合形成的物质中游离的氨基数 分别是 1、1、1,D 正确。 答案:B
高一生物 蛋白质和核酸

5.长多肽链断裂成几段短多肽链 某三十九肽中共有丙氨酸 4 个,现去掉其中的丙氨 酸得到 4 条长短不等的多肽(如图所示),分析该过 程中肽键数、游离的氨基、羧基数。C、H、O、N 数如何变化?
断裂前
(3)氨基酸的排列次序不同,构成的肽链不同。 —□—○—○—□—○— —○—□—○—□—○— (4)空间结构不同,构成的蛋白质不同。
提醒 若两个肽链中的氨基酸的数目、种类都相同, 但功能不同,是由排列次序不同造成的;若仅数目相 同,则是由氨基酸的种类和排列次序不同造成的;若 两个蛋白质分子的结构和功能都不同,则答全四个方 面。
在酶的作用下,一个氨基酸的羧基提供的-OH与 另一个氨基酸的氨基提供的-H 生成 1 分子水被脱 去,而羧基和氨基剩余的基团相连成为肽键,其结
构式为
。
2.蛋白质结构多样性的原因 (1)组成蛋白质多肽链的氨基酸在 种类 、 数量 和 排列顺序 上的不同。 (2)构成蛋白质的多肽链在 空间结构 上的不同。
考点二 蛋白质与核酸 1.肽键和磷酸二酯键的形成
(1)两种化学键的形成都伴随着 H2O 生成,都是吸 能反应,都消耗 ATP。 (2)肽键的断裂需要蛋白酶或肽酶;磷酸二酯键的形 成需 DNA 聚合酶或 DNA 连接酶(片段连接),断裂 需 DNA 水解酶或限制性核酸内切酶。 (3)肽键形成场所——核糖体;磷酸二酯键形成场所 ——细胞核、叶绿体、线粒体等。
的化学组成及它们之间的关系。下列相关说法中,
不正确的是
()
A.A 和 B 是染色体的主要成分 B.过程 1、2、4 都有水的产生 C.密码子存在于 B 和 C D.过程 3、4 进行的场所和所利用的酶不同
蛋白质和核酸的异同点

蛋白质和核酸的异同点
蛋白质和核酸是生命体中两种重要的大分子。
它们有许多相似之处,也有很多不同之处。
相似点:
1. 组成:蛋白质和核酸都是由小分子单元(氨基酸和核苷酸)组成的。
2. 功能:蛋白质和核酸都扮演着生物体内重要的功能角色。
蛋白质可以起到酶、结构蛋白、激素等多种生物学作用;核酸则是负责存储和传递遗传信息。
3. 二级结构:蛋白质和核酸都有二级结构,即由氢键、范德华力等相互作用力形成的空间结构。
蛋白质的二级结构有α-螺旋和β-折叠等;核酸的二级结构有双螺旋结构。
不同点:
1. 化学组成:蛋白质的单元是氨基酸,而核酸的单元是核苷酸。
氨基酸由氨基、羧基和侧链组成,而核苷酸由磷酸、五碳糖和碱基组成。
2. 功能:蛋白质和核酸的功能不同。
蛋白质通常参与代谢、调节、传递信号等细胞活动,核酸则通常用于存储和传递遗传信息。
3. 三级结构:蛋白质和核酸的三级结构也不同。
蛋白质的三级结构是由各种化学键和相互作用力组成的,而核酸的三级结构则是由双螺旋结构和其他形态如发夹环和三维结构等组成的。
总之,蛋白质和核酸虽然都是由小分子单元组成的大分子,但它
们有很多不同的特点和功能,是生命体中不可或缺的重要分子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十四章蛋白质和核酸一、学习要求1.掌握氨基酸的分类、结构、命名和中、英文缩写。
2.掌握氨基酸的构型和化学性质。
3.掌握肽的结构和命名,肽分子中C―端和N―端的分析方法。
4.了解蛋白质的组成元素,熟悉蛋白质的一级结构及空间结构,掌握蛋白质的化学性质。
5.熟悉核酸的分类、基本结构,掌握核酸分子的碱基及其配对规律二、本章要点(一)氨基酸1.氨基酸的结构氨基酸是分子中含有氨基和羧基的化合物。
组成蛋白质的氨基酸有20种,均为α-氨基酸L-构型,除甘氨酸外,都是手性分子,除半胱氨酸为R-构型外,其余均为S-构型。
2.氨基酸的分类根据烃基的不同可把氨基酸分为脂肪族氨基酸、芳香族氨基酸和杂环氨基酸;根据分子中氨基和羧基的数目,还可将氨基酸分为中性氨基酸、酸性氨基酸和碱性氨基酸。
3.氨基酸的命名天然氨基酸常使用俗名,也可用中文名称、英文缩写和单字符号来表示。
在氨基酸的系统名命法中,是以羧酸为母体,将氨基作为取代基而称为“氨基某酸”,氨基的位次用希腊字母α、β、γ等表示。
4.氨基酸的性质(1)物理性质:α-氨基酸为无色晶体,熔点较高(200─300℃),在熔化时分解放出二氧化碳。
溶解于水,而难溶于乙醇、醚、苯等有机溶剂中。
除甘氨酸外,均有旋光性。
(2)氨基酸的化学性质1).两性电离和等电点:氨基酸分子是两性化合物;与酸、碱可反应生成盐;本身还可生成内盐。
氨基酸晶体溶解于纯水中时,可发生酸式电离和碱式电离。
中性、酸性氨基酸在纯水中带净负电荷,水溶液显酸性,碱性氨基酸在纯水中,其水溶液呈碱性,氨基酸本身带净正电荷。
氨基酸净电荷为零时溶液的pH值称为氨基酸的等电点(isoelectric point)用pI 表示。
氨基酸的存在形式与溶液pH 值的关系可表示如下:等电点时,氨基酸的溶解度最小,可从水溶液中析出,所以可以利用等电点分离提纯氨基酸。
2).显色反应: α-氨基酸与水合茚三酮在水溶液中加热反应能形成蓝紫色化合物,可用于α-氨基酸的定量和定性分析。
3).与HNO 2反应: α-氨基酸与亚硝酸作用时定量放出氮气, 该反应可测定氨基酸、蛋白质及肽分子中的自由氨基。
4).脱羧反应:氨基酸在脱羧酶或与氢氧化钡共热可发生脱羧反应,生成少一个碳原子的伯胺。
5).成肽反应: 当两分子α-氨基酸受热时,氨基和羧基之间交叉脱水,生成环状的交酰胺(二酮吡嗪),二酮吡嗪在浓盐酸的作用下,可以水解断开一个酰胺键生成二肽。
(二)肽1. 肽的结构和命名 由氨基酸残基通过肽键(酰胺键)连接而形成的化合物叫做肽。
由多个氨基酸形成的肽称为多肽。
肽的命名是从N-端开始,由左至右依次将每一个氨酸残基写成“某氨酰”,处于C-端的最后一个氨基酸为母体称为某氨酸。
肽的名称也常用中文或英文的缩写符号来表示,符号之间用短线隔开:丙氨酰甘氨酰丝氨酸(丙甘氨丝肽) 丙-甘-丝 或Ala-Gly-Ser 。
2.肽链结构测定 可配合使用端基分析( N-端分析、C-端分析)和部分水解的方法来加以确定。
3.活性肽 在生物体内有着重要的功能的游离肽,如:γ-谷胱甘肽、催产素和加压素、神经肽等。
(三)蛋白质1.蛋白质的元素组成和分类RCHCOO 3H ++负离子两性离子正离子pH>pI pH=pI pH<pIRCHCOOH NH 3OHRCHCOO 2++(1)元素组成:天然蛋白质均含有碳(50-55%)、氢(6.7-7.3%)、氧(19-24%)、氮(13-19%),硫(0-4%)等元素。
此外,蛋白质中还含有磷、碘、铁、锰、铜、锌等元素。
生物样品中1克氮相当于6.25克蛋白质。
(2)分类:蛋白质按分子形状可分为球状蛋白质和纤维状蛋白;按分子组成可分为单纯蛋白和结合蛋白质;按功能可分为活性蛋白质和结构蛋白质。
2.蛋白质的结构(1)蛋白质的一级结构:蛋白质的一级结构是指多肽链中氨基酸残基的排列顺序及其连接方式。
肽键是一级结构中连接氨基酸残基的化学键。
(2)蛋白质的二级结构:蛋白质的二级结构是指肽链按一定的方式折叠、盘曲形成的空间构象,氢键是主要的副键,蛋白质的二级结构主要有α-螺旋、β-折叠、β-转角和无规则卷曲等。
(3) 蛋白质的三级结构:具有二级结构的蛋白质,可以进一步按一定方式折叠、盘曲形成更复杂的三维空间排布,即形成蛋白质的三级结构。
维持三级结构的力来自氨基酸侧链之间的相互作用。
主要包括盐键、二硫键、氢键、配位键、酯键、疏水基之间的亲和力(疏水键)和van der waals力等。
这些作用总称为副键。
(4)蛋白质的四级结构是由两条以上具有三级结构的多肽链组成的更大、更复杂的分子。
每一条三级结构多肽链称为一个亚基,几个亚基通过氢键、疏水键或静电吸引缔合而构成一定的空间结构。
亚基的种类、数目和空间排列都有特定的模式。
3.蛋白质的化学性质(1)胶体性质:蛋白质是高分子化合物,相对分子质量可高达几千万,其分子颗粒的直径一般在103pm ~105pm之间,属于胶体粒子,呈现胶体的性质:电泳扩散速度慢,不能透过半透膜。
(2)两性电离和等电点:在蛋白质分子中,肽链的侧链中含有未结合的碱性基团(如氨基、胍基、咪唑基)和酸性基团(羧基、酚羟基、巯基),因而蛋白质和氨基酸一样是两性化合物,也有等电点。
(3)蛋白质的沉淀:蛋白质分子在溶液中发生凝聚,并从溶液中析出的现象称为蛋白质的沉淀。
常用的方法有:盐析、加脱水剂、加入某些重金属盐和有机酸等。
(4)蛋白质的变性:蛋白质在某些物理因素或化学因素的作用下,蛋白质的性质发生改变的现象称为蛋白质的变性。
性质改变后的蛋白质称为变性蛋白质。
引起蛋白质变性的物理因素有:加热、加压、激烈的搅拌或振荡、紫外线和超声波等。
化学因素有:强酸、强碱、尿素、重金属盐、有机溶剂、生物碱试剂和表面活性剂等。
变性有可逆变性和不可逆变性两种。
(5)蛋白质的显色反应1).缩二脲反应(biure reaction ):蛋白质分子中含有许多肽键,因此所有的蛋白质均可与稀硫酸铜碱性溶液反应,呈紫色或紫红色。
2).茚三酮反应(ninhydrin reaction):蛋白质与水合茚三酮共热呈现蓝紫色。
茚三酮作为显色剂常用纸层析和电泳法中分离和鉴定蛋白质、多肽和氨基酸。
(四)核酸1.组成 核酸是由许多核苷酸结合而成的高分子化合物。
核酸在酸、碱或酶催化下水解的产物如下:2.核酸的分类 核酸包括脱氧核糖核酸(DNA )和核糖核酸(RNA: rRNA 、mRNA 和tRNA)。
3.核苷和核苷酸的结构及命名PrCOO NH 3++NH 3+COOH PrNH 2COO Pr+蛋白质负离子蛋白质两性离子蛋白质正离子pH>pI pH=pI pH<pI核酸水解核苷酸核苷磷酸碱基戊糖嘌呤碱嘧啶碱核糖脱氧核糖(1)核苷:核核苷是由碱基中嘌呤碱9位氮上的氢或嘧啶碱1位氮上的氢与戊糖1′ 位上的羟基失水所生成的β-N-苷。
为区别糖与碱基中原子的编号,规定糖中原子编号1′、2′、3′……。
核苷是按组成的碱基与戊糖来命名的(2)核苷酸:核苷酸是核苷3位或5位的羟基和磷酸所生成的酯。
自然界中存在的核苷酸主要是5′-磷酸酯。
组成DNA 的核苷酸主要有四种:脱氧腺苷酸(dAMP)、脱氧鸟苷酸(dGMP)、脱氧胞苷酸(dCMP)和脱氧胸苷酸(dTMP)。
组成RNA 的核苷主要也有四种:腺苷酸(AMP)、鸟苷酸(GMP)、胞苷酸(CMP)和尿苷酸(UMP)。
核苷酸命名时,除将戊糖和碱基部分注明外,还要指出磷酸酯键所连接的位置。
4.核酸的结构(1)一级结构: 核酸的一级结构指的是核酸中各核苷酸的排列顺序。
核酸的一级结构常采用速记法、字符式和线条式表明其结构。
(2)二级结构: DNA 具有双螺旋结构,即DNA 分子是由两条方向相反的平行多核苷酸链构成的;两条链上的碱基在螺旋的内侧,戊糖和磷酸连接成的主链在外侧,两条链由碱基间的氢键相连;两条核苷酸链之间的碱基配对有一定规律。
RNA 由一条弯曲的多核苷酸链构成,其中有间隔着的双螺旋和单股非螺旋结构的部分,链的某些部分存在着碱基配对关系。
tRNA 具有三叶草的结构。
(3)核酸的三级结构:在二级结构的基础上,多核苷酸链在空间可进一步盘曲折叠构成核酸三级结构。
tRNA 多为倒置的L 形状;DNA三、 问题参考答案问题14-1试写出L-酪氨酸、L-半胱氨酸的Fischer 投影式,并用R/S 构型标记。
解:问题14-2 苯丙氨酸在等电点时溶液为中性、酸性还是碱性?在pH 值为3.0,5.8和10.0的溶液中各带什么电荷?用离子结构式表示。
SRCH 2H 3NCOOH +H 3NCOO H +CH 2SH 酪氨酸半胱氨酸解:苯丙氨酸含一氨基一羧基,为中性氨基酸,其水溶液呈弱酸性。
因其等电点pI=5.84,故: 在pH=3.0时带正电荷:在pH=5.8时净电荷为零,为两性离子:在pH=10.0时带负电荷:问题14-3 写出一分子甘氨酸和一分子丙氨酸在浓盐酸作用下加热生成二肽的反应式。
解:四、习题参考答案1.写出下列化合物的结构式:(1)天冬酰胺 (2)脯氨酸 (3)甲硫氨酸(4)赖氨酸(5)组氨酸 (6) 还原型γ-谷胱甘肽解:CH 2CHCOOHNH 3++CH 2CHCOONH3CH 2CHCOO2CH 2COOH NH 2+CH 3CHCOOHNH 2CH 2CONHCH 2COOH2+CH 2CONHCHCOOH 2CH 3+CHCONHCH 2COOHNH 2CH 3+CH 3CHCONHCHCOOHNH 2CH 3H 2NCCH 2CHCOOONH 3+(1) H 2(2)CH 2SCH 2CH 2CHCOONH 3+(3) CH 2CH 2CH 2CH 2CHCOONH 3+NH 2(4) NH 2CHCOO NH 3+(5)H 2NCHCH 2CH 2CONHCHCONHCH 2COOH2SH(6)2.完成下列反应方程式:△解:△3.在多肽的端基分析中,常用2,4-二硝基氟苯作N-端标记,标记后的多肽经水解后,为什么2,4-二硝基氟苯相连的氨基酸很容易与其它氨基酸分离?解:这是因为2,4-二硝基氟苯具有强烈的-I 效应,与其相连的氨基碱性极弱,所以不溶于稀酸水溶液中;而其他非标记的氨基酸可溶于稀酸水溶液中,借此可以分离。
4.1个五肽部分水解得3个三肽,即G1u-Arg-GLy ,Gly-G1u-Arg, Arg-Gly-phe ,经N-端分析发现N-端为Gly ,试分别用中英文缩写写出这个五肽中氨基酸的连接顺序。
+N 2CO +NaOHHNO 2(4)(3)(2)(1)CH 3CH 3CH CH 2COO_NH 3+NH 3+CH 3CH CH 2COO CH 3ClHCH 3CH 3CH CH 2COO_NH 3+Na+H 2ONH 2CH 2CHCOOHOHCH 2CHCOOHCH 3CH 3CH CH 2COO NH 2HCH 3CH 3CH CH 2COO NH 2CH 3CHCH 2NH 2CH 3NaOHHNO (4)(3)(2)(1)3CH 3CH CH 2COO_NH 3+CH 3CH 3CH CH 2COO_NH 3+NH 2CH 2CHCOOHH 3CH 3CH CH 2COO NH 2解:Gly-G1u-ArgG1u-Arg-GLyArg-Gly-phe——————————————Gly -G1u-Arg-Gly-phe甘-谷-精-甘-苯丙5.短杆菌肽S是霉菌的代谢产物,具有抗菌作用,它是一个由十个氨基酸残基组成的环状十肽,完全水解时生成L-缬氨酸,L-亮氨酸,L-脯氨酸、D-苯丙氨酸和L-鸟氨酸,其比例都是1∶1。
