固体中的相结构分类和形成规律
固体物理学-晶体结合类型

同时,由于距离增大,价电子与原子实之间的势能相对于 自由原子时要高。但由于自由电子屏蔽作用的存在,势能的 升高相对于动能的降低要小,二者能量之差就是金属结合的 主要来源。
12
I . 固体结合类型
------共价结合和共价晶体
13
共价键(氢分子为例)
•共价结合是靠两个原子各贡献一个电子,形成共价键。这样一对为两个 原子所共有的自旋相反配对的电子结构称为共价键。
•这对自旋相反的电子在两原子核之间的区域会形成较大的电子云密度, 同时受到两个原子核较强的库仑吸引作用,这就是共价键产生的物理根 源。
这种相互作用一定包括吸引和排斥两种类型。吸引力使粒子 聚集一起,排斥力使粒子之间保持一定间距,维持固体形态。 两种作用并存,粒子处于平衡状态,从而结合形成稳定的晶体 结构。这种维系原子结合在一起的作用力或称为“键”。
粒子之间的作用力应全部归结于静电相互作用,磁力和万有 引力忽略不计。粒子间的吸引作用可以归结为异性电荷间的库 仑吸引力;而排斥作用可以归结为同性电荷之间的库仑斥力以 及由泡利原理引起的排斥力。
4
根据键的特征,固体结合类型主要有以下几种:1. 金属 性结合;2. 共价结合;3. 离子性结合;4.范德瓦尔斯结合。 与结合力类型相对应,晶体可大致分为四种基本类型: 1. 金属晶体; 2. 共价晶体;3.离子晶体;4.分子晶体。
值得指出的是,以上这些类型之间的区分不是严格的, 某些固体的结合往往具有混合的特点或过渡的性质。
材料科学基础-固体的结构
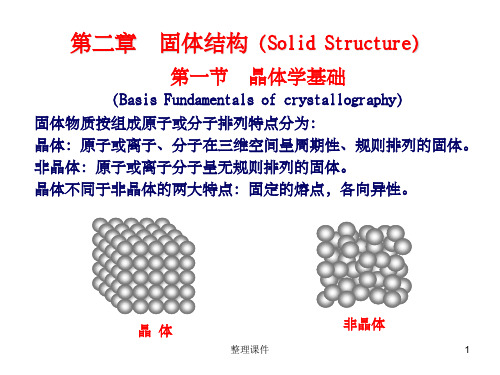
hu+kv+lw=0
此关系称为晶带定理。满足该关系的(hkl)晶面都属于以
[uvw]为晶带轴的晶带。
[uvw]
整理课件
32
第二章 固体结构
利用晶带定理:
①已知两个不平行的晶面(h1k1l1)和(h2k2l2),求出其晶带 轴[uvw]。
u : v : w ( k 1 l 2 k 2 l 1 ) : ( l 1 h 2 l 2 h 1 ) : ( h 1 k 2 h 2 k 1 )
整理课件
16
第二章 固体结构
整理课件
17
第二章 固体结构
整理课件
18
第二章 固体结构
整理课件
19
第二章 固体结构
整理课件
20
第二章 固体结构
整理课件
21
第二章 固体结构
整理课件
22
第二章 固体结构
晶面族:原子排列规律、面间距完全相同,仅空间位向 关系不同的一组晶面(等价晶面),以{h k l}表示。
如六个柱面分别为: ( 1 0 0 ),(0 1 0 ),(1 1 0 ),(1 0 0 ),(0 1 0 ),( 1 1 0 ) c
(1 1 0)
(100)
a2
a1 [100 ]
[110 ]
整理课件
25
第二章 固体结构
根据六方晶系的对称特点,通常采用a1, a2, a3和c四个晶轴确
定六方晶系的晶面指数和晶向指数。
具有相同空间点阵的不同晶体结构
晶体结构相似而具有空间点阵不同
整理课件
13
第二章 固体结构
二、晶向指数和晶面指数
(Miller Indices of Crystallographic Direction and Planes) 1、晶向与晶向指数
材料科学基础名词解释

材料科学基础名词解释第一章固体结构1、晶体 :原子按一定方式在三维空间内周期性地规则重复排列,有固定熔点、各向异性。
非晶体 :原子没有长程的周期排列,无固定的熔点,各向同性等。
2、中间相 : 两组元 A 和 B 组成合金时,除了形成以 A 为基或以 B 为基的固溶体外,还可能形成晶体结构与 A,B 两组元均不相同的新相。
由于它们在二元相图上的位置总是位于中间,故通常把这些相称为中间相。
3、晶体点阵:由实际原子、离子、分子或各种原子集团,按一定几何规律的具体排列方式称为晶体结构或晶体点阵。
4、配位数 :晶体结构中任一原子周围最近邻且等距离的原子数。
5、晶格:描述晶体中原子排列规律的空间格架称之为晶格。
6、晶胞 :在点阵中取出一个具有代表性的基本单元(最小平行六面体)作为点阵的组成单元,称为晶胞。
7、空间点阵:由周围环境相同的阵点在空间排列的三维列阵成为空间点阵。
8、晶向:在晶格中,穿过两个以节点的任一直线,都代表晶体中一个原子列在空间的位向,称为晶向。
9、晶面:由节点组成的任一平面都代表晶体的原子平面,称为晶面。
10、晶向指数(晶面指数):为了确定晶面、晶向在晶体中的相对取向、就需要一种符号,这种符号称为晶面指数和晶向指数。
国际上通用的是密勒指数。
一个晶向指数并不是代表一个晶向,二十代表一组互相平行、位向相同的晶向。
11、晶向族:原子排列相同但空间位向不同的所有晶向称为晶向族,以<uvw>表示。
12、晶面间距:相邻两个平行晶面之间的垂直距离。
低指数晶面的面间距较大,而高指数晶面的面间距较小。
晶面间距越大,则该晶面上原子排列越紧密,该原子密度越大。
13、配位数:每个原子周围最近邻且等距离的原子数目,称为配位数。
14、多晶型性:有些金属固态在不同温度或不同压力范围内具有不同的晶体结这种性质构,称为晶体的多晶型性。
15、多晶型性转变:具有多晶型性的金属在温度或压力变化由一种结构转变为另一种结时,构的过程称为多晶型性转变,也称为同素异构转变。
合金在固体状态的相结构

合金的相结构是指在固体状态下,合金中结构和成分均一的组成部分。
根据合金中各组元间相互作用不同,固态合金中的相可分为固溶体和金属化合物两类。
固溶体是指固态合金组元间互相溶解而形成的均匀相。
固溶体中保持原来晶格结构的组元称为溶剂,其含量较多;其他溶入且晶格结构消失了的组元称为溶质,其含量较少。
固溶体是合金的一种基本相结构,其晶格与溶剂组元晶格相同。
按溶质原子在溶剂晶格中所占位置不同,可分为间隙固溶体和置换固溶体两类。
间隙固溶体:溶质原子处于溶剂原子的间隙中而形成的固溶体。
由于溶剂晶格空隙有限,故间隙固溶体能溶解的溶质原子的数量也是有限的。
由于溶剂晶格空隙尺寸很小,因此能形成间隙固溶体的溶质原子,通常是一些半径很小的非金属元素,如碳、氮、硼等非金属元素溶于铁中形成的固溶体。
置换固溶体:单胞中的原子数目保持与纯溶剂相同,由一种元素替代另一种元素或替代一个化合物中的某一元素,或一个化合物替代另一个化合物。
形成置换固溶体的条件是:相互替代的组元应该具有相同的晶胞形状,原子半径差不超过15%,电负性和电子结构相近。
此外,金属化合物是指合金中的各组元通过相互作用,形成了与组元性质完全不同的新相。
金属化合物一般具有复杂的晶体结构,其晶格结构与单一组元相的晶格结构均不相同。
金属化合物在合金中以脆性相形式存在,降低合金的力学性能。
综上所述,相是组织的基本单元,组织是相的综合体。
如需了解更多关于合金在固体状态的相结构的信息,建议查阅金属学书籍或咨询材料学家获取。
材料科学基础_第6章_固态相变的基本原理

第6章 固态相变的基本原理
1
概述
固态相变:固态物质内部的组织结构的变化称为固态相变。 相是成分相同、结构相同、有界面同其他部分分隔的物质均 匀组成部分,相变是从已存的相中生成新的相。 新相,生成部分与原有部分存在着或成分不同、或相结构不 同、或有序度不同、或兼而有之,并且和原来部分有界面分隔。 原来的部分称为母相或反应相,在转变过程中数量减少,生 成部分称为新相或生成相,在转变过程中数量增加。
4
6.1 固态相变的分类与特征 6.1.1 固态相变的分类
1.按热力学分类 按照自由能对温度和压力的偏导函数在相
变点的数学特征——连续或非连续,将相变分 为一级相变和高级相变(二级或二级以上的相 变)。
n级相变:在相变点系统的化学势的第(n1)阶导数保持连续,而其n阶导数不连续。
5
一级相变的特点是,相变发生时,两平衡相的 化学势相等,但化学势的一阶偏导数不相等。
的中间转变称为过渡型。 a. 块状转变,更接近于扩散型相变,相界面是非共格的,
相界面移动通过原子扩散进行,相变时成分不变。 b.贝氏体相变,扩散性长大和非扩散性长大相互制约。
11
3. 按长大方式分类 形核长大型相变 连续型相变
4.按相变过程分类 近平衡相变 远平衡相变
12
6.1.2 固态相变的特征
1)原子的扩散速度 ➢ 由于新旧两相的化学成分不同,相变时必须有原子的扩散 ➢ 原子扩散速度成为相变的控制因素。 ➢ 当相变温度较高时,即扩散不是决定性因素的温度范围内
,随着温度的降低,即过冷度的增大,相变驱动力增大, 相变速度加快;但是当过冷度增大到一定程度,扩散称为 决定性因素,进一步增大过冷度,反而使得相变速度减小 。
13
固体物理第二章 固体的结合

(四)范德瓦耳斯结合
1879年范德瓦耳斯(Van der Waals)提出在实际气体 分子中,两个中性分子(或原子)间存在着“分子力”, 即范德瓦耳斯力。由范德瓦耳斯力的作用所组成的晶体称 为分子晶体。
范德瓦耳斯结合往往产生于原来具有稳固电子结构的 原子或分子之间,如:具有满壳层结构的惰性气体元素, 或价电子已用于形成共价键的饱和分子。
18
固体物理
固体物理学
共价键与离子键间的混合键
完全离子结合(如NaCl):正负离子通过库仑相互 作用结合在一起, Na+和Cl-的电子云几乎没有重叠。
19
固体物理
固体物理学
完全共价结合(如金刚石):相邻两个C原子各出一个 未配对的自旋相反的电子归这两个原子所共有,在这两个原 子上找到电子的概率相等,即这两个C原子对共价键的贡献
15
固体物理
固体物理学
1
1 2
(j2s
j2 px
j2 py
j2 pz
)
2
1 2
(j2s
j2 px
j2 py
j2 pz
)
3
1 2
(j2s
j2 px
j2 py
j2 pz
)
4
1 2
(j2
s
j2 px
j2 py
j2pz )
“杂化轨道”
原来在2s和2p轨道上的4个电子,分别处于 1 , 2 , 3 , 4
21
固体物理
固体物理学
1. 有效离子电荷 q*
以 GaAs 为例:GaAs的离子实分别为带+3q 和+5q 的离 子Ga3+和As5+,每一对Ga 和As 共有8个价电子。 (1) 若为完全的共价结合,共价键上的每对电子均分在两 个近邻原子上,则:Ga-1As+1。 (2) 若为完全的离子结合(设Ga原子的3个价电子转移到As 原子),则:Ga3+As3-。 (3) 实际介于二者之间,引入有效离子电荷q*,(以电子 电荷为单位)Ga原子的q*肯定介于-1和+3之间。
(完整版)材料科学基础基础知识点总结

第一章材料中的原子排列第一节原子的结合方式2 原子结合键(1)离子键与离子晶体原子结合:电子转移,结合力大,无方向性和饱和性;离子晶体;硬度高,脆性大,熔点高、导电性差。
如氧化物陶瓷。
(2)共价键与原子晶体原子结合:电子共用,结合力大,有方向性和饱和性;原子晶体:强度高、硬度高(金刚石)、熔点高、脆性大、导电性差。
如高分子材料。
(3)金属键与金属晶体原子结合:电子逸出共有,结合力较大,无方向性和饱和性;金属晶体:导电性、导热性、延展性好,熔点较高。
如金属。
金属键:依靠正离子与构成电子气的自由电子之间的静电引力而使诸原子结合到一起的方式。
(3)分子键与分子晶体原子结合:电子云偏移,结合力很小,无方向性和饱和性。
分子晶体:熔点低,硬度低。
如高分子材料。
氢键:(离子结合)X-H---Y(氢键结合),有方向性,如O-H—O(4)混合键。
如复合材料。
3 结合键分类(1)一次键(化学键):金属键、共价键、离子键。
(2)二次键(物理键):分子键和氢键。
4 原子的排列方式(1)晶体:原子在三维空间内的周期性规则排列。
长程有序,各向异性。
(2)非晶体:――――――――――不规则排列。
长程无序,各向同性。
第二节原子的规则排列一晶体学基础1 空间点阵与晶体结构(1)空间点阵:由几何点做周期性的规则排列所形成的三维阵列。
图1-5特征:a 原子的理想排列;b 有14种。
其中:空间点阵中的点-阵点。
它是纯粹的几何点,各点周围环境相同。
描述晶体中原子排列规律的空间格架称之为晶格。
空间点阵中最小的几何单元称之为晶胞。
(2)晶体结构:原子、离子或原子团按照空间点阵的实际排列。
特征:a 可能存在局部缺陷;b 可有无限多种。
2 晶胞图1-6(1)――-:构成空间点阵的最基本单元。
(2)选取原则:a 能够充分反映空间点阵的对称性;b 相等的棱和角的数目最多;c 具有尽可能多的直角;d 体积最小。
(3)形状和大小有三个棱边的长度a,b,c及其夹角α,β,γ表示。
材料科学基础复习要点

《材料科学基础》复习要点一、主要内容1. 工程材料中的原子排列(1)原子键合,工程材料种类;(2)原子的规则排列:晶体结构与空间点阵,晶向及晶面的特点及表示,金属的晶体结构,陶瓷的晶体结构。
(3)原子的不规则排列:点、线、面缺陷的类型及特征,位错的弹性性质,实际晶体中的位错。
2. 固体中的相结构(1)固溶体:分类、性能及影响固溶度的因素;(2)金属间化合物:分类、性能及特征;(3)陶瓷晶体相:分类、结构、性能及特征;(4)玻璃相:性能、特征及形成条件。
3. 凝固与结晶(1)结晶的基本规律;(2)结晶的基本条件;(3)晶核的形成:形核能量变化,临界晶核,形核功,形核率;(4)晶体的长大:长大条件,液固界面结构,长大机制,温度梯度,晶体形态;(5)凝固理论的应用。
4. 二元相图:(1)相图的基本知识;(2)二元匀晶相图、共晶相图及包晶相图:二元合金的平衡凝固及非平衡凝固,凝固过程中的成分变化及偏析,成分过冷与固溶体组织,共晶体形成机理及其形态,杠杆定律;(3)二元相图的分析方法,其他类型二元相图及其应用;(4)Fe-C相图分析及平衡凝固;(5)铸锭组织与偏析。
5. 材料中的扩散:(1)扩散定律及其应用;(2)扩散的微观机理,影响扩散的因素;(3)扩散的热力学理论;(4)反应扩散。
6. 塑性变形:(1)单晶体的塑性变形;(2)多晶体的塑性变形;(3)合金的塑性变形;(4)冷变形金属的组织与性能。
7. 回复与与结晶:(1)冷变形金属在加热时的变化;(2)回复:机制,热力学,动力学,应用,影响因素;(3)再结晶:机制,热力学,动力学,应用,影响因素;(4)再结晶后晶粒长大:机制,热力学,动力学,应用及组织控制,影响因素;(5)金属的热变形,超塑性。
二、参考书目1. 《材料科学基础》,胡庚祥,蔡珣,上海交通大学出版社,20002. 《材料科学基础》(第二版),刘智恩,西北工业大学出版社20033. 《材料科学基础》,石德珂,西安交通大学出版社,20004. 《材料科学基础》,潘金生,仝健民,清华大学出版社,1998《材料科学基础》复习纲要重要概念-键合、工程材料-晶体、非晶体、各向异性-点阵、晶体结构、晶胞、晶系、布拉菲点阵、晶面指数、晶向指数、晶面族、晶向族-晶格常数、晶胞原子数、配位数、致密度、间隙-堆垛、密排面、密排方向、堆垛次序、堆垛方向-缺陷、点缺陷、刃位错、螺位错、混合位错-柏氏矢量、滑移矢量-位错密度-滑移、攀移、交滑移、交割、割阶、扭折、塞积-位错应力场、应变能、线张力、位错线上的力-位错增殖、位错源-全位错、不全位错、堆垛层错、位错反应-晶界、相界、界面能、大角度晶界、小角度晶界、孪晶界-相、固溶体、置换固溶体、间隙固溶体-金属间化合物、玻璃相-凝固、结晶、短程有序、长程有序-结构起伏(相起伏)、能量起伏、成分起伏-过冷度、形核过冷度、动态过冷度、临界过冷度、有效形核过冷度-均匀形核、非均匀形核、晶核、临界晶核、临界形核功、形核率-光滑界面、粗糙界面、垂直长大、横向长大、温度梯度、树枝状-平衡转变(结晶)、非平衡转变(结晶)、正常凝固-匀晶、共晶、包晶、共析、包析、脱溶转变-平衡分配系数、有效分配系数-微观偏析(枝晶偏析)、宏观偏析-亚共晶、共晶、过共晶、伪共晶、离异共晶、非平衡共晶、包晶转变不完全性-铁素体、奥氏体、珠光体、莱氏体、渗碳体、工业纯铁、钢、铸铁-液相线、固相线、液相面、固相面、中间面、液相平均成分线、固相平均成分线-浓度三角形-垂直截面、水平界面、投影图-扩散、空位扩散、间隙扩散、稳态扩散、非稳态扩散-扩散系数、扩散激活能、扩散通量、迁移率-上坡扩散、反应扩散-滑移、滑移线、滑移带、滑移方向、滑移面、滑移系、临界分切应力、取向因子、吕德斯带-柯氏气团、屈服、应变时效-细晶强化、固溶强化、复相强化、弥散强化、加工硬化-纤维组织、带状组织、流线、位错胞、变形亚结构、织构-回复、再结晶、晶粒长大-低、中、高温回复,多边化,去应力退火-再结晶温度、再结晶退火-临界变形度、热蚀沟、再结晶图-动态回复、动态再结晶,热变形-复合材料、基体、增强体、界面各章知识要点一、工程材料中的原子排列§1.1 原子键合• 原子键合的种类、特点、典型例子• 工程材料的分类及其主要键合类型• 键合的多重性§1.2 原子的规则排列• 晶体的特点、晶体结构、点阵• 晶系、布拉菲点阵• 晶面指数、晶向指数(标定和作图)及其特点,晶面族、晶向族• 晶面间距• 典型金属结构(fcc、bcc、hcp)(晶胞原子数、点阵常数、配位数、致密度)(间隙种类及其特点)(堆垛方式)• 多晶型性、同素异晶转变• 陶瓷晶体结构(离子键晶体、共价键晶体)(结构规则、不等径刚球密堆原理)§1.3 原子的不规则排列• 缺陷的种类• 点缺陷的种类• 空位的平衡浓度• 点缺陷对晶体性能的影响• 位错的类型、特点• 柏氏矢量(柏氏回路)• 位错的运动方式、特点• 位错的力学性能(应力场、畸变能、位错线上的力、线张力)• 位错的交互作用(位错与点、线、面缺陷的交互作用)• 位错增殖• 实际晶体中的位错(全位错、不全位错、单位位错、部分位错、堆垛层错、弗兰克位错、肖克来位错)• 位错反应• 面缺陷(类型及其结构模型、界面能、界面的特点)二、固体中的相结构§ 2.1 固溶体-固溶体的概念、分类-影响固溶度的因素-固溶体的均匀性-固溶体的性能§ 2.2 金属间化合物-化合物的概念、分类-化合物的性能§ 2.3 陶瓷晶体相-陶瓷的概念、特征§ 2.4 玻璃相-陶瓷的概念、形成条件三、凝固§ 3.1 金属结晶的基本规律-微观规律(形核、长大、)-宏观规律(过冷)§ 3.2 金属结晶的基本条件-热力学条件(ΔG < 0、ΔT )-动力学条件(形核:结构条件、能量条件、成分条件)(长大:速度条件)§ 3.3 晶核的形成-形核的方式(均匀形核、非均匀形核)-结晶时的体系能量变化-形核的驱动力和阻力-临界晶核的概念-临界晶核半径及其计算-临界形核功及其计算-形核率(概念、影响因素、特点)-两种形核方式的比较§3.4 晶体的长大-液固界面的微观结构-晶体的长大机制-温度梯度-晶体长大的形态§3.6 凝固理论的应用-铸锭晶粒组织及其控制-单晶体的制备-定向凝固-非晶合金的制备-微晶合金的制备四、相图§ 4.1 相、相平衡及相图制作-相的定义-相平衡的定义-成分的表示方法(质量分数、摩尔分数)-相图的制作方法§ 4.2 匀晶相图-相图分析-成分变化(平衡、非平衡)(微观偏析、宏观偏析)-成分过冷(概念、形成原因)-固溶体形貌§ 4.3 共晶相图-相图分析-共晶转变特点-典型合金的结晶过程(平衡、非平衡)-成分变化(平衡、非平衡)-共晶形成机理(形核机理、长大机理)-共晶体形貌特征(平衡、非平衡)-杠杆定律计算(相组成、组织组成)§ 4.4 包晶相图-相图分析-包晶转变特点-典型合金的结晶过程(平衡、非平衡)-成分变化(平衡、非平衡)-包晶形成机理-杠杆定律计算(相组成、组织组成)§ 4.5 其它相图-相图分析方法、步骤-典型合金的结晶过程(平衡、非平衡)-成分变化(平衡、非平衡)-杠杆定律计算(相组成、组织组成)§ 4.6 Fe-C相图-相图分析-典型合金的平衡结晶过程-成分变化-典型合金的名称-杠杆定律计算(相组成、组织组成)§ 4.8 铸锭组织与偏析-偏析的类型§ 4.9 三元合金相图-成分表示法(浓度三角形)-三元匀晶相图(立体图、投影图)-三元匀晶相图(垂直截面、水平截面)-三元匀晶相图平衡结晶过程-简单三元共晶相图(立体图、投影图)-简单三元共晶相图(垂直截面、水平截面)-简单三元共晶相图平衡结晶过程五、材料中的扩散§5.1 扩散定律及其应用-扩散第一定律及其应用条件-扩散第二定律及其应用条件§ 5.2 扩散的微观机理-扩散的微观机理-原子热运动对扩散的影响-晶态、非晶态化合物中的扩散§ 5.3 扩散的热力学理论-扩散的驱动力-上坡扩散(概念、诱因)-扩散系数§ 5.4 反应扩散-反应扩散(概念、特点)陶瓷的概念、特征§ 5.5 扩散的影响因素-影响因素及其机理六、塑性变形§ 6.1 应力-应变曲线-工程应力应变曲线、真应力应变曲线及二者差别-强度及塑性指标,硬化系数§ 6.2 单晶体的塑性变形-滑移现象(滑移线、滑移带、滑移特征)-滑移系-临界分切应力-滑移的微观机理-晶体的转动、多滑移、交滑移及滑移线形貌-孪生的概念、特点§ 6.3 多晶体的塑性变形-位向差及晶界对塑变的影响-细晶强化机理、特征-霍尔-配奇公式§6.4 合金的塑性变形-固溶强化机理-屈服及应变时效-复相强化机理及特征-弥散强化机理§ 6.5 冷变形金属的组织和性能-组织变化(显微组织、变形亚结构、变形织构)-能量变化(内应力、畸变能)-力学性能(加工硬化)-物理、化学性能变化七、回复与再结晶§ 7.1 加热时的变化-显微组织变化-能量变化-力学性能变化-物理、化学性能变化§ 7.2 回复-回复机制-回复热力学-回复动力学-回复应用§ 7.3 再结晶-再结晶机制(形核机制、长大机制)-再结晶热力学-再结晶动力学-再结晶温度及其影响因素-再结晶组织及其影响因素§ 7.4 再结晶后晶粒长大-长大方式-晶粒长大(特征、热力学、动力学)-晶粒长大影响因素-再结晶应用八、固态相变-固态相变的分类九、复合效应与界面-复合材料定义、分类-复合材料的构成、各部分的作用-复合效应-界面结合种类热处理改变钢的性能的原因是因为采用不同的加热、保温、冷却方式使钢内部结构发生改变,从而获得所需性能。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2)ΔX>0.4~0.5,倾向于形成稳定的化合物,其电负性差值越大
,固溶体中固溶度越小。
7
二、影响置换固溶体固溶度的因素
3.电子浓度因素(原子价因素) 电子浓度是合金中价电子数目与原子数目的比值
e/aV(100x)ux 100
例 溶剂IB
不同溶质的溶解度(at%)
4周期Cu Zn(IIB) Ga(IIIA)Ge(IVA) As(VA)
构 1、Cu3Au型
14
四、长程有序固溶体(超结构)在fcc固溶体中形成超结构
2、CuAuI型
Cu Au
15
四、长程有序固溶体(超结构)在fcc固溶体中形成超结
构 2、CuAuII型
16
四、长程有序固溶体(超结构)在fcc固溶体中形成超结
构 4、CuPt型
17
四、长程有序固溶体(超结构) 在体心立方中形成超结
③ 温度低于某一温度下;
④ 冷却速度;
⑤
塑性变形使合金有序度下降。
22
4.长程有序参数
用来衡量有序度
定义
SPAXA PBXB 1XA 1XB
其 中 : PA、PB:表示A、B原子出现在正确位置上的几 率
XA、XB:A或B原子的摩尔分数 S=1,PA=PB=1,完全有序 S=0,PA=XA,PB=XB,完全无序
固体中的相结构分 类和形成规律
固体中的相结构分类:
合金相可归纳为 ·固溶体
·中间相
陶瓷晶体相
玻璃相
分子相
2
固溶体
一、固溶体的类型
固溶体 按溶质原子所占 间 置位 隙 换置 固 式溶 固:有 体 溶 按 按 限 体原 固 固子 溶 溶排 度 体 有 无 列 分限 限 的固 固 程溶 溶 序 有 无体 体 性 序 序分 固 固溶 溶 按基体类次 端 型级 际固 固溶 溶:以体 体金初属极间 :以 固化纯 溶合金 体物属 固 为为 溶 基基 体 的的固溶体
由两种电负性差值较大的元素按通常的化学价 规律形成的化合物,其稳定性与两组元的电负性差值大小有
关,电负性差值越大,稳定性越高,愈接近离子键合,反之趋向于金属 键合。正常价化合物包括从离子键、共价键过渡到金属键为主的一系列 化合物,通常具有较高的强度和脆性,固溶度范围极小,在相图上为一 条垂直线。
26
1.填隙型(填隙化合物) 在过渡族金属与H、B、C、N等原子半径甚小的非金属
元素之间形成。 ① 简单填隙相 ·γX/γM<0.59 γX、γM:非金属(X)与金属(M)的原
子半径。 ·具有比较简单的晶体结构,多数为面心立方和密排六
方,少数具有体心立方和简单六方结构。
·分子式一般为M4X、M2X、MX和MX2 ·成分可以在一定范围内变化
3
4
5
二、影响置换固溶体固溶度的因素
1.原子尺寸因素:溶质与溶剂原子半径的相对差小于 14~15%,才可能形成溶解度较大甚至无限溶解的固 溶体。
6
二、影响置换固溶体固溶度的因素 2.化学亲和力(电负性因素) · 电负性;原子吸引电子形成负离子的倾向,以电负性因素来衡量
化学亲和力。 1) 电负性差值ΔX<0.4~0.5时,有利于形成固溶体,随电负差值增
0 完全无序状态
0 短程有序
0原子偏聚
11
12
四、长程有序固溶体(超结构)
1.主要类型
1) 在fcc固溶体中形成超结构 1 Cu3Au型 2 CuAuI型 3 CuAuII型 4 CuPt型
2)在体心立方中形成超结构 1 CuZn型 2 Fe3Al型
3)在密排六方固溶体中形成超结构
13
四、长程有序固溶体(超结构)在fcc固溶体中形成超结
23
5.有序化对性能的影响: ① 通常提高硬度、强度、降低塑性——有序
强化; ② 电阻降低; ③ 影响铁磁性; ④ 影响弹性性质
24
五、固溶体的性质
1.固溶强化:固溶体的强度总是比组成它的纯组元高 ,且随溶质原子浓度增加,强度也增加。
2.改变物理、化学性质 3.改变点阵常数
25
§2 金属间化合物(中间相) 一、正常价化合物:源自38%20% 12%
7%
5周期Ag Cd(IIB)In(IIIA)Sn(IVA) Sb(VA)
42%
20% 12%
7%
固溶体中的电子浓度有其极限值。
8
二、影响置换固溶体固溶度的因素
4.晶体结构因素
晶体结构相同是组元间形成无限固溶体的必 要条件。
形成有限固溶体时,溶质元素与溶剂的结构 类型相同,则溶解度通常也较不同结构时为 大。
二、电子化合物(Hume-Rothery相)
合金系
中间相 电子浓度e/a 晶体结构
Cu-Zn系 β(CuZn) 3/2
体心立方
ΓCu5Zn8) 21/13
复杂立方
ε(CuZn3) 7/4
密排六方
Cu-Al系
β(Cu3Al) 3/2
体心立方
γ(Cu32Al19) 21/13 复杂立方
ε(Cu5Al3) 7/4
9
机械合金化(MA,Mechanical Alloy)
10
三、固溶体的微观不均匀性
1.无序分布
eAB
eAAeBB 2
2.偏聚状态
eABeAA2eBB
3.短程有序
eAB
eAAeBB 2
·短程序参数
1 PA
PA:固溶体中B原子周围出x A 现A
原子的几率
xA:固溶体中A原子的摩尔分数
构 1 CuZn型
18
四、长程有序固溶体(超结构) 在体心立方中形成超结
构 2、Fe3Al型
19
四、长程有序固溶体(超结构) 3)在密排六方固溶体
中形成超结构
20
四、长程有序固溶体(超结构) 2.反相畴与反相畴界
21
3. 影响有序化的因素:
① eAB<(eAA+eBB/2); ② 具有相当于一定化学式的成分;
28
29
30
三、原子尺寸因素化合物 )
1.填隙型(填隙化合物
② 复杂填隙相
·γX/γM>0.59 晶体结构很复杂 · 在碳钢和合金钢中复杂填隙相的结构主要有
M3C、M23Co和M6C三相类型。 例:Fe3C、Mn3C、Cr7C3、Cr23C6、Fe3W3C、
密排六方
Cu-Sn系
β(Cu5Sn) 3/2
体心立方
γ(Cu31Sn8) 21/13
复杂立方
ε(Cu3Sn) 7/4
密排六方
这类化合物的结构稳定性主要取决于电子浓度因素。在相图上占有一 定成分范围,结合性质为金属键,有明显的金属特性。
27
三、原子尺寸因素化合物
当两种元素形成金属间化合物时,如果它们之间的原 子半径差别很大时,便形成原子尺寸因素化合物。
