初中化学方程式书写练习题[1]
初中化学书写化学方程式实验题专题训练含答案

初中化学书写化学方程式实验题专题训练含答案姓名:__________ 班级:__________考号:__________一、实验题(共10题)) 中的一种。
根据下图回答问题:1、实验室制取 X 气体,该气体为氢气、氧气、氯气 (Cl2(1) 用高锰酸钾制取并收集氧气:①该反应的化学方程式为 _______ 。
②用 D 装置收集氧气,检验收集满的方法 _______ 。
③改用 E 装置 ( 如图放置 ) 收集氧气,气体应从 _______ 端 ( 填“a” 或“b”) 通入。
(2) ①实验室制取并收集氢气,可选用发生装置 _______ ( 填字母 ) 和收集装置 F 的组合;②实验室常用二氧化锰粉末和浓盐酸在加热条件下制取氯气,可选用的发生装置为 __ ( 填字母 ) 。
2、根据下列装置图,回答问题:(1) 仪器a 的名称是___________ 。
(2) 实验室某小组选取B 装置作为发生装置制取氧气,则反应的化学方程式为___________ 。
(3) 若选取F 装置,采用排空气法收集氧气,氧气应从___________ 端( 填“m” 或“n”) 通入。
3、化学是一门以实验为基础的科学。
根据下图回答问题。
( 1 )仪器 a 的名称是 ___________ 。
( 2 )实验室制取氢气的化学反应方程式为 ______ ,若要获得平稳气流,应选择的发生装置是 ________ ,用 F 装置收集氢气,当观察到 ________ 的现象时再开始收集。
( 3 )写出实验室用 C 装置制取氧气的化学方程式 _______ ,用装置 D 收集氧气时,其验满的方法是 _______ 。
( 4 )甲烷是一种没有颜色、没有气味、难溶于水、密度比空气小的气体。
实验室常用加热碱石灰(氧化钙和氢氧化钠固体的混合物)和醋酸钠固体制取甲烷气体,应选用的发生装置是 ________ (填标号,下同),若用 G 装置收集时,则气体要从 _______ 端通入。
初中化学方程式书写专题练习

化学方程式的书写练习一、化合反应:1、镁条在氧气中燃烧:2、红磷在氧气中燃烧:3、铁在氧气中燃烧:4、二氧化碳在灼热的碳中生成一氧化碳:5、往水中通入二氧化碳,生成碳酸:6、铁在氧气中点燃生成四氧化三铁:7、磷在氧气中点燃生成五氧化二磷:8、铜在空气中加热生成氧化铜:9、硫在氧气中点燃生成二氧化硫:10、二氧化硫加水生成亚硫酸:11、二氧化硫在空气中氧化为三氧化硫:12、三氧化硫通入水中生成硫酸:13、无水硫酸铜粉末中加水中生成五水硫酸铜:14、氢气在空气中点燃生成水:15、氢气在氯气中点燃生成氯化氢气体:16、氧化钙加水生成氢氧化钙:二、分解反应:17、在二氧化锰的催化作用下加热氯酸钾,生成氯化钾和氧气:18、加热高锰酸钾,生成锰酸钾、二氧化锰和氧气:19、电解水,生成氢气和氧气:20、在二氧化锰的催化作用下分解双氧水,生成水和氧气:21、加热碳酸,分解为二氧化碳和水:22、碳酸钙高温生成氧化钙和二氧化碳:23、加热五水硫酸铜生成硫酸铜和水:24、碳酸氢钠加热生成碳酸钠、水和二氧化碳:25、加热碱式碳酸铜,生成氧化铜、水和二氧化碳:三、置换反应:(1)金属和酸反应,置换出氢气:27、铁和稀硫酸反应,生成硫酸亚铁和氢气:29、镁和稀硫酸反应,生成硫酸镁和氢气:30、铝和稀硫酸反应,生成硫酸铝和氢气:32、锌和稀盐酸反应,生成氯化锌和氢气:(2)金属和盐溶液反应,置换出金属:34、铁和硫酸铜反应,生成硫酸亚铁和铜:38、铜和硝酸银反应,生成硝酸铜和银:四、复分解反应:(1)生成硫酸钡白色沉淀:53、氯化钡和稀硫酸反应,生成硫酸钡沉淀和稀盐酸:54、氯化钡和硫酸铜反应,生成硫酸钡沉淀和氯化铜:55、氯化钡和硫酸钠反应,生成硫酸钡沉淀和氯化钠:56、氢氧化钡和稀硫酸反应,生成硫酸钡沉淀和水:57、氢氧化钡和硫酸铜反应,生成硫酸钡沉淀和氢氧化铜沉淀:58、氢氧化钡和硫酸钠反应,生成硫酸钡沉淀和氢氧化钠:59、硝酸钡和稀硫酸反应,生成硫酸钡沉淀和稀硝酸:60、硝酸钡和硫酸铜反应,生成硫酸钡沉淀和硝酸铜:61、硝酸钡和硫酸钠反应,生成硫酸钡沉淀和硝酸钠:(2)生成氯化银白色沉淀:62、硝酸银和稀盐酸反应,生成氯化银沉淀和稀硝酸:63、硝酸银和氯化钠反应,生成氯化银沉淀和硝酸钠:67、硝酸银和氯化钾反应,生成氯化银沉淀和硝酸钾:68、硝酸银和氯化钙反应,生成氯化银和硝酸钙:69、硝酸银和氯化钡反应,生成氯化银沉淀和硝酸钡:(3)生成碳酸钙白色沉淀:70、氢氧化钙和二氧化碳反应,生成碳酸钙沉淀和水:71、氢氧化钙和碳酸钠反应,生成碳酸钙沉淀和氢氧化钠:72、氯化钙和碳酸钠反应,生成碳酸钙沉淀和氯化钠:(4)生成碳酸钡白色沉淀:74、氢氧化钡和二氧化碳反应,生成碳酸钡沉淀和水:75、氢氧化钡和碳酸钠反应,生成碳酸钡沉淀和氢氧化钠:76、氯化钡和碳酸钠反应,生成碳酸钡沉淀和氯化钠:77、硝酸钡和碳酸钠反应,生成碳酸钡沉淀和硝酸钠:(5)生成氢氧化铜蓝色沉淀:78、氢氧化钠和硫酸铜反应,生成氢氧化铜沉淀和硫酸钠:83、氢氧化钾和氯化铜反应,生成氢氧化铜沉淀和氯化钾:84、氢氧化钙和硫酸铜反应,生成氢氧化铜沉淀和硫酸钙:85、氢氧化钙和氯化铜反应,生成氢氧化铜沉淀和氯化钙:87、氢氧化钡和硫酸铜反应,生成氢氧化铜沉淀和硫酸钡沉淀:88、氢氧化钡和氯化铜反应,生成氢氧化铜沉淀和氯化钡:(6)生成氢氧化铁红褐色沉淀:90、氢氧化钠和氯化铁反应,生成氢氧化铁沉淀和氯化钠:91、氢氧化钾和氯化铁反应,生成氢氧化铁沉淀和氯化钾:92、氢氧化钙和氯化铁反应,生成氢氧化铁沉淀和氯化钙:94、氢氧化钠和硫酸铁反应,生成氢氧化铁沉淀和硫酸钠:96、氢氧化钙和硫酸铁反应,生成氢氧化铁沉淀和硫酸钙:97、氢氧化钡和硫酸铁反应,生成氢氧化铁沉淀和硫酸钡沉淀:(7)生成二氧化碳气体:98、碳酸钙和稀盐酸反应,生成氯化钙、水和二氧化碳:99、碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳:101、碳酸钡和稀盐酸反应生,成氯化钡、水和二氧化碳:102、碳酸氢钠和稀盐酸反应,生成氯化钠、水和二氧化碳:(8)酸碱中和反应,生成水:103、氢氧化钠和稀盐酸反应,生成氯化钠和水:104、氢氧化钙和稀盐酸反应生成氯化钙和水:106、氢氧化钡和稀盐酸反应生成氯化钡和水:108、氢氧化钠和稀硫酸反应,生成硫酸钠和水:110、氢氧化钙和稀硫酸反应,生成硫酸钙和水:111、氢氧化钡和稀硫酸反应,生成硫酸钡和水:(9)其他112、氢氧化钙和二氧化碳反应,生成碳酸钙沉淀和水113、氢氧化钠和二氧化碳反应(变质),生成碳酸钠和水:114、氢氧化钠和二氧化硫反应生成亚硫酸钠和水:115、氧化铜和稀盐酸反应,生成氯化铜和水:116、氧化铜和稀硫酸反应,生成硫酸铜和水:117、氧化铁和稀盐酸反应,生成氯化铁和水:118、氧化铁和稀硫酸反应,生成硫酸铁和水:119、氧化铝和稀盐酸反应,生成氯化铝和水:五、氧化还原反应:121、氢气还原氧化铜,加热,生成铜和水:122、碳还原氧化铜,高温,生成铜和二氧化碳:123、一氧化碳还原氧化铜,加热,生成铜和二氧化碳:124、一氧化碳还原氧化铁,高温,生成铁和二氧化碳:。
第五单元课题2化学方程式的书写同步测试卷(一)-2021-2022学年九年级化学人教版上册

第五单元 化学方程式的书写 测试卷(一)试卷满分:50分 考试时间:40分钟 题号 一 二 总分 得分率 得分一.选择题(共10小题,满分20分,每小题2分)1.(★)下列有关现象的描述和化学方程式均正确的是( ) A .碳在氧气中燃烧发出白光22C+O =CO B .铁丝在氧气中剧烈燃烧,火星四射2234Fe+3O 2Fe O 点燃C .硫在空气中燃烧发出淡蓝色火焰22 S+ O OS 点燃D .磷在空气中燃烧产生大量的白雾225 2P+ 5O2P O 点燃2.(★)下列化学方程式书写正确的是( ) A .4P + 5O 2↑点燃2P 2O 5 B .4Fe + 3O 2点燃2Fe 2O 3 C .Cu + AgNO 3CuNO 3+ AgD .Mg + 2HClMgCl 2+ H 2↑3.(★★)下列化学方程式中符合题意且书写正确的是( ) A .军事上利用镁作燃烧弹:Mg+O 2点燃MgO 2B .生活中利用氢气作燃料:H 2+O 2点燃H 2OC .古代利用湿铁炼铜法制铜:Fe+CuSO 4═Cu↓+FeSO 4D .工业上用石灰石制生石灰:CaCO 3高温CO 2↑+CaO4.(★)化学方程式是重要的化学用语,一定要正确书写,下列化学方程式书写正确的是( ) A .KClO 3═KCl+O 2↑ B .Mg+O 2═MgO 2C .CO+CuO═Cu+CO 2↑D .Zn+H 2SO 4═ZnSO 4+H 2↑5.(★★)下列化学方程式中符合题意且书写正确的是( ) A .正常雨水偏弱酸性原因:2224SO H O=H SO + B .用稀硫酸除铁锈:2442FeO H SO =FeSO H O ++C .用小苏打治疗胃酸过多症:322NaHCO HCl=NaCl CO H O ++↑+D .工业上用熟石灰制取烧碱:()2332=Ca(OH)2NaNO Ca NO 2NaOH ++6.(★)人在剧烈运动后,血液中会产生较多的乳酸(化学式为C 3H 6O 3),使肌肉酸痛。
初二化学式的练习题

初二化学式的练习题化学式是化学物质的一种表示方式,通过化学式可以简明地表示出化学物质的组成元素和原子数目。
初二学生在学习化学时,练习化学式的题目可以帮助他们加深对化学式的理解和掌握。
下面是一些初二化学式的练习题,供学生进行练习:1. 根据元素符号填写化学式的正确名称:a) NaCl:_______b) H2O:________c) CO2:________d) Fe2O3:________e) NH3:________2. 根据化学名字写出相应的化学式:a) 氯化钠:_______b) 二氧化碳:_______c) 水:________d) 亚硝酸:_______e) 硫酸:_______3. 化学式求摩尔质量:a) H2O的摩尔质量是多少?b) CO2的摩尔质量是多少?c) NaCl的摩尔质量是多少?d) Ca(OH)2的摩尔质量是多少?e) Al2(SO4)3的摩尔质量是多少?4. 化学式求元素的摩尔数:a) 在H2O中,氢元素的摩尔数是多少?b) 在CO2中,碳元素的摩尔数是多少?c) 在CaCl2中,钙元素的摩尔数是多少?d) 在H2SO4中,氢元素的摩尔数是多少?e) 在Al2O3中,铝元素的摩尔数是多少?5. 化学式求物质的摩尔比:a) C2H5OH中碳、氢、氧的摩尔比分别是多少?b) NH4NO3中氮、氢、氧的摩尔比分别是多少?c) Al(OH)3中铝、氢、氧的摩尔比分别是多少?d) K2Cr2O7中钾、铬、氧的摩尔比分别是多少?e) MgSO4·7H2O中镁、硫、氧、氢的摩尔比分别是多少?通过练习化学式的题目,初二学生可以加深对化学式的理解,从而提高化学知识的掌握程度。
希望以上练习题能对学生们有所帮助。
初中化学九年级 酸碱盐化学性质 方程式书写练习(含答案)

专题 酸碱盐化学性质——化学方程式的书写练习(至少写两遍)作业前的知识点识记1、巧用手掌识记酸碱盐的化学性质2、熟悉复分解反应及其发生的条件。
(1)复分解反应是两种化合物相互交换成分,生成另外两种化合物的反应呢。
AB+CD=AD+CB (双交换,价不变。
所有元素化合价不变)(2)复分解反应发生的条件是:①有酸可不溶,无酸必须溶。
②生成物中有______、______或______。
只有满足其一,复分解反应才能发生。
3、配平。
一般可以根据生成物中的气体,水,沉淀来配平。
4、熟记常见物质的溶解性(1)物质溶解性规律(口诀)碱溶钾钠钡钙铵,钾钠铵盐均可溶;盐酸盐不溶AgCl ;硫酸盐不溶BaSO 4;碳酸盐除钾钠铵外均不溶。
(2)初中化学酸碱盐溶解性初中化学常见酸(盐酸、硫酸、硝酸)均可溶;初中化学常见不溶性碱:Mg(OH)2、 Al(OH)3(白色沉淀)、Cu(OH)2(蓝色絮状沉淀);Fe(OH)3(红褐色沉淀)初中化学常见不溶性盐:AgCl 、BaSO 4(白色沉淀,不溶于酸) BaCO 3、CaCO 3(白色沉淀,可溶于酸) 初中化学常见的气体:CO 2、NH 3作业:完成下列方程式,学会描述实验现象。
一、酸的化学性质1、与酸碱指示剂反应:酸溶液能使紫色石蕊溶液____________;能使无色酚酞溶液_____________。
2、与活泼金属的反应 活泼金属+酸=盐+氢气(第八单元所学,满足金属活动性顺序,属于置换反应)(1)镁与盐酸的反应__________________________;镁与稀硫酸的反应___________________________。
(2)锌与盐酸的反应__________________________;锌与稀硫酸的反应___________________________。
(3)铁与盐酸的反应__________________________;铁与稀硫酸的反应___________________________。
化学方程式练习大全含答案

初中化学方程式大全1.镁在空气中燃烧:2.铁在氧气中燃烧:3.铜在空气中受热:4.铝在氧气中燃烧:5.氢气在空气中燃烧:6.红磷在空气中燃烧:7.硫粉在空气中燃烧:8.碳在充足的氧气中燃烧:9.碳在不充的氧气中燃烧:10.一氧化碳在氧气中燃烧:11.二氧化硫和氧气:12.二氧化碳和水反应:13.二氧化硫和水反应:14.三氧化硫和水反应:15.生石灰溶于水:16.二氧化碳通过灼热碳层:17.实验室用双氧水制氧气:18.加热高锰酸钾:19.水在直流电的作用下分解:20.碳酸不稳定易分解:21.高温煅烧石灰石:22.锌和稀硫酸23.铁和稀硫酸24.镁和稀硫酸25.铝和稀硫酸26.锌和稀盐酸27.铁和稀盐酸28.镁和稀盐酸29.铝和稀盐酸30.铁和硫酸铜溶液反应:31.锌和硫酸铜溶液反应:32.铜和硝酸银溶液反应:33.氧化铁和稀盐酸反应:34.氧化铁和稀硫酸反应:35.氧化铜和稀盐酸反应:36.氧化铜和稀硫酸反应:37.盐酸和烧碱起反应:38.盐酸和氢氧化钙反应:39.氢氧化铝药物治疗胃酸过多:40.硫酸和烧碱反应:41.硫酸和氢氧化钙反应:42.硝酸和烧碱反应:43.大理石与稀盐酸反应:44.碳酸钠与稀盐酸反应:45.碳酸氢钠与稀盐酸反应:46.硫酸和碳酸钠反应:47.硫酸和大理石反应:48.氢氧化钠与硫酸铜:49.氢氧化钙与硫酸铜:50.氢氧化钙与碳酸钠:51.氯化钙与碳酸钠:52.二氧化碳通过澄清石灰水(检验二氧化碳):53.氢氧化钠和二氧化碳反应(除去二氧化碳):54.苛性钠吸收二氧化硫气体:55.消石灰吸收二氧化硫:56.甲烷在空气中燃烧:57.一氧化碳还原氧化铁:58.一氧化碳还原四氧化三铁:59.植物的呼吸作用:60.植物的光合作用:初中化学方程式大全一、化合反应:(一)金属+氧气——金属氧化物氧气——金属氧化物1.镁在空气中燃烧:2Mg+O 22MgO 2.铁在氧气中燃烧:3Fe+2O 2 Fe3O 4 3.铜在空气中受热:2Cu+O 22CuO 4.铝在氧气中燃烧:4Al+3O 22Al 2O 3(二)非金属+氧气——非金属氧化物氧气——非金属氧化物5.氢气在空气中燃烧:2H 2+O 2 2H2O 6.红磷在空气中燃烧:4P+5O 2 2P 2O 5 7.硫粉在空气中燃烧:.硫粉在空气中燃烧: S+O 2SO 2 8.碳在充足的氧气中燃烧:C+O 2 CO2 9.碳在不充的氧气中燃烧:2C+O 22CO (三)化合物+氧气氧气10.一氧化碳在氧气中燃烧:2CO+O 22CO 2 11.二氧化硫和氧气:2SO 2+O 2 2SO3 (四)非金属氧化物+水———酸水———酸12.二氧化碳和水反应:CO 2+H 2O==H 2CO 3 13.二氧化硫和水反应:SO 2+H 2O==H 2SO 3 14.三氧化硫和水反应:SO 3+H 2O==H 2SO 4(五)金属氧化物+水———碱 15.生石灰溶于水:CaO+H 2O==Ca(OH)2 (六)其他 16.二氧化碳通过灼热碳层:.二氧化碳通过灼热碳层: C+CO 2 2CO二、分解反应二、分解反应17.实验室用双氧水制氧气:2H 2O 2 2H 2O+O 2↑ 18.加热高锰酸钾:2KMnO 4K 2MnO 4+MnO 2+O 2↑19.水在直流电的作用下分解:2H 2O 2H 2↑+O 2↑ 20.碳酸不稳定易分解:H 2CO 3H 2O+CO 2↑21.高温煅烧石灰石:CaCO 3CaO+CO 2↑三、置换反应三、置换反应 (一)金属(一)金属 + 酸 ———— 盐 + 氢气氢气22.锌和稀硫酸Zn+H 2SO 4==ZnSO 4+H 2↑ 23.铁和稀硫酸Fe+H 2SO 4==FeSO 4+H 2↑ 24.镁和稀硫酸Mg+H 2SO 4==MgSO 4+H 2↑ 25.铝和稀硫酸2Al+3H 2SO 4==Al 2(SO 4)3+3H 2↑ 26.锌和稀盐酸Zn+2HCl==ZnCl 2+H 2↑ 27.铁和稀盐酸Fe+2HCl==FeCl 2+H 2↑ 28.镁和稀盐酸Mg+2HCl==MgCl 2+H 2↑ 29.铝和稀盐酸2Al+6HCl==2AlCl 3+3H 2↑ (二)金属单质(二)金属单质 + 盐(溶液)——另一种金属盐(溶液)——另一种金属 + 另一种盐另一种盐30.铁和硫酸铜溶液反应:Fe+CuSO 4==FeSO 4+Cu 31.锌和硫酸铜溶液反应:Zn+CuSO 4==ZnSO 4+Cu 32.铜和硝酸银溶液反应:Cu+2AgNO 3== Cu(NO3)2+2Ag 四、复分解反应四、复分解反应 (一)金属氧化物(一)金属氧化物 + 酸 —————— 盐 + 水 33.氧化铁和稀盐酸反应:Fe 2O 3+6HCl==2FeCl 3+3H 2O 34.氧化铁和稀硫酸反应:Fe 2O 3+3H 2SO 4==Fe 2(SO 4)3+3H 2O 35.氧化铜和稀盐酸反应:CuO+2HCl==CuCl 2+H 2O 36.氧化铜和稀硫酸反应:CuO+H 2SO 4==CuSO 4+H 2O ( (二)酸二)酸二)酸 + 碱 —————— 盐 + 水37.盐酸和烧碱起反应:HCl+NaOH==NaCl+H 2O 38.盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl 2+2H 2O 39.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl 3+3H 2O 40.硫酸和烧碱反应:H 2SO 4+2NaOH==Na 2SO 4+2H 2O 41.硫酸和氢氧化钙反应:H 2SO 4+Ca(OH)2==CaSO 4+2H 2O 42.硝酸和烧碱反应:HNO 3+NaOH==NaNO 3+H 2O (三)酸(三)酸 + 盐 —————— 另一种酸另一种酸 + 另一种盐另一种盐43.大理石与稀盐酸反应:CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑44.碳酸钠与稀盐酸反应: Na2CO 3+2HCl==2NaCl+H 2O+CO 2↑ 45.碳酸氢钠与稀盐酸反应: NaHCO3+HCl==NaCl+H 2O+CO 2↑ 46.硫酸和碳酸钠反应:Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ 47.硫酸和大理石反应:CaCO 3+H 2SO 4 ==CaSO 4+H 2O+CO 2↑ (四)碱(四)碱 + 盐 —————— 另一种碱另一种碱 + 另一种盐另一种盐48.氢氧化钠与硫酸铜:2NaOH+CuSO 4==Cu(OH)2↓+Na 2SO 4 49.氢氧化钙与硫酸铜:Ca(OH)2+CuSO 4==Cu(OH)2↓+↓+CaSOCaSO 4 50.氢氧化钙与碳酸钠:Ca(OH)2+Na 2CO 3==CaCO 3↓+2NaOH (五)盐(五)盐 + 盐 —————— 两种新盐两种新盐 51.氯化钙与碳酸钠:CaCl 2+Na 2CO 3==CaCO 3↓+2NaCl 五、其他五、其他(一)非金属氧化物(一)非金属氧化物 + 碱 —————— 盐 + 水52.二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO 2==CaCO 3↓+H 2O 53.氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO 2==Na 2CO 3+H 2O 54.苛性钠吸收二氧化硫气体:2NaOH+SO 2==Na 2SO 3+H 2O 55.消石灰吸收二氧化硫:Ca(OH)2+SO 2==CaSO 3↓+H 2O (二)其他(二)其他56.甲烷在空气中燃烧:CH 4+2O 2CO 2+2H 2O 57.一氧化碳还原氧化铁:3CO+Fe 2O 3 2Fe+3CO 258.一氧化碳还原四氧化三铁:4CO+Fe 3O 4 3Fe+4CO 2 59.植物的呼吸作用:C 6H 12O 6+6O 2==6CO 2+6H 2O 60.植物的光合作用:6CO 2+6H 2O==C 6H 12O 6+6O 2。
化学方程式练习题(含答案)经典1
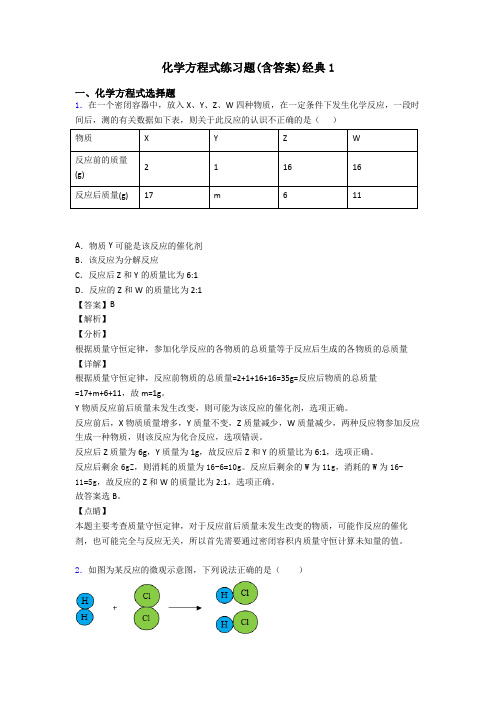
即 W 中不含有氧元素,故 C 正确;
D、W 中碳、氢元素质量比= 选C
,故 D 错误。故
4.图反映了某个化学反应各物质质量与时间的关系。下列描述正确的是
A.该反应是化合反应 B.甲的相对分子质量大于乙 C.丙是反应物,甲和乙是生成物 D.t1 时,丙的质量一定等于甲、乙的质量之和 【答案】C 【解析】 【分析】 【详解】 A、由图知从 0 到 t1 时间内丙物质逐渐减少,甲乙两物质逐渐增加。所以,丙为反应物, 甲、乙为生成物,该反应分解反应,描述错误; B、甲的生成量比乙多,但分子个数不知,相对分子质量甲不一定比乙大,描述错误; C、 丙是反应物,甲和乙是生成物,描述正确; D、t1 时,参加反应的丙质量一定等于甲、乙的质量之和,描述错误。 故选 C。
C.原子序数等于该元素原子核内的质子数 D.在化学变化中元素的种类不发生改变
【答案】B
【解析】
A、物质都是由元素组成的,正确;B、同种元素原子核质子数相同,但中子数不一定相
同,错误;C、原子序数等于原子核内的质子数,正确;D、根据质量守恒定律可知,在化
学变化中元素的种类不发生改变,正确。故选 B。
11.FeS2 常用于在接触法制硫酸过程中产生 SO2,其化学方程式为
4FeS2+11O2 2X+8SO2,则 X 的化学式为
A.FeO
B.Fe3O4
C.Fe2O3
D.FeSO4
【答案】C
【解析】
由反应的化学方程式 4FeS2+11O2
2X+8SO2,反应前铁、硫、氧原子个数分别为
4、8、22,反应后的生成物中铁、硫、氧原子个数分别为 0、8、16,根据反应前后原子种 类、数目不变,则 2X 分子中含有 4 个铁原子和 6 个氧原子,则每个 X 分子由 2 个铁原子 和 3 个氧原子构成,则物质 X 的化学式为 Fe2O3。故选 C。
初三化学方程式练习题

一化学方程式的基础知识:1化学方程式配平常用方法:最小公倍数法、奇数配偶法(先配奇数大):(1) P + O2 P2O5 (2) C + O2CO(3) Al + O2Al2O3 (4)Fe + O2Fe3O4(5) Mg + O2MgO (6) H2O2MnO2 H2O + O2↑(7) H2O H2↑+ O2↑(8) H2+ O2H2O2观察法:先金属后原子团(1)CuSO4 +NaOH —Na2SO4 + Cu(OH)2(2)Mg + HCl —MgCl2+ H2↑(3)Fe2O3 + H2SO4Fe2(SO4)3+ H2O(4)Al + H2SO4 —Al2(SO4)3+ H2↑(5)Fe(OH)3 + H2SO4Fe2(SO4)3+ H2O(6)Al2(SO4)3 +NaOH —Na2SO4 + Al(OH)33配平下列的各个化学反应的方程式:(1)KMnO4—K2MnO4+ MnO2+ O2↑(2)Al + CuSO4 —Al2(SO4)3 + Cu(3)Zn + HCl —ZnCl2 + H2↑(4)Al2O3 + H2SO4Al2(SO4)3 + H2O(5)Fe2(SO4)3+NaOH —Na2SO4+ Fe(OH)3(6)Fe(OH)3+ H2SO4Fe2(SO4)3+ H2O(7)CH4+ O2点燃CO2 + H2O(8) C + CO2高温CO(9)NH3+ O2催化剂NO + H2O(10) CO + Fe2O3高温Fe + CO2二练习1 在X + 2O2===CO2 + 2H2O的反应中,根据质量守恒定律可判断出X的化学式为:A COB CH4C CH3OHD C2H42某纯净物X在空气中完全燃烧,反应式为:X + 3 O2=== 2CO2 + 3 H2O,根据质量守恒定律可判断出X的化学式为:A C2H4B C2H4OC C2H6D C2H6O3在4Cu + 10HNO3 = 4Cu(NO3)3 + X + 5H2O反应方程式中,X的化学式为:A NOB NO2C N2OD N2O34物质X和B2能发生下列反应:2X + B2 = 2 AB3,则X的化学式是:A AB2B A2B2C AB3D A2B35某化合物R在空气燃烧后生成二氧化碳和水,下列关于R化学式叙述正确的是:A R一定含有碳,氢,氧三种元素B R一定含有碳和氢元素,不含有氧元素C R一定含有碳和氢元素,可能含有氧元素D R不一定含有碳和氢元素,但一定不含有氧元素6某物质W在氧气中充分燃烧后,生成了4.4克CO2和3.6克的水,消耗的氧气为6.4克,则W中所含有的元素判断正确的是:A 一定含有C H元素,不含O元素B 一定含有C H 元素,可能有O元素C 一定含有C H O三种元素D 条件不足,不能判断7氢气与氧气反应生成水的反应过程中,氢气与氧气的质量之比是:A 1 :1B 2 :1C 2 :32D 4 :328对于质量守恒定律的解释不正确的是:A 化学反应前后,分子的数目不变B 化学反应前后,原子的种类不变。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学方程式书写练
习题[1]
work Information Technology Company.2020YEAR
化学方程式的书写练习
一、化合反应:
1、碳在氧气中完全燃烧生成二氧化碳。
2、碳在氧气中不完全燃烧生成一氧化碳。
3、一氧化碳在氧气中点燃生成二氧化碳。
4、二氧化碳在灼热的碳中生成一氧化碳。
5、往水中通入二氧化碳,生成碳酸。
6、铁在氧气中点燃生成四氧化三铁。
7、磷在氧气中点燃生成五氧化二磷。
8、铜在空气中加热生成氧化铜。
9、硫在氧气中点燃生成二氧化硫。
10、二氧化硫加水生成亚硫酸。
11、二氧化硫在空气中氧化为三氧化硫。
12、三氧化硫通入水中生成硫酸。
13、无水硫酸铜粉末中加水中生成五水硫酸铜。
14、氢气在空气中点燃生成水。
15、氢气在氯气中点燃生成氯化氢气体。
16、氧化钙加水生成氢氧化钙。
二、分解反应:
17、在二氧化锰的催化作用下加热氯酸钾,生成氯化钾和氧气。
18、加热高锰酸钾,生成锰酸钾、二氧化锰和氧气。
19、电解水,生成氢气和氧气。
20、在二氧化锰的催化作用下分解双氧水,生成水和氧气。
21、加热碳酸,分解为二氧化碳和水。
22、碳酸钙高温生成氧化钙和二氧化碳。
23、加热五水硫酸铜生成硫酸铜和水。
24、碳酸氢钠加热生成碳酸钠、水和二氧化碳。
25、加热碱式碳酸铜,生成氧化铜、水和二氧化碳。
三、置换反应:
(1)金属和酸反应,置换出氢气。
26、铁和稀盐酸反应,生成氯化亚铁和氢气。
27、铁和稀硫酸反应,生成硫酸亚铁和氢气。
28、镁和稀盐酸反应,生成氯化镁和氢气。
29、镁和稀硫酸反应,生成硫酸镁和氢气。
30、铝和稀硫酸反应,生成硫酸铝和氢气。
31、铝和稀盐酸反应,生成氯化铝和氢气。
32、锌和稀盐酸反应,生成氯化锌和氢气。
33、锌和稀硫酸反应,生成硫酸锌和氢气。
(2)金属和盐溶液反应,置换出金属。
34、铁和硫酸铜反应,生成硫酸亚铁和铜。
35、铁和硝酸铜反应,生成硝酸亚铁和铜。
36、铁和氯化铜反应,生成氯化亚铁和铜。
37、铁和硝酸银反应,生成硝酸亚铁和银。
38、铜和硝酸银反应,生成硝酸铜和银。
39、镁和硫酸锌反应,生成硫酸镁和锌。
40、镁和硫酸亚铁反应,生成硫酸镁和铁。
41、镁和硫酸铜反应,生成硫酸镁和铜。
42、镁和氯化锌反应,生成氯化镁和锌。
43、镁和氯化亚铁反应,生成氯化镁和铁。
44、镁和氯化铜反应,生成氯化镁和铜。
45、镁和硝酸银反应,生成硝酸镁和银。
46、锌和氯化亚铁反应,生成氯化锌和铁。
47、锌和硫酸亚铁反应,生成硫酸锌和铁。
48、锌和硝酸亚铁反应,生成硝酸锌和铁。
49、锌和氯化铜反应,生成氯化锌和铜。
50、锌和硫酸铜反应,生成硫酸锌和铜。
51、锌和硝酸铜反应,生成硝酸锌和铜。
52、锌和硝酸银反应,生成硝酸锌和银。
四、复分解反应:
(1)生成硫酸钡白色沉淀。
53、氯化钡和稀硫酸反应,生成硫酸钡沉淀和稀盐酸。
54、氯化钡和硫酸铜反应,生成硫酸钡沉淀和氯化铜。
55、氯化钡和硫酸钠反应,生成硫酸钡沉淀和氯化钠。
56、氢氧化钡和稀硫酸反应,生成硫酸钡沉淀和水。
57、氢氧化钡和硫酸铜反应,生成硫酸钡沉淀和氢氧化铜沉淀。
58、氢氧化钡和硫酸钠反应,生成硫酸钡沉淀和氢氧化钠。
59、硝酸钡和稀硫酸反应,生成硫酸钡沉淀和稀硝酸。
60、硝酸钡和硫酸铜反应,生成硫酸钡沉淀和硝酸铜。
61、硝酸钡和硫酸钠反应,生成硫酸钡沉淀和硝酸钠。
(2)生成氯化银白色沉淀。
62、硝酸银和稀盐酸反应,生成氯化银沉淀和稀硝酸。
63、硝酸银和氯化钠反应,生成氯化银沉淀和硝酸钠。
64、硝酸银和氯化铁反应,生成氯化银沉淀和硝酸铁。
65、硝酸银和氯化亚铁反应,生成氯化银沉淀和硝酸亚铁。
66、硝酸银和氯化铜反应,生成氯化银沉淀和硝酸铜。
67、硝酸银和氯化钾反应,生成氯化银沉淀和硝酸钾。
68、硝酸银和氯化钙反应,生成氯化银和硝酸钙。
69、硝酸银和氯化钡反应,生成氯化银沉淀和硝酸钡。
(3)生成碳酸钙白色沉淀。
70、氢氧化钙和二氧化碳反应,生成碳酸钙沉淀和水。
71、氢氧化钙和碳酸钠反应,生成碳酸钙沉淀和氢氧化钠。
72、氯化钙和碳酸钠反应,生成碳酸钙沉淀和氯化钠。
73、硝酸钙和碳酸钠反应,生成碳酸钙沉淀和硝酸钠。
(4)生成碳酸钡白色沉淀。
74、氢氧化钡和二氧化碳反应,生成碳酸钡沉淀和水。
75、氢氧化钡和碳酸钠反应,生成碳酸钡沉淀和氢氧化钠。
76、氯化钡和碳酸钠反应,生成碳酸钡沉淀和氯化钠。
77、硝酸钡和碳酸钠反应,生成碳酸钡沉淀和硝酸钠。
(5)生成氢氧化铜蓝色沉淀。
78、氢氧化钠和硫酸铜反应,生成氢氧化铜沉淀和硫酸钠。
79、氢氧化钠和硝酸铜反应,生成氢氧化铜沉淀和硝酸钠。
80、氢氧化钠和氯化铜反应,生成氢氧化铜沉淀和氯化钠。
81、氢氧化钾与硫酸铜反应,生成氢氧化铜沉淀和硫酸钾。
82、氢氧化钾和硝酸铜反应,生成氢氧化铜沉淀和硝酸钾。
83、氢氧化钾和氯化铜反应,生成氢氧化铜沉淀和氯化钾。
84、氢氧化钙和硫酸铜反应,生成氢氧化铜沉淀和硫酸钙。
85、氢氧化钙和氯化铜反应,生成氢氧化铜沉淀和氯化钙。
86、氢氧化钙和硝酸铜反应,生成氢氧化铜沉淀和硝酸钙。
87、氢氧化钡和硫酸铜反应,生成氢氧化铜沉淀和硫酸钡沉淀。
88、氢氧化钡和氯化铜反应,生成氢氧化铜沉淀和氯化钡。
89、氢氧化钡和硝酸铜反应,生成氢氧化铜沉淀和硝酸钡。
(6)生成氢氧化铁红褐色沉淀。
90、氢氧化钠和氯化铁反应,生成氢氧化铁沉淀和氯化钠。
91、氢氧化钾和氯化铁反应,生成氢氧化铁沉淀和氯化钾。
92、氢氧化钙和氯化铁反应,生成氢氧化铁沉淀和氯化钙。
93、氢氧化钡和氯化铁反应,生成氢氧化铁沉淀和氯化钡。
94、氢氧化钠和硫酸铁反应,生成氢氧化铁沉淀和硫酸钠。
95、氢氧化钾和硫酸铁反应,生成氢氧化铁沉淀和硫酸钾。
96、氢氧化钙和硫酸铁反应,生成氢氧化铁沉淀和硫酸钙。
97、氢氧化钡和硫酸铁反应,生成氢氧化铁沉淀和硫酸钡沉淀。
(7)生成二氧化碳气体。
98、碳酸钙和稀盐酸反应,生成氯化钙、水和二氧化碳。
99、碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳。
100、碳酸钾和稀盐酸反应,生成氯化钾、水和二氧化碳。
101、碳酸钡和稀盐酸反应生,成氯化钡、水和二氧化碳。
102、碳酸氢钠和稀盐酸反应,生成氯化钠、水和二氧化碳。
(8)酸碱中和反应,生成水。
103、氢氧化钠和稀盐酸反应,生成氯化钠和水。
104、氢氧化钾和稀盐酸反应生成氯化钾和水。
104、氢氧化钙和稀盐酸反应生成氯化钙和水。
106、氢氧化钡和稀盐酸反应生成氯化钡和水。
108、氢氧化钠和稀硫酸反应,生成硫酸钠和水。
109、氢氧化钾和稀硫酸反应,生成硫酸钾和水。
110、氢氧化钙和稀硫酸反应,生成硫酸钙和水。
111、氢氧化钡和稀硫酸反应,生成硫酸钡和水。
(9)其他
112、氢氧化钙和二氧化碳反应,生成碳酸钙沉淀和水
113、氢氧化钠和二氧化碳反应(变质),生成碳酸钠和水。
114、氢氧化钠和二氧化硫反应生成亚硫酸钠和水。
115、氧化铜和稀盐酸反应,生成氯化铜和水。
116、氧化铜和稀硫酸反应,生成硫酸铜和水。
117、氧化铁和稀盐酸反应,生成氯化铁和水。
118、氧化铁和稀硫酸反应,生成硫酸铁和水。
119、氧化铝和稀盐酸反应,生成氯化铝和水。
120、氧化铝和稀硫酸反应,生成硫酸铝和水。
五、氧化还原反应:
121、氢气还原氧化铜,加热,生成铜和水。
122、碳还原氧化铜,高温,生成铜和二氧化碳。
123、一氧化碳还原氧化铜,加热,生成铜和二氧化碳。
124、一氧化碳还原氧化铁,高温,生成铁和二氧化碳。
六、其他反应:
125、甲烷在空气中点燃,生成二氧化碳和水。
126、乙炔在空气中点燃,生成二氧化碳和水。
127、丁烷在空气中点燃,生成二氧化碳和水。
