基础化学习题04
结构化学基础习题答案分子的对称性培训资料

谢谢10 解:若忽略分子中键和键之间的各种相互作用(共轭效应、空间阻碍效应和诱导效应等),则整个分子的偶极距近似等于个键距的矢量和。按矢量加和规则,C6H4ClCH3三种异构体的偶极距推算如下: ClCH3 3312222cos60CClCCHCClCCHo 2230305.17101.3410CmCm 123030125.17101.34102CmCm 304.6510Cm ClCH3 3312222cos60CClCCHCClCCHm 2230305.17101.3410CmCm 123030125.17101.34102CmCm 305.9510Cm ClCH3 3CClCCHp 30305.17101.3410CmCm 306.5110Cm 由结果可见,C6H4ClCH3 间位异构体偶极距的推算值和实验值很吻合,而对位异构体和邻位异构体,特别是邻位异构体两者差别较大。这既与共轭效应有关,更与紧邻的Cl原子和-CH3之间的空间阻碍效应有关。事实上,两基团夹角大于60。 【4.19】水分子的偶极矩为306.1810Cm,而2FO只有300.9010Cm,它们的键角值很近,试说明为什么2FO的偶极矩要比2HO小很多。 解:2HO分子和2FO均属于2vC点群。前者的键角为104.5,后者的键角为103.2。由于O和H两元素的电负性差1.24远大于O和F两元素的电负性差0.54,因而键矩OH大于键矩OF。多原子分子的偶极矩近似等于各键矩的矢量和,H2O分子和F2O分子的偶极距可分别表达为: 22104.52cos2103.22cos2HOOH称性
谢谢2 04分子的对称性 【4.1】HCN和2CS都是直线型分子,写出该分子的对称元素。 解:HCN:,C; CS2:2,,,,hCCi 【4.2】写出3HCCl分子中的对称元素。 解:3,3C 【4.3】写出三重映轴3S和三重反轴3I的全部对称操作。 解:依据三重映轴S3所进行的全部对称操作为: 1133hSC,2233SC,33hS 4133SC,5233hSC,63SE 依据三重反轴3I进行的全部对称操作为: 1133IiC,2233IC,33Ii 4133IC,5233IiC,63IE 【4.4】写出四重映轴4S和四重反轴4I的全部对称操作。 解:依据S4进行的全部对称操作为: 11213344442444,,,hhSCSCSCSE 依据4I进行的全部对称操作为: 11213344442444,,,IiCICIiCIE 【4.5】写出xz和通过原点并与轴重合的2C轴的对称操作12C的表示矩阵。 解:100010001xz, 12100010001xC 【4.6】用对称操作的表示矩阵证明: (a) 2xyCzi (b) 222CxCyCz (c) 2yzxzCz 解: (a)1122xyzzxxxCyCyyzzz, xxiyyzz
基础化学第四章习题答案

1.能够抵抗少量酸、碱或加水稀释,而本身pH 值基本保持不变的溶液,称为缓冲溶液。
2.缓冲容量是衡量缓冲能力大小的尺度。
通常用使单位体积缓冲溶液的pH 改变1个单位时,所需加入一元强酸或一元强碱的物质的量表示缓冲容量。
影响缓冲容量的主要因素是缓冲系的总浓度和缓冲比;缓冲比一定时,总浓度越大,缓冲容量越大;总浓度一定时,缓冲比越接近于1,缓冲容量越大。
缓冲容量与缓冲系中共轭酸的p K a 无关。
所以总浓度相同的HAc-NaAc 和H 2CO 3-HCO 3-缓冲系的缓冲容量相同。
3.(1)(2)(4)(5).4. 配制pH = 3的缓冲溶液,选HCOOH —HCOO -最合适,因为HCOOH 的pK a = 3.75,与所需的pH 值最接近。
5. 此混合溶液为HCO 3- -CO 32-组成的缓冲溶液。
查表4-1,H 2CO 3的p K a2=10.25。
m o l m o l g g H C O n 119.00.840.10)(13=⋅=--mol094.0molg 106g0.10)CO(123=⋅=--n代入式(4.4)得15.10mol119.0mol 094.0lg2510)HCO)CO lgp pH 323a =+⋅=+=--((n n K6. H 2C 2O 4:pKa 1 = 1.23 pKa 2 = 4.19∴应选择---242242O C O HC 缓冲体系 1]O[C ]O [HC ]O[C ]O [HC lgpKa pH 2424224242=⇒-=----则:3:2V :V NaOH O C H422=7. HAc + NaOH = NaAc + H 2O初(mol ):100×0.10 50×0.10平 (mol): 50×0.10 50×0.10c a =301501005=+(mol·L -1) c b =301501005=+(mol·L -1)pH=pKa-lg754301301754.lg.c c ba =-= 8.设需加入0.10 mol·L -1HCl 溶液x 毫升,NH 3·H 2O + HCl = NH 4Cl + H 2O生成NH 4Cl 的浓度 = 0.10x /(500+x) (mol·L -1) 剩余NH 3·H 2O 的浓度 = (0.10×500 – 0.10x )/ (500+x) (mol·L -1)pOH = 14-10 = 4 x1.0x 1.050lg75.4)x 500/(x 10.0)x 500/()x 500(10.0lg75.44--=++--=625101050.x.x .=- x = 75.5(mL) 设需加入NH 4Cl 的浓度为y mol·L -1,y1.0lg75.44-= 62.5y1.0= y = 0.018(mol/L)需加入固体NH 4Cl = 0.018×0.5×53.5 = 0.48(g)1]O[C ]O [HC ]O[C ]O [HC lgpKa pH 2424224242=⇒-=----则:3:2V :V NaOH O C H422=9.加入的NaOH 为0.20g÷40g·mol -1=0.005mol 、c (OH -)=0.005mol ÷0.100L=0.05mol ·L -1设原溶液中共轭碱 [B -]原=xmol·L -1,则加入NaOH 后,[HB]=0.25mol·L -1-0.05mol·L -1=0.20mol·L -1, [B -]=0.05mol·L -1+xmol·L -1 ,代入式(4.2)]HB []B [lga p pH -+=K11Lmol 20.0L mol )x 05.0(lg30.560.5--⋅⋅++=[B -]原=xmol·L -1=0.35mol·L -1原溶液45.5Lmol 25.0Lmol 35.0lg30.5pH 11=⋅⋅+=--10. 阿司匹林以HAsp 表示,解离后以Asp -表示。
《基础化学》课后习题参考答案(有机部分)
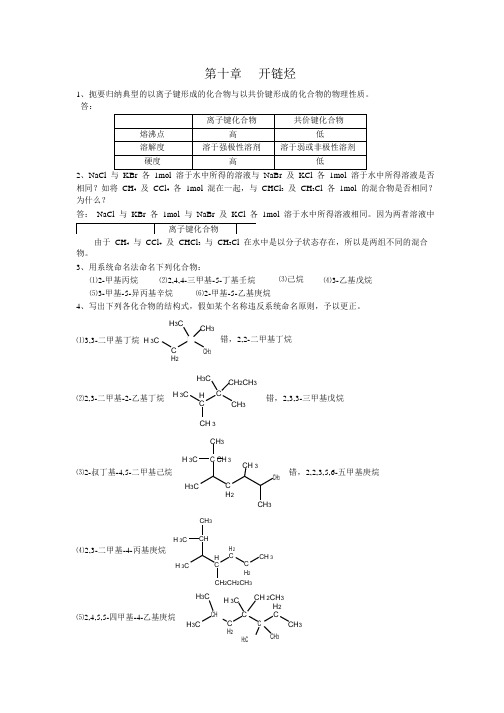
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
2004年基础化学期末考试卷

北京化工大学2004级基础化学试卷学院_____________专业_____________班级______________姓名____________学号____________日期____________(请考生注意:本试卷共页)一、是非题(判断下列叙述是否正确,正确的在括号中画√,错误的画×)(本大题分12小题,每小题1分,共12分)1、已知H 3AsO4H++H2AsO4-KH 2AsO4-H++HAsO42-KHAsO 42-H++AsO43-K则H 3AsO43H++AsO43-的K=K·K·K。
()2、O (g) + 2e-→ O2- (g),∆r H= - 639 kJ·mol-1,即氧的电子亲和能为639kJ·mol-1。
()3、HgCl2分子和H2O分子的空间构型均为V型,它们的中心原子采取相同方式的杂化轨道成键。
()4、配合物Na3[Ag(S2O3)2]应命名为二(硫代硫酸根)合银(Ⅰ)酸钠。
()5、H2O的熔点比HF高,所以O-H…O氢键的键能比F-H…F氢键的键能大。
()6、凡是中心原子采用sp2杂化方式形成的分子,必定是平面三角形构型。
()7、某原子所形成共价键的数目,等于该原子基态时未成对电子的数目。
()8、由于E(Li+/Li)最小,所以锂是金属性最强的元素。
()9、铁(Ⅱ)、钴(Ⅱ)、镍(Ⅱ)还原性强弱的次序为:Fe(Ⅱ)>Co(Ⅱ)>Ni(Ⅱ)。
()10、银的化合物易溶于水的多,而难溶于水的较少。
()11、金属离子A3+、B2+可分别形成[A(NH3)6]3+和[B(NH3)6]2+,它们的稳定常数依次为4⨯105和2⨯1010,则相同浓度的[A(NH3)6]3+和[B(NH3)6]2+溶液中,A3+和B2+的浓度关系是c(A3+)>c(B2+)。
()12、用EDTA准确滴定金属离子M2+的必要条件为lg cK≥8 。
中考化学真题专项练习题化学用语

专题04 化学用语1.(2022·陕西)化学符号具有独特的学科内涵。
下列各项对相关符号含义的说法正确的是()A.2H2O2:只能表示2个过氧化氢分子B.SO32-:只能表示硫酸根离子C.只能表示氩原子的结构示意图:D.Ag:只能表示金属银2.(2022·山东泰安)下列化学用语中表示的意义不正确的是()A.Ca:表示钙元素B.2OH-:表示2个氢氧根离子C.2N:表示2个氮分子D.2K:表示2个钾原子3.(2022·安徽)硬铝常用于制造火箭、飞机的外壳,铝元素的相关信息如图所示,下列说法正确的是()A.铝元素的相对原子质量为13B.Al2O3中Al为+2价C.硬铝的强度和硬度比铝的大D.铝是地壳中含量最多的元素4.(2022·湖南衡阳)2021年10月16日神舟十三号载人飞船发射成功,开始中国迄今为止时间最长的载人飞行。
太空舱里常用NiFe2O4作催化剂将航天员呼出的CO2转化为O2,已知NiFe2O4中Fe为+3价,则Ni的化合价为()A.+1B.+2C.+3D.+4 5.(2022·江苏扬州)“航天点亮梦想”。
搭载神舟飞船的火箭常用液氢作燃料,液氢的化学式是()A.H2B.CH4C.CO D.NH3 6.(2022·湖南怀化)下列物质对应的主要成分不正确的是()A.铁锈—Fe2O3·x H2OB.食用小苏打—NaHCO3C.天然气—CH4D.石灰石—Ca(OH)27.(2022·四川南充)某化学实验小组书写的化学式、俗名以及归类完全正确的是()A.NaOH、苛性钠、碱B.C2H5OH、酒精、无机物C.CO2、干冰、有机物D.Na2CO3、小苏打、盐8.(2022·四川自贡)元素化合价和物质类别是认识物质的两个重要维度,构建元素化合价和物质类别的二维图是学习化学的一种重要方法。
如图是碳元素的“价类二维图”,下列说法错误的是()A.A点对应的物质一定是金刚石B.B点对应的物质与C点对应的物质可以相互转化C.D点对应的物质很不稳定,容易分解D.E点对应的物质可能是K2CO39.(2022·四川达州)化学是在原子、分子水平上研究物质及其变化规律的一门基础学科。
化学基础习题库及答案

化学基础习题库及答案一、单选题(共100题,每题1分,共100分)1、下列化合物能与托伦试剂反应生成银镜的是()A、丙酸B、丙酮C、甲醇D、甲酸正确答案:D2、下列化合物中酸性最强的是()A、α-羟基丙酸B、β-羟基丙酸C、丙酸D、α,β-二羟基丙酸正确答案:D3、在氨溶液中加入少量盐酸,使:( )。
A、溶液OH-浓度变小B、NH3的Kb变大C、NH3的α增大D、pH值保持不变正确答案:C4、下列说法正确的是:()A、增大反应物的浓度,平衡向生成物浓度增大的方向移动。
B、有气体存在的可逆反应,该变压强,都会使化学平衡移动。
C、加热能使吸热反应速率加快,放热反应速率减慢,平衡向吸热反应方向移动。
D、凡能影响反应速率的因素,都能使化学平衡移动正确答案:A5、下列可用来区分葡萄糖和果糖的是( )A、斐林试剂B、苯肼C、托伦试剂D、赛利凡诺夫试剂正确答案:D6、 CH3CH2CH2CH3与CH3CH(CH3)2是什么异构体?( )A、碳架异构B、位置异构C、官能团异构D、互变异构正确答案:A7、既能发生水解反应,又能发生银镜反应的物质是()A、麦芽糖B、蔗糖C、丙酸甲酯D、葡萄糖甲苷正确答案:A8、欲使蛋白质沉淀而不变性,应选用( )A、浓硫酸B、重金属盐C、甲醛D、硫酸铵正确答案:B9、人体血浆中最重要的缓冲对是A、H2PO4 — HPO42-B、HCO3 — CO32-C、H2CO3 — HCO3-D、HPO42 — PO43-正确答案:C10、下列试剂中,常用于糖尿病患者尿液中葡萄糖含量检查的是( )A、FeCl3B、溴水C、班氏试剂D、茚三酮溶液正确答案:C11、医用生理盐水的质量浓度是多少?A、8g/LB、10g/LC、9g/LD、7g/L正确答案:C12、有关简单的饱和链烃的叙述:①都是易燃物;②特征反应都是取代反应;③相邻两个烷烃在分子上组成相差一个甲基。
正确的是( )A、②和③B、①和②C、①D、①和③正确答案:B13、可以用来判断油脂不饱和程度的是( )A、酸值B、皂化值C、碘值D、密度正确答案:C14、某缓冲溶液的共轭碱的Kb=1.0×10-6,从理论上推算该缓冲溶液的缓冲范围是( )A、5~7B、6~8C、7~9D、5~6正确答案:C15、 HPO42-的共轭酸是( )A、H2PO4-B、OH-C、H3PO4D、PO43-正确答案:A16、下列哪种物质具有致癌性( )A、蒽B、菲C、萘D、苯并芘正确答案:D17、下列有机物分子中不含有羧基的是()A、苯甲酸B、过氧乙酸C、乳酸D、苯酚正确答案:D18、人的肠胃不能消化的多糖是. ( )A、纤维素B、糖原C、右旋糖酐D、淀粉正确答案:A19、将淀粉碘化钾混合溶液装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后取出杯中液体进行试验,不能证明半透膜有破损的是:( )A、加入碘水变蓝B、加入碘化钠不变蓝C、加入FeCl3 溶液变蓝D、加入溴水变蓝正确答案:B20、下列化合物中无顺反异构现象的是()A、2-氯-2-丁烯B、2-甲基-2-丁烯C、3-甲基-2-戊烯D、2-丁烯正确答案:B21、下列不属于有机物的是 ( )A、HCOOHB、C2H4C、CH3OHD、HCN正确答案:D22、不能配制 pH = 7 左右的缓冲溶液的共轭酸碱混合物是( ) (已知HClO :K = 3.4 × 10-8 H2CO3 :K1 = 4.2 × 10-7 ,K2 = 5.6 × 10-11 H3PO4 :K1 = 7.6 × 10-3 ,K2 = 6.3 × 10-8 ,K3 = 4.4 × 10-13)A、NaHCO3-Na2CO3B、NaH2PO4-Na2HPO4C、HClO-NaClOD、H2CO3-NaHCO3正确答案:A23、构成蛋白质的基本单位是( )A、多肽B、β-氨基酸C、α-氨基酸D、肽链正确答案:C24、β-醇酸加热脱水生成( )。
大学化学基础(邓建成第二版)第四章思考题、习题

答:电负性是描述化学键中各原子对共用电子对的吸引能力。 同周期元素,从左到右,电负性数值逐渐增加,但同 周期过渡元素的电负性变化不大。 同主族元素,从上到下,电负性数值逐渐降低。
7、如何理解共价键具有方向性和饱和性? 答: 共价键的形成条件之一是原子中必须有成单电子,而 且形成的共价键的数目受到未成对电子数的限制。在形成共价 键时几个未成对的电子只能与几个自旋相反的单电子配位成键。 这说明共价键具有饱和性。 在形成共价键时,原子间总是尽可能沿着原子轨道最大重 叠的方向成键,轨道重叠越多,形成的共价键也就越稳定。原
⑤ CO2气体分子之间存在色散力。
10、晶体有几种主要类型?以下物质各属于何种晶体? ① NaCl; ④ 冰; ② SiC; ③ 石墨; ⑤ 铁。
答:晶体主要有:离子晶体、分子晶体、金属晶体、原 子晶体和过渡型晶体。 ① NaCl为离子晶体; ② SiC为原子晶体;③ 石墨为过渡 型晶体﹙混合型晶体﹚; ④ 冰为分子晶体; ⑤ 铁为金属晶
分别与三个Cl原子的p轨道重叠成键,因此 NCl3为三角锥形。
12、用分子间力说明下列事实: ① 常温下F2、Cl2是气体,Br2是液体,碘是固体; ② NH3易溶于水,而CH4却难溶于水;
③ 水的沸点高于同族其它氢化物的沸点。
答: ① F2 、 Cl2 、 Br2 、碘分子都为非极性分子,其分子量逐
体。
11、试用离子极化的观点解释AsF溶于水,AsCl、AsBr、 AsI难溶于水,溶解度由AsCl到AsI依次减少。 答:阴离子半径越大,受阳离子的极化影响,其电子云的变 形性越大,阴、阳离子的电子云重叠也就越多。离子中的共价键 成分也越多。 由于F¯ 、Cl¯ 、Br¯ 、I¯ 从左到右,离子半径逐渐增大。
基础化学知识试题及答案

基础化学知识试题及答案一、选择题(每题2分,共10分)1. 化学元素周期表中,氧元素的原子序数是多少?A. 6B. 8C. 16D. 18答案:C2. 下列哪个是碱?A. 硫酸B. 氢氧化钠C. 盐酸D. 碳酸答案:B3. 化学反应中,能量的变化通常表现为:A. 光能B. 热能C. 电能D. 机械能答案:B4. 以下哪个化合物属于有机化合物?A. 水B. 二氧化碳C. 甲烷D. 氧气答案:C5. 物质的量(mol)是表示:A. 物质的质量B. 物质的体积C. 物质的重量D. 物质中包含的粒子数答案:D二、填空题(每题2分,共10分)1. 原子由原子核和______组成。
答案:电子2. 一个水分子由______个氢原子和______个氧原子组成。
答案:2,13. 化学方程式中,反应物和生成物的系数表示的是______。
答案:物质的量4. 金属元素通常在元素周期表的______部分。
答案:左侧5. 氧化还原反应中,失去电子的物质被称为______。
答案:还原剂三、简答题(每题5分,共20分)1. 描述什么是化学键,并举例说明离子键和共价键的区别。
答案:化学键是原子之间通过电子的共享或转移形成的吸引力。
离子键通常形成于活泼金属和活泼非金属之间,如氯化钠中钠离子和氯离子之间的键。
共价键则形成于非金属原子之间,通过共享电子对来实现,如水分子中氢和氧原子之间的键。
2. 解释什么是酸碱中和反应,并给出一个例子。
答案:酸碱中和反应是酸和碱反应生成盐和水的过程。
例如,盐酸(HCl)和氢氧化钠(NaOH)反应生成氯化钠(NaCl)和水(H2O)。
3. 什么是氧化还原反应?请给出一个例子。
答案:氧化还原反应是涉及电子转移的化学反应,其中一个物质被氧化(失去电子),另一个物质被还原(获得电子)。
例如,铁与氧气反应生成铁的氧化物,铁被氧化,氧气被还原。
4. 描述什么是摩尔质量,并说明它与原子质量单位的关系。
答案:摩尔质量是1摩尔物质的质量,以克/摩尔为单位。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章 缓冲溶液 首 页 难题解析 学生自测题 学生自测答案 章后习题答案 难题解析 [TOP]例4-1 现有1.0L 缓冲溶液,内含0.01mol H 2PO 4-、0.030mol HPO 42-。
(1) 计算该缓冲溶液的pH ;(2) 往该缓冲溶液中加入0.005 0 mol HCl 后,pH 等于多少?析 题设缓冲系:H 2PO 4-HPO 42-+ H +,用公式 pH =p K a +lg )PO (H )(HPO 4224--n n 计算。
若加入HCl ,H +与HPO 42- 反应生成H 2PO 4-。
解 (1)根据H 3PO 4: p K a1=2.16; p K a2=7.21; p K a3=12.32pH =p K a +lg )PO (H )(HPO 4224--n n =7.21+lg mol 010.0mol 030.0=7.68 (2)加入0.005 0 mol HCl 后:pH =p K a +lg )PO (H )(HPO 4224--n n =7.21+lg 0.0050mol 0.010mol 0.0050mol 0.030mol +-= 7.42 例4-2 柠檬酸(缩写H 3Cit )常用于配制供培养细菌的缓冲溶液。
如用500mL 的0.200 mol·L -1柠檬酸,须加入0.400 mol·L -1的NaOH 溶液多少毫升,才能配成pH 为5.00的缓冲溶液?(已知柠檬酸的p Ka 1=3.14,p Ka 2= 4.77,p Ka 3=6.39)析 要配pH5.00的缓冲溶液,应选p K a 2,缓冲系NaH 2Cit-Na 2HCit ,用NaOH 与H 3Cit 完全反应生成NaH 2Cit ,再与NaH 2Cit 部分反应生成Na 2HCit 。
解 设H 3Cit 全部转化为NaH 2Cit 需NaOH 溶液V 1 mL :0.200 mol·L -1×500 mL = 0.400 mol·L -1×V 1 mL解得: V 1 = 250设NaH 2Cit 部分转化,组成NaH 2Cit -Na 2Hcit 缓冲系,需NaOH 溶液V 2 mL :NaH 2Cit + NaOH Na 2HCit + H 2On (Na 2HCit )= 0.400 mol·L -1×V 2 mL= 0.400V 2 mmoln (NaH 2Cit )= 0.200 mol·L -1×500 mL -0.400 mol·L -1×V 2 mL= (100-0.400 V 2)mmolpH = p Ka 2 + lg )Cit NaH ()HCit Na (22n n = 4.77+lg )mmol0.400-(100mmol 400.022V V = 5.00 解得: V 2 = 157共需加入NaOH 溶液的体积: V 1 mL + V 2 mL = 250 mL + 157 mL = 407 mL例4-3 今有500mL 总浓度0.200 mol·L -1、pH4.50的HAc -NaAc 缓冲溶液,欲将pH 调整到4.90,需加NaOH 多少克?调整后缓冲溶液的缓冲容量是多少?解 查表得HAc 的p K a= 4.76,在pH4.50的缓冲溶液中:4.50 = 4.76 + lg (HAc)(NaAc)L 0.200mol -1c c -⋅ 解得 c (HAc )= 0.130mol·L -1c (NaAc )= 0.200 mol·L -1-0.130 mol·L -1= 0.070mol·L -1加入固体NaOH m g : 4.90 = 4.76 + lg 1-1-1-1-mol g 40g L 50.0L mol 130.0mol g 40gL 50.0L mol 070.0⋅-⨯⋅⋅+⨯⋅m m 解得: m = 0.92在pH4.90的缓冲溶液中:[HAc] = 0.130 mol·L -1-L50.0mol g 40g 92.01-⨯⋅= 0.084mol·L -1 [Ac -] = 0.070 mol·L -1+L50.0mol g 40g 92.01-⨯⋅= 0.116mol·L -1 缓冲容量为: β = ][Ac [HAc]][HAc][Ac 2.303--+⨯=1-1--1-1L 0.116mol L 0.084mol L 0.116mol L 0.084mol 2.303⋅+⋅⋅⨯⋅⨯= 0.112 mol·L -1 例4-4 用0.025 mol·L -1的H 3PO 4和0.10 mol·L -1的NaOH ,配制pH7.40的缓冲溶液100 mL ,求所需H 3PO 4和NaOH 的体积比。
解 缓冲系为NaH 2PO 4-Na 2HPO 4。
设需H 3PO 4体积V 1 mL ,NaOH 体积V 2 mL 。
n (H 3PO 4) = 0.025 mol·L -1×V 1 mL = 0.025V 1 mmoln (NaOH) = 0.10 mol·L -1×V 2 mL = 0.10V 2 mmolH 3PO 4 + NaOHNaH 2PO 4 + H 2O反应前 0.025V 1mmol 0.10V 2mmol反应后 (0.10V 2-0.025V 1) mmol 0.025V 1mmolNaH 2PO 4 + NaOH Na 2HPO 4 + H 2O 起始 0.025V 1mmol (0.10V 2-0.025V 1) mmol 平衡时 [0.025V 1-(0.10V 2-0.025V 1)]mmol (0.10V 2-0.025V 1) mmol = (0.050V 1-0.10V 2) mmol pH = p K a + lg )PO NaH ()HPO Na (4242n n = 7.21 + lg mmol )10.0050.0(mmol )025.010.0(2112V V V V --= 7.40 5.2 21=V V学生自测题 [TOP] 判断题 选择题 填空题 问答题 计算题一、判断题(对的打√,错的打×,共10分)1. 缓冲溶液就是能抵抗外来酸碱影响,保持pH 绝对不变的溶液。
( )2. 缓冲溶液被稀释后,溶液的pH 基本不变,故缓冲容量基本不变。
( )3. 混合溶液一定是缓冲溶液。
( )4. 缓冲溶液的缓冲容量大小只与缓冲比有关。
( )5. 缓冲溶液中,其他条件相同时,缓冲对的p K a 越接近缓冲溶液的pH 时,该缓冲溶液的缓冲容量就一定越大。
( )6. HAc 溶液和NaOH 溶液混合可以配成缓冲溶液,条件是NaOH 比HAc 的物质的量适当过量。
( )1.× 2.× 3.× 4.× 5.√ 6. √ 7.√ 8. × 9. √ 10. √7. 由HB 和NaB 组成的缓冲溶液,HB 和B -的平衡浓度近似等于c (HB)和c (NaB)。
( )8. 因NH 4Cl -NH 3·H 2O 缓冲溶液的pH 大于7, 所以不能抵抗少量的强碱。
( )9. 同一缓冲系的缓冲溶液,总浓度相同时,只有pH=p K a 的溶液,缓冲容量最大。
( )10. 0.1mol·L -1的KH 2PO 和0.05 mol·L -1的NaOH 以等体积混合,可以配制成缓冲溶液。
()二、选择题(将每题一个正确答案的标号选出,每题1分,共22分)[TOP]1. 0.1 mol·L-1 NH3·H2O (K b=1.8×10-5)40.00mL与0.10 mol·L-1HCl20.0mL混合,所得溶液的值为()A. 1.79B. 2.25C. 4.75D. 6.75E. 9.252. 下列公式中有错误的是()A. pH=p K a+lg [B-]/[HB]B. pH=p K a-lg[HB]/[B-]C. pH=p K a+lg[n(B)]/[n(HB)]D. pH=p K a-lg[n(B)]/[n(HB)]E. pH=-lg(K w/K b)+lg[B-]/[HB]3. 用H3PO4(p K a1=2.12,p K a2=7.21,p K a3=12.67)和NaOH所配成的pH=7.0的缓冲溶液中,抗酸成分是()A. H2PO4-B. HPO42-C. H3PO4D. H3O+E. H2O4. 与缓冲容量有关的因素是()A. 外加酸量B. 总浓度C. K a或K bD. 外加碱量E. 温度5. 0.100 mol·L-1HAc加入等体积NaOH溶液配成的缓冲溶液,其最大的缓冲容量[单位是mol/(L·pH)]是()A. 0.576B. 0.2×0.576C. 0.1×0.576D. 0.05×0.576E. 0.576/26. 欲配制pH=9.0的缓冲溶液,最好选用下列缓冲系中的()A. 邻苯二甲酸(p K a1=2.89;p K a2=5.51)B. 甲胺盐酸盐(p K a=10.63)C. 甲酸(p K a=3.75)D. 氨水(p K b=4.75)E. 硼酸(p K a=9.14)7. 影响缓冲容量的主要因素是()A. 缓冲溶液的pH值和缓冲比B. 弱酸的p K a和缓冲比C. 弱酸的p K a和缓冲溶液的总浓度D. 弱酸的p K a和其共轭碱的p K bE. 缓冲溶液的总浓度和缓冲比8. 下列各组中两溶液的pH相等的是()A. 0.500 mol·L-1NaH2PO4与该溶液稀释一倍后所得溶液。
B. c(HAc)=0.100 mol·L-1的溶液与c(1/2 H2SO4)=0.100 mol·L-1的溶液。
C. 0.100 mol·L-1 NaH2PO4溶液与0.100 mol·L-1 Na2HPO4溶液D. pH=4.0的缓冲溶液与0.001mol·L-1 HClE. 0.2 mol·L-1NH3和0.15 mol·L-1HCl9. 下列各组分等体积混合的溶液,无缓冲作用的是()A. 0.2 mol·L-1邻苯二甲酸氢钾和等体积的水B. 0.2 mol·L-1 HCl和0.2 mol·L-1 NH3·H2OC. 0.2 mol·L-1 KH2PO4和0.2 mol·L-1 Na2HPO4D. 0.01 mol·L-1 NaOH和0.2 mol·L-1 HAcE. 0.01 mol·L-1 CH3CHOHCOOH 和0.01 mol·L-1 CH3CHOHCOONa10. 下列各组溶液中,能以一定体积比组成缓冲溶液的是()A. 浓度均为0.1 mol·L-1的NaAc溶液和HAc溶液B. 浓度均为0.1 mol·L-1的NaOH溶液和HCl溶液C. 浓度均为0.1 mol·L-1的NaOH溶液和NH3溶液D. 浓度均为0.1 mol·L-1的HAc溶液和HCl溶液E. 浓度均为0.1 mol·L-1的NaOH溶液和H2SO4溶液11. 欲配制=4.50的缓冲溶液,若用HAc及NaAc配制,则c(HAc)及c(NaAc)的浓度之比为(HAc的p K a=4.76) ()A. 4.76/1B. 1/4.76C. 4.50/1D. 1/1.78E. 1.78/112. 1.0L溶液中含有6.0g HAc和4.1g NaAc,已知[M r(HAc)=60g·mol-1] p K a=4.76[M r(NaAc)=82 g·mol-1],此溶液的pH为()A. 2.46B. 3.46C. 3.76D. 4.46E. 4.7613.向0.030 mol·L-1 HAc (p K a=4.76)溶液中加入NaAc晶体,使NaAc的浓度为0.100 mol·L-1,则溶液的pH接近于()A. 5.72B. 5.28C. 4.75D. 4.23E. 2.8714.下列各缓冲缓冲容量最大的是溶液()A. 500mL中含有0.15mol HAc和0.05mol NaAcB. 500mL中含有0.05mol HAc和0.15mol NaAcC. 500mL中含有0.1mol HAc和0.1mol NaAcD. 1000mL中含有0.15mol HAc和0.05mol NaAcE. 1000mL中含有0.1mol HAc和0.1mol NaAc15.人体血浆中最重要的抗酸成分是()A. H2PO4-B. HPO42-C. HCO3-D. H2CO3E. H n-1P-16.人体血液的pH值总是维持在7.35〜7.45这一狭小的范围内。
