钯泡沫镍电极进行水体中2-氯联苯电催化脱氯
钯负载泡沫镍电极电化学还原水中三氯乙酸

钯负载泡沫镍电极电化学还原水中三氯乙酸杨海明;赵小彤;安百钢;李莉香;王绍艳;鞠茂伟【摘要】The Pd-loaded Ni foam electrode was prepared by non electro deposition method and characterized by SEM.The electrochemical reduction of acetocaustin was researched using Pd-loaded Ni foam electrode as cathode and platinum wire as anode.The effects of process conditions on acetocaustin degradation were investigated,the kinetic and mechanism of the reaction were discussed.The results showed that:The Pd-loaded Ni foam electrode had high specific area and good hydrogen storage performance;Under the conditions of using 20 mmol/L sodium sulfate as electrolyte,electrolysis temperature 20 ℃,Pd-loading amount 4.5 mg/cm2,constant current 10 mA and electrolysis time 240 min,the acetocaustin degradation rate and the chlorine removal rate were 99.76%and 73.86% respectively;The electrochemical reduction process of acetocaustin and the concentration change of the residual chlorine atoms on acetocaustin both met the pseudo first order kinetic equation;The dechlorination of acetocaustin took place by removing chlorine atoms one by one.%采用非电沉积法制备了钯负载泡沫镍电极,运用SEM技术对其进行了表征,并以其阴极、铂丝为阳极进行了电化学还原三氯乙酸的研究,考察了工艺条件对三氯乙酸降解效果的影响,并对反应动力学和反应机理和进行了探讨.结果表明:钯负载泡沫镍电极具有较高的比表面积和良好的储氢性能;以20 mmol/L硫酸钠为电解质,在电解温度为20℃、钯负载量为4.5 mg/cm2的条件下恒流(10 mA)电解240 min,三氯乙酸降解率达99.76%,氯原子脱除率达73.86%;三氯乙酸的电化学还原反应过程以及三氯乙酸上未脱除氯原子浓度的变化均符合拟一级反应动力学方程;三氯乙酸在电化学还原过程中逐个脱除氯原子.【期刊名称】《化工环保》【年(卷),期】2017(037)004【总页数】5页(P404-408)【关键词】钯负载;泡沫镍电极;三氯乙酸;脱氯【作者】杨海明;赵小彤;安百钢;李莉香;王绍艳;鞠茂伟【作者单位】辽宁科技大学化学工程学院,辽宁鞍山114051;辽宁科技大学化学工程学院,辽宁鞍山114051;辽宁科技大学化学工程学院,辽宁鞍山114051;辽宁科技大学化学工程学院,辽宁鞍山114051;辽宁科技大学化学工程学院,辽宁鞍山114051;国家海洋环境监测中心,辽宁大连116023【正文语种】中文【中图分类】X703.1三氯乙酸是一种自来水氯气消毒的副产物,同时还见于化工、制药、杀虫剂等行业的生产废水中[1-2]。
流动注射钴离子催化化学发光法测定环境水体中痕量2—氯苯酚

流动注射钴离子催化化学发光法测定环境水体中痕量2—氯苯酚流动注射钴离子催化化学发光法测定环境水体中痕量2—氯苯酚摘要:在弱碱性介质中,过氧化氢能使发光试剂鲁米诺产生化学发光,Co2+对该化学发光体系具有很好的催化作用,2-氯苯酚的添加能增强该化学发光反应的发光信号,建立了测定2-氯苯酚的流动注射化学发光分析法。
结果表明,2-氯苯酚产生的相对化学发光信号强度与其浓度在1.0×10-7~4.0×10-5 mol/L 范围内呈线性关系,方法的检出限(3S/N)为5.0×10-8 mol/L。
线性方程为y=1 492.9x-1 292.9,R2=0.990 6,对浓度为4.0×10-6 mol/L的2-氯苯酚进行11次平行测定,相对标准偏差为2.98%。
关键词:流动注射;化学发光;鲁米诺;2-氯苯酚中图分类号:O657.31 文献标识码:A 文章编号:0439-8114(2016)12-3179-03DOI:10.14088/Abstract:Under alkalescent condition,o-chlorophenol has a strong enhance on the chemiluminescence (CL)reaction of oxidation (H2O2)and the chemiluminescent(luminol)under the catalysis of the Co2+. Based on the system,a flow injection-chemilumnescence method has been established for the determination of o-chlorophenol. The method is simple,convenient and sensitive. The linear range is 1.0×10-7~4.0×10-5 mol/L,its linear equation is y=1 492.9x-1 292.9,R2=0.990 6,and the detection limit of 5.0×10-8 mol/L o-chlorophenol,1the RSD is 2.98% for 4.0×10-6 mol/L o-chlorophenol(n=11).Key words:flow injection;chemiluminescence;luminol;o-chlorophenol2-氯苯酚(o-chlorophenol),别名邻氯苯酚,气味难闻,主要应用于有机合成工业,易对水体和土壤造成污染[1]。
纳米级双金属体系对水中氯苯和多氯联苯的催化还原脱氯研究

纳米级双金属体系对水中氯苯和多氯联苯的催化还原脱氯研究用纳米级零价铁(nZVI)或双金属体系对氯代脂肪烃、氯酚、PCBs和含氯杀虫剂等含氯有机污染物进行还原脱氯,使含氯有机物转化为低氯或无氯有机物,以达到低毒、可生物降解的目的,为含氯有机污染物的处理提供了一种全新的降解途径。
然而该技术在实际应用中,却存在催化剂表面易钝化、纳米催化剂易团聚等诸多制约因素。
为了较为系统的考察纳米级双金属体系对含氯有机污染物的催化还原脱氯降解效果,本文重点研究了纳米级Ni/Fe和Pd/Fe对水中氯苯和PCBs等含氯有机物的催化还原脱氯效果,考察了温度、pH、催化剂用量、初始浓度等因素对纳米级双金属去除水中氯苯和PCBs的影响,初步探讨了纳米级双金属体系去除水中氯苯和PCBs等含氯有机物的机理。
结果表明:无论是1,3-二氯苯,还是1,2,4-三氯苯,均能在5h左右被纳米级Pd/Fe有效还原脱氯。
纳米级Pd/Fe在5h内对1,3-二氯苯和1,2,4-三氯苯的去除效率分别为96.2%和86.7%,之所以1,2,4-三氯苯的去除效率比1,3-二氯苯的低,这一方面是因为相同结构时,苯环上的氯原子个数越多越难发生催化还原脱氯反应;另一方面,主要是因为1,2,4-三氯苯在邻位上存在氯原子,而邻位上的氯原子则比间位上的氯原子更难脱氯。
也就是说,在含氯有机污染物的脱氯过程中,氯原子个数较多的含氯有机物比相同结构氯原子个数较少的含氯有机物难进行催化还原脱氯反应。
腐植酸(HA)和S042-对纳米级Pd/Fe催化还原1,3-二氯苯和1,2,4-三氯苯脱氯均具有抑制作用,但其作用机理各不相同。
尽管HA中的活性基团会促进纳米级Pd/Fe对有机氯污染物的还原脱氯,但是HA在纳米级Pd/Fe表面易被吸附,催还还原受到抑制,而且这种作用占了绝对的主导作用,从而导致HA的存在会抑制纳米级Pd/Fe催化还原脱氯反应的进行。
而S042-一方面会攻击零价铁的表面,在Fe的表面形成一层钝化膜,减小Fe 的腐蚀速度,进而在一定程度上抑制反应的进行;另一方面S042-中的S会引起双金属催化剂中毒,从而降低其反应性。
高分子负载钯催化下的氯苯加氢脱氯反应

山西大学学报(自然科学版)23(2):141~143,2000Journal of Shanx i U niv ersit y(Nat.Sci.Ed.) 文章编号:0253-2395(2000)02-0141-03高分子负载钯催化下的氯苯加氢脱氯反应段新娥1 王文静2 李 竞1 乔志敏1(1.山西大学化学系,山西太原030006;2.太原化工学校030024)摘 要:首次考察了载体、碱、温度,在常压氢气氛及均相钯催化剂作用下对氯苯加氢脱氯的影响。
筛选结果表明在0.1M PaH2和65℃条件下,PV P—P dCl2/N aO A c/EtO H体系可有效还原氯苯。
关键词:氯苯;加氢脱氯;P V P—P dCl2中图分类号:O643.38 文献标识码:A 催化脱卤是卤代物还原的一个重要方法,通常使用的催化剂为贵金属催化剂,芳基碘和芳基溴在很多过渡金属均相催化剂下可以进行脱卤反应,但由于芳基氯的加氢还原存在较大热力学障碍,很难发生加氢脱氯反应[1-3]。
在氢源的选择上,由于氢的低溶解度,钯络合物一般不用氢气作为氢源[3]。
只有氢气在一定压力下,均相钯催化剂才可以有效还原芳基氯[4]。
本文寻找了高分子负载钯催化剂常压加氢脱氯的方法,得到了PVP—PdCl2/NaOAc/EtOH这一有效催化还原体系。
1 实验部分1.1 试剂 C6H5Cl,PdCl2,C2H5OH,PVP,N aOAc为分析纯,其它碱及高分子载体均为化学纯。
1.2 催化剂的制备 称取一定量可溶性高分子置于250mL烧杯中,加入无水乙醇使之溶解后,加入PdCl2溶液,室温搅拌48h,得一橙红色溶液。
1.3 加氢反应 加氢反应在夹套玻璃反应瓶中进行,先将碱加入反应瓶中,抽空换氢气两次后注射入定量溶剂,搅拌10min后加入均相催化剂,氢气氛下还原20min,加入氯苯反应。
1.4 分析测试 氯苯转化率分析采用上海分析仪器厂102型气相色谱仪(PEG20M,10%,2m× 3m m)。
钯修饰碳纳米管复合材料催化降解多氯联苯
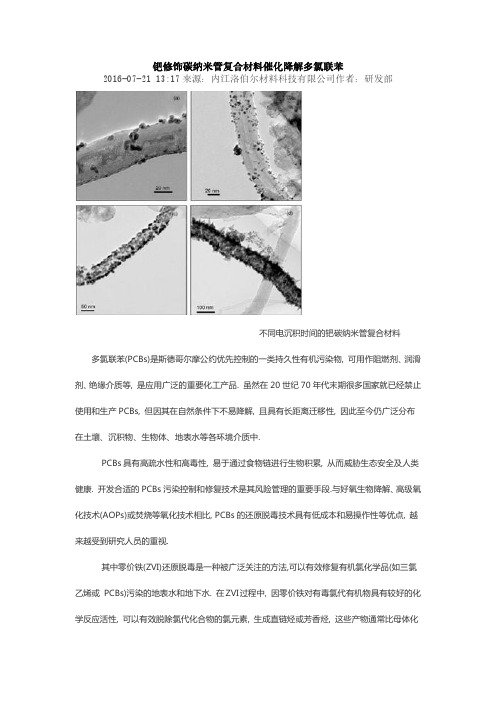
钯修饰碳纳米管复合材料催化降解多氯联苯2016-07-21 13:17来源:内江洛伯尔材料科技有限公司作者:研发部不同电沉积时间的钯碳纳米管复合材料多氯联苯(PCBs)是斯德哥尔摩公约优先控制的一类持久性有机污染物, 可用作阻燃剂、润滑剂、绝缘介质等, 是应用广泛的重要化工产品. 虽然在20世纪70年代末期很多国家就已经禁止使用和生产PCBs, 但因其在自然条件下不易降解, 且具有长距离迁移性, 因此至今仍广泛分布在土壤、沉积物、生物体、地表水等各环境介质中.PCBs具有高疏水性和高毒性, 易于通过食物链进行生物积累, 从而威胁生态安全及人类健康. 开发合适的PCBs污染控制和修复技术是其风险管理的重要手段.与好氧生物降解、高级氧化技术(AOPs)或焚烧等氧化技术相比, PCBs的还原脱毒技术具有低成本和易操作性等优点, 越来越受到研究人员的重视.其中零价铁(ZVI)还原脱毒是一种被广泛关注的方法,可以有效修复有机氯化学品(如三氯乙烯或PCBs)污染的地表水和地下水. 在ZVI过程中, 因零价铁对有毒氯代有机物具有较好的化学反应活性, 可以有效脱除氯代化合物的氯元素, 生成直链烃或芳香烃, 这些产物通常比母体化合物毒性低, 在自然环境中也更易进一步降解. 但是, ZVI颗粒在周围条件下即会失活, 因此ZVI 脱氯反应会迅速减缓.电化学技术可以通过电子的转移脱除水溶液或非水溶液中PCBs的氯元素, 是极具前景的有机氯污染物还原脱毒技术. 近年来开展了一些水溶液中PCBs的电催化还原脱氯的研究, 其研究成果提供了该项技术实现PCBs污染的地表水、沉积物和土壤的原位或异位修复的可能性. 在电化学脱氯反应中, 电极材料是获得高的脱氯效率的重要因素. 除了金属电极(如钛、镍、银等), 石墨和碳纤维等碳材料因具有良好的加氢能力也通常用作工作电极. 近年来, 碳纳米管(CNTs)作为电极材料受到越来越多的关注. 与传统碳材料相比, CNTs具有一些独特的性质, 如更好的导电性、更高的能量密度分布和贮氢性能、更大的比表面积. CNTs的这些特性有可能会更有利于有机氯化合物的电化学脱氯. 已有一些应用CNTs电极对某些氯代化合物电化学脱氯的报道. Li等人发现负载血色素的电极能够对三氯乙酸有效脱氯, 在此过程中, 完全脱氯产物乙酸为最终产物.大连理工大学环境与生命学院全燮等人采用化学气相沉积-电沉积法制备出以钛板为基底的载钯碳纳米管有序阵列电极(Pd/CNTs/Ti).钯颗粒多数粒径约10nm左右,平均粒径小于20 nm, 均匀分散在碳纳米管(CNTs)管壁表面. 应用载钯碳纳米管有序阵列电极用于甲醇-水溶液中2,4,5-三氯联苯(PCB29)的电催化还原脱氯研究.结果表明, 由于CNTs的独特性质,Pd/CNTs/Ti电极表现出比Pd/Ti 和Pd/石墨电极更高的脱氯效率,6 h内PCB29去除率达90%. 在此过程中PCB 29可以完全脱氯, 联苯被确认为是最终脱氯产物.在电催化还原反应中载钯量、阴极电压和支持电解质是影响脱氯效果的关键因素.。
研究论文题目基于钯修饰电极的多氯联苯电催化还原脱氯

论文题目:基于钯修饰电极的多氯联苯电催化还原脱氯研究作者简介:杨波,男,1975年12月出生,2002年09月师从于清华大学余刚教授,于2007年01月获博士学位。
中文摘要持久性有机污染物(POPs)是当今国际上环境污染物研究的前沿和重要课题,鉴于该类物质特殊的物化性质以及对人体健康和生态环境所造成的严重危害,2001年国际社会签署了本世纪来最重要的环境公约——《关于持久性有机污染物的斯德哥尔摩公约》。
而在该公约所规定的12种受控POPs名单中,多氯联苯(PCBs)具有显著代表性(高持久性、高毒性、全球迁移性等),是唯一被明确规定在全球范围内消除污染源的POPs,其消除期限为2025年。
因此,开展PCBs污染控制技术以及受PCBs 污染环境介质的修复研究,对于消除其环境危害和履约具有重要意义。
另一方面,近年来许多传统的污染物处置方法都有了新的发展,绿色化学是它们发展的主要方向,所遵循的标准包括:在常规条件下即可实现低耗高效的去除效果,处置过程所使用的化学试剂环境友好且成本低廉,无毒性副产物生成等。
其中,氢解还原法有别于将污染物彻底分解矿化的高温焚烧或高级氧化等方法,在常规条件下,以氢作为绿色试剂,通过其强还原作用有针对性地脱除污染物上致毒致危害原子,使得污染物在绿色低耗的过程中达到去毒的目的,因而成为环境污染控制研究的热点和重点。
近年来,电催化氢解法作为主要的氢解还原方法之一,因其可连续稳定地原位产生强还原性的原子氢,高效地用于后续氢解去毒反应,已被越来越多地应用于各种污染物的降解去除。
在氯代有机污染物的电催化氢解脱氯降解研究中,国际上所选用的目标污染物主要是氯酚、氯苯类的常规氯代芳烃,而对于分子结构更加稳定,氯原子很难脱除的POPs,相关报导非常少;另外,已有研究采用的催化电极主要是各种钯修饰的活性碳材料,电催化脱氯效率偏低。
本论文工作基于上述研究现状,在国际上首先开展了高孔密度金属材料负载贵金属催化剂进行POPs电催化氢解脱氯的研究;从新型载体的筛选和高效催化剂材料的制备、相关影响因素的考察及其作用机制的解析、电催化脱氯界面反应机理的推测与验证等三个层面出发,深入系统地研究了PCBs 电催化脱氯的增效机制和反应机理;所得结论和成果对有机污染物氢解还原去除研究和双金属材料催化机理的知识体系有新的贡献,并可为POPs的污染控制技术,特别是相关的环境修复技术提供可靠的数据支持和理论指导。
用于氯代芳烃电催化脱氯的钯负载金属基电极的制备方法[发明专利]
![用于氯代芳烃电催化脱氯的钯负载金属基电极的制备方法[发明专利]](https://img.taocdn.com/s3/m/4e49d29e168884868662d63d.png)
专利名称:用于氯代芳烃电催化脱氯的钯负载金属基电极的制备方法
专利类型:发明专利
发明人:杨波,余刚,邓述波
申请号:CN200610008107.6
申请日:20060220
公开号:CN1831197A
公开日:
20060913
专利内容由知识产权出版社提供
摘要:本发明公开了属于环境修复和钯修饰电极制作技术的一种用于氯代芳烃电催化脱氯的钯负载金属基电极的制备方法。
分为电沉积液的配制和沉积过程:将氯化钯和乙酸钠投入纯水中,配制成最终浓度为5mM的氯化钯和最终浓度为50mM~100mM的乙酸钠的混合沉积液,经加热超声溶解,使溶液颜色从黄色变成深棕色;将混合沉积液和金属基体放入三电极体系的单室电沉积池内,进行加热搅拌,采用低电流分次沉积,且每次金属基体电极都要换面,将已负载钯的金属电极取出待用。
采用这种电沉积方法能够实现多种金属材料的钯有效负载和高催化活性,提高相关电催化脱氯技术与设备的经济性和实用性。
工艺流程简单易行,可控性强,完全适于实际工业生产。
申请人:清华大学
地址:100084 北京市100084-82信箱
国籍:CN
代理机构:北京众合诚成知识产权代理有限公司
代理人:李光松
更多信息请下载全文后查看。
钯基催化剂电催化氢解处理氯代有机物的研究进展

第 35 卷 第 1 期环 境 科 学 研 究Vol.35,No.1 2022 年 1 月Research of Environmental Sciences Jan.,2022钯基催化剂电催化氢解处理氯代有机物的研究进展张 均1,2,汤木娥2,周 易2,石雪林1,吕晓书1,龚海峰1,熊 昆1,张贤明1*,蒋光明1*1. 重庆工商大学废油资源化技术与装备教育部工程研究中心,重庆 4000672. 重庆科技学院冶金与材料工程学院,纳微复合材料与器件重庆市重点实验室,重庆 401331摘要:氯代有机物(COPs)是一类重要的化工生产原料和中间体,但其高持久性、高生物累积性、致癌性及遗传毒性将对生态环境和人体健康造成巨大危害. 开发消除COPs毒性的新型技术,实现人与自然和谐共生,成为国际学术界和工业界共同关注的焦点. 电催化氢解技术(ECH)因具有高反应活性、结构简单、二次污染风险小等优势而备受青睐. 本文系统综述了钯(Pd)基催化剂上的ECH反应机制,探究强还原性氢自由基(H*)的定量分析方法,揭示脱氯反应与析氢副反应间的竞争关系. 通过分析H*产量、污染物脱附、电场等因素对脱氯速率的影响规律,建立晶面与效能间构效关系,识别不同反应条件下制约ECH速率的因素.聚焦阴极催化活性低、易受脱氯产物毒化的关键问题,通过暴露Pd活性中心位点、强化水裂解、调控电子效应和配体效应及几何效应等策略增强催化剂产H*量和抗毒化性能. 开展ECH脱氯反应路径识别、脱氯性能影响因素探讨以及生物安全性评价,并基于当前存在的关键科学问题,展望ECH技术的发展趋势,为设计和发展实用型环境催化新技术和新型催化材料指明方向.关键词:氯代有机物(COPs);电催化氢解技术(ECH);氢自由基;决速步骤;催化性能;脱氯路径中图分类号:X132; X523文章编号:1001-6929(2022)01-0119-12文献标志码:A DOI:10.13198/j.issn.1001-6929.2021.09.14Progress in Electrocatalytic Hydrogenolysis of Chlorinated Organic Compounds on Palladium-Based CatalystsZHANG Jun1,2,TANG Mu'e2,ZHOU Yi2,SHI Xuelin1,LÜ Xiaoshu1,GONG Haifeng1,XIONG Kun1,ZHANG Xianming1*,JIANG Guangming1*1. Engineering Research Center for Waste Oil Recovery Technology and Equipment, Chongqing Technology and Business University, Chongqing 400067, China2. Chongqing Key Laboratory of Nano/Micro Composites and Devices, School of Metallurgy and Materials Engineering, Chongqing University of Science & Technology, Chongqing 401331, ChinaAbstract:Chlorinated organic compounds (COPs) are important chemical raw materials and intermediates with wide applications in industry and agriculture. However, due to their high persistence, strong bioaccumulation, carcinogenicity and genotoxicity, they pose a threat to the ecological environment and human health. In the pursuit of harmonious coexistence of human and nature, efficient and green technology that can detoxify the COPs is therefore urgently needed. Electrocatalytic hydrogenolysis (ECH) is a competitive alternative due to its extremely high reactivity, mild reaction conditions and little secondary pollution. In this review, we systematically summarize the progress in the development of ECH technology for detoxication of the COPs on representative palladium-based catalysts. The initial research on ECH primarily focused on the mechanism as well as method to quantify the in-situ produced atomic hydrogen free radicals (H*) on catalyst. These free radicals are highly reductive to cleave the C—Cl bonds. Subsequently, extensive efforts were devoted to revealing the competitive relationship between ECH and side hydrogen evolution reaction. Moreover, by comparing the impacts of H*收稿日期:2021-07-19 修订日期:2021-09-16作者简介:张均(1988-),男,重庆万州人,讲师,博士,主要从事氯代有机物的电催化氢解修复技术研究,junzhang@.*责任作者:①张贤明(1955-),男,重庆忠县人,教授,硕士,主要从事废油再生研究,zxm215@;②蒋光明(1987-),男,浙江绍兴人,研究员,博士,主要从事水体废油污染控制研究,jiangguangming@基金项目:中国博士后科学基金项目(No.2020M683633XB);重庆市博士后科研项目特别资助(No.2011010006422180);教育部平台科技资助项目(No.fykf201910)Supported by China Postdoctoral Science Foundation (No.2020M683633XB);Chongqing Special Support Fund for Post Doctor,China (No.2011010006422180);Scientific Platform Project,Ministry of Education,China (No.fykf201910)generation, product desorption and electric field on the ECH kinetics, the Pd surface structure-ECH activity relationship was established, contributing to the identification of the rate-determining step under different reaction conditions. Aiming at enhancing the ECH activity, several efficient strategies were then developed to increase the H*production and enhance its anti-poisoning performance via the electronic, ligand and geometric effect. Recently, the research focused more on the ECH pathway, the effects of environmental conditions on ECH and the biological safety of the water before and after ECH treatment. On basis of the presented progress, we finally prospect the future research priorities and directions for designing and developing new practical environmental catalysis technologies and catalytic materials.Keywords:chlorinated organic compounds (COPs);electrocatalytic hydrogenolysis(ECH);atomic hydrogen;rate-determining step;catalytic performance;reaction pathway氯代有机物(COPs)是指脂肪烃、芳香烃及其衍生物分子中氢原子被氯原子取代后的产物,是化工、制革、电子、医药和农药等领域的重要化工生产原料、中间体和有机溶剂[1-2]. 几乎所有COPs均属于有毒、有害且难降解物质,具有环境持久性、生物蓄积性、长距离迁移能力和生物危害性,因此美国、欧洲和我国均将其认定为优先控制的有毒污染物[3]. 近年来,由于化工工业废弃物的不规范排放、废弃物堆积场地渗滤液的渗漏及农药的滥用,导致COPs在水体中广泛存在,严重危害生态环境和人体健康[4]. 因此,亟需开展水污染修复与治理.目前,COPs修复技术主要包括生物降解[5-6]、物理吸附[7]、高级氧化工艺[8-9]和电化学还原[10]等,其中电催化氢解技术(ECH)因高反应活性、结构简单、二次污染风险小等优势,在COPs修复领域极具潜力[11].碳氯键(C−Cl)裂解是COPs去毒的关键,在阴极表面通过电解水或氢离子(H+)产生强还原性氢自由基(H*),进攻并裂解C−Cl键进行的加氢还原脱氯反应是ECH技术的主要途径[12]. 考虑到H*不稳定,因此材料吸附H*的强度决定着脱氯性能的大小. 通常,H*的吸附取决于金属(M)中氢原子和未成对电子之间金属氢键(M−H)的形成. 金属中d电子含量越高,金属原子中存在的未成对电子越少,M−H键则越弱[13].钯(Pd)具有适中的钯氢键(Pd−H)强度和较低的析氢过电位,且对高度活化的H*具有良好的吸附能力,是ECH研究中最常用的催化剂[14]. 目前,ECH技术仍处于起步研究阶段,对其脱氯基本原理、决速步骤、脱氯反应效能及影响因素仍有待进一步研究. 该文在已有研究基础上,综述了ECH脱氯反应基本原理,并对制约ECH脱氯速率的决速步骤进行剖析,阐述增强ECH脱氯反应效能机制,开展ECH脱氯反应路径识别、脱氯性能影响因素探讨以及生物安全性评价.总结ECH研究中存在的瓶颈问题并展望未来研究方向,以期为ECH修复COPs水污染提供参考,对开发高效、低成本的催化剂材料和持久性COPs废水治理具有重要的学术意义和潜在的应用价值.1 电催化氢解脱氯反应基本原理根据电子转移和C−Cl键裂解的顺序,ECH脱氯反应包括直接电子转移机理和间接电子转移机理[15],其中直接电子转移机理分为顺序离解电子转移机理和同步离解电子转移机理[16-17]. 直接电子转移机理具体如下:①COPs吸附在电极表面形成中间吸附态,降低脱氯反应活化能. ②在顺序离解电子转移机理中,吸附态COPs接受一个电子后,形成一个稳定的π*自由基阴离子中间产物,随后C−Cl键断裂,生成自由基中间产物和氯离子. 通常,自由基中间产物的还原电位比COPs更正,将引发第二电子转移,促使中间产物进而还原为碳负离子. ③碳负离子直接从溶剂中夺取氢原子,通过质子化作用实现加氢脱氯,或同步去除相邻碳原子上2个氯离子,生成含双键或三键的产物,这主要取决于溶剂的条件及其分子结构. 此外,同步离解电子转移机理中电子转移和C−Cl键断裂是同时发生.截至目前,针对Pd基催化剂上ECH处理COPs 反应机制的研究,认为间接电子转移机制占主导,直接电子转移发生几率不高. Wu等[18]通过自由基淬灭试验证实,4-氯苯酚污染物的ECH脱氯遵循间接电子转移机理. 关键H*物种存在3种形式,分别是吸附在Pd表面的原子态吸附氢(H ads)、进入Pd晶格内的原子态吸收氢(H abs)以及在负电位下形成的分子态氢(H2). 在理解ECH反应机制研究中,Pd基催化剂上氢物种的演变与电位间的关系仍有待进一步研究.如图1所示,Jiang等[19]通过循环伏安法探究H*与电位间演变规律,提出H*定量分析方法. 在起始电位为−0.80 ~ −0.60、−0.20 ~ −0.10和−0.10 ~ 0.00 V范围内分别对应H2、H abs和H ads的生成. 此外,H ads、H abs和H2物种均出现在−0.65 V处,并随着电位负移,H abs 和H2的浓度也不断增加. 通过分析氢物种与电位间120环 境 科 学 研 究第 35 卷关系,H ads、H abs和H2的浓度在−0.65 ~ −0.85 V范围内遵循H abs<H ads<H2,在−0.85 ~ −1.00 V范围内遵循H ads<Habs <H2,在−1.00 ~ −1.10 V范围内遵循H ads<H2<H abs.值得注意的是,H ads才是ECH脱氯反应的真正关键活性氢物种,H abs是惰性氢物种,H2则对脱氯反应有负面影响.图 1 工作电压与2,4-DCP脱氯机理示意[19] Fig.1 Schematic illustration of the potential-dependentECH mechanism for 2,4-DCP[19]2 电催化氢化脱氯决速步骤识别以间接电子转移机理为主的ECH脱氯反应主要分为4个步骤:①COPs (R−Cl)和水在电极表面的吸附过程〔见式(1)(2)〕;②阴极电解水或H+产生H*过程〔见式(3)(4)〕;③C−Cl键裂解,H*取代氯原子的加氢还原脱氯过程〔见式(5)〕;④产物在电极表面的脱附过程〔见式(6)〕.明确Pd基催化剂上脱氯反应决速步骤并揭示其控制机理,对最大限度地提高ECH脱氯性能至关重要. 然而,目前国内外对ECH脱氯反应决速步骤的意见并不统一,主要包括以下几种观点.2.1原子氢产量在以间接电子转移模式为主导的脱氯反应中,H*的产生量和覆盖度对ECH脱氯性能有较大影响. 因此,大量研究聚焦在增加金属Pd表面H*产率,主要策略包括:①调控金属Pd纳米晶尺寸、形貌和结构(如多孔结构、表面缺陷、异质结构),提高Pd纳米颗粒的比表面积以提高Pd表面H*产率;②将Pd纳米颗粒负载在活性载体表面(碳材料、MnO2、泡沫镍、聚合物等);③通过引入其他金属(铁、钴、镍、银等)组成合金,增强H*产生和吸附能力[20-22]. 目前,电流效率常用于评价ECH过程中COPs转化为产物时电量的有效利用率. 据统计,大部分脱氯反应的电流效率在10%~40%之间. 电流效率较低的原因一方面可能是由于污染物浓度较低,H*利用率较低;另一方面可能是H*覆盖度较低,使其与COPs接触反应的概率降低,部分H*以Heyrovsky步骤〔见式(7)〕或Tafel步骤〔见式(8)〕转化为H2被消耗[23]. 因此,增强H*的产生量和吸附行为,提高H*与COPs接触概率,有助于加快脱氯反应进程.2.2产物脱附除了H*生成量外,催化剂表面COPs的吸附活化及产物的脱附也是制约其脱氯性能的关键因素,但一直被人们所忽略. 密度泛函理论(DFT)计算表明,2,4-DCP在电极表面自发的本征吸附有利于C−Cl 键活化,使C−Cl键更易被H*裂解[24]. 除本征吸附外,COPs的有效吸附还受脱氯产物吸附行为影响. Fu 等[25]研究发现,Pd/TiN和Pd/C上的脱氯效率分别为96.4%和80.9%. 相比Pd/TiN催化剂,2,4-DCP及产物苯酚在Pd/C上的吸附能力更强. 苯酚在Pd活性位点上的强吸附将与2,4-DCP形成竞争吸附,导致部分Pd活性位点被苯酚毒化,脱氯性能显著降低. 因此,在Pd活性位点上产物的脱附速率也是影响ECH脱氯反应决速步骤的关键因素. 通过优化Pd的d带中心削弱其与苯酚的吸附强度,促进苯酚从Pd活性位点快速脱附,是提高ECH脱氯效率的有效策略.2.3电场影响Shu等[26]研究发现,ECH脱氯效率还受阴极表面电场的排斥力影响. 随着H+的快速消耗,在大部分时间内ECH脱氯反应是在碱性条件下进行. 因此,氯苯酚上羟基基团倾向于去质子化形成表面带负电的离子化合物,并在阴极表面电场的排斥力作用下远离阴极. 随着电位的进一步负移,阴极表面电场的排斥力变大,更不利于氯苯酚从本体溶液向电极表面扩散,难以进行快速脱氯反应. 在电位低于−0.85 V时,相比去质子化作用,析氢副反应对ECH过程的影响可忽略不计. 此外,电场对不同取代位氯苯酚的脱氯性能也有影响. DFT计算表明,相比对位C−Cl键,邻位第 1 期张 均等:钯基催化剂电催化氢解处理氯代有机物的研究进展121C −Cl 键具有更高的反应活性,但试验结果显示去质子化后更有利于对位C −Cl 键的裂解. 这是由于电场排斥力的方向与去质子化的羟基位点一致,促使羟基附近邻位上的C −Cl 键远离阴极,与H *的加氢脱氯反应难度加大导致.2.4 晶面调控综合以上研究结果,制约脱氯反应速率快慢的决速步骤并不统一,且都是在特定反应条件下获得. 因此,统一以上观点并明确Pd 表面脱氯反应机制已成为当务之急. 最近,Jiang 等[27]通过研究不同阴极电位下2,4-DCP 的脱氯动力学、脱氯效率、污染物和产物,以及H *物种与Pd(100)(111)(110)晶面上吸脱附能和d 带中心的关系,建立晶面-效能间构效关系,确定ECH 脱氯效率在−0.70~−0.75 V 时受H *产率控制,在−0.80~−0.90 V 时受苯酚脱附动力学控制,在大于−0.95 V 时受去质子化的2,4-DCP 与阴极电场间排斥力控制(见图2). Pd 催化剂上具有较大活性位点密度的(110)晶面更有利于促进H *生成,具有较低d 带中心的(111)晶面更有利于苯酚的脱附.图 2 基于C-Pd(110)、C-Pd(100)和C-Pd(111)催化剂的决速步骤研究[27]Fig.2 The study of rate-determining step based on C-Pd(110), C-Pd(100) and C-Pd(111) catalysts[27]3 电催化氢化脱氯反应效能调控根据以上研究结果发现,具有强还原性H *的产生和产物苯酚的脱附是制约脱氯性能的关键因素,该文将从两个方面探索调控ECH 脱氯反应效能的策略.3.1 增产H *自由基3.1.1 增加Pd 活性中心位点鉴于贵金属Pd 价格高昂,资源稀缺,如何将Pd活性中心最大程度地暴露在三相反应界面,增加H*的产生量是提升ECH 脱氯性能亟待解决的关键问题. 在电化学体系中,相比平板电极,电解液能快速进入透水性三维电极内部,通过增加电解液的对流改善反应传质效率,提高反应速率[28]. 此外,具有大比表面积和丰富孔道结构的三维电极还将促进纳米颗粒的高度分散,充分暴露活性位点[29]. 近年来,石墨毡、三122环 境 科 学 研 究第 35 卷维石墨烯、泡沫铜和泡沫镍等三维电极在电化学还原领域极具潜力[30-32]. Wu 等[18]采用网状结构的三维石墨毡基底不但能增加钯镍活性位点的暴露程度赋予Pd 表面高H *浓度,还能提升4-氯苯酚的吸附速率和质量传递,协同作用于4-氯苯酚的快速去除. Yang 等[33]制备了泡沫镍修饰超细钯粒子的电极材料(Pd@Ni-foam),三维自支撑多孔骨架和Pd-Ni 原子微界面强化氟苯尼考的传质速率,同时Ni 相比Pd 具有更强的金属氢结合强度,在其微界面产生大量H *,从而提高H *利用率[34]. 在阴极电位为−1.2 V 下,2 h 内对氟苯尼考的脱氯效率高达99.5%,其反应速率常数(0.044 min −1)分别比泡沫镍(0.001 min −1)和商业Pd/C (0.01 min −1)高44和4.4倍. Li 等[35]在泡沫镍骨架上构筑MnO 2纳米片阵列,促使H *从Pd 表面转移到2,4-DCP 表面,使反应界面延伸至Pd 以外,减少了析氢反应对H *的消耗. Shen 等[36]发现镍基层状金属有机骨架显著改善了Pd 分散性,生成高浓度H *,该电极对2,4-二氯苯氧乙酸的脱氯行为表现出高活性、高选择性和稳定性.由于Pd 纳米粒子具有高表面能和低电荷等固有特性,Pd 纳米颗粒往往倾向于团聚长大. Shu 等[37]探索纳米尺寸与ECH 脱氯性能的内在关系时发现,以硼氢化钠、乙醇和氢气为还原剂研制的Pd 纳米颗粒尺寸分别为6.4、9.5和13.1 nm ,4-氯苯酚在30 min内的去除率分别为100%、60%和29%,这可能是由于Pd 纳米尺寸的减小将增加Pd 表面积,更多活性位点的充分暴露有益于加快H *的生成. 当活性金属的尺寸从纳米尺度减至原子级别时,金属将在均一性、配位环境和量子限域效应等性质方面发生变化,从而为催化剂提供独特性能[38]. Li 等[39]通过静电吸引法在富有缺陷差异的载体〔CeO 2、Ni(OH)2、ZrO 2〕上制备具有不同Pd 原子配位环境的Pd 单原子催化剂.Pd 单原子以Pd −O 键配位并主要以Pd 2+存在,Pd/CeO 2在20 min 内对4-氯苯酚的脱氯效率最高,其转换频率高达4.1 min −1,远超过商业Pd/C 催化剂(0.7 min −1). Gan 等[40]研究了具有高效Fe-N 4配位模式的单原子Fe-N x -C 纳米片(见图3),发现与商业20% Pt/C 催化剂相比,Fe-N x -C 对1,2-二氯乙烷ECH 脱氯反应表现出更高的反应性和乙烯选择性. 通过结合试验和理论计算,获悉Fe-N 4结构中原子形式的Fe 中心被认为是乙烯电化学生产的主要活性位点.借助阴极催化剂的电化学还原-氧化过程是分解有机化合物极具前景的技术. Li 等[41]将Co 单原子担载在硫化石墨烯载体上制备双功能催化剂,该催化剂不仅在H 2O 2合成上表现出卓越的性能,其半波电位为0.70 V ,选择性超过90%,而且在ECH 脱氯性能上对2,4-二氯苯甲酸的去除率达到91.1%,还显著降低了80%的总有机碳浓度.图 3 Fe-N x -C 纳米片合成示意[40]Fig.3 Schematic illustrations of Fe-N x -C nanosheets synthesis[40]3.1.2 强化水裂解过渡金属氧化物(如氧化镍和锰掺杂氧化物)在Volmer 步骤中对H −OH 键的断裂非常有效. Luo 等[42]制备了钯/二氧化锰/泡沫镍电极(Pd/MnO 2/Ni),认为MnO 2/Ni 比Ni 具有更正的析氢起始电位,可加速H 2O 中H −OH 键的解离,增加Pd 表面吸附H *的浓度,进而提高2,4-二氯苯甲酸的ECH 脱氯效率. 考虑到MnO 2具有较低的电导率,添加大量MnO 2可能会抑制电子转移并制约原子H *的生成,导致ECH 效率降低. Lou 等[43]通过引入MnO 2改善电极比表面积,在2 h 内Pd/MnO 2/Ni 对2,4-二氯苯甲酸的脱氯效率高达96%,而Pd 的含量仅是纯钯/镍电极的1/4. TiC第 1 期张 均等:钯基催化剂电催化氢解处理氯代有机物的研究进展123有增大电化学活性比表面积和加快界面电荷转移速率的作用,促进H *的大量生成. 理论计算表明,TiC 通过增强H *和2,4-二氯苯甲酸在电极表面的吸附强度,进而加快ECH 反应[44-45]. Huang 等[46]将二维层状过渡金属MoS 2纳米片负载在软碳毡上制备非Pd 电极,MoS 2对H 2O 中H −OH 的解离发挥积极作用,形成大量H *将有效作用于三氯乙烯的快速脱氯反应,但随着析氢反应的发生,法拉第效率急剧降低. 在−1.1 V 电位时,Co 掺杂MoS 2催化剂的脱氯效率高达100%.3.2 增强催化剂抗毒化性能3.2.1 电子效应通过优化Pd 的d 带中心削弱Pd 与产物吸附强度是提高催化剂抗毒化性能的策略之一. 金属和载体界面间强相互作用将诱导催化剂局部电荷重排,改变金属电子结构,提升催化性能[47]. 近年来,具有肖特基势垒的异质结催化剂在多相催化领域取得了可喜的进展[48-49]. 金属与半导体费米能级的相对位置决定着电子转移的方向,势垒高低决定着电子转移数. Wang等[50-51]在TiO 2颗粒和氮化碳表面沉积Pd 制备了莫特-肖特基异质结催化剂,证实莫特-肖特基异质结诱导的金属-载体强相互作用,促使具有更负费米能级和更小功函数的n 型半导体中的电子向Pd 表面转移,进而优化Pd 电子结构实现脱氯产物在其活性位上的快速脱附,提高催化剂脱氯效率和增强其抗毒化能力. 考虑到不同能带结构的半导体可在较宽范围内调控金属电子结构,如何将半导体费米能级调整到最佳位置以获取最优电子态对设计优异ECH 催化剂具有重要意义.杂原子掺杂在调控金属电子结构和改善吸脱附行为的研究引起国内外广泛关注. Jiang 等[52]将磷(P)掺杂到具有合适能带结构、大表面积的氮化碳网状结构(P-PCN)中,试验分析和DFT 表征发现P 掺杂促使氮化碳的费米能级正移,极大地削弱了Pd 与氮化碳异质结界面处金属-载体间的相互作用,有助于减轻Pd 表面电子过剩,从而最大限度地提高脱氯效率. 如图4所示,当P 掺杂量为0.25时,Pd具有最图 4 Pd/P-PCN 催化剂的脱氯性能和ECH 脱氯机理[52]Fig.4 Dechlorination performance and ECH meachinism of Pd/P-PCN catalyst[52]124环 境 科 学 研 究第 35 卷佳电子密度,对2,4-DCP 的吸附和苯酚解吸达到平衡,催化剂去除2,4-DCP 的比活性达到最大值(0.172min −1·cm −2). 此外,氮掺杂石墨烯与Pd 的强相互效应不仅调节Pd 的晶体生长方向以呈现树枝状形貌,还通过改变Pd 电子结构影响其与反应物和产物的相互作用. 在ECH 性能调控中,吡咯-N 占主导地位,其次是吡啶-N 和石墨-N. 其中,吡咯-N 有助于增强2,4-DCP 污染物的吸附/活化,并减轻产物苯酚对催化剂的毒化作用,赋予催化剂强抗毒化性能. 因此,富含吡啶/吡咯-N 和富含吡啶/石墨-N 的钯基催化剂的表观速率常数分别为0.28和0.20 min −1·cm −2,远高于C/Pd 催化剂(0.13 min −1·cm −2)[53].3.2.2 配体效应和几何效应配体效应和合金间几何效应对ECH 脱氯性能的影响显著. Chen 等[54]提出一种P 原位掺杂诱导Pd 晶体结构转变的新策略,P 掺杂将诱导晶体Pd 转变为非晶态Pd-P 纳米粒子,引起Pd 与其相邻原子间配位数的减少. 当Pd-P 和Pd-Pd 配位数分别为3和4时,在晶体效应和配位效应的协同作用下,非晶态Pd-P 催化剂表现出最高的ECH 脱氯活性和循环稳定性.DFT 计算表明,P 掺杂将促进苯酚的脱附,减弱其对Pd 活性中心的毒化作用. 电子态密度表明P 掺杂导致Pd 的d 带中心下移,有利于苯酚的解吸. Jiang 等[55]将四乙基氯化铵配体(TEAC)修饰到碳载Pd 纳米颗粒表面,其中TEAC 在还原电位作用下将演变为三乙胺 (TEA),形成强烈的配体-Pd 效应,助力ECH 脱氯动力学,其质量活性和比活性分别为2.32 min −1· g−1和0.16 min −1·cm −2. 优越的ECH 脱氯性能归因于H+泵效应增加了电极界面局部H +浓度以提高H *自由基的生成量,电子效应和空间效应协同削弱Pd 与苯酚的吸附强度,促进苯酚的解吸和Pd 活性位点的更新(见图5). 在几何效应方面,Peng 等[56]研究还发现,Ag 合金化将促使Pd 晶格膨胀,d 带中心位置升高,Pd −H 结合力增强,加快H *的生成. 苯酚与2,4-DCP 在Pd 活性中心的竞争吸附将致使催化剂中毒,而AgPd 合金化有助于缓解苯酚在Pd表面的强吸附,促图 5 Pd/三乙胺催化剂的形成过程和电子结构分析[55]Fig.5 The dealkylation andelectronicstructurebased on the Pd/amine catalyst[55]第 1 期张 均等:钯基催化剂电催化氢解处理氯代有机物的研究进展125使其快速解吸,催化活性位点再生,维持催化剂高效的ECH 脱氯效率.4 脱氯反应路径识别及脱氯性能影响因素探讨4.1 脱氯反应路径识别基于氢解脱氯-有机物矿化一体化的光电催化是一种高效、环保的COPs 完全降解新技术. Li 等[57]以三氧化钨和钼掺杂钒酸铋(WO 3/Mo:BiVO 4)为光阳极,以钯镍泡沫电极(Pd/Ni)为阴极,研究光电化学法降解2,4-DCP 污染物. 通过高效液相色谱质谱系统探讨了2,4-DCP 的降解机理〔见图6(a)〕和降解路径〔见图6(b)〕. 首先,2,4-DCP 在阴极室中通过电催化氢解脱氯转化为邻氯苯酚、对氯苯酚和苯酚. 随后,脱氯最终产物苯酚在阳极室通过光电催化氧化发生氧化反应. 在氧化过程开始时,光生空穴和羟基自由基攻击苯酚,生成对苯二酚、间苯二酚、邻苯二酚、苯醌和对羟基苯甲酸. 随着氧化时间的延长,芳环断裂,生成己二烯二酸、顺丁烯二酸、反丁烯二酸和甲酸等脂肪酸. Li 等[58]在泡沫镍表面通过恒电位聚合制备氧化石墨烯和聚吡咯复合材料,并在其电极表面电沉积制备钯镍合金催化剂(PdNi/PPy-rGO/Ni). 通过超高效液相质谱联用仪鉴定双氯芬酸污染物的脱氯反应路径为双氯芬酸→1-氯代异构体(中间产物C 14H 12ClNO 2)→2-苯胺基苯乙酸(最终产物C 14H 13NO 2)+氯离子. Jiang 等[55]以四乙基氯化铵分子配体修饰的钯碳催化剂来探索2,4-DCP 污染物的脱氯路径,证实脱氯反应路径为2,4-DCP→2-氯苯酚→苯酚+氯离子.4.2 ECH 脱氯性能影响因素探讨4.2.1 溶液pH 的影响Jiang 等[24]研究发现,受H *生成速率和污染物吸附行为的双重影响,ECH 脱氯效率和H *利用率均与溶液初始pH 呈火山形关系,在pH 为2.12和3.49时具有最佳脱氯效率(66.4%)和H *利用率(35%~40%).在较低pH 下H *的过快生成和碱性条件下电极对图 6 基于Pd/Ni 泡沫为阴极和WO 3/Mo:BiVO 4为光阳极的光电化学氧化法处理2,4-DCP 的降解机理和降解路径[57]Fig.6 Degradation mechanism and pathways of 2,4-DCP in photoelectrochemicaloxidation method using Pd/Ni foam as cathode and WO 3/Mo:BiVO 4 asphotoanode, respectively[57]126环 境 科 学 研 究第 35 卷。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钯/泡沫镍电极进行水体中2-氯联苯电催化脱氯1王姝,余刚,杨波清华大学环境科学与工程系,北京 (100084)E-mail:yg-den@摘要:实验研究了钯修饰泡沫镍电极对纯水相中2-氯联苯的电催化还原脱氯作用。
采用两室流通式隔膜电解池,考察了电流密度、水体pH值和溶液流速对2-氯联苯脱氯效率的影响。
优化条件是:电流密度为1.5mA/cm2,阴极液pH值为5.5,阴极液流速为7.4mL/min1·cm2。
在该条件下电解30min,2-氯联苯的去除率达91.4%,脱氯产物包括联苯和苯基环己烷,根据脱氯过程碳平衡关系可确定该过程为逐步加氢反应。
关键词:钯修饰泡沫镍电极;2-氯联苯;电催化脱氯;纯水相中图分类号:X5061.引言多氯联苯(PCBs)是典型的持久性有机污染物(POPs),《斯德哥尔摩公约》要求各缔约国消除PCBs污染源的最后期限为2025年。
我国曾生产和进口过超过1万吨的PCBs,主要用于制造电力电容器和变压器[1]。
PCBs进入环境的主要途径是这些设备在废弃处置或使用过程中,其内的PCBs油泄漏到周边介质。
有资料表明,约有20%-30%的PCBs已进入环境造成污染,以美国为例,到1981年为止,PCBs的总生产量约为63万吨,其中作为污染物释放到环境约7.1万t[2]。
而PCBs进入环境后,扩散到自然水体的约占7%[3]。
近年来,对我国某些地区水体开展的调查表明,PCBs的污染已相当严重,有的河流(如浙江台州地区)PCBs浓度高达2,970 ng/L,超过《地面水环境质量标准》(GB3838-2002)中20ng/L 要求的148.5倍[4]。
而对于某些受PCBs泄漏直接污染的场地,临近水体的受污染情况可能更为严重。
因此,受PCBs污染水体的环境修复研究亟待开展。
目前,钯修饰电极电催化还原脱氯的方法是进行氯代有机污染物处置较为高效、低耗的方法[5]。
该方法较零价铁颗粒还原能力更强;不存在钯/铁双金属的铁基氧化性腐蚀和氢氧化物沉淀覆盖的问题,而且析氢强度可控[6]。
而POPs完全脱氯的产物不再具备其原有的POPs 特性,毒性大幅下降,该过程的能耗也远低于焚烧等高温方法。
因此,本研究采用钯修饰泡沫镍电极,进行水体中2-氯联苯(2-CB)的电还原脱氯试验,拟实现其高效去除。
2.系统介绍2.1实验装置和试剂本研究采用流通式两室隔膜电解池进行电催化脱氯实验(如图1所示),电解池为Teflon 材质,隔膜为DuPont公司的Nafion 324阳离子交换膜,阴极室和阳极室分别为4.5mL和6.3mL,电解过程由电化学工作站(CHI 636B)控制。
阴极为Pd修饰泡沫Ni电极,阳极为铂黑电极。
2-CB、四氯间二甲苯(TCMX,内标)购自Acros Organics公司;联苯(BP)、苯基环己烷购自东京化成公司;PdCl2(99.5%)由长沙亚光公司提供;泡沫镍为长沙力源新材料公司产品;十二烷基硫酸钠(SDS)购自北京现代东方精细化学品有限公司;正己烷、异丙醇为Fisher公司产品。
1本课题得到高等学校博士学科点专项科研基金(项目编号:20040003042)的资助。
图1 电解脱氯装置流程示意图Fig. 1 Schematic diagram of electrolytic apparatus for the electrocatalytic dechlorination1.电化学工作站2.阳极室3.阴极室4.Pd/泡沫Ni阴极5.参比检测线6.阳离子交换膜7.蠕动泵 8.阳极液储瓶 9.阴极液储瓶10.恒温水浴 11.电脑2.2实验方法钯/泡沫镍电极采用无电沉积工艺制备[7],电极面积6.72cm2,厚度0.4cm,钯负载量为1.05mg/cm2。
阴极液和阳极液体积均为20mL。
阴极液为静置一周以上的2-CB饱和溶液(18 µM),并加入0.2 M的SDS(支持电解质,助溶剂),0.12mL乙酸(pH缓冲剂);阳极液采用H2SO4稀释液(pH=1)。
电解过程采用恒电流设置,定时提取0.5mL的阴极液样品进行分析,用以测量2-CB和脱氯产物随时间的变化关系。
脱氯实验后,采用20mL异丙醇循环冲洗管路30min,并对其组成进行分析,结合样品分析情况,计算碳平衡关系。
2.3分析方法水体样品前处理流程为:在0.5mL样品中加入0.2mL异丙醇和0.5mL正己烷,用滴管反复抽取下层水相到有机相中释放150次,同时辅助超声传质,随后提取上层有机相,然后再加入0.5mL正己烷进行二次萃取,两次萃取收集的有机相合并氮吹定容后,进行GC/MS分析。
仪器分析采用美国EPA SW-846方法8270C,分析的物质包括2-CB、联苯等化合物。
上述萃取方法回收率超过91%,而实际样品还采用内标法定量,在前处理时加入TCMX作内标物。
3.结果与讨论3.1电流密度的影响电催化脱氯反应的还原剂来自H+或H2O电解产生的强还原性原子氢[H],然而后续反应存在[H]用于加氢脱氯反应与生成H2从电极表面脱附的竞争关系。
H2脱附过程存在如下关系,包括电化学脱附(Heyrovsky反应)和热脱附(Tafel反应)[8]:H 2O(H 3O +) + e -+ M = M[H] + OH -(H 2O)(Volmer 反应) M[H] + H 2O + e - = H 2 + M + OH -(Heyrovsky 反应) M[H] + M[H] = H 2 + M(Tafel 反应)式中M 代表受极化的具有析氢反应催化活性的电极表面位点。
通常,这些位点上的Heyrovsky 反应要快于Tafel 反应,而理论上,随着电场强度的提高,Heyrovsky 反应会加剧,从而产生对脱氯反应的负效应。
因此为优化电场条件,考察电流密度对2-CB 电催化脱氯反应的影响,反应温度25˚C ,阳极液流速3.5mL/min·cm 2,阴极液流速设为7.4mL/min·cm 2。
pH 值设为5.5。
如图2所示,2-CB 脱氯效率随电流密度的增大而提高,电流密度为0.7mA/cm 2时电解30min 的2-CB 去除率为78.6%,1.5mA/cm 2时达到91.4%,电流继续增大时2-CB 去除率增加缓慢。
另外,电流增大导致析氢反应强度加大后,生成的H 2会形成气层覆盖到部分电极表面,阻碍脱氯反应的进行[9]。
然而,图2表明2-CB 脱氯效率未随电流增加而出现下降的趋势,这可能是由于钯/泡沫镍电极表面存在氢溢流机制所致[10-11],使得在优先极化位点产生的[H]可通过电极表面迁移到其他未极化的位点,从而形成大量新的反应活性区域,这样就克服了因电流过大,由[H]电化学脱附加剧而造成的对脱氯反应的负效应。
另一方面,由于钯/泡沫镍电极表面积有限,且钯/镍双金属材料表面特性对氢溢流的速度存在限制。
因此,当电流密度较低时,[H]产生并迁移至整个电极表面的时间较长,脱氯效率较低;而当电流密度增加到1.5mA/cm 2以后,氢溢流速度容易较快达到饱和,脱氯效率增加明显减缓。
溶液中2-C B 浓度 (µM )电解时间 (min)图2 电流值对2-CB 电催化脱氯效果的影响Fig. 2 Effect of current densities on the electrocatalytic dechlorination of 2-CB3.2水体pH 值的影响水体的pH 值直接影响脱氯反应所需氢供体的数量,因此试验考察了pH 值对2-CB 脱氯效率的影响,溶液设置的pH 值由乙酸或氨水来调制。
试验条件为电流密度1.5mA/cm 2,电解时间30min ,其他条件同图2。
结果如表1所示,2-CB 转化率随着阴极液的初始pH 增大而减小,这是不同pH 值造成的氢供体量差异所致,可从反应动力学得到解释;而阴极液电解时,pH 逐渐增加,这表明脱氯过程中有H +的消耗或OH -生成,与Volmer 反应一致。
另外,阴极液在连接到管路系统,开泵循环流动后,溶液中的2-CB 会在钯/泡沫镍电极表面发生少量的吸附,泵开动30min 后其吸附的比例定义为2-CB 的初始吸附率。
由表1可知,pH 值增大,2-CB 初始吸附率减小,这可能与溶液中存在的和SDS 胶束作用的离子电荷有关。
SDS 是阴离子表面活性剂,在酸性溶液中,H +作为反离子会导致SDS 胶束外层疏松,其内包裹的2-CB 分子易释放出来,从而具有较大的初始吸附率;而在碱性溶液中,OH -在静电斥力作用下,可压缩SDS 胶束,使其更加致密,2-CB 分子更难释放到电极表面,使得2-CB 初始吸附率下降,从而也导致了脱氯效率降低。
根据上述试验结果,综合考虑脱氯效率和试剂用量等因素,确定pH 优化值为5.5。
表1 不同pH 条件下2-CB 转化率比较Table 1 Comparison of 2-CB conversion among different pH levels in aqueous solution 溶液初始pH 值 电解结束pH 值2-CB 转化率(%) 2-CB 初始吸附率(%)4.0 4.5 95.5 24.2 5.56.2 91.4 19.67.0 7.5 78.3 17.89.0 9.3 75.0 16.3 11.0 11.3 59.78.43.3溶液流速的影响2-CB 分子靠近并接触电极表面是有效利用[H]进行脱氯反应的关键,而作为电极基材的泡沫镍具有高孔密度结构(130ppi )。
因此,2-CB 从溶液中迁移到Pd 粒催化剂表面的传质阻力主要来自泡沫镍高孔结构形成的液层滞流区,其可能阻碍2-CB 和脱氯产物在反应活性位点的连续更替。
为了确定传质过程对2-CB 脱氯效率的影响,试验考察了阴极液流速,如图3所示。
当溶液流速从1.5mL/min·cm 2增加到7.4mL/min·cm 2时,电解30min 后,2-CB 去除率增加了15.8%,但继续增大到14.9 mL/min·cm 2时,去除率仅增加了1.8%,这可能是由于流速提高到一定程度后,传质阻力已不再是限制脱氯反应的主要因素,而电化学极化成为了脱氯反应的限速步骤。
由此,确定流速的优化值为7.4 mL/min·cm 2。
溶液中2-P C B 浓度 (µM )电解时间 (min)图3 阴极液流速对2-CB 电催化脱氯效果的影响Fig. 3 Effect of flow rates on the electrocatalytic dechlorination of 2-CB3.4优化条件下的碳平衡关系通过上述实验确定的电催化脱氯优化条件为:电流密度1.5mA/cm 2,阴极液pH =5.5,阴极液流速为7.4mL/min·cm 2。
