初中化学几种离子的鉴别方法
初中化学常见离子的检验及离子反应的观察

初中化学常见离子的检验及离子反应的观察化学是我们生活中不可或缺的一部分,而离子则是化学反应中的重要组成部分。
在初中化学学习中,了解常见离子的检验方法和观察离子反应是非常重要的。
本文将介绍一些常见离子以及它们的检验方法和离子反应的观察结果。
一、阳离子1. 铁离子(Fe³⁺)检验及观察:铁离子可以通过加入硫化氢气(H₂S)来检验。
观察到黑色沉淀形成,则可以确认铁离子的存在。
此外,当铁离子与次氯酸钠(NaClO)反应时,观察到橙色沉淀,进一步证实了铁离子的存在。
2. 铜离子(Cu²⁺)检验及观察:铜离子可以通过加入氨水(NH₃·H₂O)来检验。
观察到深蓝色沉淀形成,则可以确认铜离子的存在。
与铁离子类似,铜离子与次氯酸钠反应时,会形成蓝绿色沉淀。
3. 铵离子(NH₄⁺)检验及观察:铵离子可以通过加入氢氧化钠(NaOH)和加热来检验。
若产生氨气(NH₃)并用红色湿润的红色试纸接近观察到转蓝色或转红色,则可以确认铵离子的存在。
二、阴离子1. 氯离子(Cl⁻)检验及观察:氯离子可以通过加入银离子(Ag⁺)来检验。
观察到白色沉淀(氯化银)形成,则可以确认氯离子的存在。
此外,氯化钠(NaCl)溶液加入过量的硝酸银(AgNO₃)后,观察到白色沉淀继续产生。
2. 硫酸根离子(SO₄²⁻)检验及观察:硫酸根离子可以通过加入钡离子(Ba²⁺)来检验。
观察到白色沉淀(硫酸钡)形成,则可以确认硫酸根离子的存在。
此外,硫酸钠(Na₂SO₄)和硝酸银反应时,会生成白色沉淀。
3. 碳酸根离子(CO₃²⁻)检验及观察:碳酸根离子可以通过加入盐酸(HCl)来检验。
观察到有气体释放,并用氢氧化钠溶液吸入气体,观察到产生气泡,则可以确认碳酸根离子的存在。
综上所述,通过对常见离子的检验及观察,我们可以准确地判断其存在与否。
这些离子的反应观察结果提供了实验依据,有助于我们深入理解化学反应过程和离子之间的相互作用。
如何鉴别金属离子

如何鉴别金属离子金属离子鉴别是化学领域中一项重要的技术,对于分析金属离子的种类和浓度具有重要意义。
本文将介绍几种常用的金属离子鉴别方法,包括化学试剂法、仪器分析法和电化学方法等。
一、化学试剂法化学试剂法是一种传统的金属离子鉴别方法,通过观察金属离子与特定试剂发生反应的现象来判断离子的种类。
以下为几种常见的化学试剂法:1.硫化钠法:适用于检测汞、银、铅等金属离子。
将硫化钠加入待测溶液中,若生成沉淀,则表示存在相应金属离子。
2.氨水法:适用于检测铜、铅、镍等金属离子。
将氨水加入待测溶液中,若生成沉淀,则表示存在相应金属离子。
3.氯化钡法:适用于检测硫酸根离子。
将氯化钡加入待测溶液中,若生成沉淀,则表示存在硫酸根离子。
4.硝酸银法:适用于检测氯离子。
将硝酸银加入待测溶液中,若生成沉淀,则表示存在氯离子。
二、仪器分析法仪器分析法是利用现代仪器设备对金属离子进行定性和定量分析的方法,具有高灵敏度、高准确度和快速的特点。
以下为几种常见的仪器分析法:1.原子光谱法:包括原子发射光谱法(AES)和原子吸收光谱法(AAS),适用于检测金属离子的种类和浓度。
2.电感耦合等离子体质谱法(ICP-MS):适用于多种金属离子的定量分析,具有高灵敏度和高准确度。
3. X射线荧光光谱法(XRF):适用于检测金属离子的种类和浓度,具有快速、无损的特点。
三、电化学方法电化学方法是利用金属离子在电极表面的电化学反应来鉴别金属离子种类的方法。
以下为几种常见的电化学方法:1.阳极溶出法:通过观察阳极表面的金属沉淀来判断金属离子的存在。
2.极谱法:利用金属离子在电极表面的还原或氧化反应产生电流,通过电流-电压曲线来鉴别金属离子。
3.电化学阻抗谱法(EIS):通过测量金属离子在电极表面的电化学反应产生的阻抗变化来判断金属离子的存在。
综上所述,金属离子鉴别方法多种多样,可根据实际需求选择合适的方法。
在实际应用中,化学试剂法、仪器分析法和电化学方法相互补充,共同为金属离子鉴别提供准确、高效的技术支持。
氯离子的检验方法初中

氯离子的检验方法初中氯离子概述什么是氯离子氯离子(Cl-)是指带有负电荷的氯原子。
氯离子广泛存在于自然界中,包括海水、土壤和许多化合物中。
氯离子的作用氯离子在化学反应中起着重要的作用。
它们是许多电解质溶液中的一部分,可以影响溶液的电导率和酸碱性。
氯离子的常见检验方法1. 沉淀法沉淀法是最常用的氯离子检验方法之一。
它基于氯化银(AgCl)的沉淀反应。
氯离子与硝酸银(AgNO3)溶液反应生成白色的氯化银沉淀。
检验步骤1.取待测溶液,加入几滴硝酸银溶液。
2.观察是否出现白色沉淀,如果有则表示溶液中存在氯离子。
注意事项•需要注意控制硝酸银的用量,避免过量产生沉淀。
•实验操作时要小心,避免接触硝酸银溶液和氯化银沉淀,以免造成伤害。
2. 比色法比色法是通过氯离子与某些试剂反应后溶液的颜色变化来判断氯离子的存在与否。
使用试剂及检验步骤1.取待测溶液,加入数滴高锰酸钾(KMnO4)溶液。
2.观察溶液颜色的变化,如果出现橙黄色,则表示溶液中存在氯离子。
注意事项•实验操作时需要注意溶液的浓度和比色时光照的条件,避免结果的误判。
3. 欧式方法欧式方法是通过氯离子与二溴化石蜡反应生成白色的三溴化蝇合薄片来检验氯离子。
检验步骤1.取待测溶液,加入二溴化石蜡溶液。
2.观察溶液是否出现白色的薄片,如果有则表示溶液中存在氯离子。
注意事项•操作时需小心控制二溴化石蜡的用量,避免过量导致结果的误判。
氯离子检验的原理氯离子检验方法所依据的原理是不同试剂与氯离子的特定反应。
不同的试剂会与氯离子发生化学反应,生成特定的产物,通过观察产物的特性和性质变化来判断溶液中是否存在氯离子。
氯离子检验方法的局限性氯离子检验方法虽然简便易行,但也存在一定的局限性。
- 某些离子可能干扰氯离子的检验结果,导致误判。
- 检验方法的准确性和灵敏度有限,无法检测到极低浓度的氯离子。
氯离子的应用氯离子在生活和工业中有广泛的应用。
- 氯离子被用于水处理,用于消毒和杀菌。
离子检验初中化学

离子检验初中化学离子检验是化学实验中常用的一种方法,通过对物质中的离子进行检测,可以确定物质的组成和性质。
离子是带电的原子或原子团,根据其电荷正负的不同,可以分为阳离子和阴离子。
离子检验主要包括离子的识别和离子的定性分析两个方面。
离子的识别是指通过一系列的实验操作,根据离子的特性来确定其种类。
常见的离子识别实验有火焰试验、气泡实验和沉淀实验等。
火焰试验是通过将待检物质放入火焰中,根据产生的颜色来判断其中的离子。
例如,钠离子使火焰呈黄色,钾离子使火焰呈紫色。
气泡实验是将待检物质与酸或碱反应,根据产生的气体种类来确定其中的离子。
例如,碳酸氢根离子与酸反应会产生二氧化碳气体,氯离子与酸反应会产生氯气。
沉淀实验是将待检物质与其他溶液反应,根据形成的沉淀物来判断其中的离子。
例如,钡离子与硫酸根离子反应会产生白色的硫酸钡沉淀。
离子的定性分析是指通过实验方法,确定物质中的离子种类和含量。
定性分析的方法有很多,常用的有酸碱滴定法、络合滴定法和沉淀滴定法等。
酸碱滴定法是根据酸碱中和反应的化学计量关系来确定待测物质中离子的含量。
络合滴定法是利用络合反应的特性来确定离子的含量。
沉淀滴定法是利用沉淀反应的特性来确定离子的含量。
这些方法都需要根据具体的实验条件来进行操作,并通过实验结果来进行判断。
离子检验在日常生活和工业生产中有很广泛的应用。
例如,在水质检测中,可以通过检测水中的离子含量来判断水的质量。
在农业生产中,可以通过检测土壤中的离子含量来确定适合种植的作物。
在药品生产中,可以通过检测药品中的离子含量来保证药品的质量。
在环境保护中,可以通过检测大气中的离子含量来判断空气的污染程度。
离子检验是化学实验中重要的内容之一,它的应用范围广泛,可以为我们提供很多有用的信息。
通过离子检验,我们可以了解物质的组成和性质,从而更好地应用和控制物质。
离子检验不仅在化学实验中有重要的作用,也在生活和工业生产中发挥着重要的作用。
因此,学习离子检验对于我们了解化学和应用化学知识都具有重要的意义。
初中化学教案:离子的定性分析方法

初中化学教案:离子的定性分析方法一、简介离子的定性分析方法是化学实验中常用的一种技术手段,旨在通过一系列的试剂反应和观察现象,确定物质中含有哪些离子。
初中化学教学中,教师可以通过引入离子的定性分析实验来帮助学生理解离子概念、加深对化学反应和观察技巧的理解。
本文将介绍几种常见的初中化学离子定性分析方法及其操作步骤。
二、阳离子定性分析方法1. 碳酸氢根离子(HCO3-)与酸环境下钙阳离子(Ca2+)的反应步骤:(1) 取少量待测溶液,加入适量盐酸使其呈弱酸性。
(2) 分别取适量氢氧化钠溶液和硫酸钡溶液。
(3) 在胶花碗中依次加入:待测溶液、氢氧化钠溶液、硫酸钡溶液。
结果和解释:形成白色固体沉淀即可判断待测溶液中存在Ca2+。
2. 氯离子(Cl-)与银离子(Ag+)的反应步骤:(1) 取少量待测溶液,加入适量硝酸使其呈酸性。
(2) 分别取适量硝酸银溶液和氯化钾溶液。
(3) 在胶花碗中依次加入:待测溶液、硝酸银溶液、氯化钾溶液。
结果和解释:形成白色固体沉淀即可判断待测溶液中存在Cl-。
3. 铁离子(Fe3+)与硫化氢(H2S)的反应步骤:(1) 取少量待测溶液,加入适量盐酸使其呈弱酸性。
(2) 分别取适量氨水溶液、硫化钠溶液。
(3) 在试管中依次加入:待测溶液、氨水溶液、硫化钠溶液。
结果和解释:形成黑色固体沉淀即可判断待测溶液中存在Fe3+。
三、阴离子定性分析方法1. 硬水试验步骤:(1) 取少量待测水样,用烧杯装载后加热蒸发至干燥。
(2) 观察残留物的颜色和性质。
结果和解释:白色或黄色残渣:可能含有碳酸盐;灰色或黑色残渣:可能含有硫化物。
2. 氯离子(Cl-)的试验步骤:(1) 取少量待测溶液,加入适量硝酸使其呈酸性。
(2) 分别取适量硝酸银溶液、氯化钠溶液。
(3) 在试管中依次加入:待测溶液、硝酸银溶液、氯化钠溶液。
结果和解释:形成白色固体沉淀即可判断待测溶液中存在Cl-。
3. 硫离子(SO42-)的试验步骤:(1) 取少量待测溶液,加入适量盐酸使其呈弱酸性。
初中化学常见的化合物硫酸根离子、氯离子和铵根离子的检验

(3)用熟石灰检验铵盐NH4NO3的化学方程式: ____C_a_(O__H_)_2__2_N__H_4N__O_3___C_a_(N__O_3_)_2 __2_H_2_O___2_N_H__3 ___。
解:(123)硫 氢Na酸 氧C铜 化l溶溶 钙液液 能中能与加与硝入氯酸硝化铵酸钡反酸溶应化液生的反成硝应硝酸生酸银成钙,硫、有酸 水白钡 和色沉 氨沉淀 气淀和 ,氯故填:
C化 氯a银化(O生铜H)成,2 ,故2同填NH时:4N生O成3硝 酸Ca钠(N,O故3 )2填:2H2O
2NH 3
CAugSNOO4 3BNaCaCl2lBAagSCOl4NCauNCOl23
内容 知识点名称 课程内容
教学设计
描述
硫酸根离子、氯离子和铵根离子的检验
1.离子检验的一般步骤 2.硫酸根离子(SO2)的检验 3.氯离子(Cl)的检4 验 4.铵根离子(NH4 )的检验 激趣导入:通过演示实验引出本节课的知识。 知识新授:讲授硫酸根离子、氯离子和铵根离子的检验
需要的试剂、方法以及离子方程式。 巩固练习:通过2道习题巩固本节课所学的知识。 课堂小结:总结离子检验的一般方法。
4
离子方程式:
NH 4
OH
HO 2
NH 3
巩固练习
【练习1】(1)检验NaCl中氯离子的化学方程式: _________________________________。
(2)检验CuSO4溶液中硫酸根离子的化学方程式: _________________________________。
最新离子的检验鉴别及推断
•离子的检验、鉴别及推断
分析表中实验现象,剩余的四种溶液只有加入 NaOH 溶液时,可以产生四种不同的现象,所以只 有 NaOH 溶液能鉴别上述溶液。
答案 A (3)任选试剂鉴别多种物质 此类题目不限所加试剂的种类,可用多种解法,题目 考查的形式往往是从众多的鉴别方案中选择最佳方 案,其要求是操作步骤简单,试剂选用最少,现象最 明显。
(2010·山东理综-14D) 解析 必须先加稀盐酸,以排除SO23-的干扰。
(2)某无色溶液中加Ba(NO3)2溶液产生沉淀,再 加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42(×)
(2009·天津理综-3C)
•离子的检验、鉴别及推断
(3)某气体能使湿润的红色石蕊试纸变蓝,该气 体水溶液一定显碱性( √ )
滴入酚酞试液,溶液变 红色, 滴入紫色石蕊试液,溶液变 蓝色
2.利用盐酸和其他试剂进行检验 CO32- ―→加入 BaCl2 溶液后生成 白色沉淀 , 再加入稀盐酸 沉淀消失 ,并放出 无色无味能
使澄清石灰水变浑浊 的气体
•离子的检验、鉴别及推断
SO24- ―→加入稀盐酸无沉淀生成,无气体放出, 再加入 BaCl2 溶液有 白色沉淀 产生
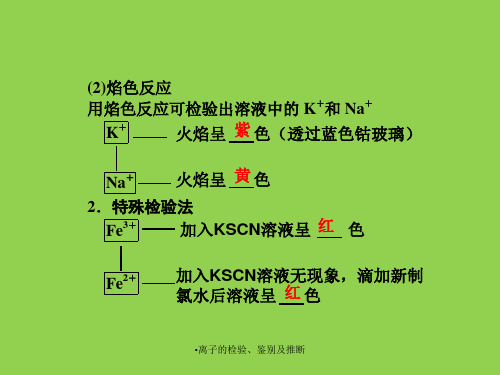
(2)焰色反应
用焰色反应可检验出溶液中的 K+和 Na+
K+
火焰呈 紫 色(透过蓝色钴玻璃)
Na+
火焰呈 黄 色
2.特殊检验法
Fe3+
加入KSCN溶液呈 红 色
Fe2+
加入KSCN溶液无现象,滴加新制 氯水后溶液呈 红 色
•离子的检验、鉴别及推断
二、常见阴离子的检验 1.利用酸碱指示剂检验
OH- ——
成棕色的碘,与Na2CO3反应产生无色的CO2气体, 与NaAlO2反应先生成白色沉淀然后溶解,与AgNO3 无明显现象,现象均不同。
常见金属离子的鉴别方法

Ca2+在碱性溶液中与乙二醛双缩生成红色螯合物沉淀,此沉淀不被碳酸钠分解,易溶于CHCl。
NH4+
NH4+能与碱作用生成NH3,加热可促使其挥发。生成的氨气可在气室中用湿润的红色石蕊试纸检验
K+
在中性、碱性或HAc酸性溶液中,K+与四苯硼化钠生成溶解度很小的白色沉淀。
Na+
在中性或HAc酸性溶液中与醋酸铀酰锌生成柠檬黄色结晶形沉淀
Cu2+
加入浓氨水,若生成深蓝色溶液,表示有Cu2+
Bi3+
在酸性溶液中与硫脲生成黄色配合物Ca(SH)2
Hg2+
加入1滴1mol/lHCl,使成微酸性,滴在新磨光的铜片上,铜可将Hg2+还原成金属汞,并与铜形成汞齐。用流水冲去试液后,在铜片上留下一个擦拭不掉的斑点,但加热时因Hg被蒸发,银白色的斑点随之消失。
常见金属离子的鉴别方法
常见金属离子的鉴别方法
常见阳离子
鉴别方法
Pb2+
在试液中加3mol/l的硫酸至酸性,生成白色PbSO4沉淀。
Hg22+
加入6mol/lHCl,得到白色沉淀后,向沉淀加氨水,亚汞存在时,沉淀变黑。(氯化亚汞见光分解为氯化汞和汞)
Ag+
加入6mol/lHCl,得到白色沉淀
Cd2+
加入过量的氨水,使Cd2+生成Cd(NH3)42+。离心分离后,将离心液加在Na2S溶液中,黄色CdS沉淀表示有Cd2+
Cr3+
Cr3+在强碱性溶液中以偏亚铬酸根离子CrO2-的形式存在,此离子可被H2O2氧化为铬酸根离子,黄色的铬酸根俩子的出现可以说明Cr3+的存在。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
知识要点:
1. 除杂题:
解答除杂质一类的题目时,要注意三原则;三要领;五种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
除杂质思路分析方法:
(1)沉淀法:加入一种试剂将被除去的杂质变为沉淀,再用过滤法除去。
(2)化气法:加热或加入一种试剂将杂质变为气体逸出。
(3)置换法:利用置换反应的原理将杂质除去。
(4)转纯法:将被除去的杂质变为提纯的物质。
(5)吸收法:常用于气体的提纯。
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
2. 混合物的分离:
(1)可溶性与难溶性物质的混合物——常用溶解、过滤、蒸发三步操作加以分离,分别得到纯净物。
如:粗盐的提纯;BaSO4和Na2SO4的混合物。
(2)两种物质均溶于水,但两种物质的溶解度一种随温度变化大,另一种变化不大时,可考虑——结晶法。
即冷却热饱和溶液的方法加以分离。
如:NaCl和KNO3的混合物。
(3)两种物质均溶于水时,可考虑用化学方法分离。
如BaCl2和NaCl的混合物。
可将混合物先溶于水,加入适量Na2CO3溶液,得到BaCO3和NaCl溶液。
BaCl2+ Na2CO3=BaCO3↓+2NaCl。
将沉淀过滤出,洗净后在沉淀中加入适量盐酸溶液,又得到BaCl2溶液,CO2逸出。
BaCO3+2HCl =BaCl2+H2O+CO2↑。
最后分别将NaCl溶液和BaCl2溶液蒸发,分别得到纯净的NaCl固体和] BaCl2固体。
注意:用化学方法或用物理方法进行混合物分离时,要区别除杂质与分离物质的不同点是:除杂质时只要求把杂质除掉、保留原物质即可;而混合物分离是几种物质用一定的方法分开,原混合物中各成分都必须保留。
3. 物质的鉴别:
鉴别是通过化学实验将几种不同特性的物质区别开来。
如鉴别两瓶无色溶液哪瓶是NaCl或KNO3。
我们只要把NaCl溶液中的Cl-检验出来,即可认定NaCl溶液,另一瓶则溶液.(1)常见离子鉴别的特效试剂
H+和OH-:紫色石蕊试液或pH试纸。
OH-:无色酚酞试液(可鉴别碱性溶液)——变红。
Cl-:AgNO3溶液和稀HNO3——有白色沉淀。
SO42-:BaCl2溶液和稀HNO3——有白色沉淀。
CO32-:稀HCl和石灰水——有CO2↑。
NH4+:强碱溶液(NaOH)——有NH3↑。
使湿润红色石蕊试纸变蓝。
(2)特征离子关系图
(3)物质鉴别的原则
①操作简便:能用物理方法鉴别的不用化学方法。
能用一种试剂鉴别的不用多种试剂。
②现象明显:使待检物质的现象对比度较大。
③防止干扰:鉴别Cl-和SO42-时,只能用BaCl2溶液不能用AgNO3溶液。
(4)物质鉴别的思路和方法
①气体鉴别:一看颜色,二用试纸,三用火点,四加试剂。
②固体、液体鉴别:一看颜色,二看气体,三辨沉淀。
③一种试剂的鉴别:
A. 几种溶液含不同阳离子时,常选用Ba(OH)2溶液或NaOH溶液做鉴别试剂。
B. 几种溶液含不同阴离子时,常选用强酸做鉴别试剂。
C. 几种溶液酸碱性不同时,常选用紫色石蕊做鉴别试剂。
D. 几种物质是金属或金属氧化物时,常选用稀强酸做鉴别试剂。
E. 一种试剂与四种溶液反应时,应是现象对比度大。
多数是有沉淀、有气体,既有沉淀又有气体、沉淀颜色不同,无明显现象。
F. 当给定的一种试剂不能鉴别出被检物时,可从已鉴别出的物质中找出一种试剂再鉴别。
④不同试剂的鉴别:
A. 观察法:根据物理性质中颜色、气味、状态、溶解性等进行鉴别。
B. 热分解法:根据不同物质的热稳定性,利用产物的不同性质特征进行鉴别。
C. 相互作用法:根据两两混合后的不同现象进行鉴别。
4. 物质的鉴定:
鉴定是根据待检物质的特性,通过不同的实验将物质的各组分逐一检验出来,从而确定某物质。
鉴定与“用实验方法确定或证明”等用语意义相同。
如:用化学方法证明某白色固体是硫酸铵。
在鉴定时不但要用化学实验检验白色固体是否是铵盐(含NH4+),还要检验它
是否是硫酸盐(含SO42-)。
从而确定此白色固体是(NH4)2SO4。
5. 推断题:
物质的推断是根据给出的实验步骤和现象,运用物质的特性,经过分析、推理作出正确的判断,以确定所给的未知物是什么物质,不可能是什么物质;确定混合物里或溶液里肯定有什么物质,肯定不含有什么物质,可能含有什么物质。
推断题是考查化学知识的综合分析能力的一种题型。
常见的有文字叙述、图表式、链条式三种形式推断题,无论哪种形式推断都必备的知识有反应规律、物理性质、化学性质、实验现象、溶解性等。
在题目分析过程中,注意关键字的分析,如某物质溶于水是“生成”还是“得到”,“生成”是反应产物,“得到”既可能有反应产物,也可能有原物质。
加酸沉淀溶解时有气体生成,一般有CO32-。
沉淀溶解但无气体生成时,一般有OH-。
部分溶解时,一定有BaSO4或AgCl等。
解推断题应注意:
(1)推理分析要紧扣实验现象,思考时要层次分明。
判断的结论要准确,既要明确的肯定,又要明确的否定。
(2)一般情况下,与试题叙述的现象完全吻合的是“一定存在”。
与现象不吻合的或有某种物质的存在使现象不正确的物质是“一定不存在”。
有某种物质的存在不影响其它反应的现象或自始至终没有参与任何反应的物质是“可能存在”。
