高三化学一轮复习——原电池 化学电源学案
高三一轮复习原电池学案(doc)

第三节化学能转化为电能---电池【考点分析】本节的重点内容为原电池工作原理及其应用.原电池工作原理的考查往往以新型能源电池或燃料电池为载体,考查原电池正负极的判断、电极反应式的书写、电子或电流的方向及溶液pH的变化等;原电池原理的应用主要考查原电池的设计、电化学腐蚀以及解释某些化学现象等.预计实物图分析、新型电池分析、电解池与原电池的联系以及设置趣味电化学实验是近年高考的热点. 【课前延伸】一、原电池1.概念:把能转化为能的装置.3.构成条件(1)两个的电极.(2)将电极插入中.(3)用导线连接电极构成.(4)能自发进行反应.二、化学电源1.一次电池——碱性锌锰干电池2.二次电池(可充电电池)铅蓄电池是常见的二次电池,电池总反应:Pb+PbO2+2H2SO4 === 2PbSO4+2H2O(1)放电时负极材料是,正极材料是.①负极反应:②正极反应:(2)充电时①阴极反应:②阳极反应:3.燃料电池氢氧燃料电池是目前最成熟的燃料电池,可分酸性和碱性两种.三、金属的腐蚀与防护1.金属腐蚀的定义金属与周围的气体或液体物质发生反应而引起损耗的现象。
2.金属腐蚀的实质金属电子被。
3.金属腐蚀的类型(1)化学腐蚀:金属直接跟周围的物质接触发生化学反应。
(2)电化学腐蚀:当两种金属相接触且又同时暴露在潮湿空气里或与电解质溶液接触时,由于形成而腐蚀。
电化学腐蚀很普遍。
5.金属的防护(1)加防护层如在金属表面加上耐腐蚀的油漆、搪瓷、陶瓷、沥青、塑料、橡胶及电镀、喷镀或表面钝化等方法。
(2)电化学防护①牺牲阳极的阴极保护法。
如在船舶的外壳装上锌块:锌作原电池的极(阳极),铁作为原电池的极(阴极)。
②外加电流的阴极保护法。
如钢闸门被保护:阳极为惰性电极(如石墨),与电源正极相连;阴极为,与电源负极相连。
(3)改变金属的内部结构。
如不锈钢。
【课前检测】1.在盛有稀H2SO4的烧杯中放入导线连接的锌片和铜片,下列叙述正确的是A.正极附近的SO42-离子浓度逐渐增大 B.电子通过导线由铜片流向锌片C.正极有O2逸出 D.铜片上有H2逸出2.(2010·广东高考)铜锌原电池(如图)工作时,下列叙述正确的是A.正极反应为:Zn Zn 2+ + 2e- B.电池反应为:Zn+Cu2+=== Zn 2+ +CuC.在外电路中,电流从负极流向正极D.盐桥中的K+移向ZnSO4溶液3.(2009·上海卷)茫茫黑夜中,航标灯为航海员指明了方向。
高三化学一轮复习导学案-原电池

高三化学一轮复习导学案课题:原电池(第一课时)【目标引领】考纲要求:1、体验化学能与电能相互转化的探究过程。
2、理解原电池的构成、工作原理及应用,能写出电极反应和电池总反应方程式。
学习目标:1、复习原电池的工作原理和构成条件,能准确判断电池的正负极、电子及溶液中离子的移动方向。
2、能够熟练地写出原电池的电极反应式和总反应式。
3、能正确设计原电池装置。
4、能运用原电池原理解决一些实际问题。
5、通过探究过程,并利用科学探究方法,提高科学探究能力,培养科学的思维方式和问题意识。
学习重点:原电池的工作原理,能设计原电池学习难点:能够熟练地写出原电池的电极反应式和总反应式【自主学习】自主学习目标:1、回忆必修二和选修四中原电池的工作原理和构成条件2、了解盐桥的作用,知道双液原电池的优点3、能准确书写简单原电池的电极反应式4、能运用原电池原理解决一些实际问题自主学习内容:I、以锌铜原电池为例1、什么样的装置就可以称为原电池?2、写出Zn片和Cu片上发生的电极反应式、现象和电池总反应式锌片:铜片:总反应离子方程式:3、什么是盐桥?盐桥有什么作用?4、在图上注明正负极和电子、阴阳离子移动方向。
5、原电池是怎样利用氧化还原反应将化学能转化为电能的?6、原电池的正负极的判断方法根据原电池电极发生的反应:发生氧化反应的极是____极,发生还原反应的极是____极[根据电子流动方向:电子流出的极是___极,电子流入的极是___极;电子由___极流向___极根据离子移动动方向:阳离子移向___极,阴离子移向___极根据电极现象:质量减少的电极通常是___极,质量增加的电极是____极有气泡冒出的电极通常为___极II、写出镁、铝作电极材料,电解质溶液分别为稀硫酸和氢氧化钠溶液,构成的原电池的总反应和电极方程式。
自我检测题:1、判断正误(1)原电池是把电能转化成化学能的一种装置()(2)在原电池中,发生氧化反应的一极一定是负极()(3)原电池的电极必须是两种活动性不同的金属,且活泼金属一定是负极()(4)HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l)能设计为原电池()2、锌-铜-硫酸原电池产生电流时,阳离子()A.移向Zn 极,阴离子移向Cu 极B.移向Cu 极,阴离子移向Zn 极C.和阴离子都移向Zn极D.和阴离子都移向Cu 极3、把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。
高三化学一轮复习《专题:原电池和化学电源》教学设计

高三化学一轮复习《专题:原电池和化学电源》
教学设计
【教学目标:】
知识目标:理解原电池的工作原理,掌握正负极的判断方法,能写出原电池电极反应和电池反应;
了解常见化学电源的种类及其工作原理;并能运用所学方法分析和解决问题。
过程与方法:引导学生回扣教材,通过由易到难的变式训练,培养学生的知识的应用迁移能力。
通过对三种化学电源工作原理的再认识,为学生解电化学试题奠定知识基础和能力基础。
情感态度价值观:通过电极反应式的书写,认识电解质溶液对电极反应的影响,培养“透过现象看本质”
的辩证唯物主义的思想;通过废旧电池危害的认识,提高学生环保意识。
【复习重难点及命题趋势】
1、原电池的原理、构成及应用。
2、常见原电池:能判断电极名称、产物,能正确写出电极反应式、正确判断电子及离子的移动方向。
【教学方法】
通过复习回顾——巩固训练,构建并深化原电池的原理;通过对不同原电池的分析和判断,掌握电极反应书写的一般方法;再通过各种化学电源反应的分析和书写,形成规律性的认识,提高解题的能力。
2024届高考一轮复习化学学案(人教版)第七章化学反应与能量第40讲原电池化学电源

第40讲原电池化学电源[复习目标] 1.理解原电池的工作原理。
2.了解常见化学电源的种类及其工作原理。
3.能够书写常见化学电源的电极反应式和总反应方程式。
考点一原电池工作原理及应用1.概念原电池是把________能转化为____能的装置。
2.构成条件反应能发生____________的氧化还原反应(一般是活泼性强的金属与电解质溶液反应)电极一般是活泼性不同的两电极(金属或石墨)闭合回路①电解质溶液②两电极直接或间接接触③两电极插入电解质溶液中3.构建原电池模型(以锌铜原电池为例)盐桥的组成和作用①盐桥中装有含KCl饱和溶液的琼胶,离子可在其中自由移动。
②盐桥的作用:a.连接内电路,____________;,使原电池不断产生电流。
③盐桥中离子移向:阴离子移向________,阳离子移向________。
4.原电池原理的应用(1)设计原电池首先将氧化还原反应分成两个半反应,其次根据原电池的反应特点,结合两个半反应找出正、负极材料和电解质溶液。
应用举例根据反应2FeCl3+Cu===2FeCl2+CuCl2设计原电池,在方框中画出装置图,指出电极材料和电解质溶液,写出电极反应式:①不含盐桥②含盐桥负极:________________正极:________________(2)比较金属的活动性强弱:原电池中,负极一般是活动性________的金属,正极一般是活动性________的金属(或能导电的非金属)。
(3)加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
(4)用于金属的防护:将需要保护的金属制品作原电池的________而受到保护。
1.盐桥是所有原电池构成的必要条件()2.原电池内部电解质中的阴离子一定移向负极,阳离子一定移向正极()3.构成原电池两极的电极材料一定是活泼性不同的金属()4.原电池中负极失去电子的总数一定等于正极得到电子的总数()5.使用盐桥可以提高电池的效率()一、原电池的设计及工作原理1.(2022·杭州模拟)实验a:将铜片、锌片和稀硫酸组成单液原电池,铜片、锌片表面均产生气泡。
2024届高考一轮复习化学教案(通用版):原电池 化学电源

第19讲原电池化学电源复习目标1.理解原电池的构成、工作原理及应用,正确判断原电池的两极,能书写电极反应式和总反应方程式;2.了解常见化学电源的种类及其工作原理;了解燃料电池的应用。
体会研制新型电池的重要性;3.能够认识和书写新型化学电源的电极反应式。
考点一原电池的工作原理及应用必备知识整理1.原电池的概念及构成条件(1)定义:把________转化为________的装置。
(2)原电池的形成条件①能自发进行的__________。
②两个金属活动性不同的电极(燃料电池的两个电极可以相同)。
③形成________,需满足三个条件:a.存在电解质;b.两电极直接或间接接触;c.两电极插入电解质溶液或熔融电解质中。
2.工作原理(以锌铜原电池为例)3.原电池在生活、研究中的应用(1)比较金属的活动性强弱原电池中,活动性较强的金属一般作________,活动性较弱的金属(或导电的非金属)一般作________。
(2)加快化学反应速率氧化还原反应形成原电池时,反应速率加快。
(3)用于金属的防护将需要保护的金属制品作原电池的________而受到保护。
如要保护一个铁质的输水管道不被腐蚀,可用导线将其与一块________相连,________作原电池的负极。
(4)设计原电池①正、负极材料的选择:根据氧化还原反应找出正、负极材料,一般选择活动性较强的金属作为________;活动性较弱的金属或可导电的非金属(如石墨等)作为________。
②电解质溶液的选择:电解质溶液一般要能够与________发生反应,或者电解质溶液中溶解的其他物质能与负极发生反应(如溶解于溶液中的空气)。
但如果氧化反应和还原反应分别在两个容器中进行(中间连接盐桥),则两个容器中的电解质溶液应选择与电极材料相同的阳离子的溶液。
③画装置图:注明电极材料与电解质溶液。
但应注意盐桥不能用________代替,要形成闭合回路。
如根据Cu+2Ag+===Cu2++2Ag设计原电池:[正误判断](1)任何氧化还原反应均可设计成原电池()(2)NaOH溶液与稀硫酸的反应是自发进行的放热反应,此反应可以设计成原电池()(3)任何原电池一定是活泼性不同的两金属电极()(4)原电池工作时,电子从负极流出经导线流入正极,然后通过溶液流回负极()(5)实验室制H2,用粗锌与稀H2SO4反应较快()(6)一般来说,带有“盐桥”的原电池比不带“盐桥”的原电池效率高()(7)Mg—Al形成的原电池,Mg一定作负极()(8)在Cu|CuSO4|Zn原电池中,正电荷定向移动的方向就是电流的方向,所以Cu2+向负极移动()对点题组训练题组一原电池的工作原理1.将相同的锌片和铜片按图示方式插入同浓度的稀硫酸中,以下叙述正确的是()A.两烧杯中铜片表面均无气泡产生B.两烧杯中溶液的H+浓度都减小C.产生气泡的速率甲比乙慢D.甲中铜片是正极,乙中铜片是负极2.如图是某同学设计的原电池装置,下列叙述中正确的是()A.氧化剂和还原剂必须直接接触才能发生反应B.电极Ⅱ上发生还原反应,作原电池的正极C.该原电池的总反应式为2Fe3++Cu===Cu2++2Fe2+D.盐桥中装有含氯化钾的琼脂,K+移向负极区[思维建模]原电池工作原理模型图特别提醒(1)若有盐桥,盐桥中的阴离子移向负极区,阳离子移向正极区。
高三化学一轮复习原电池(学案)

高三化学一轮复习原电池(学案)效果1、如右图,回答以下效果:负极的电极资料是:正极的电极资料:电极反响:正极:负极:总方程式为:。
电子的流向:电流的流向:在电解质溶液中H+运动到:极。
在电解质溶液中SO42—运动到:极。
完成的能量转化:。
上述原电池任务一段时间后,硫酸溶液的pH怎样变化:。
上述原电池任务效率不高,改成双夜带盐桥的原电池,画出装置图知识点总结:1:原电池:2:原电池正负极参与反响的物质:在负极反响,在正极反响。
3:电极反响:负极发作正极发作4:原电池的正负极现象:负极正极:5:电子的流向从流到,电流的流向从流到,6、内电路离子定向移动的方向:阳离子运动到极,阴离子运动到极7:构成原电池可以反响速率8、盐桥的作用:一、典型例题:例1:实际上不能设计为原电池的化学反响是〔〕A.C H4(g)+2O2(g)==C O2(g)+2H2O(l)△H<0B.N H3·H2O〔a q〕+H C l〔a q〕=N H4C l〔a q〕+H2O〔l〕△H<0C.2H2(g)+O2(g)==2H2O(l)△H<0D.2F e C l3(a q)+F e(s)==3F e C l3(a q)△H<0例2、依据氧化恢复反响:2Fe3+(aq)+Cu(s)=Cu2+(aq)+2Fe2+(aq)设计的原电池如图3所示。
请回答以下效果:〔1〕电极X的资料是;电解质溶液Z是;〔2〕Y电极为电池的极,发作的电极反响为X电极上发作的电极反响为;〔3〕放电进程中,盐桥中含有KCl,其中Cl-移向溶液〔选填〝FeCl3〞或〝Z〞〕。
例3、将纯锌片和纯铜片按图示方式拔出同浓度的稀硫酸中一段时间,以下表达正确的选项是〔〕A.两烧杯中铜片外表均无气泡发生B.甲中铜片是正极,乙中铜片是负极C.两烧杯中溶液的pH均增大D.发生气泡的速度甲比乙慢例4、钢铁在湿润的空气中会被腐蚀,发作的原电池反响为:2Fe+2H 2O+O 2 == 2Fe 2++4OH -。
原电池 化学电源(教学设计) 2021届高三化学一轮复习

原电池化学电源(教学设计) 2021届高三化学一轮复习原电池化学电源(教学设计)-2021届高三化学一轮复习第六章化学反应与能量〖课题〗第三课时原电池化学电源〖复习目标〗(1)了解原电池的工作原理,能写出电极反应和电池反应方程式。
(2)了解常用化学电源的类型和工作原理。
〖教学重点〗原电池的工作原理、电极方程式的书写〖教学难点〗电极方程式的书写〖教学过程〗强化知识?1、原电池概念及原理(1)原电池主电池是一种将化学能转化为电能的装置。
其反应实质是氧化还原反应。
(2)原电池的组成条件及判断①具有两个活性不同的电极(金属和金属或金属和非金属)。
②具有电解质溶液。
③ 形成闭合回路(或在溶液中相互接触)。
④ 是否有自发的氧化还原反应★☆ 判断(3)原电池工作原理示意图以铜锌原电池为例①反应原理电极名称电极材料电极反应反应类型电子流向盐桥中离子移向②两个装置的比较负极锌片zn-2e===zn2-+正极铜片cu2+2e===cu+-氧化反应由zn沿导线流向cu还原反应盐桥含饱和kcl溶液,k移向正极,cl移向负极+-装置ⅰ中还原剂zn与氧化剂cu2直接接触,易造成能量损耗;装置ⅱ盐桥原电池中,还原剂在负极+区,而氧化剂在正极区,能避免能量损耗。
③原电池的工作原理和电子流向可用下列图示表示:【说明】①在原电池装置中,电子由负极经导线流向正极,阳离子在正极上获得电子,通过电路中的电子和溶液中的离子的移动而形成回路,传导电流,电子并不进入溶液也不能在溶液中迁移。
②原电池将一个完整的氧化还原反应分为两个半反应,负极发生氧化反应,正极发生还原反应,一般将两个电极反应中得失电子的数目写为相同,相加便得到总反应方程式。
③阴离子要移向负极,阳离子要移向正极。
这是因为:负极失电子,生成大量阳离子积聚在负极附近,致使该极附近有大量正电荷,所以溶液中的阴离子要移向负极;正极得电子,该极附近的阳离子因得电子生成电中性的物质而使该极附近带负电荷,所以溶液中的阳离子要移向正极。
优质公开课化学一轮复习《电化学基础原电池-化学电源》导学案精品
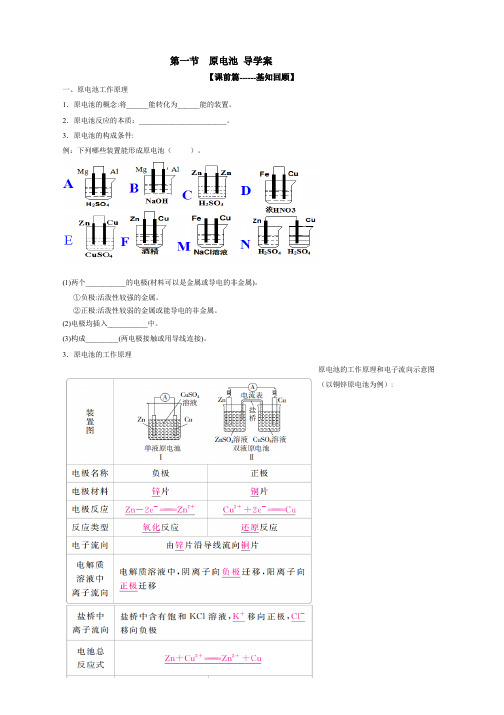
第一节原电池导学案【课前篇------基知回顾】一、原电池工作原理1.原电池的概念:将______能转化为______能的装置。
2.原电池反应的本质:________________________。
3.原电池的构成条件:例:下列哪些装置能形成原电池()。
(1)两个___________的电极(材料可以是金属或导电的非金属)。
①负极:活泼性较强的金属。
②正极:活泼性较弱的金属或能导电的非金属。
(2)电极均插入___________中。
(3)构成_________(两电极接触或用导线连接)。
3.原电池的工作原理原电池的工作原理和电子流向示意图(以铜锌原电池为例):【课中篇----诱学导思】考察角度一:原电池工作原理的灵活运用控制适合的条件,将反应Fe3++Ag Fe2++Ag+设计成如图所示的原电池(盐桥装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度).已知接通后观察到电流计指针向右偏转.下列判断正确的是()A.盐桥中的K+移向乙烧杯B.一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转C.在外电路中,电子从石墨电极流向银电极D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转考察角度二:原电池正负极的判断例:请判断以下哪一极为原电池负极【小结】原电池负极的判断方法:________________________________________________________________________________________________________________________考察角度三:原电池原理的应用1._________氧化还原反应速率。
一个自发的氧化还原反应,设计成原电池时反应速率_________ 。
2.比较金属活动性强弱金属分别作原电池的两极时,一般作负极的金属活动性比正极的_________。
3.用于金属的防护使被保护的金属制品作原电池的_________ 极而得到保护。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高三化学一轮复习——原电池化学电源学案
目标要求 1.以原电池为例认识化学能可以转化为电能,从氧化还原反应的角度认识原电池的工作原理,能设计简单的原电池。
2.体会提高燃料的燃烧效率、开发高纯清洁燃料和研制新型电池的重要性。
3.认识化学能与电能相互转化的实际意义及其重要应用,了解原电池及其常见化学电源的工作原理;能利用相关信息分析化学电源的工作原理,开发新型电池。
1.概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
2.构成条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:
①电解质溶液;
②两电极直接或间接接触;
③两电极插入电解质溶液中。
理解应用
在如图所示的4个装置中,不能形成原电池的是(填序号),并指出原因。
答案①④①中酒精是非电解质;④中未形成闭合回路
3.工作原理
以锌铜原电池为例
(1)反应原理
(2)盐桥的组成和作用
①盐桥中装有饱和的KCl、KNO3等溶液和琼胶制成的胶冻。
②盐桥的作用:a.连接内电路,形成闭合回路;b.平衡电荷,使原电池不断产生电流。
理解应用
“异常”原电池原理的深度分析
(1)铝铜浓硝酸电池
初期,活泼金属铝作负极被氧化,由于铝表面很快形成致密氧化物薄膜阻止反应继续进行,使铝钝化,钝化铝作正极,铜被浓硝酸氧化,作负极,电极反应:
铜:Cu-2e-===Cu2+;
钝化铝:2NO-3+2e-+4H+===2NO2↑+2H2O。
(2)镁铝烧碱溶液电池
镁不溶于烧碱,铝单质可溶于烧碱,铝作负极,镁作正极,电极反应,铝:2Al-6e-+8OH-===2AlO-2+4H2O;
镁:6H2O+6e-===3H2↑+6OH-。
原电池的正极和负极与电极材料的性质有关,也与电解质溶液有关,不要形成活泼电极一定作负极的思维定势。
(1)原电池工作时,正极表面一定有气泡产生(×)
(2)Mg—Al形成的原电池,Mg一定作负极(×)。
