1_2_4-三唑的制备
甲酰胺法合成1H-1,2,4-三氮唑
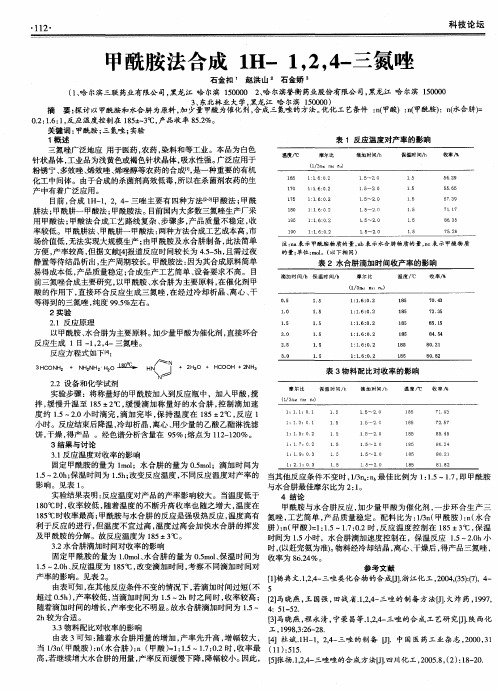
1 8 5 ' 1 2 时收率最高 ; 甲酰胺 与水合肼 的反应是强 吸热反应 , 温度高有 氮唑 , 工艺 简单 , 产品质量稳定 。配料 比为 : l / 3 n ( 甲酰 胺 ) : n ( 水 合 利于反应 的进行 , 但 温度不宜过 高 , 温度过 高会加 快水合肼 的挥发 肼 ) : n ( 甲酸 ) = 1 : 1 . 5~1 . 7 : 0 . 2时 , 反 应温度 控制在 1 8 5 -3 4 " C, 保 温 及 甲酰胺 的分解。故反应温度为 1 8 5 -3 4 o C。 时间为 1 . 5 小时 ,水合肼滴加速度控制在 ,保温反应 1 . 5~2 . 0 h小 3 . 2 水合肼滴加时间对收率的影响 时, ( 以赶完氨为准) 。 物料经冷却结晶 , 离心 、 干燥后 , 得产品三氮唑 , 固定 甲酰胺 的量为 1 . 0 o t o l 、 水 合肼 的量为 0 . 5 m o l 、 保温 时间为 收率为 8 6 . 2 4 %。 1 . 5~ 2 . O h 、 反应温度为 1 8 5  ̄ ( 2 , 改变滴加 时间 , 考察 不同滴加时 间对 参 考 文 献 产率 的影 响。见表 2 。 [ 1 】 杨典文. 1 , 2 , 4 一 三唑类化合物的合成[ J ] . 浙 江化 工 , 2 0 0 4 , ( 3 5 ) : ( 7 ) , 4 — 由表可知 , 在其 他反应条件不变 的情况下 , 若滴加时 间过短 ( 不 5 超过 0 . 5 h ) , 产率较低 , 当滴加 时间为 1 . 5— 2 h时之间时 , 收率较高 ; 【 2 】 马晓燕 , 王 国强 , 田战 省 . 1 , 2 , 4 一 三唑 的制备 方法[ J ] . 火炸药 , 1 9 9 7 , 随着滴加时间的增长 , 产率变化不 明显 。 故水合肼滴加时间为 1 . 5~ 4: 51 - 52. 2 h较为合适 。 【 3 】 马晓燕 , 程 永清 , 宁荣昌等. 1 , 2 , 4 一 三唑 的合 成工 艺研 究[ J ] . 陕西化 3 . 3 物料配 比对收率 的影响 工 , 1 9 9 8 , 3 : 2 6 — 2 8 . 由表 3 可知 : 随着水 合肼用量 的增加 , 产率先 升高 , 增幅较 大 , [ 4 ]杜 斌 . 1 H — l ,2 , 4 一 三唑的制备 [ J 】 .中 国 医药 工 业 杂 志 , 2 0 0 0 , 3 1 当1 / 3 n ( 甲酰胺 ) : n ( 水合肼 ) : n( 甲酸 ) = 1 : 1 . 5—1 . 7 : 0 . 2时 , 收率最 ( 1 1 ) : 5 1 5 . 高, 若 继续增 大水合肼 的用量 , 产率反 而缓慢下降 , 降幅较小 。 因此 , [ 5 】 张扬 . 1 , 2 , 4 一 三唑 唑 的 合 成 方 法 【 J ] . 四川 化 工 , 2 0 0 5 . 8 , ( 2 ) : 1 8 — 2 0 .
4,4′-偶氮-1,2,4-三唑的合成工艺改进

( S D C I ) 为氧化 剂与 4 . 氨 基- 1 , 2 , 4 一 三 唑 进 行 反 应 。2 0 0 7
( 1 .北 京 理 工 大 学 爆 炸 科 学 与技 术 国 家 重 点 实验 室 ,北 京 1 0 0 0 8 1 ; 2 . 中国 白城 兵 器 试 验 中心 ,吉林 白城 1 3 7 0 0 1 ; 3 .北 京航 天 试 验 技 术研 究所 ,北 京 1 0 0 0 7 4 )
摘
和生 成焓 较 高
, 具 有 良好
的爆 轰性 能和 环境 兼容 性 , 是 高 能 密度 材 料 领 域 的研
时间和得 到纯度较高 的产 品 , 2 0 1 0年 , Qi 等… 对该工 艺
进行了改进 , 将乙酸与 S D C I 反应 的时间 由 6 h ( 室温) 缩 短至 1 h ( 3 0 o C) , 虽 然之后 向溶液 中添加 4 - 氨基 - 1 , 2 , 4 一 三唑 的反应 时间一样 ( 1 h ) , 但 后 者 的温 度控 制较 为 复 杂, 先是在 7 c C 下将 4 - 氨基一 1 , 2 , 4 - 三唑溶 于水 中 , 再将 其加人溶液 后在 1 5 q C 下反应 1 h , 最后 还需 在 6 0 o ( = 下 对沉 淀物进行水洗 , 才 能得 到产 品( 收率 为 9 0 %) 。 改进 后 的工艺 虽然 使得 总体 反应 时间 由 7 h缩短 至 2 h , 但 其温 度 的控制更 为复 杂 , 且 产物 还 需 水洗 提 纯, 反应 后 同样会 留下 大量 的废液 ( 异腈 尿 酸 ) 。针对 上 述 问题 , 本 研究 采用 次氯 酸钠 为氧化 剂 , 在恒温 下 与 4 - 氨基一 1 , 2, 4 一 三唑 反应 得 到 A t r z , 并 在不 同的 反应 温 度、 光 照时 间和有 效氯 与 乙酸 的摩尔 比的条 件下 , 探 索 合成 A t r z的最 佳反 应条 件 , 最 后通 过 X . 射线 单 晶衍 射 和 DS C分 析证 明 了其 结构 与文 献 [ 1 1 ] 结果 一致 。
1,2,4三氮唑的合成方法

1,2,4三氮唑的合成方法1,2,4-三氮唑是一种重要的有机化合物,具有广泛的应用价值。
它可以作为农药、染料和荧光物质的中间体,在医药和材料科学领域也具有重要地位。
因此,合成1,2,4-三氮唑的方法备受关注。
本文将介绍几种常见的1,2,4-三氮唑的合成方法。
最常用的合成方法之一是通过氰氨酸和酮的反应来合成1,2,4-三氮唑。
除了氰氨酸和酮的反应外,还可以利用硝化反应合成1,2,4-三氮唑。
首先,将硝基化合物加入反应瓶中,并加入适量的硫酸和硝酸。
随后,加热反应混合物,使其发生硝化反应,生成1,2,4-三氮唑。
这种方法适用于合成不同取代基的1,2,4-三氮唑,但反应条件较为苛刻,需要控制温度和反应时间,以避免副反应的发生。
还可以利用过氧化物的氮氧化反应合成1,2,4-三氮唑。
首先,在反应瓶中加入过氧化氢和氨水,并加热反应混合物。
随后,加入含有亚硝酸根离子的溶液,并继续加热反应。
在反应过程中,亚硝酸根离子将被氧化为氮气,同时生成1,2,4-三氮唑。
这种方法反应条件温和,产率较高,适用于合成不同取代基的1,2,4-三氮唑。
还可以利用氧化反应合成1,2,4-三氮唑。
首先,在反应瓶中加入含有亚硝酸根离子的溶液,并加热反应混合物。
随后,加入含有氧化剂的溶液,并继续加热反应。
在反应过程中,亚硝酸根离子将被氧化为氮气,同时生成1,2,4-三氮唑。
这种方法适用于合成不同取代基的1,2,4-三氮唑,但反应条件较为苛刻,需要控制温度和反应时间。
合成1,2,4-三氮唑的方法多种多样,可以根据具体需求选择合适的合成路线。
无论是氰氨酸和酮的反应、硝化反应、过氧化物的氮氧化反应还是氧化反应,都可以高效地合成1,2,4-三氮唑。
随着对1,2,4-三氮唑的研究深入,相信会有更多新颖的合成方法被开发出来,为其在各个领域的应用提供更多可能性。
哒嗪并[3,2-c]1,2,4-三唑类化合物的合成
![哒嗪并[3,2-c]1,2,4-三唑类化合物的合成](https://img.taocdn.com/s3/m/e3a041e3856a561252d36f97.png)
clrp r aie 3  ̄3 ) hc eeo t n d f m u stt e zn n u c i a h die b hoo yi z s(a d,w i w r bm e r sb tue b n e e ad sci c n y r y d n h o i d n d
No 1。1 8 . 2 6 6 ̄ l91 6
・
研 究简报 -
哒嗪并【,-],,- 32 c1 4三唑类化合物 的合成 2
曹玲华 王彩芳 “ 陶 晶“
天津 307 ) 00 1
(新疆大学化学化工学院 。
乌鲁木齐 8 0 4 ) 3 0 6
(南开大学元素有机化学 国家重点实验室
Ab ta t A e e f p r a io 32c l24 t a oe r y te ie r m y r zd s a d 3ay -- sr c sr s o yi zn [,一] ,,一 iz ls we e s nh sz d fo h d a ie n -r l i d r 6
3氨基5巯基124三氮唑合成工艺

3氨基5巯基124三氮唑合成工艺
3氨基5巯基124三氮唑(3-amino-5-mercapto-1,2,4-triazole)是一种重要的有机合成中间体,广泛应用于农药、药物和染料工业。
以下是一种可能的合成工艺:
1. 取一定量的硫酸铵(NH4HSO4)和硝酸钠(NaNO3),按1:1的摩尔比加入到适量的水中,搅拌溶解。
2. 在搅拌的溶液中加入亚硫酸钠(Na2SO3),用于还原硝酸根离子生成亚硝酸根离子。
同时控制反应pH在4-5之间。
3. 加入3-氨基甲基-5-巯基-1,2,4-三唑(AMT),根据化学反应的需求加入适量的碱(如氢氧化钠)和催化剂(如四乙酸铅)。
4. 反应温度维持在80-100摄氏度,控制反应时间,通常需要几小时至几天的时间。
5. 反应结束后,用酸(如稀盐酸)酸化溶液,产生沉淀。
6. 将沉淀进行过滤,洗涤和干燥,得到3氨基5巯基124三氮唑产物。
需要注意的是,由于化学反应的条件和特性的不同,上述工艺仅供参考,实际的工艺条件可能需要根据具体的实验和设备要求进行调整。
在合成过程中,需要注意安全操作,并遵守相关的实验室规范和操作规程。
4-氨基-1,2,4-三唑的合成

4-氨基-1,2,4-三唑的合成
一、注意事项
甲酸与水合肼(物质的量投放比例最低为1:2)。
116摄氏度蒸馏开始,蒸馏温度最高不能超过200摄氏度,一定要控制好温度而且升温过程要缓慢,在220摄氏度左右将发生4-氨基-1,2,4-三唑的环裂解,所以温度要控制在200摄氏度,温度太低无法发生成环反应。
二、实验步骤
1在冷水浴中向水合肼中慢慢滴加甲酸,控制好时间。
2 滴加完成后将装置改成加热回流装置缓慢升温,每次升温10摄氏度,每次等10分钟,当温度达到105摄氏度时再加热半小时。
3第二步结束后迅速改成蒸馏装置,116摄氏度水合肼和水开始被蒸出。
将温度缓慢升高至200摄氏度后,在200摄氏度下反应4个小时。
加热时间可以适当延长半小时到1小
时。
4 生成的粗品用75毫升乙醇溶解,加入几克活性碳,然后加入同体积的乙醚后放到冰箱内冷却析出结晶。
冷却析出结晶时间可以为一天左右。
5 等析出结晶后进行抽滤得到4-氨基-1,2,4-三唑粗品,并进行真空干燥后真空干燥保存。
(产物吸水性很强)。
1,2,4,三唑的制备

实验项目:1,2,4,-三唑的制备一、目的与要求了解无取代三唑环的合成和应用二、实验原理1,2,4-三唑环中有两个相邻的氮原子,在合成上可以由NH2NH2来提供,通过和其他带有活性基团的化合物如甲酰胺缩合而成。
甲酰胺法是目前工业上生产1,2,4-三唑常有的方法。
另一类方法是通过1mol 的甲酰胺和1mol 甲酰胺环和而成。
但用这种方法,甲酰肼尚有需要由甲酸甲酯肼来制备,路线较长,成本较前类方法为高。
用肼的衍生物(如酰肼)代替肼,可用类似的方法合成取代的三唑化合物。
[应用与发展]由于三唑环上的1位H具有较强的活性,可与许多亲电试剂发生反应。
含三唑环的化合物(以下简称 “三唑” )广泛用于农药,医药,助剂合成的中间体。
农药工业:用于生产高效,内吸,广谱性三唑类杀菌剂,如三唑酮(商品名粉锈宁),三唑醇(又名多效唑,植物生长调节剂和广谱杀菌剂),特效唑(又名烯效唑),Baytan 以及氯甲唑等;还可以合成N取代的烷基三唑(植物生长调节的中间体),双三唑基二苯基甲烷植物生长调节剂;合成杀虫剂(如拟除虫菊酯,氨基甲酸酯等)的增效剂等。
助剂方面:可用于合成1-羟乙基-1,2,4-三唑。
后者可用于作高分子材料的抗静电剂和还氧化树脂的固化剂;用作涂料的添加剂制造防腐涂料;用作合成金属钝化剂于一些功能油、液中,如润滑油、液压系统用液体、金属加工液、变压器及开关油等;还可用作合成纤维质材料的上胶剂或防水剂以及用于造纸和纺织行业。
医药方面:三唑与芳基磺酰氯反应可合成1-芳基磺酰-1,2,4-三唑,它具有抑制中枢神经及降低血糖的药效,可用于防治人体皮肤癣症,疗效很好。
三唑环与乙炔加压反应可合成乙烯基三唑,用于合成高分子化合物。
三唑还可配制铜或铜合金的化学抛光剂,用于装饰品、电气用品和照相机零件的抛光。
三唑亦可用作热塑性塑料的添加剂、金属腐蚀抑制剂及催化剂等。
甲酰胺法3HCONH 2 + NH 2NH 2 .H 2O + 2H 2O + HCOOH + 2NH 3N NHN 180℃三、仪器和试剂1.仪器带机械搅拌回流装置(尾气吸收),蒸馏装置等。
5_甲氧基_4_甲基_1_2_4_三唑啉酮的合成

农 药AGROCHEMICALS 第49卷第8期2010年8月Vol. 49, No. 8Aug. 20105-甲氧基-4-甲基-1,2,4-三唑啉酮的合成苏江涛1,商志良2(1.湖北工业大学 生物工程学院制药工程系, 武汉 430068; 2.常州黄隆化工有限公司,江苏 常州 213022)摘要:5-甲氧基-4-甲基-1,2,4-三唑啉酮是新型磺酰脲类除草剂氟酮磺隆的关键中间体;为了简化工艺条件,降低生产成本,报道了新的合成方法。
以氯甲酸乙酯和硫氰化钠为起始原料,经过取代、S -甲基化、环化和N -甲基化4步反应得到目标化合物。
以上各步反应收率在50%~85%之间。
中间体及标题化合物的结构经过熔点、1H NMR 和MS 确证。
该合成路线具有成本低、操作安全、易工业化生产的优点。
关键词:氟酮磺隆;磺酰脲类除草剂;中间体 中图分类号:TQ460.3 文献标志码:A 文章编号:1006-0413(2010)08-0563-02Synthesis of 5-Methyoxy-4-methyl-3H -1,2,4-triazol-3-oneSU Jiang-tao 1, SHANG Zhi-liang2(1.Bioengineeg Institute, Hubei University of Technology, Wuhan 430068, China;2.Changzhou Sulfuron Chemical Co., Ltd., Changzhou 213022, Jiangsu, China)Abstract: 5-Methyoxy-4-methyl-3H -1,2,4-triazol-3-one is the key intermediate for preparing sulfonylurea herbicides-flucarbazone. In order to simplify technological conditions and reduce production costs, a new synthesis route was reported by us. Starting from ethyl chloroformate and sodium thiocyanate, the target compound was obtained by four steps of substitution, S -methyl-ation, cyclization and N -methylation. The yields of all steps was at 50-85%; the intermediates and title compound were con fi rmed by MS, 1H NMR. This method had adventage of low cost, safe operation and suitable for industrial production.Key words: flucarbazone; sulfonylurea herbicides; intermediate氟酮磺隆(flucarbazone)是拜耳公司开发的磺酰胺基羰基三唑啉酮类除草剂,其作用机理与其他磺酰脲类除草剂一样是乙酰乳酸合成酶(ALS)抑制剂,氟酮磺隆适合作物为小麦,对下荐作物安全,主要用于防除小麦田禾本科杂草和一些重要阔叶杂草,对野燕麦和狗尾草等杂草有很好防效。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工与生物技术学院
综合与设计性化学实验实验类型:设计
实验题目:1,2,4-三唑的制备
班级:轻化1101班学号:11140131 姓名:徐得欢实验日期:
1,2,4,-三唑的制备
目的与要求
了解无取代三唑环的合成和应用
了解无取代三唑环的合成和应用;
了解文献资料的收集和整理;
学会对实验数据的处理和分析。
一,前言
1.2.4一三唑类化合物具有广泛的生物活性,如抗菌lll、消炎l 2l、抗癌_3j等。
Catheyl4j指出,含有C—C—N—N骨架的有机分子对植物有促进生长的作用。
Pathok等指出1.2.4一三唑硫醚类的抗菌性比硫醇类高[5I。
考虑到羟基等基团能增加分子水溶性及负电性、有可能提高药物活性。
二、实验原理
1,2,4-三唑环中有两个相邻的氮原子,在合成上可以由NH2NH2来提供,通过和其他带有活性基团的化合物如甲酰胺缩合而成。
甲酰胺法是目前工业上生产1,2,4-三唑常有的方法。
另一类方法是通过1mol的甲酰胺和1mol甲酰胺环和而成。
但用这种方法,甲酰肼尚有需要由甲酸甲酯肼来制备,路线较长,成本较前类方法为高。
用肼的衍生物(如酰肼)代替肼,可用类似的方法合成取代的三唑化合物,。
3HCONH2 + NH2NH2 .H2O + 2H2O + HCOOH + 2NH3 N N HN 180℃(甲酰胺沸点:210℃水合肼的沸点118.5℃)。
三、仪器和试剂
1.仪器
带机械搅拌回流装置(尾气吸收),蒸馏装置等。
2.试剂
水合肼(C.P.80%或工业品),甲酰胺(C.P.99.5%或工业品),无水乙醇。
四、实验步骤
1、1,2,4_三唑制备
将86g(1.9mol)甲酰胺和5.22g(0.1mol)甲酸加入四颈瓶,加热至180℃,保持温度170-185℃边搅拌边滴入63g(1.0mol)85%的水合肼(当温度低于170℃
时,改滴加装置为蒸馏装置,蒸出反应生成的低沸点物质水),滴加时间约为1.5h。
加完后,在180℃下继续搅拌反应30min。
将反应物冷却至130-140℃出料,将反应物用冰水混合物冷却静置,有大量晶体生成。
2、乙醇重结晶
量取无水乙醇1ml加入磨口三角瓶中,加入粗产品,震荡、摇匀。
用水浴加热,如没有溶解完全补加少量乙醇,直至完全溶解。
置于冰水混合物中冷却静置,抽滤。
得重结晶产物。
五、实验记录
六、实验结果与讨论
1.产率=(46.6/7
2.08g)×100%=64.65%
2.加入水合肼后温度降低是因为与甲酰胺形成共沸,致使温度一直在140℃左右,这也是产率偏低的原因之一,因为反应在180℃时产率最高。
本次在加入水合肼时速度较快,少于2个小时,但是产品颜色纯正。
3.在两次过滤时,加入过多的水,导致部分产物溶解损失。
七.实验心得
1.反应中,甲酰胺既是反应物,同时还是溶剂,所以甲酰胺一般是过量的。
但甲酰胺用量太多不但不能提高最终产品1,2,4-三唑的得率,反而会使其得率有所下降。
因为甲酰胺沸点较高(常压下200C),还可以溶解部分1,2,4-三唑。
常压下采用蒸馏方法除去过剩的甲酰胺需要很高温度,一般采用抽真空减压蒸馏的方法,工艺条件苛刻。
况且1,2,4-三唑自身还有升华现象,所以无论高温或抽真空蒸除去过剩溶剂都会使产品得率下降。
不但如此,升华的1,2,4-三唑再冷却后会堵塞管道,给工业生产带来诸多不便。
本实验力图做到在不影响产品得率的同时将甲酰胺用量减到最低。
减少甲酰胺用量会给生产带来许多好处。
第一,产品分离不再采取减压蒸馏的方法,只需冷却过滤即可得粗产品;第二,甲酰胺价格较贵,减少用量,也可降低1,2,4-三唑的生产成本。
2.加料温度控制:加料温度也是反应的关键。
经实验研究表明,在温度低于16O℃时,反应进行得很缓慢,同样保温30min得率要低得多。
当把温度升到175℃~185℃时,得率大大提高。
所以,反应必须在180~185℃之间进行。
当然,温度太高时,甲酰胺、甲酰肼会分解,不利于反应进行。
3.在反应装置上,增加产物的蒸馏装置,在滴加甲酰肼的同时,将反应生成的水等副产物蒸馏出反应瓶是缩短加料时间和保温时间的一个关键的措施。
在反应进行的同时,蒸馏出低沸点的副产物,才能保证加料温度不致下降,提高反应得率。
