天津大学:化学工艺学
《天津大学化工设计》课件

职业卫生与安全防护措施
职业卫生措施
确保工作场所符合国家和地方的职业卫生标准,采取有效的 通风和换气措施,减少有害物质的产生和积累,提供个人防 护用品,定期进行职业健康检查。
安全防护措施
建立健全的安全管理制度和操作规程,对员工进行安全培训 和教育,提供完备的安全设施和个体防护装备,定期进行安 全检查和隐患排查。
05
环保与安全设计
环保设计理念与原则
环保设计理念
在化工设计中,应遵循绿色、低碳、循环的理念,通过减少资源消耗、降低环 境污染、提高资源利用效率等方式,实现可持续发展。
环保设计原则
遵循国家和地方的环保法律法规,采用清洁生产技术和工艺,减少废气、废水 、废渣的排放,合理利用能源和资源,确保化工生产与环境保护相协调。
安全可靠
设备应具备必要的安全保护装 置和措施,保证操作人员的安 全和生产的可靠性。
易于维护
设备的结构应简单明了,便于 安装、操作和维护,降低维修
成本。
典型化工设备设计
反应器设计
反应器是化工生产中的重要设备 之一,设计时应考虑反应速度、 温度、压力等工艺参数,以及设
备的结构、材料和安全性能。
塔器设计
详细描述
化工设计是化学工业发展的核心环节,它决定了企业的生产能力和产品质量。一个优秀的设计能够提 高生产效率、降低能耗和减少环境污染,为企业带来巨大的经济效益和社会效益。同时,化工设计也 是实现可持续发展的重要手段,通过节能减排和资源循环利用,推动企业绿色发展。
化工设计的流程
• 总结词:化工设计的流程包括工艺流程设计、设备设计与选型、管道设
通过模拟可以预测实际生产中的各种情况,为优化提 供依据和支持。
工艺流程模拟的方法
天津大学 化学工艺导师 姜浩锡

天津大学化工学院硕士生导师——姜浩锡职称:副研究员职务:副研究员导师类型:硕士生导师(硕导)专业:化学工艺联系电话: +86(0)22-27406119传真: +86(0)22-27406119通讯地址:电子信箱:hxjiang@主要教育经历1998-2003,天津大学化工学院工业催化专业,获工学博士学位。
1992-1995,天津大学化工学院有机化工专业,获工学硕士学位。
1983-1987,天津大学化工学院工业催化专业,获工学学士学位。
主要研究方向:应用催化,超临界流体技术目前承担的主要科研项目应用催化:乙醇一步法制备乙酸乙酯工业催化剂开发合作开发回收烯烃制取化工产品技术集成项目催化剂开发分项超临界流体技术:国家自然科学基金:具有纳米晶结构的MnOx-CeO2 中空纳米球催化剂合成调控机制研究天津市自然科学基金:纳米晶Cu-Ce-Zr复合氧化物催化剂的SAS制备研究代表性论著及专利论文论著:1. 超临界抗溶剂法纳米Al2O3-ZrO2颗粒的制备与表征,无机材料学报2010, l. 25(10):1065-10702. 超临界抗溶剂法制备纳米氧化铝颗粒,催化学报,2007, 28(10):890-8943. Two Kinds of Active Sites on Cu Cr Catalysts for the Dehydrogenation of Ethanol to Ethyl Acetate, The 4th International conference on green and sustainablechemistry &2nd Asia Oceanian conference on green sustainable chemistry,20094. Preparation and characterization of nano-crystalline Cex-Zr1-x-O2 catalyst by SAS, 9th International Symposium on Supercritical Fluids, 20085. Design and preparation of nano-particles by SAS, China-France Workshop on the Application of Supercritical Fluids Technology, 2008授权专利:1. 一种烷烃氧化催化剂及其制备方法, CN11911582. 用于生产顺丁烯二酸酐的钒-磷-锆混合氧化物催化剂的制备方法, CN1067189。
天津大学好的专业排名

天津大学好的专业排名天津大学好的专业排名1化学工程与工艺专业培养目标:本专业培养具备化学工程与化学工艺方面的知识,能在化工、炼油、冶金、能源、轻工、医药、环保和军工等部门从事工程设计、技术开发、生产技术管理和科学研究等方面工作的工程技术人才。
主要课程:物理化学、化工原理、化学反应工程和一门必选的专业方向课程。
就业方向:化学工程与工艺专业学生毕业后可在食品、医药、能源、环保等领域从事生物产品的研制、生产,同时可到高等院校、设计和研究单位从事教学、科研、生产、管理等方面的工作。
在教育部的高校学科排名中,天津大学的化学工程连续多年位居第一,应用化学、制药等与化工关系紧密的学科也十分强劲。
国家重点化学工程联合实验室、精馏技术国家工程中心、发酵技术国家工程研究中心和国家化工填料塔及塔内件技术、工业结晶技术推广中心等国家基地,这些都足以说明天大化工之强大。
在科学院士余国琮、张春霆,工程院士王静康、沈家祥和双聘院士刘昌孝、邹竞、吴祖泽及美国工程院院士rson、俄罗斯工程院院士RuryBreslav等国内外知名的学者的带领下,天津大学化工的实力傲视群雄。
2测控技术与仪器专业培养目标:本专业培养具备精密仪器设计制造以及测量与控制方面基础知识与应用能力,能在国民经济各部门从事测量与控制领域内有关技术、仪器与系统的设计制造、科技开发、应用研究、运行管理等方面的高级工程技术人才。
主要课程:精密机械与仪器设计、精密机械制造工程、模拟电子技术基础、数字电子技术基础,微型计算机原理与应用、控制工程基础、信号分析与处理、精密测控与系统等。
就业方向:测控技术与仪器专业毕业生主要到国民经济各部门从事测量与控制领域内有关技术、仪器与系统的设计制造、科技开发、应用研究、运行管理等方面的工作。
叶声华院士率领的天津大学测控技术与仪器专业在全国数一数二,甚至略强于清华。
精密测试技术及仪器国家重点实验室就坐落于此。
3光电信息科学与工程专业就业方向:光电信息科学与工程专业学生毕业后在科研院所、相关公司、企业从事产品研发、质量管理工作的光电子和光信息专业的工程技术人员;中等专业学校、技校、高等职业学校教师;各相关企事业单位技术及管理人员和政府机关、事业单位公务员及继续攻读硕士学位。
化学工程与工艺专业核心课程21页PPT

每个单元 操作过程布置 1~2个综合性 强、结合工程 实际的课外作 业,提高学生 的综合和工程 能力。
考试方法
试题分为 客观题和综合 题,客观题侧 重对学生基础 知识考核;综 合题侧重对学 生综合能力考 核。
16
化 工 原 理 及 实 验
课程教改及建设情况
课程教学的改革
双语教学
实物教学
课程竞赛
认识实习
有利于培养创新 人才的化工原理 及实验课程体系 和教学内容、教 学方法、教学手 段的改革与实践
天津大学 教改项目
化工原理课 程建设
化工基础实 验课程建设
14
课程教改及建设情况
化 工
课程体系的改革
原
为培养创新人才的需要,对《化工原理》课
理 及 实
程体系进行了改革。将几门相关课程的内容重新 整合,建立了新的课程体系,并根据不同专业的 需要,开设了两类不同体系的课程,使得课程体 系更具科学性、先进性和适用性。
类别
学分 比例
A. 人类和社会科学类
36.5
21%
B. 数学和自然科学类
40.5
23%
C. 学科基础和专业类
90
50%
D. 训练和健康类 E. 创新与研修类
9.5
5%
4
2%
总学分:179.5
6
C. 学科基础和专业类
工程科学(学科基础,必修+选修)
专业核心课程 专业选修课程 课程设计,实习
必修 33.0学分 选修 6.0学分
课程
化工分离工程 化工传递过程 化学工艺学 化工数学 化工设计 合计
学分
2.5 2 2.5 3 2 12
天津市 精品课
程
化学工程与工艺专业解析,报考指南及就业方向

化学工程与工艺专业解析,报考指南及就业方向当我第一遍读一本好书的时候,我仿佛觉得找到了一个朋友;当我再一次读这本书的时候,仿佛又和老朋友重逢。
我们要把读书当作一种乐趣,并自觉把读书和学习结合起来,做到博览、精思、熟读,更好地指导自己的学习,让自己不断成长。
让我们一起到店铺一起学习吧!今天为大家解读——化学工程与工艺中文名:化学工程与工艺修学年限:4年授予学位:工学学士一级学科:工科化学工程与工艺专业培养具备化学工程与化学工艺方面的知识,能在化工、炼油、冶金、能源、轻工、医药、环保和军工等部门从事工程设计、技术开发、生产技术管理和科学研究等方面工作的工程技术人才。
该专业具有两大特色,一是工程特色显著,对化学反应、化工单元操作、化工过程与设备、工艺过程系统模拟优化等知识贯穿结合,使学生具有设计、优化与管理能力;二是专业口径宽、覆盖面广,使学生具有从事科学研究、产品开发的能力,在精细化学品、涂料及应用、高分子化工与工艺等方面更有研发和应用能力。
培养要求:该专业学生主要学习化学工程学与化学工艺学等方面的基本理论和基本知识,受到化学与化工实验技能、工程实践、计算机应用、科学研究与工程设计方法的基本训练.具有对现有企业的生产过程进行模拟优化、革新改造,对新过程进行开发设计和对新产品进行研制的基本能力。
毕业生应获得以下几方面的知识和能力:1、掌握化学工程、化学工艺、应用化学等学科的基本理论、基本知识;2、掌握化工装置工艺与设备设计方法,掌握化工过程模拟优化方法;3、具有对新产品、新工艺、新技术和新设备进行研究、开发和设计的初步能力;4、熟悉国家对于化工生产、设计、研究与开发、环境保护等方面的方针、政策和法规;5、了解化学工程学的理论前沿,了解新工艺、新技术与新设备的发展动态;6、掌握文献检索、资料查询的基本方法,具有一定的科学研究和实际工作能力。
主要课程主干学科:化学、化学工程与技术。
主要课程:物理化学、化工原理、化学反应工程和一门必选的专业方向课程。
天津大学化工学院化学工程专业导师研究方向介绍
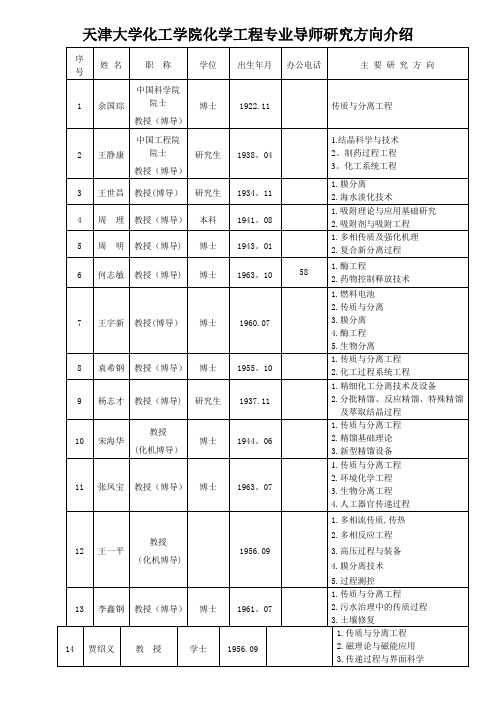
38 李凭力 副研究员
博士 1961。12
39 王化淳 研究员
学士 1944。01
40 汪宝和 副研究员
硕士 1964。09
41 宋光复 研究员
学士 1945。07
42 刘 成
副教授
硕士 1964。11
43 高瑞昶 副研究员
博士
1965.12
2.海水淡化 1.传质与分离工程 2.非牛顿流体中的气泡行为及 传质特性 3。新分离技术 4。化工热力学及流体力学 1.现代传质理论 2.复合新分离过程 1.酶工程 2.制药工程 1.传质与分离工程 2.双膜萃取技术 3.精细化工 1.传质过程 2.计算流体力学 3.多级分离 1.传质与分离工程 2.精细化工产品及其新分离过
强化。 2.分子印迹(合) 1。环境水化学 2.微量元素物理化学 1. 传质与分离工程 2. 环境化学工程 3. 化工热力学基础数据 1。膜分离技术
2。海水淡化技术
57 王纪孝 副教授
博士
196404
58 齐崴
副教授
博士
1973.09
59 徐世昌 副研究员
硕士 1966。12
60 崔现宝 副教授
博士 1971。11
1.酶工程
58
2.药物控制释放技术
1.燃料电池 2.传质与分离 3.膜分离 4.酶工程 5.生物分离 1.传质与分离工程 2.化工过程系统工程 1.精细化工分离技术及设备 2.分批精馏、反应精馏、特殊精馏
及萃取结晶过程 1.传质与分离工程 2.精馏基础理论 3.新型精馏设备 1. 传质与分离工程 2. 环境化学工程 3. 生物分离工程 4.人工器官传递过程
天津大学化工学院化学工程专业导师研究方向介绍
序 姓名
天津大学 化工导论 第六章 化学工程与工艺的科学基础PPT课件

标题添加
点击此处输入相 关文本内容
标题添加
点击此处输入相 关文本内容
总体概述
点击此处输入 相关文本内容
点击此处输入 相关文本内容
2
第六章 化学工程与工艺的科学基础
化学工业中存在着千变万化 的各种化学加工过程,即化工过 程。化工过程中不仅包含化学变 化的过程,而且还包含分离混合 物为较纯净的不同组分以及改变 其物理状态和性质的各种过程。
两方面,一是对化学反应规律的 研究,二是对反应器中传递规律 的研究。
25
2、化学反应的操作方式
(1)间歇式操作 (2)连续式操作
3、反应器的形式
(1)釜式反应器 (2)固定床放应器 (3)流化床反应器
26
27
28
29
30
31
第三节 化工过程控制
1、化工过程控制的目的
化工过程控制的目的在于保证化工 装备平稳运行、从而使生产过程平稳、 多出合格产品。
第六章化学工程与工艺的科学基础大规模装置15万吨年此装置有六台结晶器此规模中显示出其中的两台在某现有装置中进行一台结晶器的安装馏结合用于分离萘及其衍生物1322152318242325化工过程控制的目的在于保证化工装备平稳运行从而使生产过程平稳多出合格产品
现代化工导论
第六章 化学工程与工艺的科学基础
3
在某现有装置中进 行一台结晶器的安装
大规模装置(15万吨/年)
此装置有六台结晶器,此规 模中显示出其中的两台
4
结晶与精 馏结合用于 分离萘及其 衍生物
5
第一节 化工单元操作及设备
1、单元操作的概念 任何化工过程无论规模大小,都可
以分为一系列基本操作,如流体输送、 过滤、加热、冷却、蒸馏、萃取等等。 单元操作就是按照特定要求使物料发 生物理变化的这些基本操作的总称。
化工传递过程基础全部

一、课程发展简介
●第一部关于化工单元操作的专著: “Principles of Chemical Engineering”(1923年) ●单元操作又名:“化工原理”、“化工过程 及设备”或“化学工程”。
Hale Waihona Puke 一、课程发展简介3.传递过程阶段(1960年至今)
●根据单元操作的原理分类,单元操作最终都可 以归结为动量、热量和质量的传递。
发生由高速层向低速层的动量传递。
动量传递方向
u1 u2
一、平衡过程与速率过程
2. 热量传递过程—当物系中各部分之间的温度存 在差异时,则发生由高温区向低温区的热量传递。
t1> t2> t3
热流方向 t1 t2 t3
一、平衡过程与速率过程
3. 质量传递过程—当物系中的物质存在化学势差 异时,则发生由高化学势区向低化学势区域的质量 传递。
化学势的差异可以由浓度、温度、压力或电场力 所引起。最常见的是浓度差引起的质量传递过程。 此时混合物中的某个组分由高浓度向低浓度区扩散 传递。
一、平衡过程与速率过程
3. Welty J R, Wicks C E, Wilson R E, Fundamentals of Momentum, Heat and Mass Transfer,2001
4. Bennett C O, Myers J E, Momentum, Heat and Mass Transfer,2001
四、课程研究方法及参考书
●教材
陈涛,张国亮,化工传递过程基础,北京:
化学工业出版社,2001
四、课程研究方法及参考书
●参考教材
1. 王绍亭,陈涛,动量、热量与质量传递 , 1987
2. Bird R B, Stewart S E, Lightfoot E N ,Transport Phenomena,2001
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课后习题思考题(第一章)1现代化学工业的特点是什么?2化学工艺学的研究范畴是什么3简述石油化工原料乙烯的用途?4利用合成气可以合成哪些产品?思考题(第二章)1为什么说石油、天然气和煤是现代化学工业的重要原料资源?它们的综合利用途径有哪些?2生物质和再生资源的利用前景如何?3何谓化工生产工艺流程?举例说明工艺流程是如何组织的。
4何谓循环式工艺流程?它有什么优缺点?5何谓转化率?何谓选择性?对于多反应体系,为什么要同时考虑转化率和选择性两个指标?6催化剂有哪些基本特征?它在化工生产中起到什么作用?在生产中如何正确使用催化剂?7在天然气开采中,有时可获得含有C6~C8烃类的天然汽油,为了改善其辛烷值,用蒸馏塔除去其中的轻组分。
如果天然汽油、塔顶馏出物和塔底中等辛烷值汽油的摩尔百分数组成为:物料名称天然汽油中等辛烷值汽油塔顶馏出物1.C6H14250602.C7H162521.5303.C8H185078.510假设它们的密度为0.8g/cm3,那么,从5000桶天然汽油中能生产出多少吨中等辛烷值汽油?(1桶=42US加仑,1US加仑=3.78541dm3,1dm3=103cm3)8某蒸馏柱分离苯-甲苯混合物,其质量组成各占50%,进料流量为10000kg/d,从柱顶冷凝器回收的产品含95%苯;柱底馏出物含95%甲苯。
离开柱顶进入冷凝器的产物蒸气流量是8000kg/d,全部冷凝为液体后,部分产品作为回流液返回蒸馏柱的上部,其余取出即为产品。
求回流与取出产品量之比。
在一个加氢裂化器中,较大分子烃经加氢裂解成较小分子烃。
已知输入和输出的烃类组成为:a)烃类输入输出b)C5H1210mol%c)C6H1440mol%d)C7H1620mol%e)C12H26100mol%30mol%(1)每100kmol原料烃可生产出多少C5~C7烃产品?(2)每100kmol原料烃消耗多少氢气?(3)如果原料烃的密度是0.9g/cm3,输出烃的密度是0.8g/cm3,那么每输出10m3的烃物料需要输入多少m3原料烃?9假设某天然气全是甲烷,将其燃烧来加热一个管式炉,燃烧后烟道气的干基摩尔组成为86.4%N2、4.2%O2、9.4%CO2。
试计算天然气与空气的摩尔比,并列出物料收支平衡表。
10在高温下裂解天然气可获得炭黑和含氢的裂解气。
已知天然气的体积组成为82.3%CH4、8.3%C2H6、3.7%C3H8和5.7%N2,产生的炭黑可以视为纯碳,裂解气含60.2%H2、23.8%CH4、2.2%C2H6、6.5%C2H4、1.4%C3H6、2.3%C2H2和3.6%N2。
计算每100标准m3的天然气可生产多少千克炭黑和多少标准米3的裂解气。
11某燃料气含有30%CS2、26%C2H6、14%CH4、10%H2、10%N2、6%O2和4%CO,与空气一起燃烧,产生的烟道气含有3%SO2、2.4%CO,其余为CO2、H2O、O2和N2。
求空气的过剩百分数。
12一氧化碳与水蒸气发生的变换反应为CO+H2O==CO2+H2,若初始混合原料的摩尔比为H2O/CO=2/1,反应在500℃进行,此温度下反应的平衡常数4.88。
求反应后混合物的平衡组成和CO的平衡转化率。
13合成甲醇的反应为CO+2H2=CH3OH,如果初始原料混合物中H2/CO=2/1,反应温度为350℃,压力为300×105Pa,在此条件下,平衡常数1.18×10-14Pa-2。
那么,CH3OH的平衡浓度(体积%)为多少?14将纯乙烷进行裂解制取乙烯,已知乙烷的单程转化率为60%,若每100kg进裂解器的乙烷可获得46.4kg乙烯,裂解气经分离后,未反应的乙烷大部分循环回裂解器(设循环气只是乙烷),在产物中除乙烯及其它气体外,尚含有4kg乙烷。
求生成乙烯的选择性、乙烷的全程转化率、乙烯的单程收率、乙烯全程收率和全程质量收率。
思考题(第三章)1根据热力学反应标准自由焓和化学键如何判断不同烃类的裂解反应难易程度、可能发生的裂解位置及裂解产物;解释烷烃、环烷烃及芳烃裂解反应规律,造成裂解过程结焦生炭的主要反应是哪些?2试以丙烷裂解为例,阐述烃类裂解的自由基反应机理,计算600℃,700℃,800℃,900℃,1000℃下,丙烷裂解生成物中乙烯和丙烯比例(假设无其它副反应发生)。
并绘出裂解温度—乙烯(丙烯)组成的曲线。
3在原料确定的情况下,从裂解过程的热力学和动力学出发,为了获取最佳裂解效果,应选择什么样的工艺参数(停留时间、温度、压力…),为什么?4提高反应温度的技术关键在何处,应解决什么问题才能最大限度提高裂解温度?5为了降低烃分压通常加入稀释剂,试分析稀释剂加入量确定的原则是什么?6试讨论影响热裂解的主要因素有哪些?评价裂解过程优劣的目标函数(指标)是什么?7Lummus公司的SRT型裂解炉由I型发展到VI型,它的主要改进是什么?采取的措施是什么?遵循的原则是什么?你大胆的设想下一步将怎么改?8裂解气出口的急冷操作目的是什么?可采取的方法有几种,你认为哪种好,为什么?若设计一个间接急冷换热器其关键指标是什么?如何评价一个急冷换热器的优劣?9裂解气进行预分离的目的和任务是什么?裂解气中要严格控制的杂质有哪些?这些杂质存在的害处?用什么方法除掉这些杂质,这些处理方法的原理是什么?10压缩气的压缩为什么采用多级压缩,确定段数的依据是什么?11某乙烯装置采用低压法分离甲烷,整个装置中需要的最低冷冻温度为-115℃,根据乙烯装置中出现的原料、产品,设计一个能够提供这样低温的制冷系统,绘出制冷循环示意图。
并标以各蒸发器和冷凝器的温度(第一级冷凝器温度,为冷却水上水温度25~30℃)。
12裂解气分离流程各有不同,其共同点是什么?试绘出顺序分离流程、前脱乙烷后加氢流程,前脱丙烷后加氢流程简图,指出各流程特点,适用范围和优缺点。
13甲烷塔操作压力的不同,对甲烷塔的操作参数(温度、回流比…)、塔设计(理论板数,材质…),即未来的操作费用和投资有什么影响?14对于一已有的甲烷塔H2/CH4对乙烯回收率有何影响?采用前冷工艺对甲烷塔分离有何好处?15何为非绝热精馏,何种情况下采用中间冷凝器或中间再沸器,分析其利弊。
16根据本章所学知识,试设计一个简单的流程表述烃类热裂解从原料到产品所经历的主要工序及彼此的关系。
17近年来乙烯工业的主要发展方向和研究开发的热点是什么?思考题(第四章)1简述芳烃的主要来源及主要生产过程。
2芳烃的主要产品有哪些?各有何用途?3试论芳烃转化的必要性与意义,主要的芳烃转化反应有哪些?4试分析我国与美国、日本的芳烃生产各有何特点及其原因。
5简述苯、甲苯和各种二甲苯单体的主要生产过程,并说明各自的特点。
6简述芳烃生产技术的新进展及其主要特征。
7如何理解芳烃生产、转化与分离过程之间的关系,试组织两种不同的芳烃生产方案。
思考题(第五章)1有哪些原料可生产合成气?合成气的生产方法有哪些?近年来出现哪些生产合成气的新方法?它们与原有生产方法相比有什么优点?2合成气可用来制造什么化工产品?为什么近年来合成气的生产和应用受到重视?3以天然气为原料生产合成气过程有哪些主要反应?从热力学角度考虑,对反应条件有哪些要求?从动力学考虑又有哪些要求?4如何根据化学热力学、化学动力学原理和工程实际来优化天然气-水蒸气转化制合成气的工艺条件?5天然气-水蒸气转化法制合成气过程有哪些步骤?为什么天然气要预先脱硫才能进行转化?用哪些脱硫方法较好?6为什么天然气-水蒸气转化过程需要供热?供热形式是什么?一段转化炉有哪些型式?7为什么说一段转化管属于变温反应器?为什么天然气-水蒸气转化要用变温反应器?8为什么转化炉的对流室内要设置许多热交换器?转化气的显热是如何回收利用的?9由煤制合成气有哪些生产方法?这些方法相比较各有什么优点?比较先进的方法是什么?10一氧化碳变换的反应是什么?影响该反应的平衡和速度的因素有哪些?如何影响?为什么该反应存在最佳反应温度?最佳反应温度与哪些参数有关?11一氧化碳变换催化剂有哪些类型?各适用于什么场合?使用中注意哪些事项?12在合成气制造过程中,为什么要有脱碳(CO2)步骤?通常有哪些脱碳方法,各适用于什么场合?13工业上气体脱硫有哪些方法,各适用于什么场合?14由渣油制合成气过程包括哪几个步骤?渣油气化的主要设备是什么,有何结构特点?思考题(第六章)1加氢反应和脱氢反应对催化剂有什么要求?2以媒为原料和以天然气为原料合成氨生产过程有什么不同之处?3试分析比较合成气的三种精制方法。
4氨合成反应的平衡常数Kf随温度和压力是如何变化的?5影响氨平衡浓度的因素有哪些?6温度和压力对氨合成反应的平衡氨浓度及反应速率的影响。
7惰性气体对氨合成反应的平衡浓度及反应速率的影响。
8氨合成催化剂活性组分与助剂的作用。
9在氨合成工艺流程中,排放气为什么在循环压缩机前,而氨冷则在循环压缩机之后?10从节能和提高经济效益出发,氨合成塔结构应如何改进?11合成氨与合成甲醇有哪些相似的地方?12高低压合成甲醇的比较。
13根据热力学分析,合成甲醇应在低温(<100℃,Kf值大)和高压下(>30MPa,推动力大)更为有利,工业上为什么不采用此工艺条件?14乙苯脱氢制苯乙烯生产过程中温度和空速对选择性的影响。
15苯乙烯生产中,外热式工艺与绝热式工艺有什么不同?思考题(第七章)1了解氧化过程的作用及其特点。
2分析催化自氧化反应的特点并给出在化工应用中的实例。
3了解络合催化氧化原理及其在Wacker反应中的应用。
4间接氧化法生产环氧丙烷的原理和使用的催化剂是什么?5间接氧化法生产环氧丙烷过程中主反应器是什么类型?为什么这样选择?6比较分析非均相催化氧化和均相催化氧化的特点。
7了解重要的非均相催化氧化类型并举出实例。
8非均相催化氧化反应机理有几种?各自描述的特点是什么?9典型的气—固相催化氧化常见的反应器类型有哪几种?各自的优缺点是什么?10了解绿色化学及清洁生产概念,就氧化反应举例说明。
11掌握乙烯环氧化制环氧乙烷的原理、催化体系和反应主流程。
12乙烯环氧化反应工艺条件选择的依据是什么?13致稳气的作用是什么?14掌握丙烯氨氧化制丙烯腈的原理、催化体系和反应主流程15通过丙烯氨氧化Bi—Mo—Fe多元氧化物催化剂,了解各组分的相互作用。
16丙烯氨氧化制丙烯腈工艺参数选择的依据是什么?17了解共沸精馏的原理及其在丙烯腈精制过程中的应用。
18从原料的来源和价格,谈谈丙烷氨氧化制丙烯腈的前景。
19了解苯酐生产的基本原理和催化体系的构成及工艺技术走向。
20试从原子经济性的角度论述苯酐生产原料的取舍。
21从苯酐的精制过程,理解精制方法选择的重要性。
