高一必修二化学能与电能练习题(带答案详解)
人教版高中化学必修2第二章第二节化学能与电能综合练习(含答案解析)

《化学能与电能》综合练习1.我国首创的海洋电池以铝板为负极、铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。
电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是()A.正极反应式为:O2+2H2O+4e-=4OH-B.电池工作时,电流由铝电极沿导线流向铂电极C.以网状的铂作正极,可增大与氧气的接触面积D.该电池通常只需要换铝板就可继续使用2.已知金属锈蚀的原理是在潮湿空气中金属表面形成水膜,金属与杂质和水膜中溶解的电解质组成原电池,从而使金属锈蚀加快,下列制品的镀层损坏后,金属腐蚀速率最快的()A.镀铝塑扣B.食品罐头盒(镀锡铁盒)C.白铁水桶(镀锌)D.镀银铜质奖章3.随着人们生活质量的不断提高,废旧电池必须进行集中处理的问题被提到了政府的议事日程,其主要原因是()A.回收废旧电池中的石墨电极材料B.回收废旧电池外壳的金属材料C.防止废旧电池中渗漏的电解液腐蚀其他物品D.防止电池中汞、镉和铅等重金属元素对土壤和水源的污染4.如下图所示装置中,可观察到电流计指针偏转,M棒变粗,N棒变细。
下表所列M、N、P物质中,可以组合成该装置的是()选项M N PA 锌铜稀硫酸B 铜铁稀盐酸C 银锌硝酸银溶液D 锌铁硝酸铁溶液5.下列关于原电池的叙述正确的是()A.构成原电池的正极和负极必须是两种不同的金属B.原电池是将化学能转变为电能的装置C.在原电池中,电子流出的一极是负极,该电极被还原D.原电池放电时,电流的方向是从负极到正极6.一种新型燃料电池,一极通入空气,另一极通入丁烷(C4H10)气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下传导O2-。
下列对该燃料电池的说法中正确的是()A.在熔融电解质中O2-由负极移向正极B.C.通入空气的一极是正极,电极反应式为:O2+4e-=2O2-D.通入丁烷的一极是正极,电极反应式为:C4H10+26e-+13O2-=4CO2+5H2O7.在如下图所示的装置中,a在金属活泼性顺序表中排在氢的前面,b为碳棒,关于此装置的下列叙述不正确的是()A.碳棒上有气体放出,溶液pH变大B.a是正极,b是负极C.导线中有电子流动,电子从a极流到b极D.a极上发生了氧化反应8.写出下列原电池的电极反应式和总反应的化学方程式。
人教版化学必修2化学能与电能练习题100题(含解析答案)10
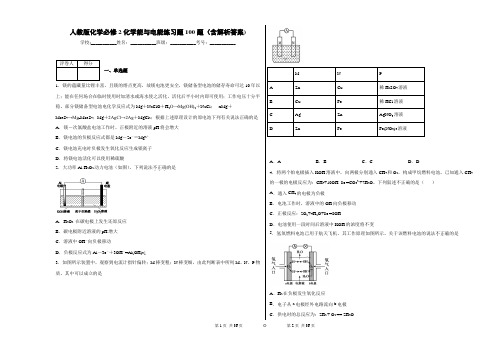
人教版化学必修2化学能与电能练习题100题(含解析答案)学校:___________姓名:___________班级:___________考号:___________一、单选题1.镁的蕴藏量比锂丰富,且镁的熔点更高,故镁电池更安全,镁储备型电池的储存寿命可达10年以上;能在任何场合在临时使用时加清水或海水使之活化,活化后半小时内即可使用;工作电压十分平稳。
部分镁储备型电池电化学反应式为Mg +NaClO +H 2O→Mg(OH)2+NaCl ; xMg +Mo 3S 4→Mg x Mo 3S 4;Mg +2AgCl→2Ag +MgCl 2;根据上述原理设计的原电池下列有关说法正确的是 A .镁-次氯酸盐电池工作时,正极附近的溶液pH 将会增大 B .镁电池的负极反应式都是Mg -2e -=Mg 2+ C .镁电池充电时负极发生氧化反应生成镁离子 D .将镁电池活化可以使用稀硫酸2.大功率Al-H 2O 2动力电池(如图),下列说法不正确...的是A .H 2O 2 在碳电极上发生还原反应B .碳电极附近溶液的pH 增大C .溶液中OH -向负极移动D .负极反应式为Al -3e -+3OH -=Al(OH)3↓3.如图所示装置中,观察到电流计指针偏转;M 棒变粗;N 棒变细,由此判断表中所列M 、N 、P 物质,其中可以成立的是A .AB .BC .CD .D4.将两个铂电极插入KOH 溶液中,向两极分别通入CH 4和O 2,构成甲烷燃料电池。
已知通入CH 4的一极的电极反应为:CH 4+10OH --8e -=CO 32-+7H 2O 。
下列叙述不正确的是( )A .通入CH 4的电极为负极B .电池工作时,溶液中的OH -向负极移动C .正极反应:2O 2+4H 2O+8e -=8OH -D .电池使用一段时间后溶液中KOH 的浓度将不变5.氢氧燃料电池已用于航天飞机,其工作原理如图所示。
高中化学人教版必修2练习:第二章第二节化学能与电能含解析

第二节化学能与电能1.化学与能源开发、环境保护、资源利用等亲密有关。
以下说法正确的选项是()A.天然气、石油、流水、风力、氢气为一次能源B.不论是风力发电仍是火力发电,都是将化学能转变成电能C.PM2.5 含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素D.发展低碳经济、循环经济,推行可利用太阳能、风能的城市照明系统分析:A 中氢气不是一次能源, B 中风力发电不是化学能转变成电能, C 中砷不是金属元素。
答案: D2.X、Y、Z 都是金属,把 X 浸入 Z 的硝酸盐溶液中, X 的表面有Z 析出, X 和 Y 构成原电池时, Y 为电池的负极。
X、Y、Z 三种金属的活动性次序为()A.X>Y>Z B.X>Z>YC.Y>X>Z D.Y>Z>X分析:依据原电池原理,负极金属比较开朗,可知Y>X ,依据开朗金属置换不开朗金属,可知X>Z ,故 Y>X>Z 。
答案: C3.研究电化学腐化及防备的装置以下图。
以下有关说法错误的是()A.d 为石墨,铁片腐化加速B.d 为石墨,石墨上电极反响为: O2+2H 2O+4e- ===4OH-C.d 为锌块,铁片不易被腐化D.d 为锌块,铁片上电极反响为:2H ++2e- ===H2↑分析:因为活动性: Fe>石墨,所以铁、石墨及海水构成原电池,Fe 为负极,失掉电子被氧化变成Fe2+进入溶液,溶解在海水中的氧气在正极石墨上获得电子被复原,比没有形成原电池时的速率快,正确。
B.d 为石墨,因为是中性电解质,所以发生的是吸氧腐化,石墨上氧气获得电子,发生复原反响,电极反响为:O2+ 2H2O +4e-===4OH-,正确。
C.若 d 为锌块,则因为金属活动性Zn>Fe ,Zn 为原电池的负极, Fe 为正极,第一被腐化的是Zn ,铁获得保护,铁片不易被腐化,正确。
D.d 为锌块,因为电解质为中性环境.发生的是吸氧腐化,在铁片上发生的电极反响为:O2+2H 2O+4e- ===4OH -,错误。
人教版高中化学必修2第二章第二节化学能与电能基础练习与提高练习(含答案解析)

《化学能与电能》基础练习第一课时一、单项选择题1.能源可分为一次能源和二次能源,自然界中以现成形式提供的能源称为一次能源,需依靠其他能源的能量间接制取的能源称为二次能源。
据此判断,下列叙述正确的是()A.天然气是二次能源B.石油是二次能源C.电能是一次能源D.水力是一次能源2.下列说法正确的是()A.需要加热的化学反应都是吸热反应B.中和反应都是放热反应C.原电池是将电能转化为化学能的一种装置D.水力发电是将化学能转化为电能的过程3.下列叙述不正确...的是()A.根据一次能源和二次能源的划分,氢气为二次能源B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源C.火电是将燃料中的化学能直接转化为电能的过程D.在火电过程中,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化4.关于原电池的叙述中正确的是()A.构成原电池的电极是两种不同的金属B.原电池是将化学能转化为电能的装置C.原电池负极发生的电极反应是还原反应D.原电池的正极是还原剂,总是溶液中的阳离子在此被还原5.某原电池总反应离子方程式为Mg+2H+=Mg2++H2↑,能实现该反应的原电池是()A.正极为铜,负极为镁,电解质溶液为稀盐酸B.正极为铜,负极为铁,电解质溶液为稀硫酸C.正极为石墨,负极为镁,电解质溶液为CuSO4溶液D.正极为银,负极为镁,电解质溶液为NaCl溶液6.下列变化是因为原电池反应而引起的是()A.在空气中金属铝表面迅速氧化形成保护膜B.常温下,铁被浓硫酸钝化形成保护膜C.在潮湿的空气中钢铁易生锈D.在潮湿的空气中过氧化钠易变质7.在图1所示的原电池中,下列说法正确的是()图1A.Zn为负极,Cu为正极B.正极反应为Zn-2e-=Zn2+C.负极反应为Cu-2e-=Cu2+D.该装置能将电能转化为化学能8.某实验兴趣小组用如图2所示装置做完实验后,在读书卡片上记下了如下6条记录,其中合理的是()图2卡片No.28Date:2013.9.12实验后的记录:①Zn为正极,Cu为负极②H+向负极移动③电子流动方向为Zn→导线→Cu ④Cu极有H2产生⑤若有1 mol电子流过导线,则产生0.5 mol H2⑥正极的电极反应式:Zn-2e-=Zn2+A.①②③B.③④⑤C.④⑤⑥D.②③④二、双项选择题9.将纯锌片和纯铜片按图3所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是()图3A.两烧杯中铜片表面均无气泡产生B.甲中铜片是正极,乙中铜片是负极C.两烧杯中溶液的pH均增大D.产生气泡的速度甲比乙快10.关于图4所示的原电池,下列说法正确的是()图4A.电子从锌电极通过电流表流向铜电极B.锌电极发生还原反应,铜电极发生氧化反应C.当有13 g Zn溶解时,电路中就有0.4 mol电子通过D.铜电极作正极,发生的电极反应为2H++2e-=H2↑三、非选择题11.用铜片、锌片和稀硫酸及若干其他器材组合成一个原电池,如图5。
人教版高一化学必修二同步练习及答案:第二章第二节化学能与电能

人教版高一化学必修2同步练习第二节化学能与电能一、单选题1.化石燃料仍是目前能源的主体,但已经面临危机,开发新能源是解决能源问题的关键.下列能量转换过程,不涉及化学变化的是()A. 利用氢氧燃料电池提供电能B. 利用太阳能分解水制备氢气C. 利用水流驱动涡轮机发电D. 利用植物秸秆为原料生产乙醇燃料2.根据下列反应不能设计为原电池的是()A. Fe+2FeCl3=3FeCl2B. CH4+2O2=CO2+2H2OC. H2+Cl2=2HClD. H2SO4+2NaOH=Na2SO4+2H2O3.某电池总反应为2Fe3++Cu=2Fe2++Cu2+,不能实现该反应的原电池是()A. 电极材料Fe、Cu,电解质溶液FeCl3溶液B. 电极材料石墨、Cu,电解质溶液Fe2(SO4)3溶液C. 电极材料Pt、Cu,电解质溶液FeCl3溶液D. 电极材料Ag、Cu,电解质溶液Fe2(SO4)3溶液4.一个原电池的总反应的离子方程式是Fe+Cu2+=Fe2++Cu,该反应的原电池组成正确的是()A. AB. BC. CD. D5.下列各装置中铜电极上能产生气泡的是()A. B. C. D.6.下列各图所示装置属于原电池的是()A. B.C. D.7.下图是锌一铜原电池示意图,下列说法错误的是()A. 电子由铜片通过导线流向锌片B. 锌片为负极,且锌片逐渐溶解C. 铜为正极,铜不易失电了而受到保护D. 该装置能将化学能转变为电能8.有关甲、乙、丙、丁四个图示的叙述不正确的是()A. 甲中负极反应式为Zn−2e−=Zn2+B. 乙中阳极反应式为Ag−e−=Ag+C. 丙中H+向碳棒方向移动D. 丁中电解开始时阳极产生黄绿色气体人教版高一化学必修2同步练习9.某化学兴趣小组将锌片和铜片出入番茄中制成水果电池(如图)下列说法中正确的是()A. 一段时间后,锌片质量会变小B. 铜片上发生氧化反应C. 电子由铜片通过导线流向锌D. 锌电极是该电池的正极10.燃料电池是一种高效、环境友好的发电装置,某氢氧燃料电池的构造示意图如下,该电池工作时,下列说法正确的是()A. a电极是该电池的正极B. O2在b电极上发生氧化反应C. 电解质溶液中OH−向正极移动D. 该装置实现了化学能到电能的转化11.有A,B,C,D四块金属片,进行如下实验,据此判断四种金属的活动顺序是()①A,B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C,D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;③A,C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B,D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应。
人教版化学必修2化学能与电能练习题100题(含解析答案)2
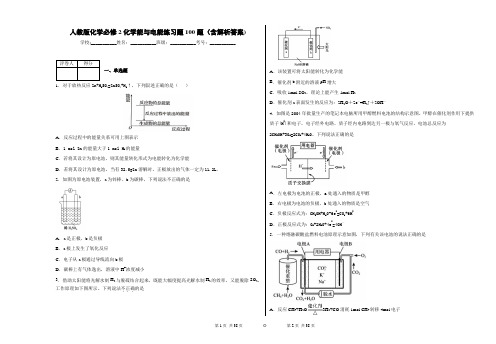
人教版化学必修2化学能与电能练习题100题(含解析答案)学校:___________姓名:___________班级:___________考号:___________一、单选题1.对于放热反应Zn+H 2SO 4=ZnSO 4+H 2↑,下列叙述正确的是( )A .反应过程中的能量关系可用上图表示B .1 mol Zn 的能量大于1 mol H 2的能量C .若将其设计为原电池,则其能量转化形式为电能转化为化学能D .若将其设计为原电池,当有32.5gZn 溶解时,正极放出的气体一定为11.2L. 2.如图为原电池装置,a 为锌棒、b 为碳棒,下列说法不正确的是A .a 是正极,b 是负极B .a 极上发生了氧化反应C .电子从a 极通过导线流向b 极D .碳棒上有气体逸出,溶液中H +浓度减小3.借助太阳能将光解水制H 2与脱硫结合起来,既能大幅度提高光解水制H 2的效率,又能脱除SO 2,工作原理如下图所示。
下列说法不正确...的是A .该装置可将太阳能转化为化学能B .催化剂b 附近的溶液pH 增大C .吸收1mol SO 2,理论上能产生1mol H 2D .催化剂a 表面发生的反应为:2H 2O +2e -=H 2↑+2OH -4.如图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。
甲醇在催化剂作用下提供质子(H +)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH 30H+302=2C02+4H 20。
下列说法正确的是A .左电极为电池的正极,a 处通入的物质是甲醇B .右电极为电池的负极,b 处通入的物质是空气C .负极反应式为:CH 30H+H 20-6e -=CO 2+6H +D.正极反应式为:02+2H 20+4e -=40H —5.一种熔融碳酸盐燃料电池原理示意如图,下列有关该电池的说法正确的是A .反应CH 4+H 2O 3H 2+CO 消耗1mol CH 4转移4mol 电子B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2OC.电池工作时,CO32-向电极B移动D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-6.将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,在四张滤纸上滴入稀H2SO4直至全部润湿。
必修2第二章第二节《化学能与电能》测试题含答案
必修二第二章第二节《化学能与电能》测试题一、选择题(每小题有一个或二个选项符合题意)1.下列产品的使用不会对环境造成污染的是()A.含磷洗衣粉B.氢气 C.含汞电池 D.煤2.废电池的污染引起人们的广泛重视,废电池中对环境形成污染的主要物质是( ) A.锌B.汞 C.石墨 D.二氧化锰3.用锌片、铜片和硝酸银组成的原电池,正极上发生的反应是()A、2H++2e- =H2B、Zn -2e- =Zn2+C、2H2O+4e-=4OH-D、Ag++e- =Ag4.将纯锌片和纯铜片按右下图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是()A.两烧杯中铜片表面均无气泡产生 B.甲中铜片是正极,乙中铜片是负极C.两烧杯中溶液的pH均增大 D.产生气泡的速度甲比乙慢5.下列各变化中属于原电池反应的是()A.在空气中金属铝表面迅速氧化形成保护层B.镀锌铁表面有划损时,也能阻止铁被氧化C.红热的铁丝与冷水接触,表面形成蓝黑色保护层D.浓硝酸比稀硝酸更能氧化金属铜6.钢铁发生吸氧腐蚀时,正极上发生的电极反应是()++2e-=H2 B. Fe 2++2e-=Fe +O2+4e-=4OH- D. Fe3++e-=Fe2+7.X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X与Y组成原电池时,Y为电池的负极。
X、Y、Z三种金属的活动性顺序为()A、X>Y>ZB、 X> Z > YC、 X > Y >ZD、Y> X > Z8.关于铁—镍蓄电池Fe+NiO2+2H2O = Fe(OH)2+Ni(OH)2的下列说法中不正确的是()A、放电时铁为负极B、放电时NiO2的反应为:NiO2 +2e- +2H2O =Ni(OH)2 +2OH-C、放电时铁为正极D、蓄电池的电极必须浸在碱性电解质溶液中9.下列现象与电化腐蚀无关的是()A、黄铜(铜锌合金)制的铜锣不易产生铜绿B、生铁比软铁芯(几乎是纯铁)容易生锈C、铁质器件附有铜质配件,在接触处易生铁锈D、银质奖牌久置后表面变暗10.埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀速率最慢的是()A、含铁元素较多酸性土壤B、潮湿疏松的碱性土壤C、干燥致密不透气的土壤D、含碳粒较多,潮湿透气的中性土壤11. 已知蓄电池在充电时作电解池,放电时作原电池。
安徽省 高一化学 2.2 化学能与电能练习 新人教版
一、选择题1.下列关于原电池的说法中正确的是( )A .把光能转变成了化学能B .把化学能转变成了光能C .把热能转变成了电能D .把化学能转变成了电能解析: 原电池是利用自发的氧化还原反应,把化学能转化为电能的装置。
答案: D2.对化学电源的叙述正确的是( )A .化学电源比火力发电对化学能的利用率高B .化学电源所提供的电能居于人类社会现阶段总耗电量的首位C .化学电源均是安全、无污染的D .化学电源即为可充电电池解析: 目前人类生活、生产的主要耗电仍然是火力发电;化学电源中常含有Cd 、Hg 、Pb 、Ni 等重金属离子,如果废旧电池随意丢弃会造成环境污染;化学电源包括可充电电池,也包括不能进行充电循环使用的一次性电池。
答案: A3.下面是四个化学反应,你认为理论上不能用于设计原电池的化学反应是( )A .2Al +2NaOH +2H 2O===2NaAlO 2+3H 2↑B .2H 2+O 2=====点燃2H 2OC .Mg 3N 2+6H 2O===3Mg(OH)2↓+2NH 3↑D .CH 4+2O 2=====点燃CO 2+2H 2O解析: 能设计成原电池的反应是能自发进行的氧化还原反应,C 项的反应为非氧化还原反应。
答案: C 4.(2012·汕头高一检测)如图为番茄电池,下列说法正确的是( )A .一段时间后,锌片质量会变小B .铜电极附近会出现蓝色C .电子由铜通过导线流向锌D .锌电极是该电池的正极解析: 番茄电池中锌是负极,铜是正极,负极锌会失去电子溶解,质量减小,A 对、D 错;铜极是正极,电子由负极锌移向正极铜,C 错;无法说明铜电极会出现蓝色,B 错。
答案: A5.某课外活动小组使用下列用品设计原电池。
用品:铜片、铁片、导线、金属夹、发光二极管、果汁(橙汁、苹果汁)、500 mL 烧杯。
下列说法正确的是( )A .该装置能将电能转化为化学能B .实验过程中铜片逐渐溶解C .电子由铁片通过导线流向铜片D .铁片上会析出红色的铜解析: 依据原电池构成条件,结合题给材料,可选择铁片作负极,铜片作正极,果汁为电解质溶液,设计成一个原电池。
人教版必修2作业5化学能与电能附答案
高一化学必修2作业(五)第二章第二节化学能与电能一、选择题(本小题共5小题,每小题3分,共15分,每小题只有一个正确答案)1.下列关于化学能和电能的叙述正确的是A. 在一定条件下,化学能和电能可以相互转化B. 任何化学反应的化学能都可以直接转化为电能C. 原电池是将电能转化为化学能的装置D. 火力发电是将化学能直接转化为电能的过程2.下列关于原电池的叙述中,错误的是A.在原电池中,负极上发生氧化反应B.电子的流动方向是从负极到正极C.电解质溶液中电流的流动方向是从负极到正极D.构成原电池的正极和负极必须是两种不同的金属3.下列化学电池不易造成环境污染的是A.氢氧燃料电池B.锌锰电池C.镍镉电池D.铅蓄电池4.人造地球卫星用到的一种高能电池—银锌电池,它在放电时的电极反应为:Zn+2OH --2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。
据此判断,氧化银是A.负极,被氧化 B.负极,被还原C.正极,被还原 D.正极,被氧化5.将锌片和铜片用导线连接后放入稀硫酸溶液中,发生原电池反应,下列叙述错误的是: A、溶液的pH增大 B、溶液中的Zn2+浓度增大C、溶液中的SO42- 浓度增大D、溶液的质量增大二、选择题(共10小题,每小题4分,计40分,每小题有1—2个正确答案)6.对于干电池的使用和保存,下列说法不正确的是A.长期不用应将电池从用电器中取出妥善保存B.用后不能随意丢弃,应回收利用C.放置过久,会自行失效D.电池的型号(如1号、5号等)表示放电电压的大小7.实验室欲加快制取H2的反应速率,应选用正确的措施是A.将锌改为铁与稀硫酸反应 B.将纯锌改用粗锌与稀硫酸反应C.使用锌跟稀硝酸反应 D.锌跟稀硫酸反应,滴入几滴硫酸铜溶液8.镍氢电池的总反应式是H2+2NiO(OH) == 2Ni(OH)2,根据此反应式判断,此电池放电时负极上发生反应的物质是A.NiO(OH) B.Ni(OH) 2C.H2D.H2和NiO(OH)9. 现有X、Y、Z三种金属片,把X、Y用导线连接后同时浸入稀硫酸中,X上有气泡;把X、Z用导线连接后同时浸入硫酸铜溶液中,Z上发生还原反应。
高一化学新课标必修二22化学能与电能测试题含答案
新课标必修二第二章第二节化学能与电能精品测试题1.废电池的污染引起人们的广泛重视,废电池中对环境形成污染的主要物质是( )。
A.锌 B.汞 C.石墨 D.二氧化锰2.实验室中制取氢气,最好的方法是( )。
A.纯锌与稀硫酸反应 B.纯锌与浓硫酸反应C.纯锌与稀盐酸反应 D.粗锌(含铜、银)与稀硫酸反应3.某金属能和盐酸反应生成氢气,该金属与锌组成原电池时,锌为负极,该金属可能为A.铝 B.铜 C.锡 D.硅4.将锌片和铜片用导线连接于同一稀硫酸溶液中。
下列叙述正确的是( )。
A.正极附近硫酸根离子的浓度逐渐增大 B.负极附近硫酸根离子的浓度逐渐增大C.正极、负极硫酸根离子的浓度基本不变 D.正极附近硫酸根离子的浓度逐渐减少5.已知空气-锌电池的电极反应为:锌片:Zn+20H--2e-=ZnO+H20石墨:02+2H20+4e-=40H-根据此判断,锌片是( )。
A.负极,并被氧化 B.负极,并被还原 C.正极,并被氧化 D.正极,并被还原6.一个原电池的总反应离子方程式是Zn+Cu2+=Zn2++Cu,该反应的原电池组成正确( )。
7.表明金属甲的活动性比金属乙的活动性强的叙述正确的是( )。
A.在氧化还原反应中,甲失电子比乙失电子多 B.甲比乙同价态的阳离子的氧化性强C.甲能与稀盐酸反应生成氢气而乙不能 D.将甲与乙组成原电池时,甲为正极8.X,Y,Z都是金属,把X浸A Z的硝酸溶液中,X的表面有Z析出,X与Y组成原电池时,Y为负极。
X,Y,Z三种金属的活动性顺序为( )。
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X9.对于锌一铜一稀硫酸组成的原电池装置中,当导线中有1 mol电子通过时,理论上的两极变化是( )。
①锌片溶解了32.5 g②锌片增重32.5 g③铜片上析出l g H2 ④铜片上析出1 mol H2 A.①和③ B.①和④ C.②和③ D.②和④10.据报道,锌电池可能取代目前广泛应用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。
