物理化学知识点归纳77421
物理化学复习知识点归纳

物理化学复习知识点归纳物理化学作为化学的一个主要分支,关注物质的物理性质、化学反应、能量转化等方面的研究。
下面将对物理化学的基本知识点进行归纳和复习。
1.原子结构和化学键:-定义:原子是化学物质中最小的粒子,由质子(正电荷)、中子(中性)和电子(负电荷)组成。
-原子核:由质子和中子组成,质子数决定了元素的原子序数,中子数可以影响同位素的形成。
-电子壳层结构:分为K、L、M等壳层,每个壳层能容纳的电子数量有限,遵循2n^2的规律(n为壳层编号)。
-原子键:包括离子键、共价键和金属键。
离子键由离子间的电荷作用力形成,共价键由相互共享电子形成,金属键由金属原子之间的电子云相互作用形成。
2.分子的构象和反应动力学:-构象:指分子在空间中的排列方式,由键角和键长决定。
分子的构象决定了其物理和化学性质。
-电离平衡:涉及酸碱反应的平衡,Kw表示了水的离子化程度和酸碱强度。
-化学动力学:研究化学反应的速率和机理。
反应速率受温度、浓度、反应物的结构和催化剂等因素影响。
3.热力学和热化学:-热力学:研究物质能量转化和热平衡的学科。
包括物质的内能、焓、熵、自由能等概念。
-熵:表示体系的无序度,体系越有序,熵值越小。
熵的增加是自然趋势,反映了热力学第二定律。
-热化学:研究化学反应中能量变化的学科。
包括焓变、标准焓变、热容、热效应等概念。
-反应热力学:研究反应的方向和热效应。
根据吉布斯自由能的变化可以判断反应是否自发进行。
4.量子化学:-波动粒子二象性:根据波粒二象性原理,微观粒子既可以表现出粒子性质,也可以表现出波动性质。
-波函数和波动函数:描述微观粒子在空间中的波动性质和定域性质。
波函数的平方可以给出粒子出现在一些空间区域的概率。
-氢原子的定态:薛定谔方程描述了电子在氢原子中的定态和能级。
以上是物理化学的一些基本知识点的归纳和复习。
在复习过程中,建议结合教材和课堂笔记,注重理解和记忆重点概念和公式,同时通过做习题和实践操作巩固知识。
物理化学各章知识点总结-86页

经此过程,所有状态函数的变量均为零。
4. 功和热
注意:
W pambdV
• 不论是膨胀还是压缩,体积功都用- pambdV
计算,公式中的压力都用外压
• 公式中的pamb不能随便写到积分号外,只有 常数才行
• 只有- pambdV这个量才是体积功,pambV或 Vdpamb都不是体积功。
不同过程功的计算分析:W p amb V
W pamb dV
(1)环境为真空态(自由膨胀):
pamb= 0,W = 0
(2)恒外压过程(pamb恒定): W = -pambΔV = -pamb(V2-V1)
(3)恒压过程(pamb=p=定值):
W=-p△V
(4)恒容过程(△V =0):
W=0
例如:在298.15 K时
1 2
H2
(g,
p
)
1 2
Cl2
(g,
p
)
HCl(
g,
p
)
反应焓变为:
r
H
m
(298
.15
K
)
92.31kJ.mol 1
这就是HCl(g)的标准摩尔生成焓:
f Hm (HCl, g,298.15K) 92.31kJ.mol1
10.可逆过程与可逆体积功
可逆过程:系统内部及系统与环境之间在无限接近平 衡条件下进行的过程,称为可逆过程,否则称为不可 逆过程。
生成物来表示反应进行的程度,所得的值都是相
同的,即:
d dnD dnE dnF dnG D E F G
当反应按所给反应式的系数比进行了一个单位的化 学反应时,即 nB / mol B,这时反应进度就是1mol。
《物理化学》知识点汇总

《物理化学》知识点汇总热力学系统:热力学系统是指热力学研究的对象,是物质或物质的集合体。
状态:状态是指热力学系统中物质的宏观性质及其变化的状态。
热力学第一定律:能量守恒定律在热力学中的表现形式,它说明能量不能被创造或消失,只能从一种形式转化为另一种形式。
能量守恒:能量既不能被创造也不能被消失,它只能从一种形式转化为另一种形式。
热力学第二定律:热力学中描述自然过程方向性的定律,它表明,在一个封闭系统中,自发过程总是向熵增加的方向进行。
熵增:在封闭系统中,自发过程总是向熵增加的方向进行,也就是说,系统总是朝着更大的混乱状态发展。
相平衡:在热力学中,相平衡是指不同物相之间达到的平衡状态。
化学平衡:在化学反应中,反应物和生成物之间达到的平衡状态。
化学动力学:研究化学反应速率以及反应机制的科学。
表面化学:研究表面吸附、表面反应等表面现象的化学分支。
胶体分散系:由一种或多种物质在另一种物质中分散而成的系统。
以上是《物理化学》中的一些重要知识点,这些知识点是理解物理化学概念和应用的基础。
在学习过程中,需要不断巩固和深化对这些知识点的理解,以更好地掌握物理化学这门学科。
《经济法基础》是会计专业技术资格考试中的一门科目,主要考察考生对经济法相关知识的掌握程度和应用能力。
考试内容涉及广泛,包括经济法的基本概念、市场主体、市场秩序、宏观调控、劳动法等。
考试形式为闭卷、笔试,考试时间为90分钟。
经济法的基本概念:经济法的定义、特征、原则等。
市场主体:各类企业、个体工商户、农村承包经营户等市场主体的设立、变更和终止的相关法律规定。
市场秩序:市场竞争、市场准入、市场退出等方面的法律规定。
宏观调控:产业政策、财税政策、货币政策等宏观调控手段的法律规定。
劳动法:劳动者的权利和义务,劳动合同的签订和履行,劳动安全卫生、社会保险等方面的法律规定。
经济法涉及的法律法规众多,需要考生具备较为扎实的法律基础。
考试内容涉及面广,考生需要全面掌握各个方面的知识。
物理化学知识点归纳

物理化学知识点归纳物理化学是化学学科的一个重要分支,它综合运用物理学的原理和方法来研究化学现象和过程。
以下是对物理化学一些重要知识点的归纳:一、热力学第一定律热力学第一定律,也就是能量守恒定律,表明能量可以在不同形式之间转换,但总量保持不变。
在热力学中,通常用公式△U = Q + W来表示,其中△U 是系统内能的变化,Q 是系统吸收或放出的热量,W 是系统对外做功或外界对系统做功。
例如,在一个绝热容器中进行的化学反应,如果体系对外做功,那么内能就会减少;反之,如果外界对体系做功,内能就会增加。
二、热力学第二定律热力学第二定律有多种表述方式,其中克劳修斯表述为:热量不能自发地从低温物体传到高温物体。
开尔文表述为:不可能从单一热源取热使之完全变为有用功而不产生其他影响。
熵(S)的概念在热力学第二定律中至关重要。
对于一个孤立系统,熵总是增加的,这意味着系统总是朝着更加混乱和无序的方向发展。
比如,混合气体自发扩散后,不会自动分离回到初始状态,因为这个过程熵增加了。
三、热力学第三定律热力学第三定律指出,绝对零度(0K)时,纯物质完美晶体的熵值为零。
这一定律为计算物质在不同温度下的熵值提供了基准。
四、化学平衡化学平衡是指在一定条件下,可逆反应中正逆反应速率相等,反应物和生成物的浓度不再随时间改变的状态。
平衡常数(K)是衡量化学平衡的重要参数。
对于一个一般的化学反应 aA + bB ⇌ cC + dD,平衡常数 K 的表达式为:K = C^cD^d / A^aB^b (其中方括号表示物质的浓度)。
影响化学平衡的因素包括温度、浓度、压强等。
例如,对于吸热反应,升高温度会使平衡向正反应方向移动;增加反应物浓度,平衡也会向正反应方向移动。
五、相平衡相平衡研究的是多相体系中各相的组成、性质以及它们之间的相互转化规律。
相律是描述相平衡体系中自由度、组分数和相数之间关系的定律,其表达式为 F = C P + 2,其中 F 是自由度,C 是组分数,P 是相数。
物理化学知识点(全)
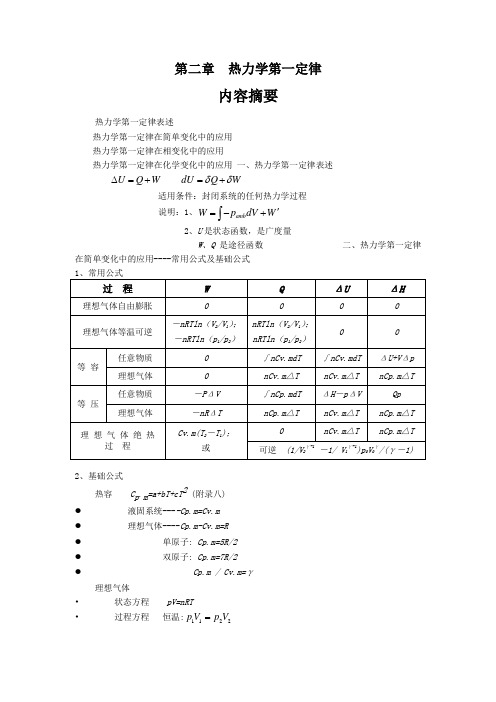
第二章热力学第一定律内容摘要热力学第一定律表述热力学第一定律在简单变化中的应用 热力学第一定律在相变化中的应用热力学第一定律在化学变化中的应用 一、热力学第一定律表述U Q W ∆=+ dU Q W δδ=+适用条件:封闭系统的任何热力学过程 说明:1、amb W p dV W '=-+⎰2、U 是状态函数,是广度量W 、Q 是途径函数 二、热力学第一定律在简单变化中的应用----常用公式及基础公式2、基础公式热容 C p .m =a+bT+cT 2 (附录八) ● 液固系统----Cp.m=Cv.m ● 理想气体----Cp.m-Cv.m=R ● 单原子: Cp.m=5R/2 ● 双原子: Cp.m=7R/2 ● Cp.m / Cv.m=γ理想气体• 状态方程 pV=nRT• 过程方程 恒温:1122p V p V =• 恒压: 1122//V T V T = • 恒容: 1122/ / p T p T = • 绝热可逆: 1122 p V p V γγ= 111122 T p T p γγγγ--=111122 TV T V γγ--= 三、热力学第一定律在相变化中的应用----可逆相变化与不可逆相变化过程1、 可逆相变化 Q p =n Δ相变H mW = -p ΔV无气体存在: W = 0有气体相,只需考虑气体,且视为理想气体ΔU = n Δ相变H m - p ΔV2、相变焓基础数据及相互关系 Δ冷凝H m (T) = -Δ蒸发H m (T) Δ凝固H m (T) = -Δ熔化H m (T) Δ凝华H m (T) = -Δ升华H m (T)(有关手册提供的通常为可逆相变焓)3、不可逆相变化 Δ相变H m (T 2) = Δ相变H m (T 1) +∫Σ(νB C p.m )dT解题要点: 1.判断过程是否可逆;2.过程设计,必须包含能获得摩尔相变焓的可逆相变化步骤;3.除可逆相变化,其余步骤均为简单变化计算.4.逐步计算后加和。
物理化学知识点

物理化学知识点物理化学知识点概述1. 热力学定律- 第零定律:如果两个系统分别与第三个系统处于热平衡状态,那么这两个系统之间也处于热平衡状态。
- 第一定律:能量守恒,系统内能量的变化等于热量与功的和。
- 第二定律:熵增原理,自然过程中熵总是倾向于增加。
- 第三定律:当温度趋近于绝对零度时,所有纯净物质的熵趋近于一个常数。
2. 状态方程- 理想气体状态方程:PV = nRT,其中P是压强,V是体积,n是摩尔数,R是理想气体常数,T是温度。
- 范德瓦尔斯方程:(P + a(n/V)^2)(V - nb) = nRT,修正了理想气体状态方程在高压和低温下的不足。
3. 相平衡与相图- 相律:描述不同相态之间平衡关系的数学表达。
- 相图:例如,水的相图展示了水在不同温度和压强下的固态、液态和气态的平衡关系。
4. 化学平衡- 反应速率:化学反应进行的速度,受温度、浓度、催化剂等因素影响。
- 化学平衡常数:在一定温度下,反应物和生成物浓度之比达到平衡时的常数值。
5. 电化学- 电解质:在溶液中能够产生带电粒子(离子)的物质。
- 电池:将化学能转换为电能的装置。
- 电化学系列:金属的还原性或氧化性排序。
6. 表面与胶体化学- 表面张力:液体表面分子间的相互吸引力。
- 胶体:粒子大小在1到1000纳米之间的混合物,具有特殊的表面性质。
7. 量子化学- 量子力学基础:描述微观粒子如原子、分子的行为。
- 分子轨道理论:通过分子轨道来描述分子的结构和性质。
- 电子能级:原子和分子中电子的能量状态。
8. 光谱学- 吸收光谱:分子吸收特定波长的光能,导致电子能级跃迁。
- 发射线谱:原子或分子在电子能级跃迁时发出特定波长的光。
- 核磁共振(NMR):利用核磁共振现象来研究分子结构。
9. 统计热力学- 微观状态与宏观状态:通过系统可能的微观状态数来解释宏观热力学性质。
- 玻尔兹曼分布:描述在给定温度下,粒子在不同能量状态上的分布。
物理化学知识点总结

第一章 热力学第一定律一、基本概念系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律热力学第一定律:ΔU =Q +W 。
焦耳实验:ΔU =f (T ) ; ΔH =f (T ) 三、基本关系式1、体积功的计算 δW = -p e d V恒外压过程:W = -p e ΔV可逆过程:1221ln ln p p nRT V V nRT W ==2、热效应、焓等容热:Q V =ΔU (封闭系统不作其他功) 等压热:Q p =ΔH (封闭系统不作其他功) 焓的定义:H =U +pV ; d H =d U +d(pV )焓与温度的关系:ΔH =⎰21d p T T T C3、等压热容与等容热容热容定义:V V )(T U C ∂∂=;p p )(T H C ∂∂=定压热容与定容热容的关系:nR C C =-V p 热容与温度的关系:C p =a +bT +c’T 2 四、第一定律的应用1、理想气体状态变化等温过程:ΔU =0 ; ΔH =0 ; W =-Q =⎰-p e d V 等容过程:W =0 ; Q =ΔU =⎰T C d V ; ΔH =⎰T C d p 等压过程:W =-p e ΔV ; Q =ΔH =⎰T C d p ; ΔU =⎰T C d V 可逆绝热过程:Q =0 ; 利用p 1V 1γ=p 2V 2γ求出T 2,W =ΔU =⎰T C d V ;ΔH =⎰T C d p不可逆绝热过程:Q =0 ; 利用C V (T 2-T 1)=-p e (V 2-V 1)求出T 2,W =ΔU =⎰T C d V ;ΔH =⎰T C d p2、相变化可逆相变化:ΔH =Q =n Δ_H ;W=-p (V 2-V 1)=-pV g =-nRT ; ΔU =Q +W3、热化学物质的标准态;热化学方程式;盖斯定律;标准摩尔生成焓。
摩尔反应热的求算:)298,()298(B H H m f B m r θθν∆=∆∑反应热与温度的关系—基尔霍夫定律:)(])([,p B C T H m p BB m r ∑=∂∆∂ν。
物理化学课本重点全方位总结

第一章热力学第一定律1、热力学三大系统:(1)敞开系统:有物质和能量交换;(2)密闭系统:无物质交换,有能量交换;(3)隔绝系统(孤立系统):无物质和能量交换。
2、状态性质(状态函数):(1)容量性质(广度性质):如体积,质量,热容量。
数值与物质的量成正比;具有加和性。
(2)强度性质:如压力,温度,粘度,密度。
数值与物质的量无关;不具有加和性,整个系统的强度性质的数值与各部分的相同。
特征:往往两个容量性质之比成为系统的强度性质。
3、热力学四大平衡:(1)热平衡:没有热隔壁,系统各部分没有温度差。
(2)机械平衡:没有刚壁,系统各部分没有不平衡的力存在,即压力相同(3)化学平衡:没有化学变化的阻力因素存在,系统组成不随时间而变化。
(4)相平衡:在系统中各个相(包括气、液、固)的数量和组成不随时间而变化。
4、热力学第一定律的数学表达式:∆U = Q + W Q为吸收的热(+),W为得到的功(+)。
12、在通常温度下,对理想气体来说,定容摩尔热容为:单原子分子系统,V m C =32R 双原子分子(或线型分子)系统 ,V m C =52R 多原子分子(非线型)系统 ,V mC 632R R == 定压摩尔热容:单原子分子系统 ,52p m C R =双原子分子(或线型分子)系统 ,,p m V m C C R -=,72p m C R =多原子分子(非线型)系统 ,4p m C R =可以看出:,,p m V m C C R -=13、,p m C 的两种经验公式:,2p m C a bT cT =++ (T 是热力学温度,a,b,c,c ’ 是经,2'p m c C a bT T=++ 验常数,与物质和温度范围有关)14、在发生一绝热过程时,由于0Q δ=,于是dU Wδ=理想气体的绝热可逆过程,有:,V m nC dT pdV =- ⇒ 22,11lnln V m T V C R T V =- 21,12ln ,ln V m p V C Cp m p V ⇒= ,,p mV mC pV C γγ=常数 =>1. 15、-焦耳汤姆逊系数:J T T =()H pμ∂∂- J T μ->0 经节流膨胀后,气体温度降低;J T μ-<0 经节流膨胀后,气体温度升高; J T μ-=0 经节流膨胀后,气体温度不变。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
110112班期末物理化学知识点归纳预祝大家物化期末考试取得好成绩!——孔祥鑫2012年5月27日第二章热力学第一定律一、热力学基本概念1.状态函数状态函数,是指状态所持有的、描述系统状态的宏观物理量,也称为状态性质或状态变量.系统有确定的状态,状态函数就有定值;系统始、终态确定后,状态函数的改变为定值;系统恢复原来状态,状态函数亦恢复到原值。
2.热力学平衡态在指定外界条件下,无论系统与环境是否完全隔离,系统各个相的宏观性质均不随时间发生变化,则称系统处于热力学平衡态。
热力学平衡须同时满足平衡(△T=0)、力平衡(△p=0)、相平衡(△μ=0)和化学平衡(△G=0)4个条件。
二、热力学第一定律的数学表达式1。
△U=Q+W或dU=ΔQ+δW=δQ-p amb dV+δW`规定系统吸热为正,放热为负。
系统得功为正,对环境做功为负。
式中p amb为环境的压力,W`为非体积功。
上式适用于封闭系统的一切过程。
2.体积功的定义和计算系统体积的变化而引起的系统和环境交换的功称为体积功。
其定义式为:δW=—p amb dV(1)气体向真空膨胀时体积功所的计算W=0(2)恒外压过程体积功W=p amb(V1—V2)=—p amb△V对于理想气体恒压变温过程W=-p△V=—nR△T(3)可逆过程体积功W r=⎰21pVVdV(4)理想气体恒温可逆过程体积功W r=⎰21pVVdV=—nRTln(V1/V2)=—nRTln(p1/p2)(5)可逆相变体积功W=—pdV三、恒热容、恒压热,焓1。
焓的定义式H def U + p V2.焓变(1)△H=△U+△(pV )式中△(pV )为p V 乘积的增量,只有在恒压下△(pV )=p(V 2—V 1)在数值上等于体积功。
(2)△H=⎰21,T T m p dT nC此式适用于理想气体单纯p VT 变化的一切过程,或真实气体的恒压变温过程,或纯的液、固态物质压力变化不大的变温过程。
3. 内能变 (1)△U=Qv式中Qv 为恒热容。
此式适用于封闭系统,W`=0、dV=0的过程。
△ U=⎰21,v T T m dT nC =)(12,v T -T m nC 式中m C ,v 为摩尔定容热容。
此式适用于n 、C V ,m 恒定,理想气体单纯p 、V 、T 变化的一切过程. 4. 热容 (1) 定义当一系统由于加给一微小的热容量δQ 而温度升高dT 时,δQ/dT 这个量即热容。
δ/d (/)p p p C Q T H T ==∂∂δ/d (/)V V V C Q T U T ==∂∂(2) 摩尔定容热容C V ,m C V ,m =C V /n=(TU mаа)V (封闭系统,恒容,W 非=0) (3)摩尔定压热容C p,mC p ,m ==n p C P⎪⎭⎫⎝⎛T H m аа (封闭系统,恒压,W 非=0) (4) C p, m 与 C V,m 的关系系统为理想气体,则有C p , m —C V ,m =R 系统为凝聚物质,则有C p, m —C V ,m ≈0(5)热容与温度的关系,通常可以表示成如下的经验式 C p , m =a+bT+cT 2或C p , m =a+b`T+c`T -2式中a 、b 、c 、b`及c`对指定气体皆为常数,使用这些公式时,要注意所适用的温度范围。
(6)平均摩尔定压热容C p,mC p ,m =⎰21,T T m p dT nC (T 2—T 1)四、理想气体可逆绝热过程方程,m 2121(/)(/)1V CR T T V V =,m2121(/)(/)1p C RT T p p -=1)/)(/(1212=r V V p pγγ2211V p V p =上式γ=m C ,p /m C ,v ,称为热容比(以前称为绝热指数),以上三式适用于m C ,v 为常数,理想气体可逆绝热过程,p ,V,T 的计算。
五、反应进度 ξ=△n B /v B上式适用于反应开始时的反应进度为零的情况,△n B =n B —n B ,0,n B,0为反应前B 的物质的量。
νB 为B 的反应计算数,其量纲为1。
ξ的单位为mol. 六、热效应的计算 1.不做非体积功的恒压过程 Q p =△H=⎰21,T T m p dT nC2.不做非体积功的恒容过程 Q v =△U=⎰21,v T T m dT nC3.化学反应恒压热效应与恒容热效应关系 Q p - Q v =(△n )RT4.由标准摩尔生成焓求标准摩尔反应焓变Θm rH △=∑ΘBm f B)(H vB △5由标准摩尔燃烧焓求标准摩尔反应焓变Θm rH △=—∑ΘBm C )(H B v B △6。
m rH △与温度的关系 基希霍夫方程的积分形式ΘmrH △(T 2)= ΘmrH △(T 1)+ ⎰Θ21)(,T T m p dT B rC △基希霍夫方程的微分形式d Θm rH △=△r Θm p ,C dT=∑ΘBm p B vBC )(,七、体积功 (1)定义式V p W d amb -=∂或 V p W d amb ∑-= (2) )()(1221T T nR V V p W--=--=适用于理想气体恒压过程。
(3) )(21amb V V p W --= 适用于恒外压过程.(4) )/ln()/ln(d 121221p p nRT V V nRT V p WV V =-=-=⎰ 适用于理想气体恒温可逆过程。
(5) ,m 21()V WU nC T T =∆=- 适用于,m V C 为常数的理想气体绝热过程。
典型题示例1—1 1mol 理想气体于27℃ 、101325Pa 状态下受某恒定外压恒温压缩到平衡,再由该状态恒容升温到97 ℃ ,则压力升到1013。
25kPa.求整个过程的W 、Q 、△U 及△H 。
已知该气体的C V ,m 恒定为20。
92J •mol —1 •K -1。
解题思路:需先利用理想气体状态方程计算有关状态: (T 1=27℃, p 1=101325Pa,V 1)→(T 2=27℃, p 2=p 外=?,V 2=?) →(T 3=97℃, p 3=1013.25kPa ,V 3=V 2)1-2水在 -5℃ 的结冰过程为不可逆过程,计算时要利用0℃ 结冰的可逆相变过程,即H 2O (l ,1 mol,—5℃ ,θp2O(s ,1 mol ,—5℃,θp ) ↓△H 2↑△H 4H 2O (l ,1 mol , 0℃,θp 2O (s ,1 mol ,0℃,θp )∴ △H 1=△H 2+△H 3+△H 41—3 在 298.15K 时,使 5。
27 克的甲醇(摩尔质量为32克) 在弹式量热计中恒容燃烧,放出 119。
50kJ 的热量。
忽略压力对焓的影响。
(1) 计算甲醇的标准燃烧焓 θm c H ∆。
(2) 已知298。
15K 时 H 2O (l) 和CO 2(g )的标准摩尔生成焓分别为-285。
83 kJ·mol -1 、-393.51 kJ·mol -1,计算CH 3OH (l)的θm f H ∆.(3) 如果甲醇的标准蒸发焓为 35。
27kJ·mol -1,计算CH 3OH (g )的θm f H ∆。
解:(1) 甲醇燃烧反应:CH 3OH (l) +23O 2(g) → CO 2(g ) + 2H 2O (l)θm c U ∆=-119.50 kJ/(5.27/32)mol =-725。
62 kJ·mol -1θm c H ∆=θm c U ∆+∑RT v )g (B= (-725。
62-0.5×8.3145×298.15×10-3)kJ·.mol -1 =-726。
86 kJ·mol -1(2) θm c H ∆=θm f H ∆(CO 2) + 2θm f H ∆(H 2O )-θm f H ∆ [CH 3OH(l)] θm f H ∆[CH 3OH (l )] =θm f H ∆ (CO 2) + 2θm f H ∆ (H 2O )-θm c H ∆= [-393.51+2×(-285。
83)-(-726。
86) ] kJ·mol -1=-238。
31 kJ·mol -1(3) CH 3OH (l) →CH 3OH (g ) ,θm vap ΔH= 35。
27 kJ·。
mol-1θm f H ∆[CH 3OH (g )] =θm f H ∆[CH 3OH (l)] +θmvap H ∆ = (-38。
31+35.27)kJ·.mol -1=-203。
04 kJ·mol -1第三章 热力学第二定律一、 卡诺循环 1.热机效率η=—W/Q 1=(Q 1+Q 2)/Q 1=(T 1—T 2)/T 1式中Q 1和Q 2分别为工质在循环过程中从高温热源T 1吸收热量和向低温热源T 2放出热量这两个过程的可逆热.此式适用于在两个不同的温度之间工作的热机所进行的一切可逆循环. 2.卡诺循环所有工作于两个确定温度之间的热机,以可逆热机效率最大。
η1r ηr即是Q 1/T 1+Q 2/T 2 ≤0⎪⎪⎭⎫⎝⎛=<可逆循环不可逆循环 式中T 1、T 2为高低温热源的温度。
可逆时等于系统的温度。
二、热力学第二定律 1。
克劳修斯说法“不可能把热从低温物体传到高温物体而不产生其他影响。
” 2.开尔文说法“不可能从单一热源吸取热量使之完全转变为功而不产生其他影响。
” 三、熵 1.熵的定义 d S def δQ r /T式中Q r 为系统与环境交换的可逆热,T 为可逆热δQ r 时系统的温度。
2.克劳修斯不等式dS ⎭⎬⎫⎩⎨⎧>=,不可逆过程δ,可逆过程δT Q T Q //3.熵判据△S iso =△S sys +△S amb ⎭⎬⎫⎩⎨⎧=>,可逆不可逆0,0式中iso 、sys 和amb 分别代表隔离系统、系统和环境。
在隔离系统中,不可逆过程即自发过程。
可逆,即系统内部及系统与环境之间处于平衡态。
在隔离系统中,一切自动进行的过程都是向熵增大的方向进行,这称为熵增原理。
此式只适用于隔离系统。
四、熵变的计算 1。
单纯的PVT 变化过程中无相变化和化学变化,W`=0,可逆。
△S=⎰21T Q rδ=⎰+21T pdV dU =⎰+21TVdp dH理想气体系统△S=nC V ,m ln 12T T +nRln 12V V = nC p,m ln 12T T - nRln 12p p = n C p ,m l n 12V V+ n C V ,m ln12p p 恒温(T 1=T 2)△S= nRln12V V =- nRln 12p p恒压(p 1=p 2)△S= nC p,m ln12T T = n C p ,m l n 12V V恒容(V 1=V 2)△S= nC V ,m ln 12T T = n C V ,m ln 12p p凝聚相系统 △S=⎰21TQ rδ 恒容△S =T,v 21dT nC m T T ⎰恒压△S=⎰21T,T Tm p dT nC恒温△S=δQ r /T 2.相变化可逆变化βα△S=βα△H/T不可逆相变,通常设计一条要包括可逆相变步骤在内的可逆途径,此可逆途径的热温熵才是该不可逆过程的熵变。
