电极电势
电极电势

电极电势一,电极电势(electrode potential)的产生—双电层理论德国化学家能斯特(H.W.Nernst)提出了双电层理论(electron double layer theory)解释电极电势的产生的原因。
当金属放入溶液中时,一方面金属晶体中处于热运动的金属离子在极性水分子的作用下,离开金属表面进入溶液。
金属性质愈活泼,这种趋势就愈大;另一方面溶液中的金属离子,由于受到金属表面电子的吸引,而在金属表面沉积,溶液中金属离子的浓度愈大,这种趋势也愈大。
在一定浓度的溶液中达到平衡后,在金属和溶液两相界面上形成了一个带相反电荷的双电层(electron double layer),双电层的厚度虽然很小(约为10-8厘米数量级), 但却在金属和溶液之间产生了电势差。
通常人们就把产生在金属和盐溶液之间的双电层间的电势差称为金属的电极电势(electrode potential),并以此描述电极得失电子能力的相对强弱。
电极电势以符号E Mn+/ M表示, 单位为V(伏)。
如锌的电极电势以EZn2+/ Zn 表示, 铜的电极电势以ECu2+/Cu 表示。
电极电势的大小主要取决于电极的本性,并受温度、介质和离子浓度等因素的影响。
2.标准电极电势为了获得各种电极的电极电势数值,通常以某种电极的电极电势作标准与其它各待测电极组成电池,通过测定电池的电动势, 而确定各种不同电极的相对电极电势E值。
1953年国际纯粹化学与应用化学联合会(IUPAC)的建议,采用标准氢电极作为标准电极,并人为地规定标准氢电极的电极电势为零。
(1)标准氢电极电极符号: Pt|H2(101.3kPa)|H+(1mol.L-1)电极反应: 2H+ + 2e = H2(g)E⊖H+/ H2 = 0 V右上角的符号“⊖”代表标准态。
标准态要求电极处于标准压力(100kPa或1bar)下,组成电极的固体或液体物质都是纯净物质;气体物质其分压为100kPa;组成电对的有关离子(包括参与反应的介质)的浓度为1mol.L-1(严格的概念是活度)。
标准电极电势

标准电极电势
标准电极电势是指在标准状况下,电极与氢气电极之间的电势差。
标准电极电势表示了电极在标准条件下的氧化还原反应倾向性。
标准电极电势通常用E表示,单位是伏特(V)。
标准状况是
指气体的压强为1 atm,溶液中物质的浓度为1 mol/L。
氢气电极被定义为标准电极,其标准电势被定义为0 V。
标准电极电势有助于我们了解溶液中的氧化还原反应的方向和强度。
正的标准电极电势表示该电极更容易被还原,反应趋向于发生还原反应;负的标准电极电势表示该电极更容易被氧化,反应趋向于发生氧化反应。
标准电极电势是通过比较氧化还原反应中的两个电极来确定的。
当两个电极连接在一起,并通过一根导线和一个盐桥连接时,就会发生氧化还原反应。
此时,两个电极之间会发生电子转移,产生电势差。
标准电极电势的测量通常是通过电池电势测量仪来进行的。
电池电势测量仪通过将待测电极与参比电极(如银/银离子电极)连接起来,测量两个电极之间的电势差来确定标准电极电势。
标准电极电势的值是通过实验测量得到的,常用的一些标准电极电势包括铜电极(Cu/Cu2+)的标准电极电势为0.34 V,铁
电极(Fe/Fe2+)的标准电极电势为-0.44 V,银电极(Ag/Ag+)的标准电极电势为0.80 V等。
标准电极电势可以用来预测氧化还原反应是否会发生以及反应的方向。
当两个电极之间的电势差大于0时,氧化还原反应会发生;当电势差小于0时,反应不会发生。
总之,标准电极电势是表示电极在标准条件下发生氧化还原反应的倾向性的物理量。
它的应用广泛,可以用于预测氧化还原反应的方向和强度,有助于我们理解化学反应的基本原理。
电极电势与氧化还原反应的关系

电极电势与氧化还原反应的关系1. 电极电势的概念电极电势是指电化学反应中电子在电极上移动所产生的电场势能。
它是一个重要的物理量,可以用来描述化学反应的进行方向和速率。
2. 电极电势的测定电极电势可以通过电池或电化学电池进行测定。
在电池的正极和负极之间产生的电势差就是电极电势。
3. 电极电势与氧化还原反应的关系氧化还原反应指的是物质失去电子(氧化)和物质获得电子(还原)的过程。
这些过程会伴随着电化学反应产生电势。
不同的氧化还原反应具有不同的电极电势。
4. 电极电势的计算根据化学反应生成或消耗的电子数目,可以利用法拉第定律和纳迪尔方程来计算电极电势。
这些定律和方程可以帮助我们理解电化学反应中电势的变化。
5. 电极电势与标准电极电势标准电极电势是指在标准状态下(通常指气压为 1 atm,溶液浓度为1 M)测定的电极电势。
它是一种用来比较不同氧化还原反应电势大小的物理量,常用标准氢电极作为参比电极。
6. 电极电势与电化学反应动力学电极电势可以影响氧化还原反应的进行速率。
通常情况下,电极电势越大,氧化还原反应越容易进行,速率越快。
7. 应用电极电势的研究在多个领域有着广泛的应用,例如在燃料电池、电化学传感器、电镀和金属腐蚀等方面都有重要的作用。
通过对电极电势的理解和控制,可以提高这些应用的效率和性能。
总结:电极电势作为电化学领域中的重要物理量,与氧化还原反应有着密切的关系。
通过对电极电势的测定、计算和应用,可以深入理解和控制氧化还原反应的进行和速率,从而推动电化学领域的发展,并促进相关应用的进步和改进。
8. 电极电势与溶液中的化学平衡在电化学反应中,溶液中的化学平衡也会影响电极电势的大小。
根据化学平衡原理,不同物质的浓度对于电极电势也会产生影响。
在有些氧化还原反应中,溶液中的氧化物或还原物质的浓度变化会导致电极电势的变化。
在研究电极电势的时候,需要考虑到溶液中的化学平衡对电极电势的影响,这可以通过应用“Nernst方程”来描述。
标准电极电势的计算

标准电极电势的计算标准电极电势是指在标准状态下,电极与溶液中的阳离子或阴离子达到平衡时的电势差。
它是评价电极的氧化还原能力的重要指标,对于电化学反应的研究和应用具有重要意义。
本文将介绍标准电极电势的计算方法及其相关知识。
首先,我们需要了解标准电极电势的定义。
标准电极电势常用符号表示为E°,它是电极在标准状态下的电势。
标准状态是指溶液中所有活性物质的浓度为1mol/L,气体的压强为1atm,温度为25℃。
在标准状态下,电极与溶液中的阳离子或阴离子达到平衡时的电势差即为标准电极电势。
其次,标准电极电势的计算方法主要有两种,一种是利用标准电极电势表直接查找,另一种是利用液体电池的原理进行计算。
首先介绍第一种方法,即利用标准电极电势表直接查找。
标准电极电势表是根据一系列标准电极电势测定结果编制而成的,其中包括了各种电极在标准状态下的电势数值。
我们可以通过查找标准电极电势表,找到所需电极在标准状态下的电势数值,从而得到标准电极电势的数值。
另一种方法是利用液体电池的原理进行计算。
液体电池是由两个电极和它们之间的电解质组成的,利用化学反应产生电能。
根据液体电池的原理,我们可以通过电极的反应方程式和反应的标准电极电势来计算标准电极电势。
具体步骤是,首先编写电极的反应方程式,然后查找反应的标准电极电势,最后根据电极反应的标准电极电势差来计算所求电极的标准电极电势。
需要注意的是,计算标准电极电势时,反应方程式的系数需要考虑反应的倍数。
另外,标准电极电势的计算还需要考虑电极的位置,即在标准氢电极之上还是之下,以及电极反应的方向等因素。
总之,标准电极电势的计算是电化学研究中的重要内容,它涉及到电极的氧化还原能力以及电化学反应的进行。
通过本文的介绍,相信读者对标准电极电势的计算方法有了更清晰的认识,希望能对您的学习和研究有所帮助。
标准电极电势

标准电极电势什么是电极电势?在电化学中,电极电势是指电极与标准氢电极之间的电势差。
标准氢电极是一个被普遍接受的参考电极,其电势被定义为0V。
电极电势可以用来描述化学反应中电子的转移方向和强度。
电极电势的测量和标准电极电势电极电势的测量可以通过将待测电极与参比电极连接在同一个电解质溶液中,然后测量电解质溶液的电位差来实现。
常用的参比电极有标准氢电极、银/银氯化银电极和饱和甘汞电极等。
标准电极电势是指在标准状况下,即1M离子浓度、1atm 气压和298K温度下,测量得到的电极电势值。
标准电极电势常用于表征化学反应的方向性和反应强度。
标准电极电势具有广泛的应用,例如在电池、电解和腐蚀等方面。
电极的分类根据电势大小,电极可以分为银电极、铜电极、铂电极等。
其中银电极常用作参比电极,铜电极常用于测量离子浓度,而铂电极则常用于催化反应。
另外,根据电极上的化学反应类型,电极可分为氧化还原电极、金属电极和气体电极等。
氧化还原电极是其中最常见的一类,它涉及电子的转移和氧化还原过程。
金属电极主要用来测量金属离子的浓度,而气体电极则用于测量气体溶解度和甲烷等气体的浓度。
影响电极电势的因素电极电势的大小受到许多因素的影响,主要包括温度、电解质浓度、气体分压和电极材料等。
1.温度:电极电势随温度的升高而增加,每10°C的温度升高,电极电势会增加约0.003V。
2.电解质浓度:电极电势与电解质的浓度呈对数关系,即Nernst方程中的对数项。
3.气体分压:气体电极的电势与溶液中气体的分压成正比,例如在氧电极中,氧分压越高,电极电势越大。
4.电极材料:电极的材料也会对电势产生影响。
不同的材料具有不同的电极电势值。
Nernst方程Nernst方程是描述电极电势与化学反应浓度之间关系的数学表达式。
对于化学反应:A +B →C + D其中,A和B是反应物,C和D是生成物,可以根据这个反应的化学计量关系和反应的电子转移数推导出该反应的Nernst方程。
电极电势的定义

电极电势的定义
电极电势的定义
电极电势是指由于在外电路上的电荷分布不均匀,电极附近电场强度随离开电极的距离而减小的现象。
电位差与场强有关。
两个电极之间的电压不一样,场强也不一样。
比如一个金属棒一端被一块很大的导体(半径r=d,长度l=d/2)覆盖着,另一端和电源负极相连,设导体的电阻率为R,那么电源负极的电势V0的大小为: V0=RCR,场强E0的大小为E0=F(r2/R),则电位差Vz=V0-V0R。
也就是说,当一个电极靠近另一个电极时,电位差就会增加。
比如,手握一根电线,会感觉到电线靠近手掌部分的电阻较大,因此电位差也较大。
再如,同一电线,放在干燥的空气中与放在潮湿的空气中相比,前者电位差较大。
场强变化电势变化例子:
( 1)平行板电容器的电势能随离平板的距离变化而变化.如果将一块带正电荷q的金属箔片和一块带负电荷q的金属箔片相接触,然后让它们分别接触一个有内电阻R的电极板,则两个电极上的电压分别为: Q=(V/R)e和Q=(V/R)e。
将Q=V/R的金属箔片放入另一块有内电阻r的电极板中,结果将得到平行板电容器。
这种金属箔片称为正极材料。
电极电势计算公式如下:
1、电极电势(内电场力) =V
电极电势可以通过电池反应实验测得。
电池反应的正极产生氧气,负极产生氢气。
测量的电势与标准状况下理想气体反应的计算值相同,但是对实际情况要做一些修正。
电极电势可以通过电池反应实验测得。
电池反应的正极产生氧气,负极产生氢气。
测量的电势与标准状况下理想气体反应的计算值相同,但是对实际情况要做一些修正。
电极电势
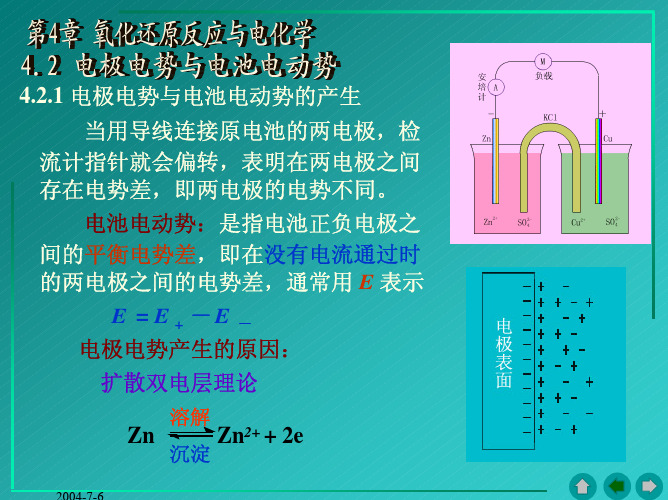
这个重要概念,用来解释沉淀反应。他用量子理论的观点 研究低温下固体的比热;提出光化学的“原子链式反应”理 论。1906年,根据对低温现象的研究,得出了热力学第三 定律,人们称之为“能斯特热定理”,这个定理有效地解决 了计算平衡常数问题和许多工业生产难题。因此获得1920
lg
[c(Red) / cP ]b [c(Ox) / cP ]a
25℃时,
E (Ox/Red )
注意:
=
E P (Ox/Red ) +
0.0592 n
lg
[c(Ox ) / cP ]a [c(Red ) / cP ]b
(1) 反应体系中是固体或纯液体时,其浓度视为1。对于气体组 分,用分压代替浓度,并要将分压作标准化处理
E = EP − 2.303RT lg Q nF
25℃时,
E = E P − 0.0592 lg Q n
4.2.3 影响电极电势的因素——能斯特方程
电极电势的能斯特方程式:
对于 a Ox + ne → bRed E P(Ox/Red)
E (Ox/Red)
=
E P (Ox/Red) −
2.303 RT nF
正值意味着标准铜电极
负值意味着标准锌电极
的电势比标准氢电极高
的电势比标准氢电极低
参
比
甘汞电极
电
KCl溶液 Pt Hg
Cl -(c) | Hg2Cl2(s)|Hg(l) 电极反应:
极
Hg2Cl2
Hg2Cl2(s) + 2e → 2Hg(l)+2Cl-(c)
素瓷头
甘汞电极的电极电势与KCl浓度的关系
电化学中电极电势的测定

电化学中电极电势的测定电极电势是电化学研究中一个重要的参数,它描述了电极与电解质溶液中离子的相互作用能力。
在分析电化学反应机制、电极材料的性质时,需要对电极电势进行测定。
本文将介绍电位差法和电动势法两种测定电极电势的方法。
一、电位差法电位差法是一种间接测定电极电势的方法。
电位差法利用标准电极与待测电极之间的电位差进行测定。
标准电极的电势是经过标准化的,可以精确地测定。
待测电极的电势可以通过与标准电极进行比较,间接地求出。
电位差法的基本原理是在电解质溶液中,电极的电位是由反应物和产物浓度之比决定的。
标准电极可以在溶液中产生一个已知的电位,这种电位称为标准电势。
在电解质溶液中,符合德拜-亨利定律的电极间电势差与反应物和产物的浓度比例成正比。
但是在实际情况下,电极电势会受到扰动因素的影响,如温度、浓度梯度变化、溶液pH值等。
因此,在使用电位差法进行测定时,需要对扰动因素进行控制。
二、电动势法电动势法是一种直接测定电极电势的方法。
该方法在电极上施加一个电动势,并测量电极上的电势差。
测得的电势差就是电极电势。
电动势法的基本原理是根据欧姆定律,在电极上施加一个电压,使电解质中的离子发生移动。
电极电势是电势差除以电流的比值,电势差通过电动势仪器测量,电流通过电极与电解质溶液的接触电阻和电阻计进行测量。
在使用电动势法进行测定时,需要注意的是使用合适的电解质、电极材料和电位范围。
电解质的类型和浓度对电极电势有较大的影响,而电极材料的选择也要考虑到电解质中离子的大小、电荷和化学反应性等因素。
另外,电位范围要控制在电极的安全极限内。
三、小结电位差法和电动势法都是测定电极电势的有效方法。
电位差法适用于间接测定电极电势,通过比较标准电势和待测电极电势之间的电位差,求出待测电极的电势。
而电动势法采用直接测定电极电势的方法,通过施加电压和测量电流,得出电极电势。
在实际应用中需要根据具体情况选择合适的方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电极电势1.电极电势的产生—双电层理论德国化学家能斯特(H.W.Nernst)提出了双电层理论(electron double layer theory)解释电极电势的产生的原因。
当金属放入溶液中时,一方面金属晶体中处于热运动的金属离子在极性水分子的作用下,离开金属表面进入溶液。
金属性质愈活泼,这种趋势就愈大;另一方面溶液中的金属离子,由于受到金属表面电子的吸引,而在金属表面沉积,溶液中金属离子的浓度愈大,这种趋势也愈大。
在一定浓度的溶液中达到平衡后,在金属和溶液两相界面上形成了一个带相反电荷的双电层(electron double layer),双电层的厚度虽然很小(约为10-8厘米数量级), 但却在金属和溶液之间产生了电势差。
通常人们就把产生在金属和盐溶液之间的双电层间的电势差称为金属的电极电势(electrode potential),并以此描述电极得失电子能力的相对强弱。
电极电势以符号E Mn+/ M表示, 单位为V(伏)。
如锌的电极电势以EZn2+/ Zn 表示, 铜的电极电势以ECu2+/Cu 表示。
电极电势的大小主要取决于电极的本性,并受温度、介质和离子浓度等因素的影响。
2.标准电极电势为了获得各种电极的电极电势数值,通常以某种电极的电极电势作标准与其它各待测电极组成电池,通过测定电池的电动势, 而确定各种不同电极的相对电极电势E值。
1953年国际纯粹化学与应用化学联合会(IUPAC)的建议,采用标准氢电极作为标准电极,并人为地规定标准氢电极的电极电势为零。
(1)标准氢电极电极符号: Pt|H2(101.3kPa)|H+(1mol.L-1)电极反应: 2H+ + 2e = H2(g)EφH+/ H2 =0 V右上角的符号“φ”代表标准态。
标准态要求电极处于标准压力(101.325kPa)下,组成电极的固体或液体物质都是纯净物质;气体物质其分压为101.325kPa;组成电对的有关离子(包括参与反应的介质)的浓度为1mol.L-1(严格的概念是活度)。
通常测定的温度为298K。
(2) 标准电极电势用标准氢电极和待测电极在标准状态下组成电池,测得该电池的电动势值,并通过直流电压表确定电池的正负极,即可根据E池= E(+)-E(-)计算各种电极的标准电极电势的相对数值。
例如在298k,用电位计测得标准氢电极和标准zn电极所组成的原电池的电动势(E池)为0.7628v,根据上式计算Zn2+/Zn电对的标准电极为-0.7628v。
用同样的办法可测得Cu2+/Cu电对的电极电势为+0.34v。
电极的E⊖为正值表示组成电极的氧化型物质,得电子的倾向大于标准氢电极中的H+,如铜电极中的Cu2+;如电极的为负值,则组成电极的氧化型物质得电子的倾向小于标准氢电极中的H+,如锌电极中的Zn2+。
实际应用中,常选用一些电极电势较稳定电极如饱和甘汞电极和银-氯化银电极作为参比电极和其它待测电极构成电池,求得其它电极的电势。
饱和甘汞电极的电极电势为0.2412V。
银-氯化银电极的电极电势为0.2223V。
3. 标准电极电势表将不同氧化还原电对的标准电极电势数值按照由小到大的顺序排列,得到电极反应的标准电极电势表。
其特点有:(l)一般采用电极反应的还原电势,每一电极的电极反应均写成还原反应形式,即:氧化型+ne =还原型,(2)标准电极电势是平衡电势,每个电对E⊖值的正负号,不随电极反应进行的方向而改变。
(3)Eφ值的大小可用以判断在标准状态下电对中氧化型物质的氧化能力和还原型物质的还原能力的相对强弱,而与参与电极反应物质的数量无关。
例如:I2+2e =2I- Eφ= +0.5355V1/2I2+e = I- Eφ= +0.5355V(4)Eφ值仅适合于标准态时的水溶液时的电极反应。
对于非水、高温、固相反应,则不适合。
三.电极电势的应用(一)、判断氧化剂和还原剂的相对强弱在标准状态下氧化剂和还原剂的相对强弱,可直接比较Eφ值的大小。
Eφ值较小的电极其还原型物质愈易失去电子,是愈强的还原剂,对应的氧化型物质则愈难得到电子,是愈弱的氧化剂。
Eφ值愈大的电极其氧化型物质愈易得到电子,是较强的氧化剂,对应的还原型物质则愈难失去电子,是愈弱的还原剂。
在标准电极电势表中, 还原型的还原能力自上而下依次减弱,氧化型的氧化能力自上而下依次增强。
[例1] 在下列电对中选择出最强的氧化剂和最强的还原剂。
并指出各氧化态物种的氧化能力和各还原态物种的还原能力强弱顺序。
MnO4-/Mn2+、Cu2+/Cu、Fe3+ /Fe2+、I2/I-、Cl2/Cl-、Sn4+/Sn2+(二)、判断氧化还原反应的方向1.根据Eφ值,判断标准状况下氧化还原反应进行的方向。
通常条件下,氧化还原反应总是由较强的氧化剂与还原剂向着生成较弱的氧化剂和还原剂方向进行。
从电极电势的数值来看,当氧化剂电对的电势大于还原剂电对的电势时,反应才可以进行。
反应以“高电势的氧化型氧化低电势的还原型”的方向进行。
在判断氧化还原反应能否自发进行时,通常指的是正向反应。
2.根据电池电动势Eφ池值,判断氧化还原反应进行方向。
任何一个氧化还原反应,原则上都可以设计成原电池。
利用原电池的电动势可以判断氧化还原反应进行的方向。
由氧化还原反应组成的原电池,在标准状态下,如果电池的标准电动势>0, 则电池反应能自发进行;如果电池的标准电动势<0, 则电池反应不能自发进行。
在非标准状态下,则用该状态下的电动势来判断。
从原电池的电动势与电极电势之间的关系来看,只有>时,氧化还原反应才能自发地向正反应方向进行。
也就是说,氧化剂所在电对的电极电势必须大于还原剂所在电对的电极电势,才能满足E >0的条件。
从热力学讲电池电动势是电池反应进行的推动力。
当由氧化还原反应构成的电池的电动势Eφ池大于零时,则此氧化还原反应就能自发进行。
因此,电池电动势也是判断氧化还原反应能否进行的判据。
电池通过氧化还原反应产生电能,体系的自由能降低。
在恒温恒压下,自由能的降低值(-△G)等于电池可能作出的最大有用电功(W电):-△G=W电=QE=nFE池即△G=-nFE池在标准状态下,上式可写成:△Gφ =-nFEφ池当Eφ池为正值时,△Gφ为负值,在标准状态下氧化还原反应正向自发进行;当Eφ池为负值时,△Gφ为正值,在标准状态下反应正向非自发进行,逆向反应自发进行。
E或Eφ愈是较大的正值,氧化还原反应正向自发进行的倾向愈大。
E池或Eφ池愈是较大的负值,逆向反应自发进行的倾向愈大。
[例2] 试判断反应Br + 2Fe 2Fe +2Br 在标准状态下进行的方向。
解:查表知:Fe + e Fe =+0.771VBr + 2e 2Br =+1.066V由反应式可知:Br 是氧化剂,Fe 是还原剂。
故上述电池反应的=+1.066-0.771=0.295V>0(三).判断反应进行的限度——计算平衡常数一个化学反应的完成程度可从该反应的平衡常数大小定量地判断。
因此,把标准平衡常数Kφ和热力学吉布斯自由能联系起来。
△Gφ=-2.303RTlgKφ△Gφ=-nFEφ则:-nFEφ = 2.303RTlgKφ标准平衡常数Kφ和标准电动势Eφ之间的关系式为:-nFEφlgKφ = ————————2.303RTR为气体常数,T为绝对温度,n为氧化还原反应方程中电子转移数目,F为法拉第常数。
该式表明,在一定温度下,氧化还原反应的平衡常数与标准电池电动势有关,与反应物的浓度无关。
Eφ越大,平衡常数就越大,反应进行越完全。
因此,可以用Eφ值的大小来估计反应进行的程度。
一般说,Eφ≥0.2~0.4V的氧化还原反应,其平衡常数均大于106( K>106 ),表明反应进行的程度已相当完全了。
Kφ值大小可以说明反应进行的程度,但不能决定反应速率。
四、影响电极电势的因素从下面的反应可以看出MnO4-在酸性、中性、碱性的反应和产物都不同。
这就说明电极电势在不同的条件下是不同的。
影响电极电势的因素是什么呢?这些因素又是为什么影响电极电势的呢?影响电极电势的因素是离子的浓度、溶液的酸碱性、沉淀剂和络合剂,判断的因素是能斯特方程。
1、能斯特方程式标准电极电势是在标准状态下测定的。
如果条件改变,则电对的电极电势也随之发生改变。
电极电势的大小,首先取决于电极的本性,它是通过标准电极电势来体现的。
其次,溶液中离子的浓度(或气体的分压)、温度等的改变都会引起电极电势的变化。
它们之间的定量关系可由能斯特方程式来表示:由于温度对电极电势的影响较小,而一般化学反应又在常温(298K)下进行,若在298K时,将自然对数变换为以10为底的对数,并将R和F等常数代入,则能斯特方程式可写为:〖说明〗:(1)Eφ为电极的标准电极电势; n为电极反应中电子转移数;(2)[氧化型]/ [还原型]表示参与电极反应所有氧化型物质浓度幂次方(包括反应式中的H+或OH-)的乘积与还原型物质浓度幂次方(包括反应式中的H+或OH-)乘积之比。
(3)浓度的幂次方应等于它们在电极反应中的系数.(4)纯固体、纯液体和水的浓度为常数,作1处理。
离子浓度单位用mol.L-1(严格地说应用活度)。
气体用分压Pa表示。
五.元素电势图及其应用大多数非金属元素和过渡元素可以存在几种氧化值,各氧化值之间都有相应的标准电极电势。
可将其各种氧化值按高到低(或低到高)的顺序排列,在两种氧化值之间用直线连接起来并在直线上标明相应电极反应的标准电极电势值,以这样的图形表示某一元素各种氧化值之间电极电势变化的关系图称为元素电势图,因是拉特默(Latimer)首创,故又称为拉特默图。
根据溶液pH值的不同,又可以分为两大类:(A表示酸性溶液)表示溶液的pH=0;(B表示碱性溶液)表示溶液的pH=14。
书写某一元素的电势图时,既可以将全部氧化值列出,也可以根据需要列出其中的一部分。
〖例如氯的元素电势图〗。
在元素电位图的最右端是还原型物质,如Cl ,最左端是氧化型物质,如ClO 。
中间的物质,相对于右端的物质是氧化型,相对于左端的物质是还原型,例如Cl 相对于Cl 是氧化型,相对于ClO 是还原型。
〖又如氧元素在酸性溶液中的电势图〗元素电势图在主要应用:1.判断歧化反应是否能进行所谓歧化反应,就是在同一个元素中,一部分原子(或离子)被氧化,另一部分原子(或离子)被还原的反应。
若在下列元素电势图中Eφ左Eφ右A ——B —— C若Eφ右>Eφ左,其中间价态B可自发地发生岐化反应,生成A和C。
且Eφ池越大,歧化反应程度越大。
相反地,若Eφ右<Eφ左,则不能发生歧化反应。
〖举例〗:2.计算未知标准电极电势根据元素电势图可从几个相邻氧化态电对的已知标准电极电势,求算不相邻氧化态电对的未知标准电极电势。
