第一章第一节第1课时 腔肠动物
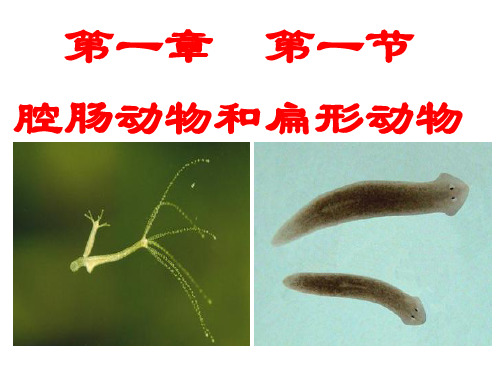
八年级生物上册《第一章-第一节-腔肠动物和扁形动物》

根据形态特征和生活习性,腔肠动物可分为水螅纲(Hydrozoa)、钵水母纲 (Scyphozoa)、珊瑚纲(Anthozoa)等。
形态特征
体型
腔肠动物体型多样,从 微小的水螅体到巨大的
珊瑚礁群体不等。
体壁
消化腔
神经系统
体壁由外胚层和内胚层 两层细胞构成,中间为
胶状物质。
具有一个原始的消化腔, 称为肠腔,与口相通。
03
数据记录和处理方法
在实验过程中及时记录观察到 的现象和数据,如动物的形态 结构特征、运动方式等。
对实验数据进行整理和分析, 比较腔肠动物和扁形动物在形 态结构和生活习性上的异同点。
结合实验数据和相关知识,对 实验结果进行解释和讨论,加 深对两类动物的认识和理解。
06 知识拓展与思考题
相关知识点回顾总结
扁形动物生活习性
扁形动物大多寄生在动物体内或体表,以吸取寄主的营养为生。少数自由生活的种类生活 在土壤或水中。
特点分析
腔肠动物和扁形动物都属于比较低等的动物类群。它们的身体结构简单,没有复杂的器官 系统。腔肠动物的体壁只有两层细胞构成,而扁形动物的体壁则是由三层细胞构成。此外 ,它们的消化系统也比较简单,食物在消化腔内进行消化和吸收。
实验步骤和操作规范
1. 观察腔肠动物
使用显微镜观察水螅的外部形态,注意其身体呈辐射对称,体表有刺细 胞。
用解剖针轻轻挑起水螅,观察其口部和触手,注意触手呈环状排列。
实验步骤和操作规范
2. 观察扁形动物 使用显微镜观察涡虫的外部形态,注意其身体扁平,呈两侧对称。
观察涡虫的感觉器官和运动器官,了解其如何感知外界环境和进行运动。
实验步骤和操作规范
3. 制作临时装片
第一章第一节 腔肠动物和扁形动物-人教优质课教学设计精品

【你认识它吗】
展示水螅图片和基本信息。
教师准备实验材料时并提问小时候常见的水螅怎么找不到了呢?
你怎么知道是环境污染呢?
【合作学习,思考与讨论】
阅读教材P4~P5,组织学生完成任务:
【水螅的身体结构】
邀请小组代表回答问题A,其他小组可以评价补充:
1.不能,你能详细说说吗?
2.你能说出生活中什么物体也可以这样分?怎么分?
3.你说的切面我也可以这样分,但是不对称呀?
4.所以你说的从中间分有没有什么特殊要求?
5.这样体形对于捕食的意义?
【水螅的捕食、消化】
【播放视频】观看水螅的捕食。
邀请小组代表回答问题B,其他小组可以评价补充:(展示图片)
1.水螅摄食通过身体的哪部分结构,排除食物残渣通过身体的哪部分结构?
四、教学方法
以问题为引领,采用任务驱动法,“做中学”,自主学习与合作学习相结合等策略,引导学生调动已有知识经验,通过观察、分析、对比、归纳等方法达成学习目标。
五、教学手段
采用多媒体手段,配以视频、图片资料,使知识信息传递立体化,激发学生学习兴趣。
六、课时安排:1课时。
教学准备
教师准备:教学课件PPT(含图片、视频等资源)。
在书上关键字词标注重点。
图文结合,增加感性认识。
渗透环保教育。
引导与教材对话,提高图文分析能力。
从学生认知水平出发,对话、评价中学习新知识。
视频展示,使抽象知识直观化。
呈现过程,锻炼图文讲解能力。
知识拓展,图片展示生殖过程,易于理解。
锻炼图文理解能力。
梳理知识。
探究主题二:腔肠动物与人类生活的关系
指导学生阅读教材P5,尝试概括腔肠动物与人类生活的关系。
八年级上册生物-第一章-第一节《腔肠动物和扁形动物》

身体扁平,呈两侧对称;具有口和肛 门两个开口,但消化管有两个开口; 体表通常具有纤毛或具有其他运动器 官,如肌肉或足等。
生活习性对比
腔肠动物
大多数生活在水中,如水螅、海葵等;少数生活在潮湿的陆地上,如蚯蚓。
扁形动物
大多数生活在淡水或海水中,如涡虫、血吸虫等;少数种类寄生在人体或其他动物体内,如猪肉绦虫 、蛔虫等。
八年级上册生物-第一章-第一 节《腔肠动物和扁形动物》
目
CONTENCT
录
• 腔肠动物概述 • 扁形动物概述 • 腔肠动物与扁形动物的比较 • 腔肠动物和扁形动物与人类的关系 • 实验探究:观察腔肠动物和扁形动
物
01
腔肠动物概述
定义与分类
定义
腔肠动物是一类具有消化腔和原始神经系统的低等动物,包括水 螅、海葵、海蜇等。
生活环境与习性
生活环境
扁形动物广泛分布于海洋、淡水、陆地等各种环境中,其中 涡虫主要生活在淡水或海水中,而吸虫和绦虫则多寄生于其 他动物体内。
生活习性
扁形动物多为肉食性,以捕食其他小动物或腐食为生。涡虫 具有感光器官,能够感知外界光线变化;吸虫和绦虫则通过 体表感觉器官感知外界环境。
形态结构特点
形态
扁形动物身体扁平,呈两侧对称,这种对称性有利于动物在水中或寄主体内保持 平衡和稳定。
结构
扁形动物具有消化系统、神经系统、生殖系统等基本结构。其中,涡虫具有口、 咽、肠等消化器官;吸虫和绦虫则通过体表吸收寄主体内的营养物质。
繁殖与发育过程
繁殖方式
扁形动物多采用有性生殖方式,雌雄异体或同体。涡虫通过交配后产卵,卵在水中孵化成幼虫;吸虫和绦虫则通 过寄生于寄主体内进行繁殖。
02
八年级上册生物第一章第一节《腔肠动物和扁形动物》

结构特点 有口无肛门, 体表有刺细胞
摄食和消 刺细胞协助捕
化
食
有口无肛门,有肠 和咽等
涡虫的咽可以伸出 口外,另外多数扁 形动物营寄生生活
【合作探究】
有些人喜欢吃生鱼片等食物,你认为食用 未煮熟的鱼是否安全?
【达标检测】
1.腔肠动物所具有的特殊细胞是( ) A.腺细胞 B.刺细胞 C.变形细胞 D.领细胞
• 背腹扁平、两侧对称
有前后、左右、背腹
有头部,背部有一对
黑色眼点,只感光,
无视觉
两侧对称:又称左右对称,是指通过身体的纵轴, 只有一个切面可以将身体分成对称的两部分。
猪带绦虫
华枝睾吸虫的寄主: 纹沼螺 淡水鱼虾 人
华枝睾吸虫的寄主: 纹沼螺 淡水鱼虾 人 日本血吸虫的寄主:
钉螺 人Βιβλιοθήκη 扁形动物的主要特征2.下列动物中营自由生活的腔肠动物是( )
A.血吸虫 B.猪肉绦虫 C.涡虫
D.海葵
3.水螅在营养条件好时,会进行( ) A.有性生殖 B.分裂生殖 C.出芽生殖 D.孢子生殖
4.营自由生活的扁形动物是( ) A.血吸虫 B.涡虫 C.疟原虫 D.猪肉绦虫
7.血吸虫是通过下列哪种方式传播的( ) A.接触疫水 B.食未熟的鱼 C.蚊虫叮咬 D.不讲卫生
哺乳动物 两栖动物
被子植物
本章节按照生物由低等到高等的顺序将动物为腔肠动物、 扁形动物、线形动物、环节动物、软体动物、节肢动物、 鱼类、两栖动物、爬行动物、鸟类和哺乳动物等。
第一章 第一节 腔肠动物、扁形动物
水母
水螅
海葵 珊瑚虫
代表动物——水螅
生态习性
水螅多生活在水 流缓慢、水草繁 茂的清洁淡水中 常附着在水草或 他物上,以小型 的水蚤、蠕虫为 食。它的身体几 乎透明。
腔肠动物和扁形动物教案

第一章动物的主要类群第一节腔肠动物和扁形动物第1课时?腔肠动物?教学设计教学目的:1.知识方面〔1〕知道腔肠动物是一类构造简单的低等多细胞动物。
〔2〕知道腔肠动物与人类的关系。
〔3〕识记腔肠动物的主要特征。
2.才能方面通过对活体水螅和水螅切片的观察,培养学生的动手才能。
观察才能和分析才能。
3.思想情感方面通过对水螅的观察,培养学生爱科学、勇于探究、实事求是的科学精神。
重点难点:1.水螅的形态构造和腔肠动物的主要特征是本课的重点。
因为水螅具备了腔肠动物所有的共同特点。
2.准备活体水螅是上好本课的关键和难点。
因为进展本课教学时,正值三月上旬,我国许多地方从自然环境中采不到水螅,为此需要提早作好准备。
教具准备:活体水螅、水螅纵切切片、显微镜、放大镜、教学软件。
课时安排:本章参考课时1课时。
教学过程1.教学过程设计思路:创设情境提出问题导出课题→ 观察实物→识别构造→作好记录→ 汇报交流→观察结果→归纳整理知识要点→ 观看录像认识理解其他腔肠动物;知道腔肠动物与人类的关系,归纳特征2.教学过程说明:①本课从引导学生复习已经学过的知识入手,如:“原生动物是单细胞动物,还是多细胞动物?〞在学生答复的根底上,老师进一步指出:“在动物界中,只有原生动物是单细胞的,其他动物都是多细胞的。
腔肠动物就是一类低等的多细胞动物。
腔肠动物是怎样构成的?具有什么特点?常见的种类有哪些?与人类有什么关系?腔肠动物的主要特征是什么?这些问题就是我们这节课要研究的问题。
〞由此入手既设置了悬念,又激发了学生渴望学习新知识的欲望,还导出了本课的课题,为上好本课打下良好的根底。
②关于活体水螅和水螅体壁切片的观察,是本节课学生活动的重头戏,也是培养学生才能的关键所在。
有条件的学校最好让学生亲自做一做,没有条件的学校可观察课本上的插图。
处理好这个环节,主要是通过老师的精心组织,正确指导,来调动学生学习的积极性。
备课时,每组要装备观察用具和实物标本各一套,让每位学生都有充分的观察时间,活体水螅应放在小烧杯中,水量应以水螅能充分舒展活动为宜。
腔肠动物的主要特征
代表动物——日本血吸虫
1、危害:血吸虫病,肝脾肿大、腹水、丧失劳动力,死亡 2、寄生部位:哺乳动物的门静脉和肠系膜静脉; 3、中间宿主:钉螺 4、感染状态:尾蚴
•解放前,我 国长江以南省 份大约有1000 多万人患此病, 受此病威胁1 亿多人。
扁形动物门的主要特征
1、身体呈两侧对称, 2、背腹扁平, 3、有口无肛门。
水螅摄食照片
出芽生殖-----无性繁殖
• 芽体长成小水 螅后,就会从 母体上脱落下 来,独立生活。
水 螅 - 芽 体
水螅的运动
借助触手和身体弯曲作尺蠖样运动或翻筋斗运动。
腔肠动物的主要类群
• 现生的腔肠动物约11000种,除少数淡水生活外, 其余皆海产且多数为浅海种类 – 1、水螅纲; – 2、钵水母纲; – 3、珊瑚虫纲
第一章 第一节 腔肠动物和扁形动物
Байду номын сангаас
学习目标
1.描述腔肠动物和扁形动物的主要特征 是什么?
2.说明它们与人类的生活有什么关系?
第一课时 腔肠动物
一、自学(独立阅读教材P3-5,思考下列问 题) 1.腔肠动物生活环境分别是怎样的? 2.腔肠动物常见种类有哪些? 3.腔肠动物主要特征分别是什么?
4.腔肠动物与人类的生活有什么关系?
腔肠动物的主要特征
1、身体呈辐射对称; 2、体表有刺细胞; 3、有口无肛门。
腔肠动物与人类的关系
• 食用:海蜇可加工成营养较高的海 产品;
• 形成珊瑚礁:是海洋生物的主要栖 息场所
归纳: (1)生活环境:水中 (2)常见种类: 海水:水母、海葵、海蜇、珊瑚虫 淡水:水螅 (3)身体特点:外胚层和内胚层构成,身体呈辐射对称。 (4)利用刺细胞,触手捕食、在消化腔内消化食物;利用刺细 胞攻击和防御; (5)水螅可进行有性生殖,也可进行无性生殖——出芽生殖。 (6)主要特征:身体呈辐射对称,具有的刺细胞,有口无肛门。 (7)与人类生活的关系: 食用:海蜇 形成珊瑚礁:珊瑚虫
人教版生物八年级上册第五单元第一章第一节《腔肠动物和扁形动物》

身体扁平,两侧对称
人教版生物八年级上册第五单元第 一章第一节《腔肠动物和扁形动物》
两侧对称:又称左右对称,是指通过身体的 纵轴,只有一个切面可以将身体分为对称的 两部分。 这样的体形有利于动物运动,捕食,和防御。
• 捕食过程:
• 触手将捕获物移向口部;
• 口张开,食物进入消化腔;
• 腺细胞分泌酶行细胞外消化;
• 消化后形成的食物颗粒,由内 皮肌细胞吞入进行细胞内消化。
• 不能消化的残渣再经口排出体 外。
人教版生物八年级上册第五单元第
水螅摄食照片 一章第一节《腔肠动物和扁形动物》
刺细胞的作用
• 刺细胞是腔肠动物特有的攻击 和防御的利器,里面大多藏着 刺丝和毒液,在触手处尤其多。 当遇到猎物或捕食者时,能迅 速弹出刺丝,并将毒液通过刺 丝注入猎物或捕食者体内,将 其麻醉或杀死。
3、通过阅读P4及观察图5-4,概述水螅的内部结构有
什么特点?水螅又是怎样捕食水蚤的?推测他是如何 将水蚤消化的?
4、水螅是怎样繁衍生息的?
5、腔肠动物的主要类群有那些?主要特征是什么?
6、腔肠动物与人类有什么关系?
人教版生物八年级上册第五单元第 一章第一节《腔肠动物和扁形动物》
二、扁形动物
绦虫
水螅
涡虫
身体的对称性 辐射对称
两侧对称
身体的胚层数 两胚层
三胚层
运动能力
较弱
较强
人教版生物八年级上册第五单元第 一章第一节《腔肠动物和扁形动物》
代表动物——水螅
八年级上册生物第一章第一节知识点

八年级上册生物第一章第一节知识点八年级上册生物第一章第一节知识点第一节:腔肠动物和扁形动物1.常见的腔肠动物有:海葵、海蜇、水螅、珊瑚虫等2.水螅的生活环境:水螅通常生活在水流缓慢、水草繁茂的清洁淡水中。
3.水螅的体型:水螅的身体呈辐射对称。
4.水螅的消化腔:体壁由内外胚层和中胶层构成,内胚层围成消化腔,消化食物,有口无肛门。
5.水螅的刺细胞是它攻击和防御的利器。
6.腔肠动物的主要特征:身体呈辐射对称,体表有刺细胞,有口无肛门,食物从口入,残渣从口出。
7.腔肠动物与人类的关系:海蜇经过加工可以食用,珊瑚虫分泌的石灰质形成的珊瑚可供参观。
8.涡虫的形态:身体背腹扁平,前端具有眼点9.涡虫的摄食与消化:口中有咽,食物在消化腔内消化,不能消化的食物残渣由口排出。
10.涡虫的体型:涡虫的身体呈两侧对称。
11.扁形动物的主要特征:身体呈两侧对称,背腹扁平,有口无肛门。
八年级人教版生物上册第一章练习题第一节腔肠动物和扁形动物练习题1 、腔肠动物有 ___ 、 ___ 、 ___ 、 ___ 、 ___ 。
2 、水螅生活在水流缓慢、水草繁茂的 _____ 淡水中;它的体形呈 ____ ,便于 ____ 来自各个方向的刺激。
3 、水螅的身体是由 ______ 和 ______ 两层细胞构成, ______ 围成的空腔叫消化腔,消化腔与 ___ 相通,食物在消化腔内被 ______ 消化,食物残渣从 ___ 排出。
因此水螅有 ___ 无 _____ 。
4 、 _____ 是水螅特有的攻击和防御利器,在 ____ 尤其多。
水螅的生殖方式 _____ 。
5 、腔肠动物的主要特征:○1_______ ; ○2________ ; ○3_______ 。
6 、扁形动物有:自由生活的 ____ ,寄生生活的 ___ 、 ___ 、 ____ 。
7 、涡虫的背腹 ____ ,前端背面有两个黑色 ____ ,口长在 ___ ,口中有一管状的 ___ ,食物在 ___ 内消化,残渣从 ___ 排出。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章动物的主要类群
第一节腔肠动物和扁形动物
第1课时腔肠动物
一、选择题
1.水母、海蜇、珊瑚虫和海葵是常见的腔肠动物。
腔肠动物绝大多数生活在()
A.草原中B.海洋中
C.森林中D.土壤中
2.腔肠动物的主要特征是()
A.身体呈辐射对称B.体表有刺细胞
C.有口无肛门D.以上都正确
3.水螅的生活环境是()
A.有丰富绿藻的海水
B.被污染的废水
C.清澈的急流的大河
D.清澈而水草丰富的池塘或小河
4.水螅的身体只能分出上下,分不出前后、左右和背腹,经过身体的纵轴有多个切面将身体分成完全对称的两部分。
这种体形叫()
A.辐射对称B.左右对称
C.上下对称D.两侧对称
5.水螅属于腔肠动物,如图5-1-3为水螅体壁横切面示意图,下列说法正确的是()
图5-1-3
A.水螅的体壁有3层细胞
B.①是外胚层,②是内胚层
C.水螅身体呈现两侧对称
D.食物残渣通过肛门排出
6.蜇和珊瑚虫排出消化后食物残渣的结构是()
A.肛门B.口
C.胞肛D.体壁
7.水螅体内的结构叫作()
A.空腔B.消化腔
C.体腔D.内脏
8.在水螅周围放些水蚤,活水蚤进入水螅体内的方式()
A.水蚤游到水螅口中
B.水蚤被水螅的触手捕捉,送入口中
C.水蚤被水螅的外胚层吸附,外胚层分泌消化液将其分解
D.水蚤被吞入水螅口中
9.在水温适宜,食物充足时,水螅身体下端三分之一处的体壁会向外突起,渐渐成长为一个小水螅。
成长到一定时期后脱离母体,独立生存,这种生殖方式叫()
A.有性生殖B.分裂生殖
C.出芽生殖D.孢子生殖
10.2019·重庆关于腔肠动物,下列哪一项是错误的()
A.珊瑚虫、海葵、海蜇是腔肠动物
B.身体呈辐射对称
C.腔肠动物有口有肛门
D.都是生活在水中
11.珊瑚礁是如何形成的()
A.水螅分泌的石灰质堆积形成的
B.海蜇分泌的液体形成的
C.珊瑚虫分泌的石灰质形成的
D.海葵分泌的石灰质形成的
二、非选择题
12.图5-1-4所示为水螅的纵切面示意图,据图回答:
图5-1-4
(1)写出图中下列标号的名称:
[①]_________,[②]_________,
[③]_________,[④]_________,
[⑤]_________,[⑥]_________。
(2)食物由________进入;在_________内消化,食物残渣由________排出。
(3)水螅特有的攻击和防御的利器是________,在_______处分布最多。
(4)水螅主要通过_________方式进行生殖。
________长成小水螅后,就会从母体上脱落下来,独立生活。
(5)水螅的体形对于它的生活有何意义?
________________________________________________________________________ ________________________________________________________________________。
1.B[解析] 腔肠动物是一种简单的多细胞动物,大多生活在海洋中,如水母、海蜇、海葵、珊瑚虫等;少数生活在淡水中,如水螅。
2.D
3.D[解析] 水螅通常生活在水流缓慢、水草繁茂的清洁淡水中。
4.A
5.B[解析] 水螅是腔肠动物,腔肠动物的主要特征有:生活在水中;结构简单,体壁由内胚层(内层)、外胚层(外层)构成;身体呈辐射对称,有口无肛门,食物残渣通过口排出。
由图看出①是外胚层,②是内胚层。
6.B[解析] 海蜇和珊瑚虫属于腔肠动物,身体结构简单,辐射对称,有口无肛门,食物由口进入,食物残渣仍然由口排出。
7.B
8.B[解析] 水螅的一端有口,口的周围有触手,用于探寻和捕获食物。
所以在水螅周围放些水蚤,水蚤会被水螅的触手捕捉,送入口中。
9.C
10.C[解析] 珊瑚虫、海葵、海蜇具有腔肠动物的特征,腔肠动物身体呈辐射对称,有口无肛门,食物和食物残渣都由口进出,腔肠动物大都生活在水中。
11.C
12.(1)外胚层内胚层消化腔芽体触手口
(2)口消化腔口
(3)刺细胞触手
(4)出芽芽体
(5)辐射对称的身体结构,便于它感知周围环境中来自各个方向的刺激,从各个方向捕获猎物、进行防御
[解析] 本题考查水螅的形态结构特征。
(1)图示中[①]为外胚层,[②]为内胚层,[③]为消化腔,[④]为芽体,[⑤]为触手,[⑥]为口。
(2)水螅在摄食时,食物由口进入消化腔,在消化腔内消化,消化后的食物残渣仍由口排出。
(3)刺细胞是腔肠动物特有的攻击和防御的利器,在触手处尤其多。
在刺细胞里大多藏有刺丝和毒液,当遇到猎物或捕食者时,水螅能迅速弹出细长而中空的刺丝,并将毒液通过刺丝注入猎物或捕食者体内,将其麻醉或杀死。
(4)水螅主要通过出芽的方式进行生殖。
芽体长成小水螅后,就会从母体上脱落下来,独立生活。
(5)水螅是附着生活的,猎物和捕食者可能来自各个方向,辐射对称的身体结构,便于它感知周围环境中来自各个方向的刺激,从各个方向捕获猎物、进行防御。
