第四章 纳米二氧化钛精讲
纳米二氧化钛

产品简介:纳米二氧化钛是金红石型白色疏松粉末,作为紫外线屏蔽剂,防止紫外线的侵害。
也可用于高档汽车面漆,具有随角异色效应。
纳米技术在光催化领域扮演着重要的角色。
纳米二氧化钛的光催化作用能将光能转变为电能和化学能,实现许多难以实现或不可能进行的反应。
屏蔽紫外线作用强,有良好的分散性和耐候性。
可用于化妆品、功能纤维、塑料、涂料、油漆等领域,。
目前,环境污染的控制与治理是我们面临的亟待解决的重大问题,在众多环境治理技术中,利用太阳光作为光源来活化纳米二氧化钛,使其在室温下进行氧化还原反应,杀灭有害菌、清除污染物,这一技术已成为一种理想的环境治理技术。
纳米二氧化钛属非溶出型抗菌剂,本身具有很好的化学稳定性,无毒性,重金属含量少,抗菌性广且长效,被越来越广泛地应用于日常生活之中。
如太阳能电池、抗菌材料、空气净化器、自清洁材料、精细陶瓷及建筑材料等。
将对提高我们的生活质量发挥无穷潜力。
分类:纳米二氧化钛主要有两种结晶形态:锐钛型(Anatase)和金红石型(Rutile)。
金红石型二氧化钛比锐钛型二氧化钛稳定而致密,有较高的硬度、密度、介电常数及折射率,其遮盖力和着色力也较高。
而锐钛型二氧化钛在可见光短波部分的反射率比金红石型二氧化钛高,带蓝色色调,并且对紫外线的吸收能力比金红石型低,光催化活性比金红石型高。
在一定条件下,锐钛型二氧化钛可转化为金红石型二氧化钛。
结构:纳米材料的两个重要特征是纳米晶粒与高浓度晶界。
纳米TiO2的微观结构特征的研究报道较少。
其中用拉曼散射和高分辨电镜研究了纳米TiO2陶瓷, 显示的结果与通常粗晶材料无多大的区别,晶粒间界处亦含有短程有序的结构单元。
纳米TiO2晶粒基本是等轴晶粒, 与从气体凝聚法得到的原子团簇形状相同, 尺寸相同并都服从对数正态分布。
性能:™纳米TiO2有白色和透明状的两种颗粒,常见的TiO2粉体有金红石、锐钛矿、板钛矿等3 种晶型。
™其中金红石和锐钛矿是四方晶系,板钛矿是正交晶系。
纳米二氧化钛的应用与发展讲义(PPT 78页)

2)我国纳米TiO2生产的发展建议
a.生产工艺的比较
气相法反应速度快,能实现连续化生产,而且 制备的纳米TiO2纯度高、分散性好、团聚少、比表 面活性大,产品特别适合于精细陶瓷材料、催化剂 材料和电子材料。但气相法反应在高温下瞬间完成, 要求反应物料在较短的时间内达到微观上的均匀混 合,对反应器的形式、设备的材质、加热方式、进 料方式均有很高的要求。目前气相法在我国处于小 试阶段,欲达到工业化生产,还要解决一系列工程 问题和设备材质问题。
纳米粉体制备技术研究的科学院所和高校几乎都
在进行和进行过纳米TiO2的研究。重庆大学应用 化学系是国内最早(1989年)研究纳米TiO2的单位, 华东理工大学、中国科学院上海硅酸盐研究所是
目前研究技术较全面、报道最多的单位。
国内主要研究单位与制备方法见表2:
目前,国内涉足纳米TiO2生产的公司约有十家, 总生产能力在1000多吨。四川攀枝花钢铁(集团)公司 钢铁研究院年产200t生产装置是我国技术装备较先进、 品种最为齐全的装置,可以生产金红石型和锐钛型两 大系列各有4个(10~40)nm的粉体品种;
由淮北芦岭煤矿和腾岭工贸有限公司共同组建 的安徽科纳新材料有限公司年产100t生产基地在宿 州市建成;
安徽科纳新材料有限公司生产的KN100A锐钛矿 型纳米级二氧化钛(光触媒) 具有良好的光催化活 性及独特紫外光激活催化作用,其吸收紫外光后形 成的电子-空穴对与吸附与其表面的O2和H2O作用, 生成氢氧自由基,具有很强的氧化能力,能够使绝 大多数的有机物被光催化氧化分解为水和二氧化钛, 从而减轻乃至完全消除原有的危害性。它的性能稳
纳米微粒的小尺寸效应、表面效应、量 子尺寸效应及宏观量子隧道效不具备的特性。
二、纳米TiO2概述
纳米二氧化钛
纳米二氧化钛1引言纳米微粒是指尺寸为纳米量级的超微颗粒,它的尺度大于原子簇,小于通常的微粒,粒径一般在1~100 nm之间。
由于纳米微粒有小尺寸效应、量子尺寸效应、表面效应和宏观量子隧道效应等基本特性,使得纳米微粒以及纳米材料具有常规微粒和常规材料没有的独特的光、电、磁、热以及催化性能。
自从1984年Gleiter 等人关于纳米材料的报道以来,纳米材料以其优异的性能引起人们的普遍关注。
纳米TiO2 是一种附加值很高的功能精细无机材料。
因其具备良好的耐侯性、耐化学腐蚀性、抗紫外线能力强、透明性优异等特点,被广泛应用于汽车面漆、感光材料、光催化剂、化妆品、食品包装材料、陶瓷添加剂、气体传感器及电子材料等。
但由于纳米TiO2 大的比表面及较多的表面空键,在制备和应用过程中极易发生团聚,使其优异的性能得不到充分的发挥。
近年来人们关于纳米TiO2 改性方面的工作已经做了很多,达到了改性的目的,现综述纳米TiO2 的性质与改性的关系及改性的方法和机理。
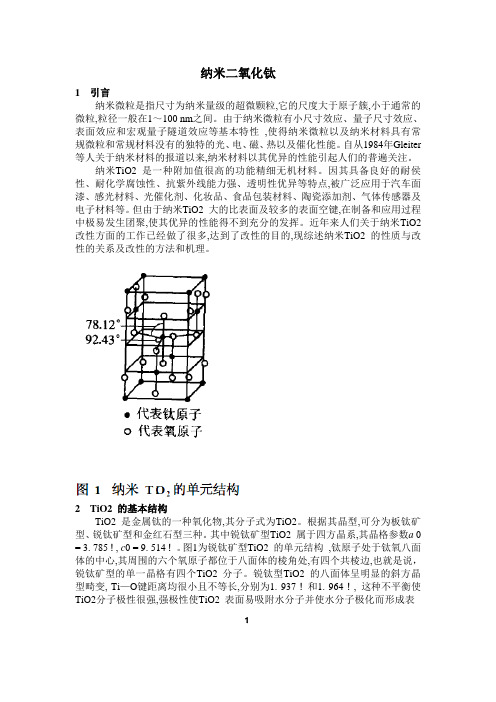
2TiO2 的基本结构TiO2 是金属钛的一种氧化物,其分子式为TiO2。
根据其晶型,可分为板钛矿型、锐钛矿型和金红石型三种。
其中锐钛矿型TiO2 属于四方晶系,其晶格参数a 0 = 3. 785 ! , c0 = 9. 514 ! 。
图1为锐钛矿型TiO2 的单元结构,钛原子处于钛氧八面体的中心,其周围的六个氧原子都位于八面体的棱角处,有四个共棱边,也就是说,锐钛矿型的单一晶格有四个TiO2 分子。
锐钛型TiO2 的八面体呈明显的斜方晶型畸变, Ti—O键距离均很小且不等长,分别为1. 937 ! 和1. 964 ! , 这种不平衡使TiO2分子极性很强,强极性使TiO2 表面易吸附水分子并使水分子极化而形成表1面羟基。
这种表面羟基的特殊结构使其表面改性成为可能,它可作为广义碱与改性剂结合,从而完成对TiO2 的表面改性。
3TiO2 的表面性质3. 1表面超亲水性目前的研究认为,在光照条件下, TiO2 表面的超亲水性起因于其表面结构的变化:在紫外光照射下,TiO2 价带电子被激发到导带,电子和空穴向TiO2 表面迁移,在表面生成电子空穴对,电子与Ti4 +反应,空穴则与表面桥氧离子反应,分别形成正三价的钛离子和氧空位。
新型材料介绍——纳米二氧化钛

纳米TiO2的制备方法
--------液相法
• 液相法主要包括均匀沉淀法、萃取法、溶胶- 凝胶法、溶剂热法等。
• 均物—匀—沉淀钛法液以为硫原酸料法制制备备出纳TiO米2工金艺红的石中型间二产氧化 钛粒子;萃取法也以钛液为原料,采用萃取法 将纳T米iO钛2转白为粉有体机;物溶溶胶胶-,凝再胶将法此一溶般胶以蒸钛馏醇制盐成及 无水乙醇为原料,加入少量水及不同的酸或有 机聚合添加剂,经搅拌、陈化制成稳定的涂膜 溶胶,再利用溶胶将TiO2附着在各种载体上。
Seul-Yi Lee,Journal of Industrial and Engineering Chemistry,19(2013).1761-1769
纳米TiO2 光催化氧化的应用
• (三) 降解有机农药废水。利用纳米TiO2 光催化去除农药虽然不能使所有的污染物完 全矿化,但是不会产生毒性更高的中间产物, 这是其它方法无法相比的。
• 在光催化、光电转换及太阳能制氢领域中, 人们普遍认为TiO2是一种比较理想的太阳 能转换材料。因为它不仅具有优越的光催 化和光电转换性能,而且还拥有绝大多数 半导体材料所不具备的一些特性,如耐化 学及光化学腐蚀、成本低最多的一种光催化材料。
YANG LiXia,Chinese Sci Bull February (2010) Vol.55 No.4-5,331-338
TiO2的研究进展——面临问题
• (2)太阳光谱利用率低
• TiO2仅能吸收占整个太阳光谱不到5%的紫外光 ,太阳能利用率低,限制了其实际应用。为了 提高TiO2对太阳光谱的利用率,人们进行了很 多研究,但是提高光谱利用率所付出的代价非 常高。目前,提高TiO2纳米粒子的光谱响应性 ,使其保持足够的化学及光化学稳定性,仍是 尚需解决的重要问题。TiO2作为光催化剂降解 有机物的速度还不能满足大多数实际应用的需 要。
光催化剂纳米二氧化钛

光催化技术发展概况
• 1972年,Fujishima在n-型半导体 年 在 型半导体TiO2电极上发现了水的光 电极上发现了水的光 型半导体 催化分解作用,从而开辟了半导体光催化这一领域。 催化分解作用,从而开辟了半导体光催化这一领域。 • 1977年,Yokota T等发现在光照条件下, TiO2对丙烯环氧 年 等发现在光照条件下, 等发现在光照条件下 对丙烯环氧 化具有光催化活性,从而拓宽了光催化的应用范围, 化具有光催化活性,从而拓宽了光催化的应用范围,为有 机物氧化反应提供了新思路。 机物氧化反应提供了新思路。 近十年来,光催化技术环保、卫生保健、 近十年来,光催化技术环保、卫生保健、自洁净等方面的 应用研究发展迅速, 应用研究发展迅速,半导体光催化成为国际上最活跃的研 究领域之一。 究领域之一。
1.3 TiO2光催化剂的制备
2. TiO2光催化原理
半导体能带结构
半导体存在一系列的满带, 半导体存在一系列的满带,最上面的满带称 为价带(valence band,VB);存在一系列 为价带( band,VB);存在一系列 ); 的空带,最下面的空带成为导带( 的空带,最下面的空带成为导带(conduction band,CB);价带和导带之间为禁带。 );价带和导带之间为禁带 band,CB);价带和导带之间为禁带。 当用能量等于或大于禁带宽度(Eg) 当用能量等于或大于禁带宽度(Eg)的光照 射时, 射时,半导体价带上的电子可被激发跃迁到 导带, 产生相应的空穴, 导带,同时在价带 产生相应的空穴,这样 就在半导体内部生成电子( 空穴( 就在半导体内部生成电子(e-)-空穴(h+) 对。
TiO2光催化反应步骤 TiO2光催化反应步骤
价带空穴诱发氧化反应
H+VB
[讲解]纳米二氧化钛制备方法
![[讲解]纳米二氧化钛制备方法](https://img.taocdn.com/s3/m/a17acac532d4b14e852458fb770bf78a64293a58.png)
1.纳米TiO 2粉体制备方法物理法 气相冷凝法:预先处理为气相的样品在液氮的气氛下冷凝成核制得纳米TiO2 粉体,但该法不适于制备沸点较高的半导体氧化物高能球磨法:工艺简单,但制得的粉体形状不规则,颗粒尺寸分布宽,均匀性差化学法 固相法:依靠固体颗粒之间的混合来促进反应,不适合制备微粒液相法:就是将钛的氯化物或醇盐先水解生成氢氧化钛(或羟基氧钛) ,再经煅烧得到TiO2. 研究最广泛。
以四氯化钛为原料,其反应为TiCl4 + 4H2O → Ti (OH) 4 + 4HCl ,Ti (OH) 4 → TiO2 + 2H2O.以醇盐为原料,其反应为Ti (OR) 4 + 4 H2O → Ti (OH) 4 + 4 ROH ,Ti (OH) 4 −−−→煅烧TiO2 + 2 H2O.主要包括硫酸法、水解法、溶胶-凝胶(Sol2gel) 法、超声雾化、热解法等。
溶胶- 凝胶法就是将钛醇盐制备成二氧化钛溶胶. 为了得到多孔催化剂,通常采用煅烧等方法将凝胶进行干燥,去除溶剂,制得干凝胶. Dagan 等[25 ]采用超临界干燥法所制得的TiO2气凝胶孔隙率为85 % ,比表面积高达600 m2·g - 1 ,晶粒尺寸为5. 0 nm ;对水杨酸的光催化氧化表明该催化剂具有比Degussa P - 25 TiO2粉末更高的催化活性.气相法:其核心技术是反应气体如何成核的问题. 通过四氯化钛与氧气反应或在氢氧焰中气相水解获得纳米级TiO2 ,目前德国Degussa 公司P-25 粉末光催化剂是通过该法生产的常用的化学制备方法有溶胶-凝胶法、沉淀法、水解法、喷雾热解法、水热法和氧化- 还原法等。
10. 纳米TiO2薄膜制备方法:除了与粉体制备相同的制备方法如溶胶-凝胶法、热解法外,还有液相沉积法、化学气相沉积法、磁控溅射法等。
溶胶-凝胶法(Sol-Gel):制备的薄膜纯度高,且制备工艺简单,易批量生产;水热合成法:通过水解钛的醇盐或氯化物前驱体得到无定形沉淀,然后在酸性或碱性溶液中胶溶得到溶胶物质,将溶胶在高压釜中进行水热Ostwald熟化。
纳米二氧化钛

1、直接沉淀法 直接沉淀法的反应过程为(以Ti(so4)2为反应 物) Ti(so4)2 +2NH3· 20=TiO(OH)2+(NH4)2so4, H TiO(OH)2=TiO2(s)+H2o。 以四氯化钛和碳酸胺为原料制备出了超细高纯 TiO2 分别为200~400nm的球形金红石TiO2以及2一 5nm的不规则锐钦型TiO2和40-400nm的TiO2微 粒。
2、均匀沉淀法
均匀沉淀法是利用某一化学反应使溶液中的构晶离 子由溶液中缓慢均匀地释放出来。向钛盐中直接加 沉淀剂,易造成沉淀剂的局部浓度过高,使沉淀中夹杂 其他杂质。而采用均匀沉淀法后,只要控制好生成沉 淀剂的速度,就可避免浓度不均匀现象,使过饱和度控 制在适当范围内,从而控制粒子的生长速度,获得粒度 均匀、致密、纯度高、便于洗涤的纳米粒子。 例如,以尿素为沉淀剂制备纳米TiO2粉体,其反应原理 如下 CO(NH2)2+3H2O=CO2+2NH3· 2O, H TiOS04+2NH3· 2O=TiO(OH)2+(NH4)2so4, H TiO(OH)2= TiO2(s)+H2O。
氧化钛的水样有大量的杂质峰,用二氧化
钛作光催化氧化剂后,杂质峰明显减少,说 明加入二氧化钛后,降解比较彻底.
光催化原理分析
迁移到表面的光致电子和空穴如果没
有与适当的电子和空穴浮获剂作用,
储备的能量在几个微秒内就会复合而
耗掉。因此,在光催化反应过高光催化活性至关重要。
X射线衍射表征的结果说明纳米二氧化钛
粉体经过不同温度的处理所得粉体呈现不同
的结晶状态.低温300℃为锐钛矿相,其中含有 少量不定形态,400℃为锐钛矿相且纯度较 高,500℃时有少量锐钛矿相转化为金红石 相,600℃为金红石相.透射电镜表征的结果说
纳米二氧化钛

纳米二氧化钛1.概述纳米级二氧化钛,亦称钛白粉。
物理性质为细小微粒,直径在100纳米以下,产品外观为白色疏松粉末,它是一种新型的无机化工材料。
具有透明性、紫外线吸收性、熔点低、磁性强、抗菌、自洁净、抗老化等性能,广泛应用于化妆品、功能纤维、塑料、油墨、涂料、油漆、精细陶瓷等众多领域。
本文将从制备、应用两个方面入手,简要介绍纳米二氧化钛材料。
2.制备目前,制备纳米二氧化钛的方法有很多,可分为气相法、液相法[1]两大类。
2.1.气相合成法制备TiO2纳米粒子中典型的气相法主要包括四氯化钛氢氧火焰水解法、四氯化钛气相氧化法、钛醇盐气相氧化或水解法等方法。
四氯化钛氢氧火焰水解法最早由德国Degussa公司开发成功,并生产出当前纳米级超细TiO2粉体的著名牌号之一(P25 );还有美国的卡伯特公司和日本Aerosil公司等也采用该方法生产超细TiO2粉体。
TiCl4气相氧化法的反应初期,TiCl4和O2发生均相化学反应,生成Ti02的前驱体分子,通过成核形成TiO2的分子簇或粒子。
由于非均相成核比均相成核在热力学上更容易,随着反应的进行,TiCl4在Ti02粒子表面吸附并进行非均相反应,使粒子变大[2]。
施利毅等[3]利用N2携带TiCl4气体,预热到435℃后,经套管喷嘴的内管进入高温管式反应器,O2经预热后经套管喷嘴的外管也进入反应器,TiCl4和O2在900-l400℃下反应。
研究了氧气预热温度、反应器尾部氮气流量、反应温度、停留时间和掺铝量对TiO2颗粒大小、形貌和晶型的影响,结果表明:提高氧气预热温度和加大反应器尾部氮气流量对控制产物粒径有利,纳米TiO2,颗粒的粒径随反应温度升高和停留时间延长而增大,当反应温度为1373 K,AlCl3与TiCl4摩尔比为0.25、停留时间为1.73 s时,纯金红石型纳米Ti02颗粒的粒径分布为30-50nm。
华东理工大学[4]首先让可燃气体与过量氧气燃烧,生成高温含氧气流,然后再与经过预热的气态TiCl4呈一定角度交叉混合,使反应在高速下进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
弯曲已退化至接近平带状态。
例如,单个 TiO 2 纳米粒子的中心与表面间的电位差仅约 0.3
mV。当超微粒受光激发后,光生电子、空穴很快传递给吸附 在表面的电子受体和电子给体,避免了深能级复合,或其它 体相复合,有效降低了复合几率,提高了电荷分离效率。
由于带弯“退化”,纳 米粒子基本上丧失了对 光生电荷自动分离功能,
进入纳米尺度时,光生载流子的转移路径很短,颗粒中原子数目
也很少。因此,由于载流子相互碰撞及与晶格碰撞的几率大大减
少,这部分热损失可显著降低并以热动能形式提高电荷转移速度, 相应地提高了能量转换效率。这种大于带隙的激发能被利用的过 程称为热载流子注入或热载流子效应。
综上,半导体超微粒效应表现在:
(1)量子尺寸效应
(6)量子点的荧光寿命长。
有机荧光染料的荧光寿命一般仅为几纳秒(这与很多生物样本的自发 荧光衰减的时间相当)。而量子点的荧光寿命可持续数十纳秒 (20ns一50ns),这使得当光激发后,大多数的自发荧光已经衰变, 而量子子点荧光仍然存在,此时即可得到无背景干扰的荧光信号。
总而言之,量子点具有激发光谱宽且连续分布,
万立骏 院士
中国科学技术大学校长
兼任北京分子科学国家实验室(筹)主任、中科院 分子纳米结构与纳米技术重点实验室主任。著名化 学家,长期从事扫描隧道显微学、电化学和表面科 学的交叉科学研究,探索了电化学和纳米科学交叉 研究新方向,致力于纳米材料在能源和环境保护中 的应用研究,取得了突出成绩。
北京大学校长 林建华 清华大学校长 邱勇
所谓纳米材料,是指晶粒尺度介于原子簇和通常所说的尺度大于亚 微米粒子之间的超细材料,其晶粒尺寸一般为1~100nm。
在这个尺度范围内,电子波函数的相关长度与体系的特征尺寸相当, 或者说,固体颗粒的尺度与第一激子的德布洛依半径相当,电子的
波动性在电子输运过程中得到充分的展现。由于体系在维度上的限
4.2.1 量子尺寸效应 当半导体颗粒的尺寸小到纳米尺度,即光生电子和空穴的波 函数尺寸可与颗粒的物理尺度相比拟时,光生载流子的运动
在三维方向受到量子限域,相对于包含有无数个原子(即导
电电子数 N →∞)的块体材料来说,由于纳米颗粒中原子聚 集数有限,即 N 值很小,随粒径减小,则逐步显示出分子能 级特征,因而大块晶体的准连续能带变成具有分子特性的分 立能级结构,带隙也随之变宽,出现了新的跃迁规律和吸收 光谱带兰移,这种现象称为量子尺寸效应 。
分子-团簇-体相材料能级结构的变化
Kubo理论
日本科学家久保提出了能级间距和金属颗粒直径的 关系,并给出了著名Kubo公式: δ =EF/3N (δ为能级间距,EF为费米能级,N为总电子数)
宏观物体包含无限个原子(即所含电子个数N ),即大粒子或 宏观物体的能级间距几乎为零;而纳米微粒包含的原子数有 限,N值很小,导致有一定的值,即能级间距发生分裂。 当颗粒尺寸降到最低时,费米能级附近的电子能级由准连续 变为离散能级现象。
量子点,通常是一种由II一Vl族或III-V族元素组成的纳米颗粒,
尺寸小于或者接近激子波尔半径(一般直径不超过10nm),具 有明显的量子效应。
量子点是20世纪90年代提出来的一个新概念,它是把导带电子、
价带空穴及激子在三个空间方向上束缚住的半导体纳米结构。
由于电子和空穴被量子限域,连续的能带结构变成具有分子特 性的分立能级结构,受激后可以发射荧光。基于量子效应,量
通过减小颗粒的尺寸,某些块体材料上不能进行的反应,有可
能会表现出一定的光催化性能。
表4.1 几种半导体的光活性与粒度的关系
PbSe 反应 <5nm H+ + e- →1/2H2 MV2+ + e- → MV+ CO2 +2H+ +2e- → HCOOH Yes Yes >100n m No No <5nm Yes
量子点的荧光强度比最常用的有机荧光材料“罗丹明6G”高20倍,
它的稳定性更是“罗丹明6G”的100倍以上。因此,量子点可以对 标记的物体进行长时间的观察,这也为研究细胞中生物分子之间长 期相互作用提供了有力的工具。近年,在染料敏化太阳能电池中亦 有广泛应用。
PL Intensity
CdTe QDs
Chlorophyll
研究的进一步深化与发展,具有重要的指导意义。
4.3 二氧化钛的物理结构和化学性质
4.3.1二氧化钛的晶体结构和电子结构
二氧化钛有无定型(amorphous)、锐钛矿型(Anatase)、金红石型
(Rutilc)和板钛矿型(Brookite),在制备过程中可以通过温度处理而 发生晶型转变。
研究表明,锐钛矿型TiO2较金红石型TiO2具有更高的光催化活性,但也有 人认为,两者以一定方式和一定比例组成的混晶材料(如P25- TiO2), 则为更佳的光催化材料。板钛矿型(Brookite)基本没有光催化活性。
纳米丝,纳米棒,纳米管等。 Nhomakorabea(3)二维量子阱:空间中有一维处在纳米尺度。如超薄膜,
多层膜及超晶格材料等 。
纳米材料的三个层次:
(1)纳米微粒
(2)纳米固体 (3)纳米组装体系
纳米材料的特点: (1)原子畴尺寸小于100 nm (2)处于晶界环境的原子占很大比例 (3)畴与畴之间存在相互作用
4.2 半导体超微粒效应
子点在太阳能电池,发光器件,光学生物标记等领域具有广泛
的应用前景。
量子点的主要性质
1. 量子点的发射光谱可以通过改变量子点的尺寸大小 来控制。
CdTe量子点的粒径从2.5nm生长到4.0nm时,它们的发射波长可以从510nm 红移到660nm
不同粒径的量子点在同一光下的颜色对比
(2)量子点具有很好的光稳定性。
原子总数的比例为:
N A( surf ) N A0 20% 50%
表面原子数目的增加,意味着表面不饱和键浓度和表面态密度
的增高,这种高表面能的表面极不稳定,易与其他原子结合,
因而有更多的表面原子参与反应,将会显著提高材料的利用效 率和反应速度。
其次,随着纳晶粒子粒粒径的减小,比表面则急剧增高,如粒
每个八面体与10个相邻的八面体接触 (两个与晶棱的氧配位,其他8个与 晶角氧原子配位),偏向于斜方晶系。
每个八面体与相邻的8个八面体 接触(4个分居晶棱,另4个分居 晶角)。
TiO6
根据有效质量近似原理,用三维量子限阈模型,可以预测纳米
半导体粒子的带隙宽度与粒径间的关系:
第一项:体相半导体的带隙
第二项:光生电子和空穴的限阈能量之和
第三项:电子与空穴的库伦相互作用能量
随R减小,第三项库伦项使Eg向较低能量方向移动,第二项量子县域
能则使Eg向高能方向移动。其结果是:超微粒的带隙能Eg(R)总是大于块 体材料的带隙,即:纳米晶半导体出现光谱兰移的现象。
1. 提高宽禁带半导体光吸收的方法? 2. 染料敏化纳晶半导体电极PEC电池的工作原理
3. 高效复合半导体 构成的条件?
第四章 纳米半导体与纳米二氧化钛
4.1 纳米材料的基本概念
早在1959年,著名的诺贝尔奖金获得者,物理学家 Richard曾经预言,如果我们对物体微小规模上的排 列加以某种控制的话,我们就能使物体具备大量奇 异的特性,材料的性能将会产生丰富的变化。今天 纳米材料的成功合成与蓬勃发展,正式这一预言的 科学印证。
制,使固体中电子态、元激发过程及各种相互作用表现出与三维常 规颗粒体系十分不同的效应,相应地,纳晶材料在物理、化学及力 学性质等方面均显示出不同于常规材料的奇异特性。
1990.7美国召开第一届国际纳米材料科学会议,正式宣布纳米材料 科学为材料科学的一个分支。我国也将其列入“十五”期间的重点 发展学科。
且无拖尾,多色量子点同时使用时不容易出现光谱交叠。
(4)量子点具有较大的斯托克斯位移。
量子点不同于有机染料的另一光学性质就是宽大的斯托克斯位移, 这样可以避免发射光谱与激发光谱的重叠,有利于荧光光谱信号的 检测。
(5)生物相容性好。
量子点经过各种化学修饰之后,可以进行特异性连接,其细胞毒性 低,对生物体危害小,可进行生物活体标记和检测。
(2)表面效应
(3)超微粒的体效应 (4)热载流子效应
4.3 二氧化钛的物理结构与化学性质
TiO2具有资源丰富,廉价稳定,能级结构与水的氧还电位匹 配较好等突出优点,近年来,光催化特别是环境光催化方面 的研究,以TiO2半导体材料为基础材料的研究占相当比例。
对TiO2基本结构与物理、化学性质的了解,将对TiO2光催化
纳米材料又可定义为三维空间中至少有一维处于纳米尺寸范围, 并由它们作为基本结构单元组成的材料。
纳米材料的三种结构形式
根据量子限域特征,纳米材料可分为:
(1)零维量子点:系指三维方向均为量子限域或三维尺度均 为纳米尺寸的材料,如原子团簇,纳米颗粒等。
(2)一维量子线:指空间中有两维处于纳米尺寸的材料,如
Irradiation time / s CdTe量子点和叶绿素在小眼虫体内的淬灭曲线
(3)量子点具有宽的激发谱和窄的发射谱。 使用同一激发光源就可实现对不同粒径的量子点进行同步检 测,因而可用于多色标记,极大地促进了荧光标记的应用。 而传统的有机荧光染料的激发光波长范围较窄,不同荧光染 料通常需要多种波长的激发光来激发,这给实际的研究工作 带来了很多不便。此外,量子点具有窄而对称的荧光发射峰,
HgSe >100n m No <5nm
CdSe >100n m
Yes
No
量子点
量子点(quantum dot)是准零维(quasi-zero-dimensional)的纳米
