红外光谱讲义
红外光谱解析讲义
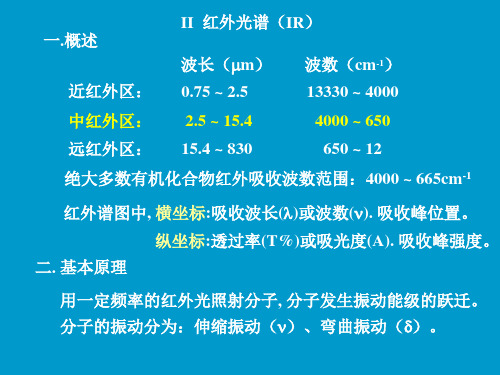
NMR H/ppm : 1.1(d,6H),3.8(m,1H),4.4(s,1H)
CH3
CH CH3 OH
2. 根据给出的分子式及IR NMR主要数据, 推测化合物的结构。
分子式: C10H12O2 IR: 3010,2900,1735,1600,1500cm-1 NMR: 1.3 (t, 3H),2.4 (q, 2H),5.1 (s, 2H),7.3 (s, 5H)
O CH3CH2CCl
O CH3 C O
2)共轭效应 键长平均化。双键键长增长,力常数减小。吸收频率移向 低波数。
O R C R' VC=O ~1715 O R C C=C 1685~1670 O R C ~1695 O R C NH2 ~1675cm-1
O C6H5C CH2CH3
试比较下列两组化合物中哪一个羰基的振动波数相对较高?
NMR /ppm : 2.5( s,3H ), 3.95( s,3H ), 7.5( q,峰形对称,4H ) (2) 反式和顺式-1,2-环戊二醇在3450~3570cm-1处均有一个宽 的吸收带,如何用IR来区分顺反异构体。
作
“有机化学”相应 章节的习题!!!
业
7. 醚类 VC-O-C 1275~1020cm-1
8. 胺类 一级胺 VN-H 3490~3400 二级胺 VN-H 3500~3300 三级胺 无VN-H 吸收峰 N-H 1650~1590, 900~650 N-H 750~700 无N-H 吸收峰
应用 IR、1HNMR 谱中的哪一种可快速有效鉴别下列化 合物, why?
3000
C C
C=C 1680~1620
C C 1200~700
v cm-1
红外光谱基本原理课件

红外光谱仪的性能指标
波长范围
表示仪器能够测量的红外 光波长范围,常用的波长 范围有近红外、中红外和 远红外。
分辨率
表示仪器能够分辨的最小 波长差,分辨率越高,仪 器性能越好。
信噪比
表示仪器输出信号与噪声 的比值,信噪比越高,仪 器性能越好。
扫描速度
表示仪器完成一次光谱扫 描所需的时间,扫描速度 越快,仪器性能越好。
谱带形状
不同化学键或基团的红外 光谱谱带形状也不同,谱 带形状与分子内部的对称 性和振动模式有关。
02
红外光谱仪器
红外光谱仪的基本构造
光源
发射一定波长的红外 光,常用光源有碘钨 灯和溴钨灯。
干涉仪
将光源发出的红外光 变成干涉光,常用的 干涉仪有迈克尔逊干 涉仪和马赫-曾德尔干 涉仪。
检测器
检测干涉光的强度, 常用的检测器有热电 堆检测器和量子化能 检测器。
在生物学中的应用
生物大分子结构研究
红外光谱可以用于研究蛋白质、核酸等生物大分子的结构和构象 变化。
生物活性物质分析
红外光谱可以用于分析生过红外光谱研究药物与靶点分子间的相互作用,有助于药物设计 和筛选过程的优化。
在环境科学中的应用
有机污染物分析
红外光谱可以用于检测和鉴定水 体、土壤等环境样品中的有机污
染物,如农药、石油烃等。
气体分析
红外光谱可以用于分析大气中的气 体成分,如二氧化碳、甲烷等,有 助于监测和评估大气环境质量。
地质样品分析
红外光谱可以用于分析岩石、矿物 等地质样品,通过分析其成分和结 构,有助于地质学研究和矿产资源 勘探。
04
数据处理系统
对检测器输出的信号 进行处理,计算出光 谱图。
红外光谱(最全最详细明了)课件

THANKS
感谢观看样ຫໍສະໝຸດ 制备固体样品液体样品
气体样品
注意事项
研磨成粉末,与KBr混合 压片或涂在ZnSe窗片上
。
稀释在适当的溶剂中, 涂在CaF2或ZnSe窗片
上。
通过干燥管进入光谱仪 。
避免样品中的水分和二 氧化碳干扰,确保样品
纯净。
实验操作
打开红外光谱仪电源,预热 稳定。
调整仪器至最佳状态,如光 路对中、调零等。
对实验操作的要求
总结词
红外光谱实验操作需要一定的技巧和经验,以确保结 果的准确性和可靠性。
详细描述
红外光谱实验涉及到样品的制备、仪器操作和谱图解析 等多个环节。每个环节都需要一定的技巧和经验,以确 保结果的准确性和可靠性。例如,在样品的制备过程中 ,需要选择合适的制样方法,以获得均匀、平整的样品 ;在仪器操作中,需要正确设置参数,以保证谱图的质 量;在谱图解析中,需要具备丰富的经验和专业知识, 以准确解析谱图特征。因此,进行红外光谱实验的人员 需要经过专业培训和实践经验的积累。
红外光谱(最全最详细 明了)课件
contents
目录
• 红外光谱基本原理 • 红外光谱与分子结构的关系 • 红外光谱的应用 • 红外光谱实验技术 • 红外光谱的局限性
01
红外光谱基本原理
红外光谱的产生
分子振动
分子中的原子或分子的振动,导致偶 极矩变化。
偶极矩变化
辐射吸收
分子吸收特定波长的红外光,导致振 动能级跃迁。
02
01 03
放入样品,记录光谱。
实验结束后,关闭仪器,清 理样品。
04
05
注意事项:保持室内温度和 湿度的稳定,避免仪器受到
红外吸收光谱讲课文档

CH
NH OH
2800-3000cm-1
3000-3600cm-1
第十二页,共72页。
分子中基团的基本振动形式
伸缩振动 亚甲基:
弯曲振动
亚甲基
第十三页,共72页。
影响峰位变化的因素
❖ (1) 内部因素
❖ ① 电子效应 ❖ 1)诱导效应:由于取代基具有不同的电负性,通过静电诱导
作用,引起分子中电子分布的变化,从而引起键力常数的变化, 改变了基团的特征频率,这种效应通常称为诱导效应。
(3)炔烃
❖ 末端炔烃的C-H伸缩振动一般在3300 cm-1处出现
强的尖吸收带。
❖
一取代:2150~2100cm-1
❖ C≡C伸缩振动
❖
二取代:2270~2150cm-1
第二十九页,共72页。
(4)芳烃
❖ vC-H:3100~3000cm-1 ❖ γC-H:面外弯曲振动在900~650cm-1,反映苯环上取代
动光谱,简称振转光谱。
❖ 分子在未受光照射之前,能量处于最低能级, 称之为基态。
❖ 当分子受到红外光的辐射,产生振动能级的跃迁, 在振动时伴有偶极矩改变者就吸收红外光子,形 成红外吸收光谱。
第三页,共72页。
区域 λ(μm)
σ(cm-1 )
能级跃迁类型
近红外 0.ቤተ መጻሕፍቲ ባይዱ5~2.5 13330~4000 OH 、NH及CH键倍频吸收区
❖ (2) 照射分子的红外光的频率与分子某种振动的频率相 同时(红外=振),分子吸收能量后,才能产生跃迁,在 红外谱图上出现相应的吸收带。
第五页,共72页。
❖ 已知任何分子就其整个分子而言,是呈电中性 的,但由于构成分子的各原子因价电子得失的 难易,而表现出不同的电负性,分子也因此而 显示不同的极性。
红外光谱讲义

电子能级跃迁
E0
E = hn 其中 h 为普朗克常数 (6.626 × 10-34 焦耳· 秒) n 为频率
Polarizability——极化率 Polarity——极性 (related to dipole moment) 红外非活性 拉曼活性 Polarizability change 红外活性 拉曼非活性
可拆液体池,用 于非挥发性样品
密封液体池,用 于挥发性样品
气体样品制样
• 气体样品的测定:气体池
气体池:5cm光程(左);10cm光程(右)
• 傅立叶变换红外光谱仪(Fourier Transform IR Spectrometer):用干涉仪代替色散装置
– 70年代傅立叶变换光谱仪
2.2.1 傅立叶变换红外谱仪的结构
干涉仪 He-Ne 准直激光 光源
检测器
样品室
检测器检测到的干涉图
v1
v2 v3
A’(v2)
A(v1)
强度
红外光谱
瑞利散射
反斯托克斯
斯托克斯
瑞利散射:比入射光强弱 1000到10000倍 拉曼散射:比瑞利散射弱 10000到100000倍
n0 拉曼频移
n
H H H
H O O H H
芳香环的取代类型——弯曲振动区
羧酸
官能团区
指纹区
芳环上C—H伸缩振动 羧基上O—H伸缩振动 可能的氢键作用
波长 (mm)
0.15
波数 (cm-1)
0
12,800 4000
4000 3750 3500 3250 3000 2750 2500 2250 2000 1750 1500 1250 1000 750 Polyethylene
红外光谱(IR)讲义
6
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
2.4.3 常见基团的特征频率
7
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
8
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
9
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
18
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
19
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
20
10
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
11
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
12
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
13
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请全体班委整理, 请勿外传!
第二章
红外光谱
2.1 红外光及红外光谱 2.1.2 红外光谱仪
1、色散型红外光谱仪
色散型红外光谱仪结构示意图 1
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
色散型红外光谱仪工作原理(零点平衡法)
14
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
15
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
16
红外光谱(IR)讲义 Chem.—08— (1) 全体班委整理, 请勿外传!
《红外光谱》PPT课件

HC=C
U 1
例3 某未知物分子式为C10H12O, 试根据其IR数 据3020(w)、2820、2720、1700、1610、1575、
1390、1365、830cm-1,推测其结构。
1
1
Ω 2 (2n4 n3 n1 2) 2 (210 12 2) 5
H3C
O
CHO
CH
CH
C3H7
H3C
1. 否定法
如果某个基团的特征频率 吸收区,找不到吸收峰,我们就判断 样品中部不存在该基团。 2. 肯定法
3. 否定法与肯定法结合
C9H10O
IR主要吸收峰:3060,3030,
2980,2920,1700,1600,
1580,
690cm-1。150120(,214935,1013720,) 7550,
Therefore, n = 8, m = 8
(2n 2) m 8 8 1 5
2
2
U 1 (2 8 8 2) 5 2
Compound A, with molecular formula C6H10, reacts with H2/Ni to give compound B, with molecular formula C6H12. The IR spectrum of compound A is provided. From this
Infrared Spectrometry
红外光谱
UV-Vis
IR
讲义P10-12
1 K 130.2 K (cm1) m1m2
2c
ห้องสมุดไป่ตู้
m1 m2
K:化学键的力常数(键能和键长) :双原子的折合质量;m:相对原子质量;
红外光谱室实验讲义(红外辐射与黑体实验)

三、红外辐射源能量光谱分布测试(一)实验目的1. 了解测量红外辐射源能量光谱分布的意义2. 掌握测量红外辐射源能量光谱分布的方法3. 理解物体的温度与红外辐射能量的关系(二)实验原理红外辐射(俗称红外线)是波长在0.78~1000μm 的一段电磁波谱,是人眼看不见的光线,只有借助于仪器才能探测到并转换成人们可感受的信息,如数字、图像、曲线等。
凡温度在绝对零度以上的物体均能够发出红外辐射,其辐射的峰值波长与物体的温度有确定的关系:T b m =λ 式中 λm ——物体辐射的峰值波长T —— 物体的温度B —— 常数 (2898μm ·K )此为辐射度学中的维恩位移定律,意为只要物体有温度,则一定有固定波长的辐射,自然界的物体温度如果在-40℃~3000℃(233K ~3273K )范围,则根据上述公式,峰值辐射波长在0.88~12μm 之间,即人们通常所说的红外波段。
红外光谱仪器能将红外辐射源的辐射能量按波长的分布以曲线的形式给出。
我们可以清楚地看出一个红外辐射源在某个波长的相对辐射能量,进而可以验证维恩位移定律等红外辐射定律,并可以对红外辐射源进行深入的研究。
红外单色器的光学原理图如下图1 红外单色器光学原理图M1反射镜、M2准光镜、M3物镜,M4反射镜、M5 深椭球镜G 平面衍射光栅、S1入射狭缝、S2,S3出射狭缝、T 调制器入射狭缝、出射狭缝均为直狭缝,宽度范围0-2mm 连续可调,光源发出的光束进入入射狭缝1S ,1S 位于反射式准光镜2M 的焦面上,通过1S 射入的光束经2M 反射成平行光束投向平面光栅G 上,衍射后的平行光束经物镜3M 成像在2S 上。
(三)、实验仪器红外光栅光谱仪及配套附件;红外光源及驱动电源;电子稳压器;计算机及处理软件;打印机(四)、实验步骤首先按原理图检查各部分连接和摆放位置是否正确,经教师同意后,按下述步骤进行实验:1、打开红外辐射源的电源开关进行预热;2、打开计算机并进入相关程序,选定测量参数(相对强度、能量等),设置扫描波长范围、扫描间隔、幅度范围等参数;3、红外辐射源经预热达到稳定时,开始进行扫描,得到相应曲线;4、储测试结果,打印测试曲线;5、行相关计算,完成实验报告。
