沉积物中酶的测定方法
酶检测方法[001]
![酶检测方法[001]](https://img.taocdn.com/s3/m/a7cd3ad2846a561252d380eb6294dd88d1d23d77.png)
酶检测方法酶是生物体内一类具有特定功能的蛋白质,它们在生物体内发挥着关键的催化作用。
酶的活性能够反映生物体内代谢的运行状态,因此酶检测在生物学研究、临床诊断和生物工程等领域起着重要的作用。
本文将介绍酶检测的方法,并分析其原理和应用。
一、酶检测的原理每种酶都具有特定的底物,当底物被酶催化后产生一定的产物,可以通过测量产物的数量或者相关反应的速率来间接反映出酶的活性。
酶的检测方法主要有光度法、荧光法、比色法和电化学法等。
光度法是利用酶催化反应后产生的物质溶液的吸收特性来检测酶活性的方法。
首先,选择具有特定光学属性的底物,使酶催化后的产物能够吸收特定波长的光线。
然后,通过测量反应体系中吸光度的变化来确定酶的活性。
举例:以辣根过氧化物酶的检测为例,辣根过氧化物酶能够将辣根过氧化物(HRP)和底物间的过氧化氢催化成高活性的自由基,进而氧化显色底物,形成有色产物。
利用比色法测定产物的吸光度变化,即可定量检测出辣根过氧化物酶的活性。
荧光法是利用酶催化反应产物的荧光特性来检测酶活性的方法。
在酶催化反应中,有些底物和产物具有荧光特性,通过测量产物的荧光强度变化可以确定酶的活性。
举例:以葡萄糖氧化酶的检测为例,葡萄糖氧化酶能够将葡萄糖氧化成葡萄糖酸,产生荧光物质NADH。
通过测量NADH的荧光强度变化,可以判断葡萄糖氧化酶的活性。
比色法是利用酶催化反应后产生的有色产物来检测酶活性的方法。
在酶催化反应中,底物与其他试剂反应产生有色产物,通过测量产物的吸光度变化来确定酶的活性。
举例:以碱性磷酸酶的检测为例,碱性磷酸酶能够将对硝基苯磷酸钠底物催化成黄色产物对硝基苯胺。
通过测量对硝基苯胺的吸光度变化,可以确定碱性磷酸酶的活性。
五、电化学法电化学法是利用酶在电极表面催化产生电流来检测酶活性的方法。
在电极表面固定酶,底物被酶催化后,产生电荷转移,可以通过测量电流变化来确定酶的活性。
举例:以谷胱甘肽还原酶的检测为例,谷胱甘肽还原酶能够将还原型谷胱甘肽(GSH)氧化为氧化型谷胱甘肽(GSSG)。
酶的测定(详细)

一、脲酶测定(比色法)1.方法原理脲酶广泛存在于土壤中,它能酶促尿素分解生成氨、二氧化碳和水。
测定脲酶的方法很多,包括比色法、扩散法、电极法等,其中比色法最为常用。
现介绍苯酚一次氯酸钠比色法,该方法以尿素为基质,根据酶促产物氨与苯酚次氯酸钠作用(在碱性溶液中及在亚硝基铁氰化钠催化剂作用下)生成蓝色的靛酚,来分析脲酶活性。
2.试剂配制(1)pH6.7柠檬酸盐溶液:取368g柠檬酸溶于600mL蒸馏水中,另取295g氢氧化钾溶于水,再将两种溶液合并,用1N氢氧化钠将pH调至6.7,并用水稀释至2L。
(2)苯酚钠溶液:称取62.5g苯酚溶于少量乙醇中,加2mL甲醇和18.5mL丙酮,后用乙醇稀释至100mL(A液),保存再冰箱中。
称取27g氢氧化钠溶于100mL水中(B液),保存于冰箱中。
使用前,取A、B两液各20mL混和,并用蒸馏水稀释至100mL备用。
(3)次氯酸钠溶液:用水稀释制剂至活性氯的浓度为0.9%,溶液稳定。
(4)10%尿素溶液:10g尿素溶于100mL水中。
(5)N的标准溶液:精确称取0.4717g硫酸铵溶于水稀释至1L,则得1mL含0.1mgN的标液,再将此液稀释10倍制成氮工作液(0.01mg/mL)。
3.操作步骤取5g风干土置于50mL三角瓶中,加1mL甲苯。
15min后加10mL10%尿素溶液和20mLpH=6.7柠檬酸盐缓冲液。
摇匀,37℃恒温箱中培养24h。
过滤,取1mL滤液注入50mL 容量瓶中,然后按配制标准曲线显色方法进行比色测定(为了消除土壤中原有的尿素而引起的误差,每一土壤需做无基质对照,整个试验需做无土壤对照。
)。
标准曲线配制:分别取0、l、3、5、7、9、11、13mL氮工作液,移于50mL容量瓶中,然后加蒸馏水至20mL。
再加4mL苯酚钠溶液和3mL次氯酸钠溶液。
随加随摇匀。
20min 后显色,定容。
lh内在分光光度计上于波长578nm处比色。
根据吸光值与氮溶液浓度绘制标准曲线。
沉积物检测相关标准

沉积物检测相关标准沉积物亦可以由风(风成过程(eolian processes))及冰川搬运。
沙漠的沙丘及黄土是风成运输及沉积的例子。
冰川的冰碛石(Moraine)矿床及冰碛(Till)是由冰所运输的沉积物。
简单的重力崩塌制造了如碎石堆、山崩沉积及喀斯特崩塌特色的沉积物。
每一种类型的沉积物有不同的沉降速度,依据其大小、容量、密度及形状而定。
(14.11.28)(001)检测项目:六六六、滴滴涕、油类、多氯联苯、汞、镉、铅、总铬、砷、铜、锌、硒、硫化物、有机碳等。
检测标准:GB/T20260-2006海底沉积物化学分析方法GB/T25282-2010土壤和沉积物13个微量元素形态顺序提取程序GB/T27853-2011化学品水-沉积物系统中好氧厌氧转化试验GB/T27858-2011化学品沉积物-水系统中摇蚊毒性试验加标于水法GB/T27859-2011化学品沉积物-水系统中摇蚊毒性试验加标于沉积物法GB/T30738-2014海洋沉积物中放射性核素的测定γ能谱法GB/T30739-2014海洋沉积物中正构烷烃的测定气相色谱-质谱法GB/T30740-2014海洋沉积物中总有机碳的测定非色散红外吸收法GB/T31270.8-2014化学农药环境安全评价试验准则第8部分:水―沉积物系统降解试验HJ642-2013土壤和沉积物挥发性有机物的测定顶空/气相色谱-质谱法HJ650-2013土壤、沉积物二噁英类的测定同位素稀释/高分辨气相色谱-低分辨质谱法HJ679-2013土壤和沉积物丙烯醛、丙烯腈、乙腈的测定顶空-气相色谱法环境保护部HJ680-2013土壤和沉积物汞、砷、硒、铋、锑的测定微波消解/原子荧光法HJ703-2014土壤和沉积物酚类化合物的测定气相色谱法HJ77.4-2008土壤和沉积物二噁英类的测定同位素稀释高分辨气相色谱-高分辨质谱法HY/T132-2010海洋沉积物与海洋生物体中重金属分析前处理微波消解法HY/T147.2-2013海洋监测技术规程第2部分:沉积物HY/T153-2013海水、沉积物中致突变性的测定鼠伤寒沙门氏菌/哺乳动物微粒体酶试验HY/T172-2014海洋沉积物标准物质研制及保存技术规范JT/T494-2003汽油机进气阀沉积物模拟试验方法NB/SH/T0834-2010发动机油适度高温活塞沉积物的测定热氧化模拟试验法(TEOSTMHT)SH/T0514-1992汽油机油低温沉积物评定法(MS程序VD法)SH/T0672-1998汽油机油低沉积物性能评定法(CEPT-V法)SH/T0750-2005发动机油高温氧化沉积物测定法(热氧化模拟试验法)SN/T0801.6-2011出口动植物油脂第6部分:豆油中沉积物的检验方法。
深海沉积物宏基因组文库中产蛋白酶克隆CAPRO2的筛选及酶学性质分析

蛋 白酶是 应用 得 最 为 广 泛 的一 类 酶 , 工 业 上 在
法 的优 点 是 目的性 强 , 培 养 的 菌 株 也便 于 后 续 的 纯 基 因工程 、 白质工 程 等操 作 J但 是 , 蛋 . 自然 环 境 中
有着广泛的用途 , 例如洗涤 业 、 品加 工、 食 制药 、 皮 革 、 断试 剂 等 ¨ 大部 分 投 入 应 用 的蛋 白酶 都 是 诊 . 中温酶 , 它们在 3 5 ℃范 围内活力最高. 0~ 0 而对于 工业应用来说 , 高温酶 由于在高温下具有高的催化
克 隆 ( A R 0 2 , 其 进 行 了酶 学性 质 分析 . 果表 明该 酶 的 最 适作 用 温 度 为 6 c 最适 作 用 C P O 0 )对 结 5c,
p H值 为 9 0 该蛋 白酶具有较好 的热稳 定性 , 4 c .. 在 0c以下的温度 中可长期保持稳 定 , 5 ℃ 中 在 0
绝大部分 的微生 物是 目前的技术所无 法进行培养 的, 尤其是在深海极 端条件下 的微生物更是难 以获
收 稿 日期 :00 1 . 2 1—13 0
基金项 目: 国家 8 3 6 计划资助项 目(0 7 A 9 4 7 ; 2 0 A 0 10 ) 中国大洋矿产资源研究开发协会 资助项 目( Y M 15 22 4 D X 一1- - 0 ) 0 -
CPO A R 2蛋 白酶在 p H值 为 7 5~ . 。 9 5时 活 力较 高, H 值 为 7 5时 可 保 持 约 8 % 的 活 力 ,H 值 p 。 0 p
为 9 5时保 持 6 % 的 活力 , . 0 而在 p 值 高于 9 5的 条件 下 酶 活 力 下 降较 快 ,H值 为 1 . H . p 0 0时活 力 降为 约 1% , 明 C P O 5 表 A R 2属 于 碱 性 蛋 白 酶 . 氨 酸 蛋 白 酶 抑 制 剂 P F E6 丝 MS 、 一4和 AE S B F对
测定酶活性浓度的两大类方法
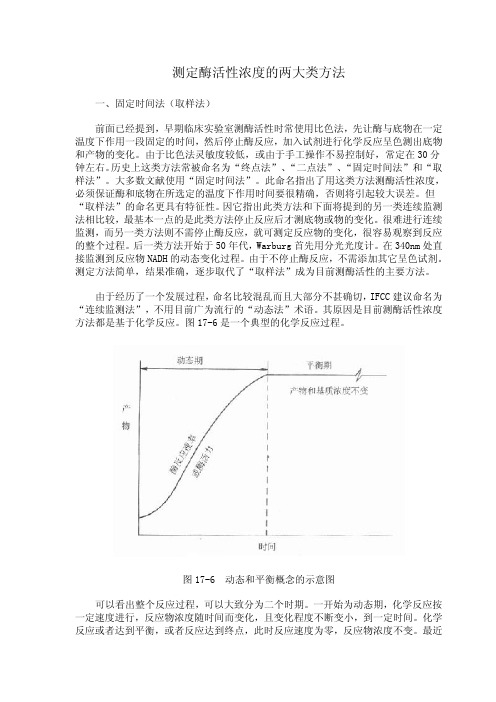
连续监测法具有众多的优点,随着科学技术的发展,自动生化仪的使用,正在逐 步取代“固定时间法”,发达国家从 50 年代到 70 年代末用了约 20 余年的时间,我 国从 80 年代初开始使用连续监测法,虽然发展很快,但至少仍有不少地区医院实验 室仍使用老的方法,就是已使用新法的实验室,也不一定掌握得很好,本节将比较详 细地从分类,酶偶联反应,测定注意事项等方面对连续监测法加以介绍。
当测定酶的反应速度明显大于指示酶,此时 A 很快转变为 B,由于指示酶反应慢, 中间产物 B 大量推积,最终产物产生速度明显慢于底物 A 的消失速度。
当指示酶速度加大后,中间产物 B 堆积减小,指示酶反应速率偏差程度也变小。 只有当指示酶大量 达到高峰后的时期),C 和 A 的变化速度非常一致。 也就是只有在些情况下,才是测定酶浓度的理想条件。
⒉间接连续监测法直接法试剂简单,操作方便,可惜的是只有当底物与产物之间, 在光学性质或其它理化性质有显著差异时,才有可能使用此法。到目前为止,大部分 酶都无法用直接法测定。
科学家还曾设法在原来反应体系中添加一些试剂,这些试剂必须不与酶作用也不 影响酶活性,同时又能与酶反应物迅速作用,产生可以被直接测定的物质,典型的例 子是 Ellman 的胆碱酯酶测定法,底物为硫代乙酰胆碱,酶水解产物硫代胆碱与添加 的二硫代硝基苯甲酸(DTNB)作用立刻生成黄色化合物,可在 412nm 用分光光度法连 续监测。
从理论上说,用酶偶联反应测酶活性浓度时,最好条件应是测定酶反应为限速反 应。动力学上为零级反应,而指示酶为一级反应,酶反应速度与指示酶底物浓度相关。
(二)指示酶、辅助酶的种类和浓度
指示酶、辅助酶的种类:常规化验中常用的酶偶联法中,多以脱氢酶为指示酶, 在常规化验中的自动分析仪几乎无一例外都有 340nm 波长,通过 NAD(P)H 系统可以很 方便地监测到指示酶反应。但从理论上说,往往可以有不止一种偶联方法,只要设法 使偶联反应中最后一个是指示酶反应,前面已提到测 CK 可以正向逆向二个方向建立 二种不同酶偶联的反应。又如在丙氨酸转氨基酶(ALT)测定法中,正向反应后产生 丙酮酸和谷氨酶,目前最常用的是用乳酸脱氢酶与丙酮酸偶联反应,伴有 NADH 下降。 但也可以用谷氨酸脱氢酶与谷氨酸作用,伴有 NADH 生成。
生化基础物质检测—酶活性检测

反应进程曲线(速率
时间(s)
法) 317 334 351 368 385 402
吸光度(A) 1.253 1.204 1.178 1.146 1.126 1.097
据此计算此酶的∆A/min
419 1.048
1.450
1.400
1.350
延滞期
1.300
预孵育期
终点法
1.250 1.200
速率法
线性期
指示酶
Ex
Ea
Ei
A
B
C
P
待测物质 中间产物
终产物
酶偶联反应的原理:
在应用酶偶联法测定时,关键在于确定恒态期,因为只有 恒态期才能代表酶活性。如酶促反应底物动力学所述,恒态期 可以通过测定指示酶的Km和Vmax等动力学因数加以计算确定
常用指示酶及其指示反应
1.脱氢酶 用作工具酶的脱氢酶都是以NAD(P)H为辅酶的脱
反应如下:
色原物质
Trinder反应:
POD
2H2O2 + 4-AAP + 酚
醌亚胺(红色) + 2H2O
应用:GOD、COD、GPO、甘油氧化酶、尿酸酶(属于氧化酶类)
等都可以将各自的底物氧化为过氧化氢,因此都可以与POD偶联,通 过Trinder反应加以测定
酶偶联法测定ALT的吸光度变化图
吸光度(A)
氢酶,例如LDH、MDH、G-6-PD、GLDH等,它们催化下 列反应:
P + NAD(P)H + H+ PH2 + NAD(P)+ 可对NAD(P)H在紫外吸收或紫外激发荧光进行测定
应用:ALT、AST、CK等酶活性测定
2.过氧化物酶(POD)
三种主要酶活测定方法

土壤纤维素酶活性测定(3,5- 二硝基水杨酸比色法)一、原理纤维素是植物残体进入土壤的碳水化合物的重要组分之一。
在纤维素酶作用下,它的最初水解产物是纤维二糖,在纤二糖酶作用下,纤维二糖分解成葡萄糖。
所以,纤维素酶是碳素循环中的一个重要的酶。
纤维素酶解所生成的还原糖与3,5- 二硝基水杨酸反应而生成橙色的3-氨基-5-硝基水杨酸。
颜色深度与还原糖量相关,因而可用测定还原糖量来表示蔗糖酶的活性。
二、试剂1)甲苯2)1%羧甲基纤维素溶液:1g 羧甲基纤维素钠,用50%的乙醇溶至100ml。
3)pH5.5醋酸盐缓冲液:0.2mol/L 醋酸溶液 11.55ml 95% 冰醋酸溶至1L.0.2mol/L 醋酸钠溶液 16.4g C2H3O2Na或27.22g C2H3O2Na.3H2O溶至1L.取11ml 0.2mol/L 醋酸溶液和88ml 0.2mol/L 醋酸钠溶液混匀即成PH 5.5醋酸盐缓冲液. 4)3,5-二硝基水杨酸溶液:称1.25g二硝基水杨酸,溶于50ml 2mol/LNaOH和125ml水中,再加75g酒石酸钾钠,用水稀释至250ml(保存期不过7天),5)葡萄糖标准液(1mg/mL)预先将分析纯葡萄糖置80℃烘箱内约12小时。
准确称取50mg葡萄糖于烧杯中,用蒸馏水溶解后,移至50mL容量瓶中,定容,摇匀(冰箱中4℃保存期约一星期)。
若该溶液发生混浊和出现絮状物现象,则应弃之,重新配制。
三、操作步骤葡萄糖标准曲线:分别吸1mg/mL的标准葡糖糖溶液0、0.1、0.2、0.4、0.6、0.8mL 于试管中,再补加蒸馏水至1mL,加DNS溶液3ml混匀,于沸腾水浴中加热5min,取出立即泠水浴中冷却至室温,以空白管调零在波长540nm处比色,以OD值为纵坐标,以葡萄糖浓度为横坐标绘制标准曲线。
称10g土壤置于50ml三角瓶中,加入1.5ml甲苯,摇匀后放置15min,再加5ml 1%羧甲基纤维素溶液和5ml pH5.5醋酸盐缓冲液,将三角瓶放在37℃恒温箱中培养72h。
城市河流表层沉积物碱性磷酸酶分布及其成因探讨

城市河流表层沉积物碱性磷酸酶分布及其成因探讨马天海;孙娟【摘要】以南京城市河流秦淮河、运粮河为研究对象,通过测定11个点位表层沉积物中碱性磷酸酶活性(APA),分析了不同类型城市河道沉积物APA分布差异性;通过测定沉积物pH值、营养元素(碳、氮、磷)含量,探讨了沉积物理化特征对APA 分布影响.结果表明:(1)外秦淮河沉积物APA平均浓度最低,为10214.9m·g·kg-1·h-1,内秦淮河最高,为20021.2 mg·kg-1·h-1,APA分布与河道水力流通性及优势植物类型有关;(2)APA含量与总磷、氨氮、硝酸盐氮、有机质含量显著正相关(p<0.05),与pH显著负相关(p<0.05),表明表层沉积物丰富的营养成分充足情况下,将促使微生物新陈代谢,使得APA升高,而pH升高则会抑制APA.【期刊名称】《青海环境》【年(卷),期】2018(028)004【总页数】4页(P170-172,202)【关键词】碱性磷酸酶;营养元素;表层沉积物;城市河流【作者】马天海;孙娟【作者单位】南京大学金陵学院,江苏南京 210089;南京大学金陵学院,江苏南京210089【正文语种】中文【中图分类】X52水体沉积物是水体营养元素的重要蓄积库,是水体营养盐的缓冲剂,维持水中营养盐平衡,在水体缺乏营养时,水生生物的生长主要是靠沉积物释放的营养盐维持调节。
磷是造成水质富营养化的关键性的限制性因素之一[1]。
城市河流闸控滞流,水力流通性差,造成大量沉积物淤积,内源负荷累积。
城市河流沉积物磷的沉积物-水界面交换和输送研究具有重要意义。
本文研究了南京城市河流秦淮河、运粮河表层沉积物中碱性磷酸酶分布特征,测定了相应沉积物中pH值、营养元素(碳、氮、磷)含量及氮、磷形态,分析了南京城市河流中表层沉积物中碱性磷酸酶活性(APA)与营养元素、pH值的相关性。
研究结果可初步揭示南京城市河流表层沉积物中碱性磷酸酶的分布状况,以及与营养元素的关系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
沉积物中酶的测定方法水解酶一、脲酶(靛酚比色法)大多数细菌、真菌和高等植物均具有脲酶(urease)。
它是一种酰胺酶(amidase),能酶促有机质分子中肽键的水解。
土壤的脲酶活性与土壤的微生物数量、有机质含量、全氮和速效氮含量呈正相关。
人们常用土壤的脲酶活性表征土壤的氮素状况。
根据脲酶水解时生成的氨与苯酚钠及次氯酸钠反应,形成兰色靛酚这一原理。
此法的精确性较高,重现性较好。
试剂配制:1.甲苯(分析纯)2.10%尿素:尿素(分析纯)10g溶于100ml蒸馏水中。
3.柠檬酸盐缓冲液:368g柠檬酸(分析纯)溶于600ml蒸馏水中;295g氢氧化钾溶于1000ml蒸馏水;将二种溶液合并,用1mol/L氢氧化钠调pH至6.7,并用蒸馏水稀释至2L。
4.苯酚钠溶液:A.62.5g苯酚溶于少量95%乙醇,加2ml甲醇和18.5ml丙酮,用乙醇稀释至100ml,存于冰箱中。
B.27g氢氧化钠溶于100ml水中保存于冰箱中。
使用前,将溶液A、B各吸取20ml混合,用蒸馏水稀释至100ml备用。
5.次氯酸钠溶液:用蒸馏水稀释试剂,至活性氯浓度为0.9%。
(次氯酸钠活性氯浓度为5.2%)。
标准溶液:氮的标准溶液:精确称取称0.4717g硫酸铵(105℃烘干)溶于水,稀释至1L,则得1ml含0.1mg氮的标准溶液,即100ppm。
将100ppm的标准溶液稀释为10ppm。
标准曲线绘制:分别吸取0.5ml、1.5ml、2.5ml、3.5ml、4.5ml、5.5ml、6.5ml、7.5ml稀释后的标准溶液于50ml容量瓶或刻度试管中,然后加蒸馏水至25ml。
再加4ml苯酚钠溶液和3ml次氯酸钠溶液,随加随摇匀。
20min后显色,定容至50ml。
1h内在分光光度计上于波长578nm处比色。
根据吸光度和溶液浓度绘制标准曲线。
(溶液浓度为:0.1ppm、0.3ppm、0.5ppm、0.7ppm、0.9ppm、1.1ppm、1.3ppm、1.5ppm。
)分析步骤:称2-5g过20目风干土于50ml三角瓶中,加5-10滴甲苯,盖好,15分钟后加10ml 10%尿素和20ml pH6.7柠檬酸盐缓冲液,摇匀后,在37℃恒温箱中培养24小时,过滤。
取滤液1~3毫升(视样品浓度定)于50ml刻度试管中,加蒸馏水至25ml,再加入4ml苯酚钠溶液和3ml次氯酸钠溶液,边加边摇匀。
20分钟后定容,在分光光度计波长578nm处比色(1cm比色皿)。
反应生成的靛酚兰能在60分钟以内稳定。
每一土样设置用水代替基质(即尿素)的对照,以除掉土壤中氨态氮引起的误差。
还需减去无土基质(尿素+柠檬酸盐)。
结果计算:脲酶活性以24小时内每克土中氨态氮的毫克数来表示。
NH3-N(mg/1g土24h)=(浓度×稀释倍数×比色体积)÷(1000×干土重)1000为ug换算成mg二、磷酸酶(磷酸苯二钠比色法)磷酸酶(phosphatase)能酶促有机磷化合物的水解。
试验表明,土壤微生物对于土壤含磷有机物的矿化起着重要的作用;某些高等植物的根系也有磷酸酶活性。
土壤的磷酸酶活性可以表征土壤的肥力状况(特别是磷的状况),是评价土壤磷素生物转化方向与强度的指标。
研究证明,磷酸酶有三种最适pH:4-5,6-7和8-10。
所以,测定酸性、中性和碱性反应土壤的磷酸酶,要提供相应的pH缓冲液才能测出该土壤的磷酸酶最大活性。
测定磷酸酶常用的pH缓冲体系有醋酸缓冲液(pH5.0-5.4),柠檬酸盐缓冲液(pH7.0),硼酸缓冲液(pH9-10)。
本法测定是以磷酸苯二钠为基质,在磷酸酶的作用下,用水解基质所生成的苯酚的量来表示酶的活性。
试剂配制:1.甲苯(CR)2.①pH5醋酸盐缓冲液:(酸性土壤)A:0.2N醋酸溶液:称取1.776g冰醋酸和9.58g醋酸钠溶解,加蒸馏水定容到1000毫升。
B:0.2mol/L氢氧化氨溶液:取含25%~28%的氨水14.02ml稀释至500毫升。
取A、B溶液各250ml用蒸馏水定容至1000ml。
②pH7柠檬酸盐缓冲液:(中性土壤)A:0.1M柠檬酸溶液:称21.01g柠檬酸溶于1000ml蒸馏水中。
B:0.2M磷酸氢二钠溶液:Na2HPO4•7H2O53.63g或Na2HPO4•12H2O71.7g稀释至1000ml。
取A溶液64ml,B溶液436ml稀释至1000ml。
③pH10硼酸盐缓冲液:(碱性土壤)A:0.05M硼砂溶液(Na2B4O710•H2O)称取19.05g硼砂溶于1000ml蒸馏水中。
B:0.2M氢氧化钠:8g氢氧化钠溶于1000ml蒸馏水中。
取A溶液50ml,B溶液43ml,加水稀释至200ml。
3.pH9.8氨性氯化铵溶液:称取20g氯化氨溶于100ml浓氨水中,储存在橡皮塞瓶中,保存于冰箱。
4.0.5%磷酸苯二钠(Na2C6H5PO4•2H2O):称5g磷酸苯二钠溶于1000ml缓冲液。
5.2%4-氨基安替匹林:称取2g4-氨基安替匹林,先用少量水溶解,最后稀释至100ml,浑浊时用滤纸过滤后使用。
(一周内有效)6.8%铁氰化钾溶液:称8g铁氰化钾溶于少量水,定容至100ml,储存在棕色瓶中。
(一周内有效)酚的标准溶液:a.原液配制:0.5g重蒸酚溶于蒸馏水中,稀释至500毫升,储存于棕色瓶中,浓度即为1000ppm。
b.工作液配制:取2.5ml原液稀释至250ml,即浓度为10ppm,储存于棕色瓶中。
标准曲线绘制:分别取工作液1、3、5、7、9、11、13、15毫升于50毫升容量瓶或50毫升比色管中,加蒸馏水至25ml,再加0.25ml氨性氯化铵,0.5ml2%4-氨基安替匹林和0.5ml 8%铁氰化钾溶液,边加边摇匀,15分钟后定容,1.5h内在波长510nm处比色。
(溶液的浓度分别为0.2、0.6、1.0、1.4、1.8、2.2、2.6、3.0ppm试剂与测定相同。
)分析步骤:称过20目的风干土2g于50ml三角瓶中,加5-10滴甲苯,盖好瓶塞,15分钟后加0.5%磷酸苯二钠溶液20ml(对照直接加20ml缓冲液),摇匀并置37℃恒温培养24小时,培养结束后立即过滤。
吸滤液1~5毫升于50ml容量瓶(或比色管)中,加蒸馏水至25ml,再加入0.25ml氨性氯化氨,0.5ml2%4-氨基安替匹林和0.5ml8%铁氰化钾溶液,边加边摇匀,15分钟后定容,在波长510nm处比色。
(用1cm比色杯,显色后1.5h内稳定)每一土样设置用水代替基质的对照,还需减去无土基质。
结果计算:磷酸酶活性以24小时1克土酚的毫克数表示酚(mg/1g土•24h)=(土样浓度×分取倍数×比色体积)÷(1000×干土重)1000:ug换算成mg氧化还原酶一、过氧化氢酶土壤过氧化氢酶是研究的最早的土壤酶,与土壤有机质含量、土壤呼吸强度和土壤微生物含量等有关,在一定程度上反映了土壤微生物学过程的强度。
此方法是定量滴定酶促反应后剩余的过氧化氢来表示酶活性反应式为2KMnO4 + 5H2O2 + 3H2SO4– 2MnSO4 + K2SO4 + 8H2O + 5O2,此法测定结果较好。
试剂配制:1.0.3%H2O2:按1:100将30%H2O2用水稀释。
2.1.5mol/L的H2SO4。
3.0.002mol/LKMnO4溶液:称取高锰酸钾0.3161g,溶于1000ml无CO2蒸馏水中,储于棕色瓶中,备用。
分析步骤:1.称取5g过1mm筛的风干土,置于150ml三角瓶中,注入40ml蒸馏水和5ml0.3%过氧化氢。
2.同时设置对照,即三角瓶中注入40ml蒸馏水和5ml0.3%过氧化氢,而不加土样。
3.塞紧瓶塞,置于120r/min往返式摇床上,震荡30min。
4.随即注入5ml1.5mol/L硫酸以终止反应,用致密滤纸过滤。
5.取滤液25ml,用0.002mol/L高锰酸钾溶液滴定至微红色。
结果计算:以单位土重消耗的0.002mol/L高锰酸钾毫升数(对照与试验测定的差)表示土壤过氧化氢酶活性,其计算式为土壤过氧化氢酶活性(mlKMnO4/g干土)=V/dwt式中,V为0.002mol/L高锰酸钾毫升数(ml);dwt为烘干土壤重量(g)。
二、过氧化物酶(邻苯三酚比色法)过氧化物酶能酶在腐殖质的形成过程中具有重要作用。
过氧化物酶酶促有机物质氧化成醌,可通过有色化合物(如焦性没食子酸)比色测定。
试剂配制:1.1%1,2,3-邻苯三酚溶液:取10g1,2,3-邻苯三酚溶于蒸馏水中,并定容至1000ml。
2.0.5%H2O2溶液。
3.乙醚(分析纯)。
4.0.5mol/L盐酸。
标准溶液:重铬酸钾标准溶液:取0.75g重铬酸钾溶于1000ml0.5mol/L盐酸中,此溶液相当于50ml乙醚中含5mg焦性没食子酸。
取重铬酸钾标准溶液,用0.5mol/L盐酸再稀释成各种浓度,然后在比色计上,于波长430nm处比色。
分析步骤:1.称取1g过1mm筛的风干土样于50ml三角瓶中,然后加入10ml 1%邻苯三酚溶液和2ml 0.5%过氧化氢溶液,摇匀,塞好塞子,置于30℃培养箱中,培养2h (活性低时刻延长培养时间)。
与此同时进行12ml蒸馏水代替基质的对照。
2.培养结束后,取出三角瓶,加入0.5mol/L盐酸2.3ml(4 ml柠檬酸-磷酸缓冲溶液),摇匀,用乙醚将生成的焦性没食子酸抽出(如含量高时需提取多次)于50ml比色管中,合并提取液并定容,于430nm处比色。
结果计算:以1g土壤,在2h内生成的焦性没食子酸的毫克数表示酶的活性单位,其计算式为土壤过氧化物酶活性[mg焦性没食子酸/(g干土.h)] = m/(dwt.h)式中,m为2h内生成的焦性没食子酸的毫克数(mg);dwt为烘干土壤重量(g)。
三、多酚氧化酶(邻苯三酚比色法)测定土壤多酚氧化酶的活性,能在一定程度上了解土壤的腐殖化进程。
土壤中基质邻苯三酚,经多酚氧化酶的酶促作用生成红紫棓精,用乙醚萃取,萃取液经紫外光谱比色,测得红紫棓精的量,即可表示多酚氧化酶的活性。
试剂配制:1.1%1,2,3-邻苯三酚溶液:取10g1,2,3-邻苯三酚溶于蒸馏水中,并定容至1000ml。
2.柠檬酸-磷酸缓冲液(pH4.5):A. 0.1mol/L的柠檬酸溶液;B. 0.2mol/L的磷酸二氢钠溶液。
取A液45.03ml,B液54.97ml混合即为pH4.5的柠檬酸-磷酸缓冲溶液。
3.乙醚(分析纯)。
4.0.5mol/L盐酸。
标准溶液:重铬酸钾标准溶液:称取0.75g重铬酸钾溶于1000ml0.5mol/LHCl,相当于50ml 乙醚中含5mg红紫棓精。
取重铬酸钾标准溶液,用0.5mol/L盐酸再稀释成各种浓度,然后在比色计上,于波长430nm处比色。
