金属材料的熔点、热导率及比热容
高温储热材料熔点、比热容等指标统计表

高温储热材料熔点、比热容等指标统计表近年来,随着节能环保理念的深入人心,高温储热技术备受关注。
在太阳能、风能等可再生能源的快速发展下,高温储热材料作为能量储存的重要手段,其性能指标备受关注。
其中,熔点和比热容等指标则成为评判高温储热材料性能的重要因素。
本文将围绕这些指标展开深入探讨。
1. 熔点统计熔点是指物质由固态转变为液态的温度。
在高温储热领域,材料的熔点直接关系到其在高温环境下的稳定性和可靠性。
为了更全面地了解高温储热材料的熔点情况,我们统计了以下几种代表性材料的熔点数据:- 盐类储热材料:氯化钠(801°C)、氯化钾(776°C)、氯化钙(772°C)- 金属氧化物储热材料:氧化铁(1539°C)、氧化铝(2072°C)、氧化镁(2800°C)- 硝酸盐类储热材料:硝酸钾(334°C)、硝酸钠(307°C)、硝酸钙(363°C)从统计数据可以看出,不同类型的高温储热材料的熔点存在较大差异。
盐类储热材料的熔点相对较低,而金属氧化物和硝酸盐类储热材料的熔点较高。
这也说明了不同类型材料在高温条件下的适用性存在一定差异。
在实际应用中,需要根据具体的工况要求选择合适的高温储热材料。
2. 比热容统计比热容是指单位质量物质在温度升高1摄氏度时吸收或释放的热量。
较高的比热容意味着材料具有更高的热容量,能够在储热过程中吸收更多的热量。
以下是几种常见高温储热材料的比热容数据统计:- 盐类储热材料:氯化钠(3.7 J/g·°C)、氯化钾(2.3 J/g·°C)、氯化钙(1.4 J/g·°C)- 金属氧化物储热材料:氧化铁(0.45 J/g·°C)、氧化铝(0.92J/g·°C)、氧化镁(1.1 J/g·°C)- 硝酸盐类储热材料:硝酸钾(1.5 J/g·°C)、硝酸钠(1.7 J/g·°C)、硝酸钙(1.1 J/g·°C)从比热容数据统计中可以看出,不同类型的高温储热材料具有不同的比热容数值。
金属材料与热处理
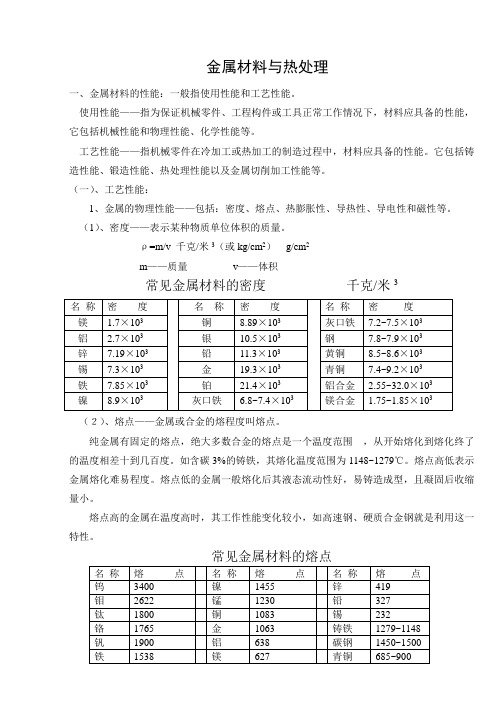
金属材料与热处理一、金属材料的性能:一般指使用性能和工艺性能。
使用性能——指为保证机械零件、工程构件或工具正常工作情况下,材料应具备的性能,它包括机械性能和物理性能、化学性能等。
工艺性能——指机械零件在冷加工或热加工的制造过程中,材料应具备的性能。
它包括铸造性能、锻造性能、热处理性能以及金属切削加工性能等。
(一)、工艺性能:1、金属的物理性能——包括:密度、熔点、热膨胀性、导热性、导电性和磁性等。
(1)、密度——表示某种物质单位体积的质量。
ρ=m/v 千克/米3(或kg/cm2)g/cm2m——质量v——体积常见金属材料的密度千克/米3(2)、熔点——金属或合金的熔程度叫熔点。
纯金属有固定的熔点,绝大多数合金的熔点是一个温度范围,从开始熔化到熔化终了的温度相差十到几百度。
如含碳3%的铸铁,其熔化温度范围为1148~1279℃。
熔点高低表示金属熔化难易程度。
熔点低的金属一般熔化后其液态流动性好,易铸造成型,且凝固后收缩量小。
熔点高的金属在温度高时,其工作性能变化较小,如高速钢、硬质合金钢就是利用这一特性。
(3)、热膨胀——固态金属或合金因温度变化而具有一定的温-度,在一定温度下,固体的各个线度是一定的。
当固休受热后,随着温度升高,它的各种线度都要增长。
工程上对金属的热膨胀大小常用线膨胀系数来表示。
线膨胀系数——单位长度每升高1℃所引起的延伸量。
即:αL=L1-L0//L0(t1-t0)厘米/厘米—℃(1/℃)式中:αL——线膨胀系数L1——升温后的长度t0——升温前的温度t1——升温后的温度体膨胀系数可用线膨胀系数的三倍近似计算,αV=3αL;面膨胀系数可用线膨胀系数的二倍近似计算,αS=2αL。
金属的热膨胀量虽然很微小,但会产生很大的内应力,使工件变形或断裂。
但工业上也常利用这一特性来装配组合件。
(4)、导热性——金属在加热或冷却时能够传导热量的性质称为导热性。
不同金属的导热性各有不同,导热性的好坏用热导率来表示。
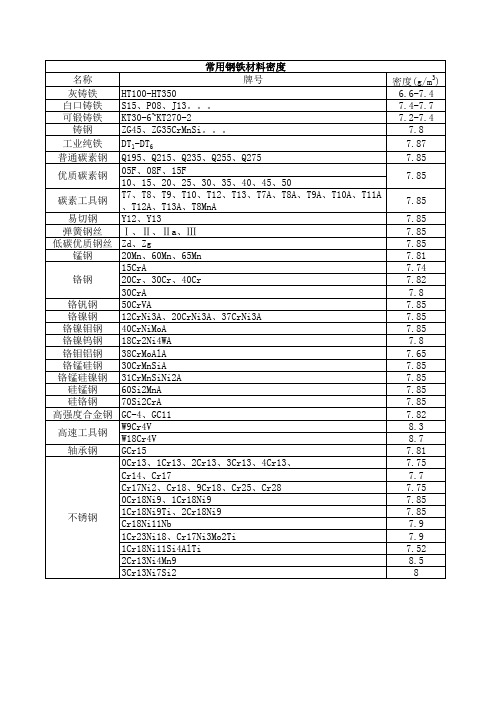
常用钢铁材料密度、硬度、熔点
钢
铸铁 硬铝 硅铝合金 巴氏合金 铅青铜 铝 铜
硬度HBS 80-220 225-400 400-600 600-750 900-1250 100-250 550-650 40-55 90-120 50-65 65-100 18-30 20-25 20-50 20-55
非合金钢、低合金钢和合金钢的合金元素规定含量界限值(GB/T 13304-1991) 合金元素规定质量分数界限值(%) 合金元素 非合金钢〈 低合金钢 合金钢≥ Al 0.1 —— 0.1 B 0.0005 —— 0.0005 Bi 0.1 —— 0.1 Cr 0.3 0.3-〈0.5 0.5 Co 0.1 —— 0.1 Cu 0.1 0.1-〈0.5 0.5 Mn 1 1-〈1.4 1.4 Mo 0.05 0.05-〈0.1 0.1 Ni 0.3 0.3-〈0.5 0.5 Nb 0.02 0.02-〈0.06 0.06 Pb 0.4 —— 0.4 Se 0.1 —— 0.1 Si 0.5 0.5-〈0.9 0.9 Te 0.1 —— 0.1 Ti 0.05 0.05-〈0.13 0.13 W 0.1 —— 0.1 V 0.04 0.04-〈0.12 0.12 Zr 0.05 0.05-〈0.12 0.12 RE(混合稀土元素) 0.02 0.02-〈0.05 0.05 其他规定元素 0.05 —— 0.05 (S、P、C、N 除外)
名称 灰铸铁 白口铸铁 可锻铸铁 铸钢 工业纯铁 普通碳素钢
常用.6-7.4 7.4-7.7 7.2-7.4 7.8 7.87 7.85 7.85 7.85 7.85 7.85 7.85 7.81 7.74 7.82 7.8 7.85 7.85 7.85 7.8 7.65 7.85 7.85 7.85 7.85 7.82 8.3 8.7 7.81 7.75 7.7 7.75 7.85 7.85 7.9 7.9 7.52 8.5 8
常见材料的熔点和比热容

常见材料的熔点和比热容(总9页)-CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除工程材料的比热容物质比热物质比热镍铬合金石蜡砂有机玻璃聚苯乙烯镍铝锰合金柏油(沥青)丙酮玄武岩汽油苯甘油花岗岩木材11 424~15491 3402155854206017452412煤炭胶合板瓷(器)氟塑料硬质橡胶甲醇混凝土磷青铜纸聚氯乙烯塑料水空气聚脂塑料软木13172512~1040255041821 0071088~2 3031 7582殷钢橡胶煤油康铜黄铜冰(0)锰钢植物油机油石油聚乙烯41038041871633~19681885橡皮二硫化碳云母乙醇石英玻璃钠玻璃窗用玻璃温度计用玻璃燧石玻璃布层塑料冕玻璃1 00624224901465(在和一大气压下测得)冰、水在不同温度下的比热容水冰物质比热容c水酒精煤油冰蓖麻油砂石铝干泥土铁、钢铜汞铅对表中数值的解释:(1)比热此表中单位为kJ/(kg·℃);(2)水的比热较大,金属的比热更小一些;(3)c铝>c铁>c钢>c铅 (c铅<c铁<c钢<c铝)。
补充说明:⒈不同的物质有不同的比热,比热是物质的一种特性;⒉同一物质的比热一般不随质量、形状的变化而变化,如一杯水与一桶水,它们的比热相同;⒊对同一物质、比热值与物体的状态有关,同一物质在同一状态下的比热是一定的,但在不同的状态时,比热是不相同的,如,水的比热与冰的比热不同。
⒋在温度改变时,比热容也有很小的变化,但一般情况下忽略。
比热容表中所给的数值都是这些物质的平均值。
⒌气体的比热容和气体的热膨胀有密切关系,在体积恒定与压强恒定时不同,故有定容比热容和定压比热容两个概念。
但对固体和液体,二者差别很小,一般就不再加以区分。
参考资料:水(kg·℃)/ *10³J/(kg·℃)冰(kg·℃)/ *10³J/(kg·℃)酒精(kg·℃)/ *10³J/(kg·℃)煤油(kg·℃)/ *10³J/(kg·℃)蓖麻油(kg·℃)/ *10³J/(kg·℃)橡胶(kg·℃)/ *10³J/(kg·℃)砂石(kg·℃)/ *10³J/(kg·℃)干泥土(kg·℃)/*10³J/(kg·℃)玻璃(kg·℃)/*10³J/(kg·℃)铝(kg·℃)/*10³J/(kg·℃)钢铁(kg·℃)/*10³J/(kg·℃)铜(kg·℃)/*10³J/(kg·℃)汞(kg·℃)/*10³J/(kg·℃)铅(kg·℃)/*10³J/(kg·℃)理论上说,常见液体和固体物质中,水的比热容最大对上表中数值的解释:(1)比热此表中单位为kJ/(kg·℃)/ J/(kg·℃),两单位为千进制1kJ/(kg·℃)/=1*10³J/(kg·℃);(2)水的比热较大,金属的比热更小一些;(3)c铝>c铁>c钢>c铅 (c铅<c铁<c钢<c铝)熔点就是凝固点。
金属材料熔点表

金属材料熔点表....常见金属材料的比重及熔点表海纳百川:收集整理金属材料名称镁铝铁镍铅汞钨金银铜元素符号Mg Al Fe Ni Pb Hg W Au Ag Cu比重1.742.77.878.911.3713.619.319.3210.498.96金属材料名称灰口铁白口铁碳素钢黄铜青铜钢元素符号————————————比重6.8-7.47.2-7.57.81-7.858.5-8.857.5-8.97.8-7.9常用金属材料熔点金属名称铝铜锰铅钡钴铁钼锑铋铬镁镍锡元素符号Al Cu Mn Pb Be Co Fe Mo Sb B Cr Mg Ni Sn熔点660.210831245327.41285149515392622630.5271.318556501455231.9金刚石:3550 钨:3410 纯铁:1535各种钢:1300~1400 各种铸铁:1200左右铜:1083 金:1064银:962铝:660 锌:419.5铅:327锡:232 硫代硫酸钠:48冰:0汞:-38.9 固态水银:-39固态酒精:-117 固态氮:-210 固态氢:-259 固态氦:-272 (有些不是金属也全给列出来了)名称熔点℃热导率W/(m2·K)比热容J/(kg·K)名称熔点℃热导率W/(m2·K)比热容J/(kg·K)灰铸铁120046.4-92.8544.3铝658203904.3铸钢1425489.9铅32734.8129.8低碳钢1400-150046.4502.4锡23262.6234.5黄铜95092.8393.6锌419110393.6青铜99563.8385.2镍145259.2452.2。
估算金属熔化热和熔化熵的经验公式

估算金属熔化热和熔化熵的经验公式任何系统都不可能通过有限的过程使自身温度降低至绝对零度,这就是热力学第三定律。
在绝对零度时(0K=-273.15℃),所有纯物质的完美晶体的熵值为零,绝对零度是不可能达到,所以宇宙中存在温度的下限,即零下答:这是固体熔化的吸热现象。
在物态变化中,物体从固态变成液态的现象叫做熔化,而且在这个过程中要吸收热量。
白糖是固体,放入口中吸收人口腔的热量而熔化,所以,人的口腔就会有清凉的感觉。
这就是白糖固体放入口中有清凉感觉的原因。
1.性状:无色透明液体,有刺激性气味。
2.熔点(℃):-97.83.沸点(℃):64.74.相对密度(水=1):0.795.相对蒸气密度(空气=1):1.16.饱和蒸气压(kPa):12.3(20℃)7.燃烧热(kJ/mol):7238.临界温度(℃):2409.临界压力(MPa):7.9510.辛醇/水分配系数:-0.82~-0.7711.闪点(℃):8(CC);12.2(OC)12.自燃温度(℃):43613.爆炸上限(%):36.514.爆炸下限(%):615.溶解性:溶于水,可混溶于醇类、乙醚等多数有机溶剂。
16.折射率(N/D,20℃):1.328417.黏度(mPa·s,25℃):0.552518.蒸发热(KJ/mol,b.p.):35.3219.熔化热(KJ/kg):98.8120.比热容:KJ/(kg·K),20℃,定压:2.5121.沸点上升常数:0.78522.电导率(S/m,25℃):1.5×10-923.热导率(W/(m·K),30℃):21.352724.体膨胀系数(K,20℃):0.25.临界密度(g/cm):0.27326.临界体积(cm/mol):11727.临界压缩因子:0.22328.偏心因子:0.56629.Lennard-Jones参数:3.8632(A);419.86(K)30.溶度参数(J/cm):29.53231.van der Waals体积(cm/mol):21.71032.气相标准燃烧热(焓)(kJ/mol):764.933.气相标准生成热(焓)( kJ/mol):- 201.534.气相标准熵(J·mol-1/K):239.8835.气相标准生成自由能( kJ/mol):- 161.636.气相标准热熔(J·mol-1/K):44.0637.液相标准燃烧热(焓)(kJ/mol):- 726.938.液相标准生成热(焓)( kJ/mol):- 239.139.液相标准熵(J·mol-1/K):127.2440.液相标准生成自由能( kJ/mol):- 166.8841.液相标准热熔(J·mol-1/K):81.4。
重金属熔点表

7.8-7.9
常用金属材料熔点
金属名称
铝
铜
锰
铅
钡
钴
铁
钼
锑
铋
铬
镁
镍
锡
元素符号
Al
Cu
Mn
Pb
Be
Co
Fe
Mo
Sb
B
Cr
Mg
Ni
Sn
熔点
660.2
1083
1245
327.4
1285
1495
1539
2622
630.5
271.3
1855
650
1455
231.9
金刚石:3550钨:3410纯铁:1535
重金属熔点表
金属材料名称
镁
铝
铁
镍
铅
汞
钨
金
银
铜
元素符号
Mg
Al
Fe
Ni
Pb
Hg
W
Au
Ag
Cu
比重
1.74
2.7
7.87
8.9
11.37
13.6
19.3
19.32
10.49
8.96
金属材料名称
灰口铁
白口铁
碳素钢
黄铜
青铜
钢
元素符号
——
——
——
——
——
——
比重
6.8-7.4
7.2-7.5
7.81-7.85
8.5-8.85
各种钢:1300~1400各种铸铁:1200左右
铜:1083金:1064银:962
铝:660锌:419.5铅:327
金属的热容计算公式

金属的热容计算公式热容是物质单位质量在温度变化时吸收或释放的热量的量度。
金属作为一种常见的材料,其热容的计算对于工程和科学领域具有重要意义。
金属的热容计算公式可以帮助我们了解金属在温度变化时的热量变化情况,从而在工程设计和科学研究中提供重要的参考依据。
金属的热容计算公式可以用来计算金属在温度变化时吸收或释放的热量。
金属的热容通常用符号C来表示,单位是焦耳每千克每摄氏度(J/kg°C)。
金属的热容计算公式可以表示为:Q = mcΔT。
其中,Q表示金属吸收或释放的热量(单位为焦耳,J);m表示金属的质量(单位为千克,kg);c表示金属的比热容(单位为焦耳每千克每摄氏度,J/kg°C);ΔT表示温度变化(单位为摄氏度,°C)。
通过金属的热容计算公式,我们可以计算金属在温度变化时吸收或释放的热量。
这对于工程设计和科学研究具有重要意义。
例如,在工程设计中,我们需要考虑金属在温度变化时的热量变化情况,以确保工程结构的稳定性和安全性。
在科学研究中,我们可以通过金属的热容计算公式来研究金属在不同温度下的热量变化情况,从而深入了解金属的热学性质。
金属的比热容是金属在单位质量下,温度升高1摄氏度时所吸收的热量。
金属的比热容是金属热学性质的重要参数,不同金属的比热容是不同的。
一般来说,金属的比热容与其晶体结构、原子量、原子半径等因素有关。
通过金属的比热容,我们可以了解金属在温度变化时的热学性质,从而为工程设计和科学研究提供重要的参考依据。
金属的热容计算公式还可以用来研究金属的热传导性质。
金属的热传导性是金属在温度梯度下传导热量的性质。
金属的热传导性与其热容有密切关系,通过金属的热容计算公式,我们可以了解金属在温度变化时的热传导性质,从而为工程设计和科学研究提供重要的参考依据。
在工程设计和科学研究中,金属的热容计算公式是一个重要的工具。
通过金属的热容计算公式,我们可以了解金属在温度变化时的热量变化情况,从而为工程设计和科学研究提供重要的参考依据。
