有机合成 甲醇工艺学
甲醇合成原理方法与工艺
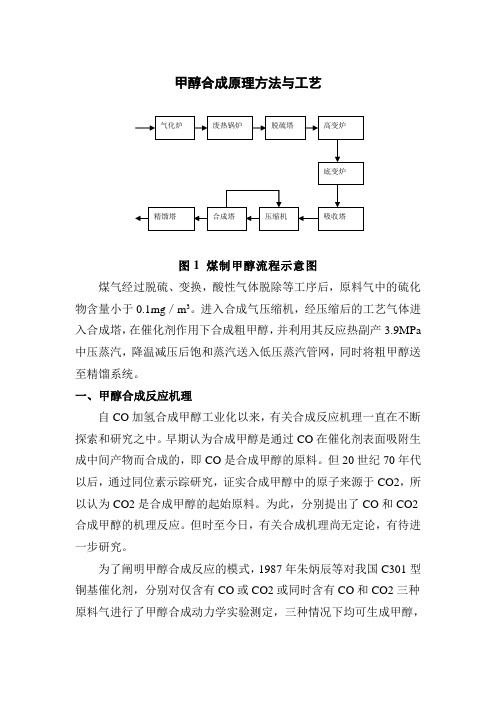
甲醇合成原理方法与工艺图1 煤制甲醇流程示意图煤气经过脱硫、变换,酸性气体脱除等工序后,原料气中的硫化物含量小于0.1mg/m3。
进入合成气压缩机,经压缩后的工艺气体进入合成塔,在催化剂作用下合成粗甲醇,并利用其反应热副产3.9MPa 中压蒸汽,降温减压后饱和蒸汽送入低压蒸汽管网,同时将粗甲醇送至精馏系统。
一、甲醇合成反应机理自CO加氢合成甲醇工业化以来,有关合成反应机理一直在不断探索和研究之中。
早期认为合成甲醇是通过CO在催化剂表面吸附生成中间产物而合成的,即CO是合成甲醇的原料。
但20世纪70年代以后,通过同位素示踪研究,证实合成甲醇中的原子来源于CO2,所以认为CO2是合成甲醇的起始原料。
为此,分别提出了CO和CO2合成甲醇的机理反应。
但时至今日,有关合成机理尚无定论,有待进一步研究。
为了阐明甲醇合成反应的模式,1987年朱炳辰等对我国C301型铜基催化剂,分别对仅含有CO或CO2或同时含有CO和CO2三种原料气进行了甲醇合成动力学实验测定,三种情况下均可生成甲醇,试验说明:在一定条件下,CO和CO2均可在铜基催化剂表面加氢生成甲醇。
因此基于化学吸附的CO连续加氢而生成甲醇的反应机理被人们普遍接受。
对甲醇合成而言,无论是锌铬催化剂还是铜基催化剂,其多相(非匀相)催化过程均按下列过程进行:①扩散——气体自气相扩散到气体一催化剂界面;②吸附——各种气体组分在催化剂活性表面上进行化学吸附;③表面吸附——化学吸附的气体,按照不同的动力学假说进行反应形成产物;④解析——反应产物的脱附;⑤扩散——反应产物自气体一催化剂界面扩散到气相中去。
甲醇合成反应的速率,是上述五个过程中的每一个过程进行速率的总和,但全过程的速率取决于最慢步骤的完成速率。
研究证实,过程①与⑤进行得非常迅速,过程②与④的进行速率较快,而过程③分子在催化剂活性界面的反应速率最慢,因此,整个反应过程的速率取决于表面反应的进行速率。
提高压力、升高温度均可使甲醇合成反应速率加快,但从热力学角度分析,由于CO、C02和H2合成甲醇的反应是强放热的体积缩小反应,提高压力、降低温度有利于化学平衡向生成甲醇的方向移动,同时也有利于抑制副反应的进行。
年产10万吨甲醇工艺设计

甲醇是一种重要的有机化工品,广泛应用于合成有机化合物、涂料、塑料等工业领域。
甲醇工艺设计的关键目标是实现高产量、高质量的甲醇生产,同时考虑能源消耗、环境污染和安全性等方面的要求。
本文将对一种年产10万吨甲醇工艺设计进行详细介绍,包括原料选择、反应过程、设备选型、能源消耗和环境污染控制等方面。
1.原料选择甲醇的主要原料为天然气或煤炭。
在本工艺设计中,我们选择优质天然气作为甲醇的主要原料。
天然气中的甲烷通过蒸汽重整反应生成合成气,包括一氧化碳和氢气。
该合成气经过净化处理后,进入甲醇合成反应器进行反应。
2.反应过程甲醇的合成反应是一种催化反应,主要基于甲醇合成催化剂的作用。
在本工艺设计中,我们选择了高效的铜锌氧化物催化剂,能够在相对低的温度和压力下实现高效率的甲醇合成。
反应过程主要包括气相反应和液相吸收两个步骤。
气相反应器中,一氧化碳和二氧化碳与氢气发生反应生成甲醇。
反应后的气体进入液相吸收器,通过溶剂的吸收和分离,将甲醇从废气中回收。
3.设备选型甲醇生产设备主要包括气体净化、蒸汽重整、合成反应、分离和脱水等装置。
对于年产10万吨甲醇的工艺设计,我们选用了适宜的设备类型和规格,确保设备能够满足预期产量和质量要求。
例如,气体净化装置采用活性炭吸附和分子筛吸附的组合方式,提高气体净化效果。
合成反应器采用多床催化剂装置,提高反应效率和催化剂的使用寿命。
分离装置采用精馏和吸附等工艺,实现甲醇的回收。
4.能源消耗甲醇生产需要消耗大量的能源,包括天然气和蒸汽等。
为了降低能源消耗和提高能源利用效率,我们在工艺设计中采取了多项措施。
例如,在蒸汽重整过程中,我们采用余热回收技术,将废弃热量回收利用。
在合成反应过程中,我们优化反应条件和催化剂的使用方式,降低能源消耗。
此外,我们还考虑了电力和水的节约措施,提高整体能源利用效率。
5.环境污染控制甲醇生产过程中会产生废气、废水和废渣等污染物。
为了控制环境污染,我们在工艺设计中采取了多项措施。
甲醇合成工艺

甲醇合成工艺甲醇合成第一节甲醇产品介绍一、物理性质甲醇是最简单的饱和一元醇,俗称“木精”、“木醇”,其分子式为CH3OH,分子量为32.04。
常温常压下,纯甲醇是无色透明、易燃、极易挥发且略带醇香味、刺激性气味的有毒液体。
甲醇能和水以任意比互溶,但不形成共沸物,能和多数常用的有机溶剂(乙醇、乙醚、丙酮、苯等)混溶,并形成恒沸点混合物。
甲醇能和一些盐如CaCl2、MgCl2等形成结晶化合物,称为结晶醇,如CaCl2?CH3OH、MgCl2?6CH3OH,和盐的结晶水合物类似。
甲醇能溶解多种树脂,但不能与脂肪烃类化合物互溶。
甲醇水溶液的密度随甲醇浓度和温度的增加而减小;甲醇水溶液的沸点随液相中甲醇浓度的增加而降低。
甲醇蒸汽和空气混合能形成爆炸性混合物,遇明火、高热能引起爆炸。
甲醇燃烧时无烟,其燃烧时显蓝色火焰。
与氧化剂接触发生化学反应或引起燃烧。
在火场中,受热的容器有爆炸危险,其蒸汽比空气重,能在较低处扩散到相当远的地方,遇明火会引起回燃,属危险性类别;试剂甲醇常密封保存在棕色瓶中置于较冷处。
甲醇有很强的毒性,口服5~10ml可以引起严重中毒,10ml以上造成失明,30ml以上可致人死亡。
甲醇属神经和血液毒物,它可以通过消化道、呼吸道和皮肤等途径进入人体,对中枢神经系统有麻醉作用;对视神经和视网膜有特殊选择作用,引起病变;可导致代谢性酸中毒,故空气中甲醇蒸汽的最高允许浓度为操作区5mg/m3,居民区0.5 mg/m3。
甲醇在常温下无腐蚀性,但对于铅、铝例外。
表一:甲醇物性参数表序号项目单位数值1 沸点(1.013×105Pa)℃ 64.5~64.72 凝固点℃ -97~-97.83 闪点℃ 12(闭口)~16(开口)4 自燃点℃ 473(空气中)~461(氧气中) 5相对密度(d20)(g/ml) 0.7915 6蒸汽压力(20℃)Pa 11825 蒸汽压力(21.2℃) Pa 133337 临界压力 MPa 7.95, 8 临界温度℃ 240 13 爆炸上限 % 36.5 8 爆炸下限 % 6 9 最小点火能量 MJ 0.216 10 相对分子量 32.04 表二:甲醇饱和蒸汽温度与压力平衡表(1mmHg = 133.322Pa)温度℃蒸汽压mmHg 温度℃蒸汽压mmHg 温度℃ 蒸汽压mmHg-67.4 0.102 20 96.0 130 6242-60.4 0.212 30 160 140 8071-54.5 0.378 40 260.5 150 10336-48.1 0.702 50 406 160 13027-44.4 0.982 60 625 170 16292-44.0 1 64.7 760 180 20089-40 2 70 927 190 24615-30 4 80 1341 200 29787-20 8 90 1897 210 35770-10 15.5 100 2621 220 425730 29.6 110 3561 230 5041410 54.7 120 4751 240 59660表三:精甲醇的质量国家标准甲醇质量标准GB338—2004检测项目指标优等品一等品合格品色度(铂—钴号)5 10 密度(20℃)g/cm3 0.791~0.792 0.791~0.793温度范围(101325Pa)℃ 64—65.5 沸程℃≤ 0.8 1 1.5高锰酸钾试验min≥ 50 30 20水混溶性试验 1:03 1:09 水份含量%≤ 0.1 0.15 酸度(以HCOOH)%计≤ 0.0015 0.003 0.005碱度(以NH3)%计≤ 0.0002 0.0008 0.0015 羰基化合物(HCHO)%≤ 0.002 0.005 0.01蒸发残渣含量%≤ 0.001 0.003 0.005 硫酸洗涤试验/铂—钴色号50 —乙醇的质量百分数% 供需双方协商表四:精甲醇的质量美国联邦规格AA标准:美国联邦规格AA级O-M-232E相对密度0.7928 馏程(101.325KPa)℃不大于1℃,并包括64.6±0.1℃纯度% 99.85酸度% 以醋酸计,最大为0.003醛酮% <0.003 KMnO4试验min >30 水份% <0.1不挥发物<0.001乙醇% <0.001 二、甲醇的化学性质甲醇不具酸性,也不具碱性,对酚酞和石蕊均呈中性。
年产30万吨甲醇工艺设计

甲醇是一种重要的有机化学品,广泛应用于化工、能源、医药、农药等领域。
设计年产30万吨甲醇的工艺需要充分考虑原料、设备、反应条件等多方面的因素。
下面将详细介绍年产30万吨甲醇的工艺设计。
首先,我们需要确定甲醇的生产原料。
甲醇的主要原料是合成气,它由一定比例的一氧化碳和氢气混合而成。
合成气的生产方式有多种,常用的有煤气化和天然气重整。
煤气化将煤炭在高温高压下转化为合成气,天然气重整则通过将天然气进行催化转化来得到合成气。
在选择原料时,需要综合考虑成本、供应稳定性和环境因素等因素。
其次,我们需要确定甲醇的合成反应。
甲醇的合成主要通过低温低压下的催化反应进行。
目前常用的合成甲醇催化剂有铜锌基催化剂和铝酸胶体催化剂。
催化剂的选择需要考虑反应速度、选择性和稳定性等因素。
确定了原料和反应条件之后,我们需要设计甲醇的工艺流程。
一般而言,甲醇的工艺流程包括合成气的制备、催化反应、分离纯化等步骤。
合成气的制备是整个工艺流程的核心环节之一、在煤气化过程中,需要将煤炭进行气化反应,产生合成气。
煤气化反应通常在高温高压下进行,需要合适的催化剂和气化剂。
气化产生的合成气含有大量的杂质,如硫化物、氮气和灰份等。
因此,还需要进行合适的净化处理,以提高合成气的质量。
催化反应是甲醇的合成过程,需要注意反应温度、压力和催化剂的选择。
一般而言,合成甲醇反应温度在200-300摄氏度之间,压力在一定范围内进行调节。
催化剂的选择和工艺条件的优化是提高甲醇合成效率和选择性的关键。
分离纯化是甲醇工艺流程中的重要环节。
合成气反应产生的甲醇需要进行分离和纯化处理,以除去杂质和提高产品纯度。
一般而言,甲醇通过蒸馏、吸附、结晶等分离过程进行纯化。
最后,进行工艺设计时还需要考虑能源消耗和废物处理。
甲醇的生产过程需要消耗大量的能源,需要选择节能的设备和优化工艺条件。
废物处理是环保的重要环节,需要合理处理反应废气和废水,以减少对环境的影响。
以上是年产30万吨甲醇工艺设计的简要介绍,设计过程中需要充分考虑原料、设备、反应条件、能源消耗和废物处理等多方面的因素。
甲醇的合成PPT课件
甲醇用途
(1)甲醇是一种用途广泛的有机化工产品,在农药、 医药、染料、香料、涂料等生产中都需要甲醇 作为原料或溶剂。甲醇作为有机产品在世界范 围内其产量仅次于乙烯、丙烯及纯苯等基础原 料,是基本的有机化工原料。
(2) 甲醇在世界范围内最大的用途是作为生产甲 基丁基醚(MTBE)的原料,甲醛和醋酸也占 有一定的比例。
•6
反应特点及催化剂
反应特点:甲醇合成反应是在有催化剂存在的 一个体积缩小的、可逆的、伴有多种副反应发 生的放热反应。
催化剂:铜基催化剂 主要成分:CuO、ZnO、AL2O3,其中有活性的
是铜,必须还原后使用。 还原方程式为: CuO+H2=Cu+H2O
•7
甲醇合成技术
气相法:气相法甲醇生产过程由于温度控制、床层温升 和换热的限制,合成气的单程转化率低,出口甲醇质 量分数较小,循环量大,经济性难以令人满意。
•4
甲醇合成工艺原理
甲醇的化学式:CH3OH 甲醇合成反应是一个放热反应,化学反应方程式如下 主反应:
CO+2H2→CH3OH +102.5kJ/mol CO2+3H2→CH3OH+H2O+59.6kJ/mol CO+H2O→CO2+H2+41.19 kJ/mol
•5
甲醇合成的副反应
2 CO+4H2 →CH3OCH3+H2O 2CO+4H2→C2H5OH+H2O 2CO+3H2→CH4+H2O nCO+2nH2→(CH2)n烃类+nH2O
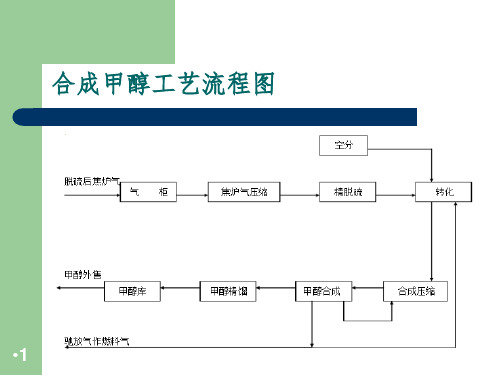
合成甲醇工艺流程图
•1
甲醇简介
主要性质
甲醇是一种无色,略带乙醇香气的挥发性可燃液 体,在常压情况下,密度0.8100g/ml,甲醇沸点为 64.7 ,自燃点473 (空气中),461 (氧气中)可与水 互溶,在汽油中有较大的溶解度。
甲醇合成原理方法与工艺

甲醇合成原理方法与工艺
一、甲醇合成原理
甲醇合成的机理简单概括为:催化剂起作用于乙烯,使它在氢气的作
用下发生氢化反应,从而形成甲醇的反应过程。
甲醇合成的反应分为三步:乙烯氢化合成乙醇,乙醇的氢化反应形成乙醇的氢化物,最后由乙醇氢化
物再次氢化反应,形成甲醇。
甲醇合成的主要反应过程为:
1、乙烯氢化反应:乙烯+H2→乙醇
2、乙醇氢化反应:乙醇+H2→乙醇的氢化物+H2O
3、乙醇的氢化物氢化反应:乙醇氢化物+H2→甲醇
二、甲醇合成工艺
1、反应器
甲醇合成反应器主要由容积箱、催化剂填料、表内管、安全阀、加料口、进料口、流量计、温度计等组成。
容积箱用于容纳催化剂和乙烯,表
内管用于分离氢气和乙烯,安定器可以确保反应器的安全,加料口用于进
行乙烯和氢气的进料,进料口用于将反应产物进行收集,流量计可以确定
矿物质的流量,温度计可以控制反应温度和防止温度过高等。
2、催化剂
甲醇合成工艺中使用的催化剂一般是活性碳粉末或负活性氧化铝粉末等。
甲醇工艺流程简述

甲醇工艺流程简述甲醇是一种无色、挥发性较强的液体化合物,也是常见的有机化学品之一、甲醇的制备工艺流程通常分为合成气制甲醇和天然气制甲醇两种。
下面将对这两种制备工艺流程进行详细的描述。
一、合成气制甲醇工艺流程合成气制甲醇工艺是将天然气(或石油)转化成合成气,然后通过催化反应将合成气转化成甲醇的一种工艺。
合成气主要由一氧化碳和氢气组成,生成甲醇的反应是以一氧化碳为起始物质,经过一系列的反应途径得到甲醇。
1.准备原料:当用天然气作为原料时,首先需要通过净化处理去除其中的杂质,然后将天然气和蒸汽混合,在蒸汽重整反应器中进行催化重整反应,产生合成气。
2.合成气的催化:将合成气送入低压合成气转化反应器,在催化剂的催化下,一氧化碳和氢气发生醇合反应,生成甲醇。
3.分离和纯化:甲醇在反应混合物中以蒸汽的形式存在,需要通过冷凝和分离装置将甲醇与其他组分分离开来。
可以采用常压或低压蒸馏进行分离和纯化。
4.精制和储存:通过精制过程,去除甲醇中的杂质并调节甲醇的含量和纯度,然后将精制后的甲醇储存起来,以备后续使用或销售。
二、天然气制甲醇工艺流程天然气制甲醇工艺是以天然气为原料进行甲醇合成的工艺。
相对于合成气制甲醇,天然气制甲醇工艺更简化,生产成本更低。
1.原料处理:天然气在经过净化处理后,去除其中的硫化物、水、杂质等物质,以减少对催化剂的毒性影响。
2.反应装置:将处理好的天然气与水蒸气混合,进入反应装置,进行催化转化反应。
通常采用气相催化反应器和流化床反应器。
3.催化反应:在反应装置中,天然气与水蒸气经过区域催化剂层,发生反应生成合成气,然后经过醇化层的催化作用,生成甲醇。
4.分离和纯化:通过分离和纯化设备将反应混合物中的甲醇与其他组分进行分离纯化。
一般采用压力和温度以及蒸馏等方法进行分离。
5.精制与储存:将精制后的甲醇进行附加处理,去除其中的杂质和溶解的气体,提高甲醇的纯度。
然后将精制后的甲醇储存在储罐中,供以后使用或销售。
低压法甲醇合成工艺流程

低压法甲醇合成工艺流程
《低压法甲醇合成工艺流程》
甲醇是一种重要的工业化学品,广泛用于合成有机化合物、溶剂、燃料等。
低压法甲醇合成工艺是目前甲醇生产中最为常用的一种方法,其工艺流程简单、成本低、效率高,因此备受青睐。
该工艺流程主要分为气化反应、合成反应和提取分离三个步骤。
首先,通过对天然气、煤炭或生物质等原料进行气化处理,产生一氧化碳和氢气。
然后,将一氧化碳和氢气经过催化剂反应,生成甲醇。
最后,通过蒸馏等方法,将甲醇与副产物分离提取,得到纯净的甲醇产品。
在气化反应中,气化原料的选择和气化条件的控制直接影响到生成的一氧化碳和氢气的气化效率,进而影响到后续合成反应的产率和质量。
而在合成反应中,催化剂的选择和反应条件的控制是关键,直接影响到甲醇的产率和纯度。
因此,工艺流程中的气化和合成反应环节都需要严格控制工艺参数和提高催化剂的活性和稳定性。
除了气化反应和合成反应,提取分离过程也是非常重要的一环。
该过程需要采用适当的溶剂、蒸馏温度和操作条件,将甲醇和副产物进行有效分离,以获得高品质的甲醇产品。
总的来说,低压法甲醇合成工艺流程是一种经济实用、效率高的甲醇生产方法。
通过对气化和合成反应的优化以及提取分离
过程的精细控制,可以实现甲醇生产的高产率和优质产品的生产。
随着科学技术的不断进步,相信低压法甲醇合成工艺流程在未来会更加成熟和完善。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
D 甲醇的氯化制氯甲烷
甲醇与氯气、氢气混合,在130-150℃通过金属氯化物 作催化剂的水溶液,或在300-350℃通过沉积在硅胶单 体上的氯化锌(铜、铝)催化剂,可生成一、二、三氯甲 烷和四氯化碳 CH3OH+ Cl2+H2 CH3Cl + Cl2 CH3Cl+HCl+H2O CH2Cl2+HCl
甲醇的化学性质
A 甲醇的氧化制甲醛和甲酸
甲醇在空气中可被氧化为甲醛,进而氧化为甲酸, CH3OH+1/2O2 Ag HCHO+H2O HCHO+ 1/2O2 Ag HCOOH
B 甲醇的氨化制甲胺
CH3OH+NH3
活性氧化铝 CH NH +H O 3 2 2
2CH3OH+NH3
370-420 ℃
(CH3)2NH+2H2O
保证程度/年 41 219 80 222 33 18 43 51 45 20 161
我国GDP与物耗占世界的份额 2003年 •GDP •物耗: 钢铁 原煤 氧化铝 水泥 石油 我国占世界份额 4% 27% 31% 25% 40% 7.4%
能源消耗水平比较------1美元GDP所消耗的能源(相对值)
干气
催化裂化 原油 催化裂解
冷凝水 蒸汽
燃料油1000万吨/年
聚乙烯
乙烯 100万吨/年
其他化工产品 电能2*30万千瓦 淡水 卤水 氯碱工业 电能4*100万千瓦 精苯
LNG 海水
燃气发电 海水淡化 超临界发电
焦炉煤气
煤
焦化炉 焦炭 高炉煤气 铁矿石
25万吨
粗苯
精制
炼钢炉 炉渣
炭黑、石墨 煤焦油30万吨/年 合成 甲醇、二甲醚 精品钢1000万吨/年 超细粉 240万吨/年 水泥
常压
40atm
高压工艺流程: 在300-400℃,30MPa高温高压下合成甲醇。 一般指的是使用锌铬催化剂,自从1923年第一次用 这种方法合成甲醇成功后,差不多有50年的时间, 世界上合成甲醇生产都沿用这种方法。目前使用已 不多。 ICl低压甲醇法: 英国ICl公司在1966年研究成功,是甲醇生产工艺上 的一次重大变革。 在5MPa低压下,220-260℃,一般使用Cu基催化剂, 能耗低,是目前普遍采用的工艺。
巴西的乙醇汽油之所以广泛推广是因为那里一年四季都盛产甘蔗。美国 的使用是因为有转基因玉米且粮食过剩
吉林燃料乙醇有限责任公司
年产60万吨乙醇 日消耗玉米5000吨
乙烯代表了一个国家石油化工的水平和能力 催化裂解 石油 (50年)
乙烯、丙烯
煤 (200年)
?
气化
煤
合 成 气 成熟
铜基 催化 剂
甲 醇
CH3OH+催化剂
甲醇催化剂
催化剂的两大特点: (1)而反应前后其 物理、化学性质不变 (2) 改变了反应历程,加快反应速度
• 催化剂种类:
1) 锌-铬系Zn-Cr 分子式:xZnO· yZnCrO4· 2O zH 典型组成:ZnO,55.0±1.5%、CrO3,34.0±1.0% 2) 铜基催化剂 Cu-Zn-Al, Cu-Zn-Cr 活性组分:Cu 载体:Al2O3 特点:活性温度低,对生成甲醇的平衡有利, 选择性好,可在较低压力下使用
中压甲醇法:
是在低压法研究基础上进一步发展起来的,由于低 压法操作压力低,导致设备体积相当庞大,不利于 甲醇生产的大型化。 发展了压力为10MPa左右的甲醇合成中压法。它能 更有效地降低建厂费用和甲醇生产成本。这种流程 目前主要用于联醇工艺
2007年中国新建甲醇装置统计
公司 中海油-建滔 山东聊城鲁西化工 华鲁恒升 河南峰峰集团 内蒙古庆华集团 内蒙古博源联合化工 黑龙江宝泰隆煤化工 神华集团 重庆建滔 湖北三宁 湖北宜化 南京惠生 产能(万吨/年) 60 20 20 10 20 100 10 25 45 8.5 20 20
2007年中国新建甲醇装置统计
公司 唐山中润 河北旭阳焦化 山东明水大化 安徽临泉 陕西榆林煤化科技 山东兖矿国宏 云南云维 山西孝义 山西丰喜
产能(万吨/年) 10 14 10 15 10 50 20 10 20
2008年中国新建甲醇装置统计
希望集团 河南峰峰集团 安阳化学 内蒙古乌拉山化肥厂 山西焦化 大连大化 兰花晋城 唐山中润 山东滕州凤凰化肥公司 上海焦化公司 河南永煤集团 中原大化 河南开祥一期 陕西神木 福建富宝 四川达州钢铁集团有限公司 凯跃集团 山西大川中天 20 10 20 15 20 30 20 10 36 45 50 25 40 11 30 20 70
89.5 83.5
甲醇:
用作碳一化学的基础原料 直接添加到汽油中
甲醇价格持续走高
制取二甲醚的原料
化学溶剂
石油价 格的飙 升为推 动
以物质短缺为特征的社会发展史
资源环境能源短缺 国家安全 高新技术短缺
资金短缺 土地短缺 资本主义社会,资本家
封建社会,地主
劳动力短缺
奴隶制社会,奴隶主
矿产名称
石油 煤 天然气 铝 铜 铅 水银 镍 锡 锌 铁矿石
甲醇
CO和H2
高压
CO和H2
甲醇(300吨/年)
甲醇
铜催化剂 低压
1966英
我国甲醇工业
兰州、吉林、太原
(渣油) 高压法锌铬
50年代
60至70年代
上海吴泾化工厂
(焦炭和石脑油)
中压法铜
甲醇
山东齐鲁石化公司(渣油) 70至80年代 四川维尼纶厂(乙炔尾气) 低压法铜
90年代
上海焦化厂、 中小氮肥厂联醇
低压法铜
甲醇用途
• 甲醇作为有机化工原料,是一种大宗有机化学品, 仅次于乙烯、丙烯和苯,主要用来生产甲醛、甲 基叔丁基醚 (MTBE)、醋酸、甲酸甲酯、氯甲烷、 甲胺、硫酸二甲酯、丙烯酸甲酯和二甲醚等有机 化工产品。 • 甲醇还是一种重要的有机溶剂,可以掺入汽油或 者直接作为燃料,近年来随着甲醇汽车、二甲醚 汽车的推广,甲醇已从单一的化工原料拓展为液 体燃料,需求量成倍增长。
2008年中国新建甲醇装置统计
山西孝义 10 苏里格天然气公司 17 山东鲁西化工 25 山西原平 20 河北建滔 10 山东鲁南化肥厂 60 贵州贵化 20 旭阳焦化集团甲醇二期 10 河南延化化工有限责任公司 18 唐山中润公司二期 15 宁夏宝丰投资集团 20 山西兰花清洁能源公司 20 中煤能源 25 陕西榆林煤化科技新建 10
— 直排可达欧洲3号标准
— 单位里程耗用量与柴油相当
二甲醚与石油液化气性质比较
蒸气压 平均热 理论空 理论燃 爆炸下 燃料种类 分子量 /MPa 60 值 气量 烧温度/ ( 限/% /m3/kg ℃ ℃) /kJ/kg 二甲醚 液化气 46.0 56.6 1.35 1.92 31450 45760 3.5 1.7 6.96 11.32 2250 2055
F 甲醇的脱水制二甲醚
活性氧化铝 2CH3OH 250 ℃ CH3OCH3+H2O 二甲醚
二甲醚 - 甲醇的大宗用户
燃料二甲醚用途广 — 代替液化气作民用燃料 — 代替柴油为车用燃料 — 作为生产乙烯、丙稀原料 — 作为联合循环发电的调峰燃料 • 使用性能好 — 16烷值50-55,高于柴油,噪音低10分贝
每个催化剂都有一个活性温度,在这个温度范 围内,催化剂才能与反应物结合,发挥作用。
锌-铬系Zn-Cr: 385-420℃
Cu-Zn-Al : 240-400℃
需要对反应物加热, 到催化剂的活性温度
在常压下,即使有催化剂反应 速度仍然很慢,由于反应器过 大,而难以在工业上实现。
加压下操作!
加压下操作,实质上是增加反应物的浓度
3CH3OH+NH3 5.0-20.0MPa (CH3)3N+3H2O
甲醇的化学性质
C 甲醇的酯化制甲酯类
(1) 甲醇与甲酸反应生成甲酸甲酯 CH3OH+HCOOH HCOOCH3+H2O
(2) 甲醇与硫酸反应生成硫酸二甲酯 2CH3OH+ H2SO4 (CH3)2SO4+2H2O
(3) 甲醇与硝酸反应生成硝酸二甲酯 CH3OH+ HNO3 CH3NO3+H2O
Sr-SAPO-34催化剂活性测定
活性评价
样品
转化率
甲烷
乙烯
乙烯+丙烯
Sr-sapo34
Sr-sapo34
97.86
99.75
4.38
3.77
48.72
49.20
80.29
80.84
SAPO-34
Mobil Sr-sapo34 Mobil
99.60
-
5.26
-
45.86
67.1 49.2
78.15
CH3Cl + Cl2
CH3Cl + Cl2
CH2Cl2+HCl
CH2Cl2+HCl
甲醇的化学性质
甲醇与一氧化碳在250℃、50-70MPa下通过碘化钴均相催 E 甲醇的羰基化制醋酸
化剂,或在180℃、3-4MPa下通过铑的碳基化合物为催化
剂(以碘为助催化剂),能合成醋酸。
CH3OH+ CO
CH3COOH
二甲醚与F-T合成产物分配
二甲醚:
2CO 4H 2 CH 3 O CH 3 H 2O 二甲醚 / 水=46 / 18=2.5 / 1
•F-T合成:
20CO 41H 2 C20 H 42 20 H 2 O 粗柴油 / 水=282 / 360=0.78 /1
二甲醚作为煤基液体燃料可显著节约资源、能源。
