2018届高考化学二轮专题复习精选——电化学
2018高考化学专题突破:选择题命题——电化学 突破策略word答案版3.20

1.(2017·全国卷Ⅰ)支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。
下列有关表述不正确的是() A.通入保护电流使钢管桩表面腐蚀电流接近于零B.通电后外电路电子被强制从高硅铸铁流向钢管桩C.高硅铸铁的作用是作为损耗阳极材料和传递电流D.通入的保护电流应该根据环境条件变化进行调整解析:选C2.(2017·全国卷Ⅱ)用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为H2SO4-H2C2O4混合溶液。
下列叙述错误的是()A.待加工铝质工件为阳极B.可选用不锈钢网作为阴极C.阴极的电极反应式为Al3++3e-===AlD.硫酸根离子在电解过程中向阳极移动解析:选C3. (2016·全国卷Ⅰ)三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO2-4可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是()A.通电后中间隔室的SO2-4向正极迁移,正极区溶液pH增大B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品C.负极反应为2H2O-4e-===O2+4H+,负极区溶液pH降低D.当电路中通过1 mol电子的电量时,会有0.5 mol的O2生成解析:选B4.(2016·全国卷Ⅱ)Mg-AgCl电池是一种以海水为电解质溶液的水激活电池。
下列叙述错误的是()A.负极反应式为Mg-2e-===Mg2+B.正极反应式为Ag++e-===AgC.电池放电时Cl-由正极向负极迁移D.负极会发生副反应Mg+2H2O===Mg(OH)2+H2↑解析:选B5.(2015·全国卷Ⅰ)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。
下列有关微生物电池的说法错误的是()A.正极反应中有CO2生成B.微生物促进了反应中电子的转移C.质子通过交换膜从负极区移向正极区D.电池总反应为C6H12O6+6O26CO2+6H2O解析:选A。
高考化学二轮复习教案:专题十 电化学原理(学生版)
专题十电化学原理【命题规律】电化学内容是高考试卷中的常客,对原电池和电解池的考查往往以选择题的形式考查两电极反应式的书写、两电极附近溶液性质的变化、电子的转移或电流方向的判断等。
在第Ⅱ卷中会以应用性和综合性进行命题,如与生产生活(如金属的腐蚀和防护等)相联系,与无机推断、实验及化学计算等学科内知识综合,尤其特别注意燃料电池和新型电池的正、负极材料分析和电极反应式的书写。
题型新颖,但不偏不怪,只要注意基础知识的落实,以及能力的训练便可以从容应对。
【知识网络】【重点知识梳理】一、原电池电极的判断以及电极方程式的书写1.原电池正、负极的判断方法:(1)由组成原电池的两极材料判断。
一般是活泼的金属为负极,活泼性较弱的金属或能导电的非金属为正极。
(2)根据电流方向或电子流动方向判断。
电流由正极流向负极;电子由负极流向正极。
(3)根据原电池里电解质溶液内离子的流动方向判断。
在原电池的电解质溶液内,阳离子移向正极,阴离子移向负极。
(4)根据原电池两极发生的变化来判断。
原电池的负极失电子发生氧化反应,其正极得电子发生还原反应。
(5)电极增重或减轻。
工作后,电极质量增加,说明溶液中的阳离子在电极(正极)放电,电极活动性弱;反之,电极质量减小,说明电极金属溶解,电极为负极,活动性强。
(6)有气泡冒出。
电极上有气泡冒出,是因为发生了析出H2的电极反应,说明电极为正极,活动性弱。
2.原电池电极反应式和总反应式的书写(1)题目给定原电池的装置图,未给总反应式:①首先找出原电池的正、负极,即分别找出氧化剂和还原剂。
②结合介质判断出还原产物和氧化产物。
③写出电极反应式(注意两极得失电子数相等),将两电极反应式相加可得总反应式。
(2)题目中给出原电池的总反应式:①分析原电池总反应式中各元素的化合价变化情况,找出氧化剂及其对应的还原产物,氧化剂发生的反应即为正极反应;找出还原剂及其对应的氧化产物,还原剂参加的反应即为负极反应。
②当氧化剂、还原剂、氧化产物、还原产物由多种元素组成时,还应注意介质的反应。
2018年高考化学“电化学”知识点总结

2018年高考化学“电化学”知识点总结一、原电池:(一)概念:化学能转化为电能的装置叫做原电池。
(二)组成条件:1.两个活泼性不同的电极2.电解质溶液3.电极用导线相连并插入电解液构成闭合回路(三)电子流向:外电路:负极——导线——正极内电路:盐桥中阴离子移向负极的电解质溶液,盐桥中阳离子移向正极的电解质溶液。
(四)电极反应:以锌铜原电池为例:负极:氧化反应:Zn-2e=Zn2+(较活泼金属)正极:还原反应:2H++2e=H2↑(较不活泼金属)总反应式:Zn+2H+=Zn2++H2↑(五)正、负极的判断:1.从电极材料:一般较活泼金属为负极;或金属为负极,非金属为正极。
2.从电子的流动方向:负极流入正极3.从电流方向:正极流入负极4.根据电解质溶液内离子的移动方向:阳离子流向正极,阴离子流向负极5.根据实验现象:(1)溶解的一极为负极(2)增重或有气泡一极为正极二、化学电池(一)电池的分类:化学电池、太阳能电池、原子能电池(二)化学电池:借助于化学能直接转变为电能的装置(三)化学电池的分类:一次电池、二次电池、燃料电池1.一次电池常见一次电池:碱性锌锰电池、锌银电池、锂电池等2.二次电池(1)二次电池:放电后可以再充电使活性物质获得再生,可以多次重复使用,又叫充电电池或蓄电池。
(2)电极反应:铅蓄电池放电:负极(铅):Pb-2e- =PbSO4↓正极(氧化铅):PbO2+4H++2e- =PbSO4↓+2H2O充电:阴极:PbSO4+2H2O-2e- =PbO2+4H+阳极:PbSO4+2e- =Pb两式可以写成一个可逆反应:PbO2+Pb+2H2SO4 ⇋ 2PbSO4↓+2H2O(3)目前已开发出新型蓄电池:银锌电池、镉镍电池、氢镍电池、锂离子电池、聚合物锂离子电池3.燃料电池(1)燃料电池:是使燃料与氧化剂反应直接产生电流的一种原电池(2)电极反应:一般燃料电池发生的电化学反应的最终产物与燃烧产物相同,可根据燃烧反应写出总的电池反应,但不注明反应的条件。
高考化学大二轮复习 专题8 电化学基础

课件ppt
4错误认为电解质溶液导电的原因是电子通过了电解质溶 液,在原电池内部和电解池内部,都没有电子的流动,而是离 子的移动。实际上在闭合的电路中电子只走“陆路”导线或电 极,离子只走“水路”电解质溶液。
课件ppt
2. 电解池:
课件ppt
(1)电解时,a 极是 阴 极,电极反应式为Cu2++2e-===Cu; b 极发生氧化反应,电极反应式为 4OH--4e-===2H2O+O2↑ ; 电解总反应化学方程式为
电解 2CuSO4+2H2O=====2Cu+O2↑+2H2SO4 。
课件ppt
(2)电解完成后,若溶液的体积为 2 L,整个电解过程中共转 移 0.2 mol e-,则溶液的 pH 为 1 ,若使电解质溶液复原,需 加入 CuO 的物质的量为 0.1 mo
课件ppt
课件ppt
Z主干整合•认知盲区清
课件ppt
一、原电池和电解池 1. 原电池:
[串联拾忆]
课件ppt
(1)上述装置中能形成原电池的是 B ,该原电池工作时, 负极发生 氧化反应 ,电极反应式为 Fe-2e-===Fe2+;
正极发生 还原反应,电极反应式为2Ag++2e-===2Ag; 电池总反应式为 Fe+2Ag+===Fe2++2Ag 。
答案:A
课件ppt
电化学原理中易忽视的问题 (1)错误地根据“异性相吸”的电性理论,认为在原电池中 电解质溶液中的阳离子移向负极,阴离子移向正极。其实在原 电池工作时,阳离子移向正极,阴离子移向负极。在电解池 中,电子由电源负极流向阴极,由阳极流向电源正极。
高考电化学专题复习知识点总结完美版
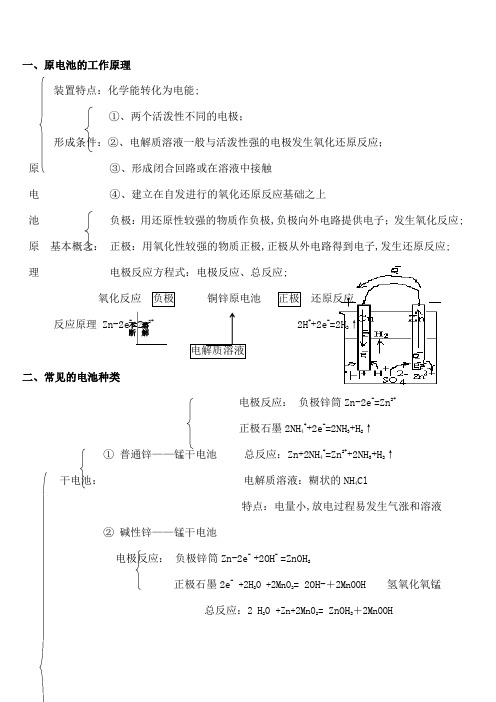
一、原电池的工作原理装置特点:化学能转化为电能;①、两个活泼性不同的电极;形成条件:②、电解质溶液一般与活泼性强的电极发生氧化还原反应;原③、形成闭合回路或在溶液中接触电④、建立在自发进行的氧化还原反应基础之上池负极:用还原性较强的物质作负极,负极向外电路提供电子;发生氧化反应; 原基本概念:正极:用氧化性较强的物质正极,正极从外电路得到电子,发生还原反应;理电极反应方程式:电极反应、总反应;氧化反应负极铜锌原电池正极还原反应反应原理 Zn-2e-=Zn2+ 2H++2e-=2H2↑电解质溶液二、常见的电池种类电极反应:负极锌筒Zn-2e-=Zn2+正极石墨2NH4++2e-=2NH3+H2↑①普通锌——锰干电池总反应:Zn+2NH4+=Zn2++2NH3+H2↑干电池:电解质溶液:糊状的NH4Cl特点:电量小,放电过程易发生气涨和溶液②碱性锌——锰干电池电极反应:负极锌筒Zn-2e- +2OH- =ZnOH2正极石墨2e-+2H2O +2MnO2= 2OH-+2MnOOH 氢氧化氧锰总反应:2 H2O+Zn+2MnO2= ZnOH2+2MnOOH溶解不断电极:负极由锌改锌粉反应面积增大,放电电流增加;使用寿命提高 电解液:由中性变为碱性离子导电性好;正极PbO 2 PbO 2+SO 42-+4H ++2e -=PbSO 4+2H 2O 负极Pb Pb+SO 42--2e -=PbSO 4总反应:PbO 2+Pb+2H SO 4 2PbSO 4+2H 2O电解液:cm 3~cm 3的H 2SO 4 溶液特点:电压稳定, 废弃电池污染环境 Ⅰ、镍——镉Ni ——Cd 可充电电池;其它 负极材料:Cd ;正极材料:涂有NiO 2,电解质:KOH 溶液NiO 2+Cd+2H 2O NiOH 2+ CdOH 2Ⅱ、银锌蓄电池正极壳填充Ag 2O 和石墨,负极盖填充锌汞合金,电解质溶液KOH;反应式为: 2Ag+ZnOH 2 ﹦ Zn+Ag 2O+H 2锂亚硫酰氯电池Li-SOCl 2:8Li+3SOCl 2 = 6LiCl+Li 2SO 3+2S锂电池 用途:质轻、高能比能量高、高工作效率、高稳定电压、工作温度宽、高使用寿命,广泛应用于军事和航空领域; ①、燃料电池与普通电池的区别不是把还原剂、氧化剂物质全部贮藏在电池内,而是工作时不断从外界输入,同时燃 料 电极反应产物不断排出电池;放电 充电放电放电` 充电 放电`充电放电`电池②、原料:除氢气和氧气外,也可以是CH4、煤气、燃料、空气、氯气等氧化剂;③、氢氧燃料电池:总反应:O2+2H2=2H2O 特点:转化率高,持续使用,无污染;2.氢氧燃料电池反应汇总:介质电池反应2H2 +O2= 2H2O酸性负极 2H2- 4e- = 4H+正极O2 + 4H+ + 4e-= 4H2O中性负极 2H2- 4e- = 4H+正极O2 + 2H2O + 4e-= 4OH-碱性负极2H2 +4OH-- 4e- = 4H2O正极O2 + 2H2O + 4e-= 4OH-3.固体氢氧燃料电池:固体电解质介质电池反应: 2H2 +O2= 2H2O负极2H2 - 4e- +2O2-= 2H2O正极O2+ 4e-= 2O2-负极 2H2- 4e- = 4H+正极O2 + 4H+ + 4e-= 2H2O4.甲烷新型燃料电池以两根金属铂片插入KOH溶液中作电极,又在两极上分别通入甲烷和氧气;电极反应为:负极:CH4+ 10OH --8e-= CO32- + 7H2O正极:2O2+ 4H2O +8e-= 8OH -电池总反应:CH 4+ 2O 2 + 2KOH = K 2CO 3 + 3 H 2O分析溶液的pH 变化;C 4H 10、空气燃料电池、电解质为熔融K 2CO 3, 用稀土金属材料作电极具有催化作用负极:2C 4H 10 -52e- + 26CO32-- = 34 CO 2+ 10H 2O 正极:13O 2 +52e- + 26CO 2 =26CO3 2-电池总反应:2C 4H 10+ 13O 2 = 8CO 2 + 10 H 2O 5.铝——空气燃料电池海水: 负极:4Al -12e- = 4Al 3+ 正极:3O 2 +12e- + 6H 2O =12OH - 电池总反应:4Al +3O 2 +6H 2O = 4AlOH 3 三、原电池的主要应用:1.利用原电池原理设计新型化学电池;2.改变化学反应速率,如实验室用粗锌与硫酸反应制取氢气;3.进行金属活动性强弱比较;4.电化学保护法,即将金属作为原电池的正极而受到保护;如在铁器表面镀锌;5.解释某些化学现象 四、金属的腐蚀与防护腐蚀概念:金属或合金与周围接触到的气体或液体进行化学反应而腐蚀损耗的过程;概述: 腐蚀危害:腐蚀的本质:M-ne -→M n+氧化反应分类:化学腐蚀金属与接触到的物质直接发生化学反应而引起的腐蚀、电化腐蚀电化学腐蚀定义:因发生原电池反应,而使金属腐蚀的形式; 负极Fe :Fe-2e -=Fe 2+; 吸氧腐蚀: 正极C :O 2+2H 2O+4e -=4OH - 总反应:2Fe+O 2+2H 2O=FeOH 2后继反应:4FeOH 2 +O 2 +2H 2O =4FeOH 3钢铁的腐蚀 2FeOH 3====Fe 2O 3 +3H 2O负极Fe :Fe-2e -=Fe 2+;析氢腐蚀: 正极C :2H ++2e -=H 2↑总反应: Fe+2H +=Fe 2++H 2↑影响腐蚀的因素:金属本性、介质;金属的防护: ①、改变金属的内部组织结构;保护方法: ②、在金属表面覆盖保护层;③、电化学保护法牺牲阳极的阴极保护法电解池原理 一、 电解池基础定义:使电流通过电解质溶液而在阴阳两极引起氧化还原反应的过程; 装置特点:电能转化为化学能;①、与电源本连的两个电极;形成条件 ②、电解质溶液或熔化的电解质③、形成闭合回路;金属的腐蚀与防护电极 阳极:与直流电源正极相连的叫阳极;概念 阴极:与直流电源负极相连的叫阴极;电极反应:原理:谁还原性或氧化性强谁先放电发生氧化还原反应离子放电顺序: 阳极:阴离子还原性 S 2->I ->Br ->Cl ->OH ->SO 42-含氧酸根>F -阴极:阳离子氧化性 Ag +>Fe 3+>Cu 2+>Pb 2+>Sn 2+>Fe 2+>Zn 2+>H +>Al 3+>Mg 2+>Na +电子流向 e - e-氧化反应 阳极 阴极 还原反应反应原理:4OH --4e -=2H 2O +O 2 Cu 2++2e -=Cu 电解质溶液电解结果:在两极上有新物质生成;总反应:2CuSO 4+ 2H 2O= 2Cu+2H 2SO 4+O 2↑ 二、 电解池原理粗铜板作阳极,与直流电源正极相连; ①、装置 纯铜作阴极,与直流电源负极相连;用CuSO 4 加一定量H 2SO 4作电解液; 阴极:Cu 2++2e -=Cu电解精炼铜 阳极:Cu-2e -=Cu 2+、Zn-2e -=Zn 2+②、原理: Ni-2e -=Ni 2+阳极泥:含Ag 、Au 等贵重金属; 电解液:溶液中CuSO 4浓度基本不变③、电解铜的特点:纯度高、导电性好;移向阴离子移向 阳离子电解池原理①、概念:利用电解原理在某些金属的表面镀上一薄层其它金属或合金的过程;②、方法:镀层金属与电源正极相连作阳极; 将待镀金属与电源负极相连作阴极;电镀: 用含镀层金属离子的电解质溶液配成电镀液;③、原理:阳极 Cu-2e -=Cu 2+ ;Cu 2++2e -=Cu ④、装置 如图⑤、电镀工业:镀件预处理→电镀液添加剂→装置:现象 ①、阴极上有气泡;②、阳极有刺激性气体产,能使湿润的淀粉KI 变蓝;电解食盐水 ③、阴极区附近溶液变红,有碱生成通电前: NaCl =Na ++Cl - H 2O H ++OH -原理 阴极Fe:Na +,H +移向阴极;2H ++2e -=H 2↑还原反应 通电后: 阳极C :Cl -、OH -移向阳极;2Cl --2e -=Cl 2↑氧化反应总反应:2NaCl +2H 2O 2NaOH +Cl 2↑+H 2↑阳极、阴极、离子交换膜、电解槽、导电铜棒等 ①、组成:阳极:金属钛网涂有钌氧化物;阴极:碳钢网涂有Ni 涂层阳离子交换膜:只允许阳离子通过,阻止阴离子和空气通过;电解的应氯碱工业 电解离子交换膜法制烧碱②、装置:食盐 湿氯气 氯气 ③生成流程: 淡盐水 氢气 NaOH 溶液 → NaOH 固体精制食盐水 + — 纯水含少量NaOH 粗盐水含泥沙、Cu 2+、Mg 2+、Ba 2+、SO 42-等阳离子交换树脂:除Cu 2+、Mg 2+等 加BaCl 2,Ba 2++SO 42-=BaSO 4↓④、粗盐水精制: 加Na 2CO 3:Ca 2++CO 32-=CaCO 3↓;Ba 2++CO 32-=BaCO 3↓加NaOH :Mg 2++2OH -=MgOH 2↓;Fe 3++3OH -=FeOH 3↓三、电解实例及规律电解液 溶质类别 电解总反应式相当于电解溶液pH NaOH 溶液 强碱 2H 2O电解2H 2↑+O 2↑水升高 H 2SO 4溶液 含氧酸 降低 Na 2SO 4溶液 活泼金属的含氧酸盐 不 变 两极混合液 CuCl 2溶液 不活泼金属的无氧酸盐 CuCl 2 电解Cu+Cl 2↑ 电解质本身接近7HCl 溶液无氧酸2HCl电解H 2↑+Cl 2↑升高NaCl 溶液 活泼金属的无氧酸盐2NaCl+2H 2O 电解H 2+2NaOH+Cl 2↑ om电解质与水升高。
高考化学专项练复习《电化学》含答案

高考化学专项练复习《电化学》含答案一、选择题(本题共20小题,每题只有一个选项符合题意)1.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。
下列分析正确的是A .脱氧过程是吸热反应,可降低温度,延长糕点保质期B .脱氧过程中铁作原电池正极,电极反应为:Fe -3e -=Fe 3+C .脱氧过程中碳作原电池负极,电极反应为:2H 2O+O 2+4e -=4OH -D .含有1.12g 铁粉的脱氧剂,理论上最多能吸收氧气0.015mol【答案】D【解析】A .脱氧过程是放热反应,可吸收氧气,延长糕点保质期,A 不正确;B .脱氧过程中铁作原电池负极,电极反应为Fe -2e -=Fe 2+,B 不正确;C .脱氧过程中碳作原电池正极,电极反应为2H 2O+O 2+4e -=4OH -,C 不正确;D .含有1.12g 铁粉的脱氧剂,铁的物质的量为0.02mol ,其最终被氧化为氢氧化铁,电子转移总量为0.06mol ,理论上最多能吸收氧气0.015mol ,D 正确。
故选D 。
2.“自煮火锅”发热包的成分为碳酸钠、硅藻土、铁粉、铝粉、活性炭、焦炭粉、NaCl 、生石灰,向发热包中加入冷水,可用来蒸煮食物。
下列说法错误的是 A .活性炭作正极,正极上发生还原反应B .负极反应为--22Al-3e +4OH =AlO +2H O -C .Na +由活性炭区向铝粉表面区迁移D .硅藻土结构疏松,使各物质分散并均匀混合,充分接触【答案】C【解析】发热包发热过程中有微小原电池形成,如铝粉和活性炭在水溶液中,活性炭作正极,O 2得到电子发生还原反应,电极反应式为:O 2+2H 2O+4e -=4OH -,铝粉作负极,失去电子发生氧化反应,电极反应式为:--22Al-3e +4OH =AlO +2H O -。
A .根据分析,活性炭作正极,O 2得到电子发生还原反应,A 正确;B .若铝粉作负极,失去电子发生氧化反应,电极反应式为:--22Al-3e +4OH =AlO +2H O -,B 正确;C .活性炭作正极,铝粉作负极,原电池中阳离子向正极移动,即Na +向活性炭区迁移,C 错误;D .硅藻土结构疏松,可以使各物质分散并均匀混合,充分接触,D正确;答案选C。
高中化学《电化学二轮专题复习》优质课教学设计、教案

D.a 电极的反应为 3CO2+18H+-18e-===C3H8O+5H2O 规律总结 1:
【我会做】1、某电池以 K2FeO4 和Zn 为电极材料,KOH 溶液为电解质溶液。下列说法正确的是(
Reference source not found 混合溶液。下列叙述错误的是( )
A.待加工铝质工件为阳极
B.可选用不锈钢网作为阴极
C.阴极的电极反应式为:Error: Reference
source not found D.硫酸根离子在电解过程
中向阳极移动
★4、(2015·江苏)一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( ) A. 反应 CH4+H2O=====3H2+CO,每消耗 1 mol CH4 转移 12 mol 电
B.氢燃料电池
C.铅蓄电池
D.镍镉电池
2. 烧杯 A 中盛入 0.1mol·L-1 的 H2SO4 溶液,烧杯 B 中盛放 0.1mol·L-1 的 CuCl2 溶液(两种溶液均 足量),装置如图所示,下列说法不正确的是( )
A.A 中 Fe 极质量减少,C 极有气体产生 B.A 为电解池,B 为原电池 C. 当 A 烧杯中产生 0.1mol 气体时,B 烧杯中产生气体的物质的量也为 0.1mol D. 经过一段时间,B 烧杯中溶液的 pH 增大 3、用电解氧化法可以在铝制品表面形成致密、 耐腐蚀的氧化膜,电解质溶液一般为 Error:
授课教师: 课型: 专题复习 教学目标:
班级: 高三 二班 课题: 电化学专题复习
1. 了解原电池、电解池和二次电池的工作原理。
高考化学二轮复习教案:专题十 电化学原理(教师版)
【命题规律】电化学内容是高考试卷中的常客,对原电池和电解池的考查往往以选择题的形式考查两电极反应式的书写、两电极附近溶液性质的变化、电子的转移或电流方向的判断等。
在第Ⅱ卷中会以应用性和综合性进行命题,如与生产生活(如金属的腐蚀和防护等)相联系,与无机推断、实验及化学计算等学科内知识综合,尤其特别注意燃料电池和新型电池的正、负极材料分析和电极反应式的书写。
题型新颖,但不偏不怪,只要注意基础知识的落实,以及能力的训练便可以从容应对。
【知识网络】【重点知识梳理】一、原电池电极的判断以及电极方程式的书写1.原电池正、负极的判断方法:(1)由组成原电池的两极材料判断。
一般是活泼的金属为负极,活泼性较弱的金属或能导电的非金属为正极。
(2)根据电流方向或电子流动方向判断。
电流由正极流向负极;电子由负极流向正极。
(3)根据原电池里电解质溶液内离子的流动方向判断。
在原电池的电解质溶液内,阳离子移向正极,阴离子移向负极。
(4)根据原电池两极发生的变化来判断。
原电池的负极失电子发生氧化反应,其正极得电子发生还原反应。
(5)电极增重或减轻。
工作后,电极质量增加,说明溶液中的阳离子在电极(正极)放电,电极活动性弱;反之,电极质量减小,说明电极金属溶解,电极为负极,活动性强。
(6)有气泡冒出。
电极上有气泡冒出,是因为发生了析出H2的电极反应,说明电极为正极,活动性弱。
2.原电池电极反应式和总反应式的书写(1)题目给定原电池的装置图,未给总反应式:①首先找出原电池的正、负极,即分别找出氧化剂和还原剂。
②结合介质判断出还原产物和氧化产物。
③写出电极反应式(注意两极得失电子数相等),将两电极反应式相加可得总反应式。
(2)题目中给出原电池的总反应式:①分析原电池总反应式中各元素的化合价变化情况,找出氧化剂及其对应的还原产物,氧化剂发生的反应即为正极反应;找出还原剂及其对应的氧化产物,还原剂参加的反应即为负极反应。
②当氧化剂、还原剂、氧化产物、还原产物由多种元素组成时,还应注意介质的反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电化学(2)[典例1](2017·全国卷Ⅲ)全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为16Li+x S8===8Li2S x(2≤x≤8)。
下列说法错误的是()A.电池工作时,正极可发生反应:2Li2S6+2Li++2e-===3Li2S4B.电池工作时,外电路中流过mol电子,负极材料减重0.14 gC.石墨烯的作用主要是提高电极a的导电性D.电池充电时间越长,电池中Li2S2的量越多[解析]原电池工作时,正极发生一系列得电子的还原反应,即:Li2S8→Li2S6→Li2S4→Li2S2,其中可能有2Li2S6+2Li++2e-===3Li2S4,A项正确;该电池工作时,每转移mol电子,负极有mol Li(质量为0.14 g)被氧化为Li+,则负极质量减少0.14 g,B项正确;石墨烯能导电,利用石墨烯作电极,可提高电极a的导电性,C项正确;充电过程中,Li2S2的量逐渐减少,当电池充满电时,相当于达到平衡状态,电池中Li2S2的量趋于不变,故不是电池充电时间越长,电池中Li2S2的量越多,D项错误。
[答案] D[针对训练]1.世界某着名学术刊物近期介绍了一种新型中温全瓷铁-空气电池,其结构如图所示。
下列有关该电池放电时的说法正确的是()A.a极发生氧化反应B.正极的电极反应式为FeO x+2x e-===Fe+x O2-C.若有22.4 L(标准状况)空气参与反应,则电路中有4 mol电子转移D.铁表面发生的反应为x H2O(g)+Fe===FeO x+x H2解析:选D a极通入空气,O2在该电极发生得电子的还原反应,A错误;O2在正极发生反应,电极反应式为O2+4e-===2O2-,B错误;由B项分析可知,电路中有4 mol电子转移时正极上消耗1 mol O2,在标准状况下的体积为22.4 L,则通入空气的体积约为22.4 L×5=112 L,C错误;由图可知,铁表面H2O(g)参与反应生成H2,则发生的反应为x H2O(g)+Fe===FeO x+x H2,D正确。
题型二带离子交换膜的化学电源[典例2]液体燃料电池相比于气体燃料电池具有体积小等优点。
一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。
下列关于该电池的叙述正确的是() A.b电极上发生氧化反应B.a电极反应式:N2H4+4OH--4e-===N2↑+4H2OC.放电时,电流从a电极经过负载流向b电极D.其中的离子交换膜需选用阳离子交换膜[解析]A项,b电极上发生还原反应,错误;C项,放电时,电子从a电极经过负载流向b电极,错误;D项,其中的离子交换膜需选用阴离子交换膜,错误。
[答案] B[题后悟道][2.用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。
其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是()A.X为直流电源的负极,Y为直流电源的正极B.阳极区pH增大C.图中的b>aD.该过程中的产品主要为H2SO4和H2解析:选B A项,由图示可知Pt(Ⅰ)极上H+→H2,发生还原反应,故Pt(Ⅰ)为阴极,X为直流电源的负极,Y为直流电源的正极,正确;B项,Pt(Ⅱ)为阳极,在阳极,SO2-3、HSO-3被氧化为H2SO4,SO2-3+H2O-2e-===2H++SO2-4,HSO-3+H2O-2e-===3H++SO2-4,溶液的酸性增强,pH减小,错误;C项,由上面的分析可知,阳极有H2SO4生成,故b>a,正确;D项,阳极产物为H2SO4,阴极产物为H2,正确。
题型三可逆电池[典例3](2016·全国卷Ⅲ)锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH-+2H2O===2Zn(OH)2-4。
下列说法正确的是()A.充电时,电解质溶液中K+向阳极移动B.充电时,电解质溶液中c(OH-)逐渐减小C.放电时,负极反应为Zn+4OH--2e-===Zn(OH)2-4D.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况)[解析]A项,充电时装置为电解池,溶液中的阳离子向阴极移动。
B项,充电时的总反应为放电时的逆反应:2Zn(OH)2-4===2Zn+O2+4OH-+2H2O,c(OH-)逐渐增大。
C项,放电时负极失电子发生氧化反应,由放电时的总反应可知,负极反应式为Zn+4OH--2e-===Zn(OH)2-4。
D项,由放电时的总反应可知,电路中通过2 mol电子时,消耗mol O2,其体积为11.2 L(标准状况)。
[答案] C[题后悟道]有关可逆电池的解题思路[3.(2016·四川高考)某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为Li1CoO2+Li x C6===LiCoO2+C6(x<1)。
下列关于该电池的说法不-x正确的是()A.放电时,Li+在电解质中由负极向正极迁移B.放电时,负极的电极反应式为Li x C6-x e-===x Li++C6C.充电时,若转移1 mol e-,石墨(C6)电极将增重7x gD.充电时,阳极的电极反应式为LiCoO2-x e-===Li1-x CoO2+x Li+解析:选C A.原电池中阳离子由负极向正极迁移,正确;B.放电时,负极发生氧化反应,电极反应式为Li x C6-x e-===x Li++C6,正确;C.充电时,若转移1 mol电子,石墨电极质量将增重7 g,错误;D.充电时阳极发生氧化反应,电极反应式为LiCoO2-x e-===Li1-x CoO2+x Li+,正确。
题型四电解原理在环保、新材料制备中的应用[典例4](2015·四川高考)用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是()A.用石墨作阳极,铁作阴极B.阳极的电极反应式:Cl-+2OH--2e-===ClO-+H2OC.阴极的电极反应式:2H2O+2e-===H2↑+2OH-D.除去CN-的反应:2CN-+5ClO-+2H+===N2↑+2CO2↑+5Cl-+H2O [解析]A项,若铁作阳极,则铁失电子生成Fe2+,则CN-无法除去,故铁只能作阴极,正确;B项,阳极Cl-放电生成ClO-,Cl的化合价升高,故在阳极发生氧化反应,又已知该溶液呈碱性,正确;C项,阳离子在电解池的阴极得电子发生还原反应,在碱性条件下,H2O提供阳离子(H+),正确;D项,由于溶液是碱性条件,故除去CN-发生的反应为2CN-+5ClO-+H2O===N2↑+2CO2↑+5Cl-+2OH-,错误。
[答案] D[针对训练]4.(2017·广州模拟)用电化学法制备LiOH的实验装置如图,采用惰性电极,a口导入LiCl溶液,b口导入LiOH溶液,下列叙述正确的是() A.通电后阳极区溶液pH增大B.阴极区的电极反应式为4OH--4e-===O2↑+2H2OC.当电路中通过1 mol电子的电量时,会有mol的Cl2生成D.通电后Li+通过交换膜向阴极区迁移,LiOH浓溶液从d口导出解析:选D A项,左端为阳极,Cl-放电生成Cl2,Cl2溶于水,生成酸,pH减小,错误;B项,右端是阴极区得到电子,电极反应式为2H2O+2e-===2OH -+H2↑,错误;C项,2Cl--2e-===Cl2,通过1 mol电子,得到mol Cl2,错误;D项,根据电解原理,阳离子通过阳离子交换膜,从阳极区向阴极区移动,LiOH浓溶液从d口导出,正确。
题型五新环境下金属的腐蚀与防护[典例5](2015·上海高考)研究电化学腐蚀及防护的装置如图所示。
下列有关说法错误的是()A.d为石墨,铁片腐蚀加快B.d为石墨,石墨上电极反应为O2+2H2O+4e-―→4OH-C.d为锌块,铁片不易被腐蚀D.d为锌块,铁片上电极反应为2H++2e-―→H2↑[解析]A.由于活动性:Fe>石墨,所以铁、石墨及海水构成原电池,Fe 为负极,失去电子被氧化变为Fe2+进入溶液,溶解在海水中的氧气在正极石墨上得到电子被还原,比没有形成原电池时的速率快,正确。
为石墨,由于是中性电解质,所以发生的是吸氧腐蚀,石墨上氧气得到电子,发生还原反应,电极反应为O2+2H2O+4e-―→4OH-,正确。
C.若d为锌块,则由于金属活动性:Zn>Fe,Zn为原电池的负极,Fe为正极,首先被腐蚀的是Zn,铁得到保护,铁片不易被腐蚀,正确。
为锌块,由于电解质为中性环境,发生的是吸氧腐蚀,在铁片上电极反应为O2+2H2O+4e-―→4OH-,错误。
[答案] D[针对训练]5.城市地下潮湿的土壤中常埋有纵横交错的管道和输电线路,当有电流泄漏并与金属管道形成回路时,就会引起金属管道的腐蚀。
原理如图所示,但若电压等条件适宜,钢铁管道也可能减缓腐蚀,此现象被称为“阳极保护”。
下列有关说法不正确的是()A.该装置能够将电能转化为化学能B.管道右端腐蚀比左端快,右端电极反应式为Fe-2e-===Fe2+C.如果没有外加电源,潮湿的土壤中的钢铁管道比较容易发生吸氧腐蚀D.钢铁“阳极保护”的实质是在阳极金属表面形成一层耐腐蚀的钝化膜解析:选B A项,该装置相当于电解池,能将电能转化为化学能,正确;B项,左端是阳极,腐蚀得更快,错误;C项,如果没有外加电源,潮湿的土壤(接近中性)中的钢铁管道发生原电池反应,所以发生的是吸氧腐蚀,正确;D项,根据题意,此种腐蚀较慢,所以“阳极保护”实际上是在金属表面形成了一层致密的保护膜,正确。
[课堂练——练熟方法]1.MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。
已知该电池的总反应为2H2+O2===2H2O,下列有关该电池的说法正确的是()A.该电池的正极反应式为4OH-+4e-===O2↑+2H2OB.该电池的负极反应式为H2-2e-===2H+C.放电时OH-向负极移动D.当生成1 mol H2O时,转移2 mol电子解析:选D该燃料电池的燃料为H2,电解质为熔融的K2CO3,总反应为2H2+O2===2H2O,负极反应式为2H2+2CO2-3-4e-===2H2O+2CO2,正极反应式为O2+2CO2+4e-===2CO2-3,故A、B均错误;电解质中移动的阴离子为CO2-3,不是OH-,故C错误;根据负极反应式知,生成1 mol H2O时转移2 mol 电子,故D正确。
