高中化学选修5葡萄糖的结构和性质
葡萄糖的性质

化师二班黄小雪2221
“葡萄糖得性质”教学设计
一、教材分析
“葡萄糖”就是人教版高中化学教材选修5第4章第2节糖类得重要内容,在必修2中已经认识了糖类,也知道葡萄糖得特征反应,但未从结构角度与性质角度来认识葡萄糖。
教材中将糖类安排在烃类衍生物学习之后,教材已对官能团性质做了详细得介绍,葡萄糖作为多个官能团构成得复合物质,官能团相互影响,需让学生理解。
二、学情分析
本节课针对高一下学期学生,此时学生对糖类已有了初步理解,学习了葡萄糖得特征反应可用于葡萄糖得检验;此时学生已经学习了烃得衍生物,对官能团有了较好得掌握。
但学生对葡萄糖得性质与结构并不了解,这也就是本次课得重点教学内容。
三、教学目标
1、知识与技能:
(1)掌握葡萄糖得物化性质,尤其就是葡萄糖得还原性;
(2)通过对葡萄糖性质得学习,了解关于人体健康得一些知识,增强利用化学知识解决日常生活实际问题得能力。
2、过程与方法:
(1)学习从已有得生活经验出发,归纳总结出葡萄糖得物理性质;
(2)通过实验验证以及结合已学知识得类比,来推理出葡萄糖得化学性质。
3、情感态度与价值观:
葡萄糖应用于生活,以生活中材料入手,让学生明白化学源于生活,服务与生活得真理,提升对化学得认识。
四、教学重难点
葡萄糖还原性得讲解
五、教学方法
讲授法、合作探究法
六、教学过程
1、教学准备
教具准备:10%葡萄糖溶液、2%AgNO3溶液、2%氨水、10%NaOH溶液、2%CuSO4溶液、热水、中试管、烧杯
2、教学环节
七、板书设计。
选修五,第四章第二节第一课时 单糖 二糖

[答案] D
针对训练1
下列叙述正确的是(
)
A.糖类也叫碳水化合物 B.符合Cn(H2O)m通式的物质均可称为碳水化合物 C.由于糖的分子式可以用通式Cn(H2O)m来表示,所 以在它们的分子中H和O的原子数比一定等于2:1 D.橡胶、电木、葡萄糖都是高分子化合物
答案:A
葡萄糖的结构与性质
[典例2] 分别取1 mol葡萄糖进行下列实验: (1)银镜反应时,需银氨络离子________mol,反应后 葡萄糖变为________,其结构简式是________________。 (2)与乙酸反应生成酯,从理论上讲完全酯化需要 ________g乙酸。 (3)若使之完全转化为CO2和H2O,所需氧气的体积在 标准状况下为________L,反应的方程式是___________。
(1)其原因是(
)
A.蔗糖尚未水解 B.加热时间不够 C.煮沸后的溶液中没有加碱中和作催化剂的酸 D.蔗糖水解的产物中没有葡萄糖 (2)正确的操作是________。
答案:(1)C (2)待煮沸后的溶液冷却后加入适量的 NaOH 溶液至溶 液呈现碱性,再加入新配制的银氨溶液,水浴加热
互为同分异构体
规律技巧
一、葡萄糖和果糖的比较
二、葡萄糖 1.组成和结构
2.物理性质 葡萄糖为无色晶体,熔点为146℃,有甜味,但甜度 不如蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。 3.化学性质 (1)葡萄糖分子中的官能团及反应类型
(2)氧化反应 ①与银氨溶液反应: △ CH2OH(CHOH)4CHO+2Ag(NH3)2OH――→ CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O。 ②与新制的Cu(OH)2反应: △ CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH――→ CH2OH(CHOH)4COONa+Cu2O↓+3H2O。
高中化学选修5:有机化学基础知识点大全

有机化学知识点归纳(一)一、有机物的结构与性质1、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无;通式:CnH2n+2;代表物:CH4B) 结构特点:键角为109°28′,空间正四面体分子。
烷烃分子中的每个C原子的四个价键也都如此。
C) 化学性质:(2)烯烃:A) 官能团:;通式:CnH2n(n≥2);代表物:H2C=CH2B) 结构特点:键角为120°。
双键碳原子与其所连接的四个原子共平面。
C) 化学性质:(3)炔烃:A) 官能团:—C≡C—;通式:CnH2n—2(n≥2);代表物:HC≡CHB) 结构特点:碳碳叁键与单键间的键角为180°。
两个叁键碳原子与其所连接的两个原子在同一条直线上。
(4)苯及苯的同系物:A) 通式:CnH2n—6(n≥6);代表物:B)结构特点:苯分子中键角为120°,平面正六边形结构,6个C原子和6个H原子共平面。
C)化学性质:①取代反应(与液溴、HNO3、H2SO4等)(5)醇类:A) 官能团:—OH(醇羟基);代表物:CH3CH2OH、HOCH2CH2OHB) 结构特点:羟基取代链烃分子(或脂环烃分子、苯环侧链上)的氢原子而得到的产物。
结构与相应的烃类似。
C) 化学性质:(与官能团直接相连的碳原子称为α碳原子,与α碳原子相邻的碳原子称为β碳原子,依次类推。
与α碳原子、β碳原子、……相连的氢原子分别称为α氢原子、β氢原子、……)④酯化反应(跟羧酸或含氧无机酸)(6)醛酮B) 结构特点:醛基或羰基碳原子伸出的各键所成键角为120°,该碳原子跟其相连接的各原子在同一平面上。
C) 化学性质:(7)羧酸3、常见糖类、蛋白质和油脂的结构和性质(1)单糖A) 代表物:葡萄糖、果糖(C6H12O6)B) 结构特点:葡萄糖为多羟基醛、果糖为多羟基酮C) 化学性质:①葡萄糖类似醛类,能发生银镜反应、费林反应等;②具有多元醇的化学性质。
探究葡萄糖的结构和性质

再思考:葡萄糖中含氧元素吗?怎么验证? 再思考:葡萄糖中含氧元素吗?怎么验证?
设计实验: 设计实验:葡萄糖和镁粉反应
有氢气产生 含氧元素
提示: 提示: 活泼金属置换出有机物中羟基氢中的氢。 羟基氢中的氢 活泼金属置换出有机物中羟基氢中的氢。 结论:葡萄糖由C 结论:葡萄糖由C、H、O三种元素组成。 三种元素组成。
新课标人教版高中化学选修5
探究葡萄糖的结构和性质
合肥一中 化学教研组 张春
思考与交流
生活处处有化学,葡萄糖是生活中 一种非常重要的有机物。你能列举一些 和葡萄糖有关的物质吗?
生活中的关于葡萄糖的物质——供能 供能 生活中的关于葡萄糖的物质
生活中的关于葡萄糖的物质——补剂 补剂 生活中的关于葡萄糖的物质
4.葡萄糖是单糖的主要原因是
(B )
A.在糖类物质中含碳原子最少 A.在糖类物质中含碳原子最少 B.不能水解成更简单的糖 B.不能水解成更简单的糖 C.分子中有一个醛基 C.分子中有一个醛基 D.分子结构最简单 D.分子结构最简单
半缩醛式葡萄糖
本节小结
1、本节课通过实验探究的方法,一步 本节课通过实验探究的方法, 一步的推导出了葡萄糖的分子组成和结 构特征。 构特征。再由结构推测出葡萄糖的化学 性质, 体现了实验化学的学科特点。 性质, 体现了实验化学的学科特点。 2、由葡萄糖和果糖的结构特征,归纳 由葡萄糖和果糖的结构特征, 出糖类的特征定义, 出糖类的特征定义,学会糖类的分类方 法。
单糖、低聚糖、多糖 单糖、低聚糖、
2、按照分子中所含碳原子数的多少
如:单糖中碳原子数分:丙糖、丁糖、戊糖、己糖……
葡萄糖的化学式结构式

葡萄糖的化学式结构式葡萄糖的化学式结构式为C6H12O6。
葡萄糖是一种简单的单糖,也是人体能量的重要来源之一。
它在自然界中广泛存在于水果、蔬菜和甘蔗等植物中。
葡萄糖的化学式结构式C6H12O6中,C代表碳,H代表氢,O代表氧。
葡萄糖分子由6个碳原子、12个氢原子和6个氧原子组成。
这些原子通过共价键连接在一起,形成了一个稳定的分子结构。
葡萄糖是一种六元醇,具有六个羟基(-OH)官能团。
这些羟基团使葡萄糖具有许多重要的化学性质和生物活性。
葡萄糖是一种可溶于水的白色结晶固体,在水中具有良好的溶解度。
它的溶液呈甜味,是一种天然甜味剂。
葡萄糖在生物体内起着重要的能量供应作用。
当人体消化和代谢食物时,葡萄糖被分解为能量,并供给给身体各个组织和细胞使用。
葡萄糖还是合成各种生物分子的原料,如蛋白质、核酸和脂肪等。
除了在人体内发挥重要作用外,葡萄糖还广泛应用于食品工业和医药工业。
在食品工业中,葡萄糖被用作甜味剂、防腐剂和增稠剂等。
在医药工业中,葡萄糖被用作药物的原料和辅料,如葡萄糖注射液和葡萄糖片剂等。
葡萄糖还可以通过化学反应转化为其他有用的化合物。
例如,葡萄糖可以通过酵母发酵产生乙醇,用于酿造酒精饮料。
此外,葡萄糖还可以通过氧化反应转化为葡萄糖酸,用于制造柠檬酸和其他有机酸。
葡萄糖的化学结构和性质使其在生命科学和工业领域中具有广泛的应用前景。
科学家们不断研究葡萄糖的性质和应用,以开发新的生物技术和医药产品。
葡萄糖的研究和应用有助于人们更好地理解生命的奥秘,促进人类的健康和发展。
总结起来,葡萄糖是一种重要的单糖,具有丰富的化学结构和生物活性。
它在人体内起着能量供应和生物合成的重要作用,同时在食品工业和医药工业中也有广泛的应用。
通过研究和应用葡萄糖,我们可以更好地探索生命的奥秘,为人类的健康和发展做出贡献。
高二化学苏教版选修5专题5第一单元糖类油脂学案含解析

互动课堂疏导引导一、糖类概念1。
糖类指多羟基醛或多羟基酮以及水解生成它们的物质.2。
分类糖类按水解状况进行分类:单糖、低聚糖和多糖。
低聚糖和多糖在一定条件下可以水解生成单糖.单糖一般就是多羟基醛或多羟基酮,不能进一步水解。
按照分子中含碳原子数的多少,单糖可以分为丙糖、丁糖、戊糖(如核糖、脱氧核糖)和己糖(如葡萄糖、半乳糖、果糖)等。
按照与羰基连接的原子或原子团的情况不同,单糖又可以分为醛糖和酮糖,最简单的醛糖是甘油醛.二、常见的单糖及性质1.分子式为C6H12O6的单糖葡萄糖属于己醛糖,其结构简式为CH2OH—(CHOH)4—CHO;果糖属于己酮糖,其结构简式为CH2OH—(CHOH)3—CO—CH2OH。
互为同分异构体,结构式分别为:2。
葡萄糖的化学性质(1)银镜反应:CH 2OH(CHOH)4CHO+2[Ag(NH3)2]OH CH2OH (CHOH)4COONH4+3NH3↑+2Ag↓+H2O。
(2)与新制Cu(OH)2悬浊液反应:CH2OH(CHOH)4CHO+2Cu (OH)2△CH2OH(CHOH)4COOH+Cu2O↓+2H2O。
知识总结①Cu(OH)2悬浊液必须新制,制备时NaOH要过量.②实验中用酒精灯加热到沸腾,但温度不能太高,否则Cu(OH)2分解为CuO。
③该反应可用于检验醛基的存在。
④医疗上用于检查糖尿病。
(3)加成反应:CH2OH(CHOH)4CHO+H2CH2OH(CHOH)4CH2OH己六醇(4)生理氧化反应:C6H12O6(s)+6O2(g)6CO2(g)+6H2O(l)葡萄糖ΔH=—2 804 kJ·mol—1(5)酯化反应:5H2O(6)发酵成酒精C6H12O6催化剂2C2H5OH+2CO2↑知识总结葡萄糖分子中含有一个和5个—OH,兼有醛基和羟基的性质。
发生在—CHO上的反应:发生在—OH上的反应:三、常见的二糖及性质1.低聚糖通常把由不到20个单糖缩合形成的糖类化合物称为低聚糖,彻底水解后将得到单糖。
人教版高中化学选修5 第四章第二节 糖类--葡萄糖果糖麦芽糖蔗糖的结构和转化
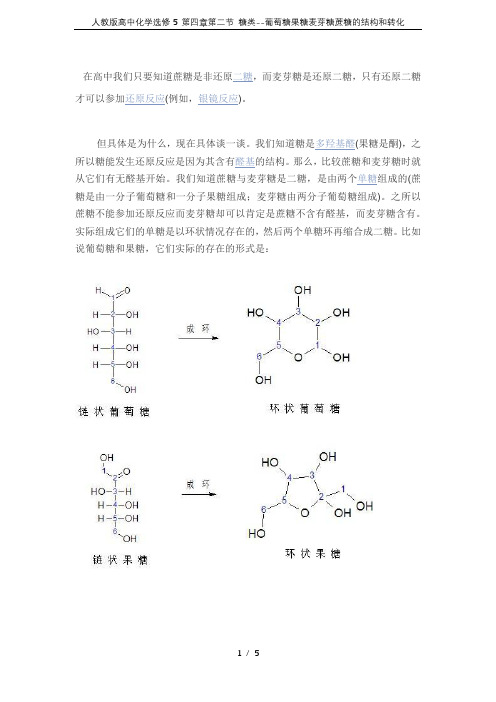
才可以参加还原反应(例如,银镜反应)。
但具体是为什么,现在具体谈一谈。
我们知道糖是多羟基醛(果糖是酮),之所以糖能发生还原反应是因为其含有醛基的结构。
那么,比较蔗糖和麦芽糖时就从它们有无醛基开始。
我们知道蔗糖与麦芽糖是二糖,是由两个单糖组成的(蔗糖是由一分子葡萄糖和一分子果糖组成;麦芽糖由两分子葡萄糖组成)。
之所以蔗糖不能参加还原反应而麦芽糖却可以肯定是蔗糖不含有醛基,而麦芽糖含有。
实际组成它们的单糖是以环状情况存在的,然后两个单糖环再缩合成二糖。
比如说葡萄糖和果糖,它们实际的存在的形式是:在环状的单糖的结构中,只要和环上的氧原子相邻最近碳上连有羟基,那么该糖就含有还原性,就像所举的例子中环状葡萄糖1号碳上有羟基,果糖2号碳上有羟基,所以它们都是还原糖,都可以发生还原反应。
现在,开始解释蔗糖和麦芽糖的还原性问题。
实际蔗糖和麦芽糖的结构如下:我们发现,麦芽糖的两个含氧环中有一个环的离环上氧最近的碳(即1号碳)上有羟基,所以它有还原性可以参加还原反应;而蔗糖的两个环中找不到这样的羟基,所以它没有还原性,不能参加还原反应。
补充:环状的糖中如果有上述像麦芽糖中1号碳这样的羟基,或者葡萄糖1号碳和果糖2号碳上的羟基的话,就会解离出醛基,那么就会有还原性了。
如果你是高中生,那么能理解到这里就可以了。
下面我解释的是高中以外的内容,可以试着理解一下。
链状的糖是怎么形成环状的?其实是它反生了半缩醛(酮)反应,反应式如下:上述反应中,如果R1和R2中至少有一个为H时,产物就为半缩醛,如果都为烃基那么就称为半缩酮~其实链状单糖就是反生了这个反应才成环的。
比如说链状葡萄糖中(如上述图),1号的醛基碳就与5号碳的羟基缩合成了半缩醛而成环的。
通过观察半缩醛(酮)反应,发现该反应是可逆反应,也就是说在反应过程中环状的糖是可以再变回链状的糖,从而会产生游离的醛基(或酮基)产生还原性从而可以参加还原反应。
观察半缩醛或半缩酮发现,它们的结构特点是两个氧原子夹着一个碳原子(两个氧原子必须直接连在所夹的碳原子上),其中一个氧原子必须得连着H原子,另一个必须连着非H原子(一般为烃基)。
人教版高中化学选修5 第四章第二节 糖类--葡萄糖果糖麦芽糖蔗糖的结构和转化

才可以参加还原反应(例如,银镜反应)。
但具体是为什么,现在具体谈一谈。
我们知道糖是多羟基醛(果糖是酮),之所以糖能发生还原反应是因为其含有醛基的结构。
那么,比较蔗糖和麦芽糖时就从它们有无醛基开始。
我们知道蔗糖与麦芽糖是二糖,是由两个单糖组成的(蔗糖是由一分子葡萄糖和一分子果糖组成;麦芽糖由两分子葡萄糖组成)。
之所以蔗糖不能参加还原反应而麦芽糖却可以肯定是蔗糖不含有醛基,而麦芽糖含有。
实际组成它们的单糖是以环状情况存在的,然后两个单糖环再缩合成二糖。
比如说葡萄糖和果糖,它们实际的存在的形式是:在环状的单糖的结构中,只要和环上的氧原子相邻最近碳上连有羟基,那么该糖就含有还原性,就像所举的例子中环状葡萄糖1号碳上有羟基,果糖2号碳上有羟基,所以它们都是还原糖,都可以发生还原反应。
现在,开始解释蔗糖和麦芽糖的还原性问题。
实际蔗糖和麦芽糖的结构如下:我们发现,麦芽糖的两个含氧环中有一个环的离环上氧最近的碳(即1号碳)上有羟基,所以它有还原性可以参加还原反应;而蔗糖的两个环中找不到这样的羟基,所以它没有还原性,不能参加还原反应。
补充:环状的糖中如果有上述像麦芽糖中1号碳这样的羟基,或者葡萄糖1号碳和果糖2号碳上的羟基的话,就会解离出醛基,那么就会有还原性了。
如果你是高中生,那么能理解到这里就可以了。
下面我解释的是高中以外的内容,可以试着理解一下。
链状的糖是怎么形成环状的?其实是它反生了半缩醛(酮)反应,反应式如下:上述反应中,如果R1和R2中至少有一个为H时,产物就为半缩醛,如果都为烃基那么就称为半缩酮~其实链状单糖就是反生了这个反应才成环的。
比如说链状葡萄糖中(如上述图),1号的醛基碳就与5号碳的羟基缩合成了半缩醛而成环的。
通过观察半缩醛(酮)反应,发现该反应是可逆反应,也就是说在反应过程中环状的糖是可以再变回链状的糖,从而会产生游离的醛基(或酮基)产生还原性从而可以参加还原反应。
观察半缩醛或半缩酮发现,它们的结构特点是两个氧原子夹着一个碳原子(两个氧原子必须直接连在所夹的碳原子上),其中一个氧原子必须得连着H原子,另一个必须连着非H原子(一般为烃基)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
糖
低聚糖
1mol糖水解后能产生2~10 mol单糖
蔗糖、麦芽糖、乳糖
1mol糖水解后能产生很多摩尔单糖
多糖 淀粉、纤维素
4、多糖属于天然高分子化合物
你对糖类了解吗?
判断下列说法是否正确,并说明理由:
1、糖类都有甜味,有甜味的都是糖 × 鼠李糖
糖类
甜味 乙酸
C6H12O5
C2H4O2
× 2、糖类就是碳水化合物,分子组成都符合Cn(H2O)m
CH2OOCCH3
五乙酸葡萄糖酯
葡萄糖的化学性质
(3)在体内生理氧化反应:
C6H12O6 (s)+6O2 (g) →6CO2 (g)+6H2O (l)
(4)发酵生成酒精:
C6H12O6 酒曲酶 2CH3CH2OH+CO2
小结
葡萄糖的分子组成
C6H12O6
探究
结构决 定性质
-CHO -OH
CH2OH(CH OH)4CHO
葡萄糖的化学性质
结构
(1) —CHO的性质
决定 体现
性质
ห้องสมุดไป่ตู้① 还原性
A、 银镜反应
△
CH2OH(CHOH)4CHO+2Ag(NH3)2OH → CH2OH(CHOH)4COONH4+3NH3+2Ag↓+H2O
B、与新制Cu(OH)2碱性浊液反应
△
CH2OH(CHOH)4CHO+2Cu(OH)2 → CH2OH(CHOH)4COOH+Cu2O+2H2O
小结 葡萄糖的应用
1 葡萄糖的物理性质
葡萄 糖
1 无色晶体
2
熔点为146℃,易溶于水, 稍溶于乙醇,不溶于乙醚
。
3 有甜味,但甜度不如蔗糖。
2 葡萄糖的结构
经实验得出葡萄 糖能发生银镜反 应和菲林反应说 明葡萄糖中含有
醛基-CHO
葡萄糖的分子式:C6H12O6
葡萄糖是直链化合物, 且在一定条件下,
② 加氢还原成已六醇 CH2OH(CHOH)4CHO + H2 催化剂 CH2OH(CHOH)4CH2OH
葡萄糖的化学性质
(2)-OH的性质 酯化反应
CHO
CH2OH —(CHOH)4 — CHO
(CHOH )4 + CH3COOH 浓H2SO4
CH2OH
CHO
(CHOOCCH 3) 4 + H2O
糖类
葡萄糖的结构和性质
201104034008 聂婷婷
糖类
糖类在生命活动过程中起着重要的作用,是一切生物体 维持生命活动所需要的主要能量来源。
1、糖的定义:
多羟基醛或多羟基酮,和它们的脱水缩合物。
2、 组成元素:
C、H、O
Cn(H2O)m
3、分类
能否水解以及水解产物的多少
单糖
不能水解的糖 葡萄糖、果糖、核糖、脱氧核糖
糖类
碳水化合物
3、糖类主要由绿色植物通过光合作用合成,是生 命活动的主要能量来源
葡萄糖
葡萄糖是自然界中分布最广的 单糖,因最初是从葡萄汁中分离 而得名。
葡萄糖存在于葡萄及其他带有 甜味的水果、蜂蜜中,植物的 种子、叶、根、花,动物的血 液、脑脊液和淋巴液中也含有 葡萄糖。
目录
葡萄糖物理性质 葡萄糖的结构 葡萄糖的化学性质
结构简式 分子组成
结构简式
化学 性质
葡萄糖的应用
营养物质:在酶的催 化作用下进行氧化反 应放出热量,以维持 生命所需的能量
用于糖果制 造业,酿酒
等
用于制镜, 热水胆制银 等工业
用于医药业:血糖 过低的患者直接静 脉注射葡萄糖溶液 以补充营养
1.能说明葡萄糖是一种还原性糖,其依据是( BD ) A.与H2加成生成六元醇 B.能发生银镜反应 C.能发生酯化反应 D.能与新制Cu(OH)2悬浊液共热生成红色沉淀
4.葡萄糖是单糖的主要原因是 (B) A.在糖类物质中含碳原子最少 B.不能水解成更简单的糖 C.分子中有一个醛基 D.分子结构最简单
Thank you !
0.1mol葡萄糖与0.5mol 乙酸完全酯化,生成五 乙酸葡萄糖酯。说明葡
萄糖中含有羟基-OH
3 葡萄糖的化学性质
讨论:根据葡萄糖的结构分析它具有哪些化学性质呢?
含葡有T一it萄le个in糖h醛ere的基 结含有构5个式羟基
CH2—CH—CH—CH—CH—CHO OH OH OH OH OH
结论: 葡萄糖是一种多羟基醛, 它既具有醛的性质又具有醇的性质。
2.在一定的条件下,既可以发生氧化反应,
又可以发生还原反应,还可以和酸发生
酯化反应的是( D )
A、乙醇
B、乙醛
C、乙酸
D、葡萄糖
3、下列关于葡萄糖的叙述错误的是(B) A.葡萄糖的分子式是C6H12O6 B.葡萄糖是碳水化合物,因其分子是由6 个碳原子和6个H2O构成 C.葡萄糖是一种多羟基醛,所以既有醇的 性质又有醛的性质 D.葡萄糖是单糖
