精馏分离方法及原理(路平)
精馏原理与基本操作课件PPT

2021/3/10
13
3 热量平衡
QB + QF = QC + QD + QW + QL QB——再沸器加热剂带入的热量 QF——进料带入热量 QC——冷凝器冷却剂带出的热量 QD——塔顶产品带出热量 QW——塔底产品带出热量 QL——散失于环境的热量 操作中要保持热量的平衡,再沸器、冷凝器的负荷要满足
2021/3/10
8
一、工艺原理
精馏是在塔设备中进行的,可用板式塔亦 可用填料塔。汽相和液相在塔板上或填料 表面上进行着传质传热。易挥发组分从液 相转移至汽相,难挥发组分从汽相转移至 液相
2021/3/10
9
2021/3/10
10
2021/3/10
11
F QF
QB
2021/3/10
2 物料平衡
2021/3/10
5
一、工艺原理
2021/3/10
6
一、工艺原理
平衡蒸馏:平衡蒸馏又称为闪蒸,是一连 续稳定过程。原料连续进入加热器中,加 热至一定温度经节流阀骤然减压到规定压 力,部分料液迅速汽化,汽液两相在分离 器中分开,得到易挥发组分浓度较高的顶 部产品与易挥发组分浓度甚低的底部产品。
2021/3/10
精馏操作知识简介
2021/3/10
1
目录
一、工艺原理
1 精馏原理 2 物料平衡 3 热量平衡 二、工艺控制
1 温度、压力、组成之间关系 2 工艺参数影响 3 产品控制
三、开停工及日常操作
2021/3/10
2
一、工艺原理
1.精馏原理
化工生产常需将液体混合物分离以达到提纯或 回收有用组分的目的。分离互溶液体混合物有 许多种方法,蒸馏是广泛应用的一种方法。
简述精馏原理及过程

简述精馏原理及过程1. 嘿,你知道精馏是咋回事不?就好比把一堆乱七八糟的东西仔细挑拣出来一样!它的原理呢,就是利用混合物中各组分的沸点不同,来实现分离啦。
比如说酒精和水,通过精馏就能把它们分得清清楚楚。
过程嘛,就像是一场精细的舞蹈,逐步把不同的部分区分开。
2. 哎呀呀,精馏原理其实超简单的啦!就像把不同口味的糖果分开一样,沸点就是它们的特点呀。
那过程呢,就如同一个耐心的工匠,一点点地雕琢出纯净的部分。
比如说石油提炼,不就是靠精馏把各种有用的成分弄出来嘛。
3. 哇塞,精馏原理其实不难理解哦!就好像是在一群人里找出特定的那几个。
过程嘛,就像是走迷宫,得沿着正确的路径才能达到目的。
比如从海水里提取盐分,就是利用精馏的原理和过程呀。
4. 嘿,你想想看,精馏不就是把混合的东西变纯净嘛!就像把杂乱的拼图整理好一样。
过程中呢,各组分就像排队一样,按沸点依次出来。
比如从矿石里提取金属,不也得靠精馏嘛。
5. 哟呵,精馏原理说起来很容易呀!就像把不同颜色的豆子分开。
过程呢,就像是一场神奇的魔术,把混合物变得井井有条。
像从植物中提取精油,不就是这样嘛。
6. 哇哦,精馏这事儿啊,原理就是找不同嘛!就像区分不同性格的人。
过程呢,就像一场细腻的表演,把每个部分都展现出来。
比如化工生产中很多物质的分离,都是靠精馏呀。
7. 嘿呀,精馏原理很直白的啦!就像把不同种类的水果挑出来。
过程呢,就像是一个细心的园丁,精心呵护着每一步。
像从天然气中分离出各种成分,不就是用精馏嘛。
8. 哎呀,精馏原理其实不复杂呀!就像给一群小动物分类。
过程呢,就像是解开一个复杂的谜题,慢慢找到答案。
比如从空气中提取氧气,也得靠精馏呀。
9. 哇,精馏原理好有趣的哦!就像把不同的玩具分开摆放。
过程呢,就像是一场精彩的冒险,逐步探索出真相。
像从废料中回收有用物质,这不就是精馏的功劳嘛。
10. 嘿,你可别小看精馏哦!它的原理就像是在混乱中找到秩序。
过程呢,就像一场耐心的战斗,最终取得胜利。
精馏基本知识

精馏基本知识精馏原理和流程3.3.1精馏原理精馏:把液体混合物进行多次部分气化,同时又把产生的蒸气多次部分冷凝,使混合物分离为所要求组分的操作过程称为精馏。
一、全部气化或全部冷凝设在1个大气压下,苯~甲苯混合液的温度为,其状况以A点表示,将此混合液加热,当温度到达(J点),液体开始沸腾,所产生的蒸气组成为(如D点),与成平衡,而且> ,当继续加热,且不从物系中取出物料,使其温度升高到(E点),这时物系内,汽液两相共存,液相的组成为(F点),蒸气相的组成为与成平衡的(G点),且> 。
若再升高温度达到(H点),液相终于完全消失,而在液相消失之前,其组成为(C点)。
这时蒸气量与最初的混合液量相等,蒸气组成为,并与混合液的最初组成相同。
倘再加热到H点以上,蒸气组成为过热蒸气,温度升高而组成不变的为。
自J点向上至H点的前阶段,称为部分气化过程,若加热到H点或H点以上则称全部汽化过程,反之当自H点开始进行冷凝、则至J点以前的阶段称为部分冷凝过程,至J点及J点以下称为全部冷凝过程。
部分汽化和部分冷凝过程实际上是混合液分离过程。
二、部分汽化、部分冷凝全部汽化、全部冷凝与部分汽化、部分冷凝的区别:(1)不从物系中取出物料,(2)温度范围不同。
部分汽化:将混合液自A点加热到B点,使其在B点温度下部分汽化,这时混合液分成汽液两相,气相浓度为,液相为(< ),汽液两相分开后、再将饱和液体单独加热到C点,在温度下部分气化,这时又出现新的平衡或得的液相及与之平衡的气相,最终可得易挥发组分苯含量很低的液相,即可获得近似于纯净的甲苯。
部分冷凝:将上述蒸气分离出来冷凝至,即经部分冷凝至E点,可以得到浓度为的汽相及液相,与成平衡> ,依次类推、最后可得较近于纯净的气态苯。
三、一部分气化、部分冷凝将液体进行一次部分气化,部分冷凝,只能起到部分分离的作用,因此这种方法只适用于要求粗分或初步加工的场合。
显然,要使混合物中的组分得到几乎完全的分离,必须进行多次部分气化和部分冷凝的操作过程。
精馏与精馏原理PPT

第六章 精馏
组员:
零梅妹 朱喜迎 尚赟 李桂浩 赵兴云 罗世波 农雄机 黄勇胜
1.气液相平衡
1.1 定义 1.2 两组分理想溶液的气液平衡相图 1.3 气液相平衡关系
A xA pB B
定义式 xB 代入 pA
α 愈大,A、B两组分愈容易分离; α =1不能用普通精馏分离。
对理想溶液:
0 p p x 拉乌儿 A A A 0 x x p A 0 A A 0 p p x p B B B B 定律 x x B B
d.下曲线为t-x线,也称为饱和 苯—甲苯混合液的t-x-y图 液体线(泡点线)
1.2.2 x-y图
a.以x(气相或液相的浓度) 为横坐标,y(温度)为纵坐 标 b.曲线表示液相组成与之平衡 的气相组成间的关系。 c.对角线x=y的直线 ,作查图 时参考用 。 d.平衡线位于对角线上方
苯—甲苯混合液的x-y图
分冷凝相结合的操作。
精馏中的两个重要概念:
轻组分:挥发性高的组分(沸点低的组分)
重组分:挥发性低的组分(沸点高的组分)
液体混合物经过多次部份汽化后可变为高纯度的
难挥发组分 。
气体混和物经过多次部分泠凝后可变为高纯度的
易挥发组分。
2-2 精馏原理
① 回流
塔顶液相回流和塔底汽相回流,为偏离衡的气 液相在塔内各板上提供了接触条件,实现了气 液相间的质量传递。
馏出液 进料
塔顶蒸汽进入全(冷)凝器被
全部冷凝,将部分冷凝液用泵( 或借重力作用)送回塔顶作为回 流液体,其余部分作为塔顶产品 (称为馏出液)采出。
精馏分离的原理-概述说明以及解释

精馏分离的原理-概述说明以及解释1.引言1.1 概述概述部分的内容可以根据以下方向来写:精馏分离是一种重要的物理分离方法,通过利用不同物质的沸点差异,将混合物中的组分分离出来。
精馏分离广泛应用于化工、石油、石化、制药等领域,是许多工业过程中至关重要的环节之一。
精馏分离的基本原理是根据物质沸点的不同,通过升温使混合物中的不同组分逐渐汽化,然后再通过冷凝使其凝结为液体,从而获得纯度较高的物质。
在精馏过程中,液体混合物首先进入塔体,经过加热后产生蒸汽,然后在塔体内通过填料层或板层进行传质和传热,最终在顶部冷凝为液体,从而实现分离纯化的目的。
精馏分离的应用领域非常广泛,例如在石油行业,精馏被用于原油的分离和提纯,以生产出不同沸点范围的馏分,如汽油、柴油、航空煤油等。
在化工领域,精馏可用于分离和纯化各种化工产品,如酒精、有机溶剂、氨水等。
此外,精馏还广泛应用于制药、食品工业、环保行业等各个领域。
总之,精馏分离作为一种高效可靠的物理分离方法,在众多领域中发挥着重要作用。
通过精心设计和选择适当的操作条件,可以实现对混合物的有效分离和纯化,为各行业的生产和发展提供了可靠的技术支持。
展望未来,随着科学技术的不断进步和应用领域的不断拓展,精馏分离技术也将得到更广泛的应用和进一步的发展。
1.2文章结构1.2 文章结构本文按照以下结构组织内容:引言:首先,我们将概述精馏分离的基本概念和原理,并介绍文章的结构和目的。
正文:接着,我们将详细讨论精馏分离的定义和原理,包括其基本原则、操作流程以及影响分离效果的因素等内容。
此外,我们还将探讨精馏分离在不同领域中的应用情况,介绍一些实际案例,以便读者更好地理解其实际应用和重要性。
结论:最后,我们将总结精馏分离的重要性和优势,并展望其未来发展的前景。
通过对精馏分离技术的深入了解和探讨,我们可以更好地认识到其在化工、石油、食品等行业中的广泛应用,并为相关领域的科研工作者和工程师提供一定的参考和指导。
(化工原理)精馏原理

精馏的原理和过程
原理
基于物质的沸点不同,通过加热和冷凝的方法,将不同沸点的物 质分离出来。
过程
将液体混合物加热至沸腾,产生的蒸汽在冷凝器中冷凝,再通过 回流装置将冷凝液返回精馏塔中,重复进行加热和冷凝的过程, 直至达到分离目的。
操作温度应根据进料组成 和产品要求进行选择,以
实现最佳分离效果。
操作压力应根据进料组成 和产品要求进行选择,以
实现最佳分离效果。
操作条件的优化
实验法
通过实验方法测定不同操作条件下的分离效果,找 出最优的操作条件。
模拟法
利用计算机模拟软件对精馏过程进行模拟,通过优 化算法找出最优的操作条件。
经济分析法
石油化工原料的制备
通过精馏技术可以制备石油化 工原料,如乙烯、丙烯等,这 些原料是生产塑料、合成橡胶 等材料的重要基础。
精馏在其他领域的应用
01
02
03
食品工业
精馏技术可用于食品工业 中,如分离果汁中的果糖 和乙醇饮料中的酒精等。
制药工业
精馏技术可用于药品的生 产和提纯,如分离抗生素、 维生素等。
精馏的分类
02
01
03
根据操作方式的不同,精馏可以分为连续精馏和间歇 精馏。
根据进料位置的不同,精馏可以分为侧线精馏、塔顶 精馏和塔底精馏。
根据操作压力的不同,精馏可以分为常压精馏、加压 精馏和减压精馏。
02
精馏塔的构造和工作原理
精馏塔的结构
塔体
进料板
塔板
溢流管
冷凝器
精馏塔的主要部分,用于 容纳待分离的液体混合物 和进行传热传质过程。
3精馏原理和流程
4、塔釜的作用 使回流下的液体部分汽化产生蒸汽,以作为各板上液体 部分汽化的加热蒸汽。
1.4.2.精馏操作流程
tB x2 x1
y2
y1
tA
2、部分冷凝
将混合物的饱和蒸汽冷却至气、液共存区内的某点,使其 在此点温度下部分冷凝,混合物分成平衡的气、液两相的 过程。
tB方法
使部分汽化产生的温度较高的蒸汽与相应的部分冷凝时所 产生的温度较低的液体直接混合,进行换热,利用高温蒸 汽的热量加热低温液体并使其汽化,而蒸汽自身则被部分 冷凝,同时完成传质。 精馏就是多次而且同时运用部分汽化和部分冷凝,使混合液 得到分离的过程。
2、精馏段与提馏段的作用 ①、精馏段作用 自下而上逐步增浓气相中的易挥发组分, 即浓缩轻组分,以提高塔顶产品中易挥发组分浓度。
②、提馏段作用
自上而下逐步增浓液相中的难挥发组分,即浓缩重组分。
3、回流的作用 精馏塔中第n块板上的操作 情况。
xn-1
yn
n块板 yn+1
xn
回流液是使蒸汽部分冷凝是冷却剂,并使精馏稳定进行。
3工业方法使部分汽化产生的温度较高的蒸汽与相应的部分冷凝时所产生的温度较低的液体直接混合进行换热利用高温蒸汽的热量加热低温液体并使其汽化而蒸汽自身则被部分冷凝同时完成传质
1.4精馏原理和流程
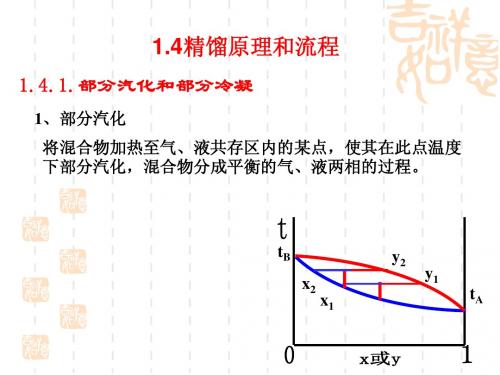
1.4.1.部分汽化和部分冷凝
1、部分汽化
将混合物加热至气、液共存区内的某点,使其在此点温度 下部分汽化,混合物分成平衡的气、液两相的过程。
4、精馏装置的作用
精馏塔设备
1、塔板的作用 塔板是这样一种装置,它使由塔 顶逐板下降的回流液与塔底逐板 上升的蒸汽在塔板上接触,同时 进行部分汽化和部分冷凝,即在 每一块塔板上同时进行着传热与 传质作用。
精馏的原理

精馏的原理
精馏是一种分离技术,它通过不断地加热、蒸发和冷凝的方法,使混合物在温度和压力上发生变化,从而将其分离成组分。
精馏原理如下:
1. 加热:将混合物加热,使其温度升高。
当温度达到一定值时,混合物中的某些成分会被蒸发;
2. 蒸发:将混合物的温度提高,使其中的一些组分以气体形式被蒸发;
3. 冷凝:将蒸气冷却,使其中的部分成分凝结;
4. 收集:将冷凝物收集,然后重新加热,循环整个过程,使混合物中的各组分分离出来。
因此,精馏就是通过不断地加热、蒸发、冷凝来达到分离混合物中不同组分的目的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
典型的顺序深冷分离流程
4.2 脱甲烷塔
• 分离氢气、甲烷与乙烯
4.2 脱甲烷塔
• P=4→0.2MPa, • 塔顶温度:
T= -98→ -141℃, • 提高压力,可节省冷 量。 • 要提高乙烯回收率, 应降低塔顶温度。
4.2 脱甲烷塔
• 压力升高,甲烷
对乙烯的相对挥 发度降低。 • P=4.4MPa, α→1
3.6 多组分精馏分离
– 对其他组分: • 当各组分间沸点相差较大,可近似认为轻组 分全部在塔顶馏出,重组分全部在塔釜排出。 • 当各组分间沸点相差不大,则轻、重组分在 塔顶、塔釜排出的组成可由理论板数确定。
• 说明各组分在塔顶和塔釜的分配,不仅受
理论板数和塔操作条件限制,而且受全塔 物料衡算的限制。
4.2 脱甲烷塔
• 压力升高,和回流
比降低,可节省冷 量。但塔釜甲烷组 成升高,而且分离 也不易。 • 但为了节省冷量, 故只有牺牲设备投 资,增加塔板数。
4.3 脱乙烷塔
• 分离乙烷与丙烯
4.3 脱乙烷塔
• 操作压力2.27MPa,
4.4 乙烯精馏塔
• 分离乙烯与乙烷 • 侧线采出乙烯 • 压力↑或X乙烯↑ →α↓
80.10 65.40 76.60 69.60 65.20 67.00 56.90 54.00
THR-DC裂解原料产品收率(vol% )
原料 H2 石脑油 2.50 1.40 煤油 3.00 2.40 轻柴油 3.50 1.70 减压柴油 0.80 1.70
CO
CO2 CH4 C2H6 C2H4 C3H8 C3H6
ij xi • α表达式—— yi 1 ( ij 1) xi
• T-x-y图
• X-y图
• 注意:上述汽液平衡关系仅表达形式不同,汽、液
相组成是一致的。
双组分汽液平衡关系T-x-y图
①理想溶液,拉乌尔定律p=p°x; ②理想气体,道尔顿分压定律p=Py。 总压:
0 P pA pB p0 x p A A Bx B 0 p0 x p A A B (1 - x A ) 0 P p0 p x A 0 B0 ; y A A x A pA pB P
即提高塔顶产品组成。但受全塔物料衡算 的限制。
3.6 多组分精馏分离
• 对多组分精馏其精馏原理与双组分相同。
理论板数和操作条件对分离效率的影响趋 势也相同。不同在于处理对象由双组分变 为多组分,导致考虑问题的方法有所变化。
– 根据对多组分分离的要求确定预分离混合物中 的轻、重关键组分。以轻、重关键组分作为双 组分考虑对设备的要求和操作条件改变对分离 效率的影响。
用于分离物系沸点较高,易结焦
分 常压 连续式 分馏 多组分
类
用于混合物各组 分沸点相近,且 要获得较高收率 的分离
减压
精馏
特殊精馏
用于混合物各组分沸 点相差不大,且要获 得较高收率的分离
用于获得一定馏程范围产品的分离
3 分离基本原理
3.1 分离的基本原理
3.2 操作压力对汽液平衡的影响
3.3 分离方法及原理
890
0.098 0.130 25.70 13.7 25.70 9.80
750
0.098 0.348 10.90 10.00 23.70 16.90
840
0.098 0.015 1.10 8.80 23.00 14.30
900
0.392 0.035 3.60 16.20 30.30 4.00
1.3 精馏分离的对象和目的
0.10
1.00 4.80
1.30
5.60 4.00
0.00
3.30 6.00
0.00
4.40 5.40
0.00
1.40 3.70
0.00
5.70 5.50
0.00
2.40 6.60
0.00
0.30 1.90
THR-DC裂解条件与主要产品收率
原料 石脑油 煤油 轻柴油 减压柴油
裂解温 度,℃
裂解压 力,℃ 停留时间,s CO2 CH4 C2H4 C3H6
2.50
13.80 17.30 1.80 36.30 0.90 13.40
0.20
6.40 10.70 1.90 23.90 0.40 15.90
9.60
19.70 13.80 1.90 29.80 0.40 15.40
0.90
16.70 10.40 2.40 25.60 0.50 16.50
5.30
裂解是利用高温将烷烃、环烷烃、芳烃等通过 原油:石脑油、煤油、轻柴油、重柴油 脱氢、断链等反应生成烯烃、碳原子数较少的 催化干气精制生产乙烯 产物。分蒸汽裂解和加氢热裂解。 原油:石蜡基原油渣油、环烷基原油渣油
• 甲醇制乙烯的MTO 工艺
• 甲烷氧化偶联法(OCM)制乙烯
1.2 石油裂解的产物
• 裂解原料性质
汽液平衡关系
对多组分汽液平衡关系表达形式
• K表达式——yi=Kixi
– Ki值称汽液平衡常数——由K图获得
• α表达式——yi/yj=αijxi/xj
– αij值称相对挥发度——αij=Ki/Kj
轻 烃 汽 液 平 衡 关 系 K 图 ( 高 温 段 )
汽液平衡关系
对双组分汽液平衡关系表达形式
精馏分离方法及原理
江汉大学 化学与环境工程学院 路 平
精馏分离方法及原理
1 乙烯生产
2 精馏分离方法 3 精馏分离基本原理
4 乙烯生产中分离方法及原理
1 乙烯生产
1.1 乙烯生产方法 1.2 石油裂解的产物 1.3 精馏分离的对象和目的
1.1 乙烯生产方法
• 原油裂解制乙烯
• 原油渣油裂解制乙烯 •
4.4 乙烯精馏塔
• 回流比影响,压力确定
4.5 前脱丙烷塔加氢回流流程
• 说明 • 可用反应回流
烃的名称 CH4 C2H4 C2H6 C3H6 C3H8 n-C4H10 n-C5H12 n-C6H14 常压下沸点℃ -161.495 -103.68 -88.60 -47.72 -42.045 -0.50 36.064 68.732
•
4.1 裂解气预分馏
• 轻烃裂解装置裂解气预分馏
4.1 裂解气预分馏
3.5 操作条件对精馏分离效率 的影响——进料状态
• 在回流比恒定的情况
下,进料温度降低, 提馏段操作线远离平 衡线,所需理论板少, 实际分离效果好。 冷液进料不足,塔釜 加热量大,易使物料 产生聚合或结焦。
•
说 明
• 操作压力降低,分离效果提高。 • 回流比提高,分离效果提高。 • 进料温度降低,分离效果提高。 • 改变上述操作工艺条件,可提高分离效果,
25.70 13.7 1.40 25.70 0.30 9.80
0.30
10.90 10.00 2.90 23.70 0.50 16.90
0.30
1.10 8.80 2.10 23.00 0.70 14.30
1.50
3.60 16.20 1.10 30.30 1.80 4.00
C4H10
C4H8 C4H6
• 精馏分离对象
– 分离具有不同挥发 烃的名称 分子量 常压下沸点℃ CH4 C2H4 C2H6 C3H6 C3H8 n-C4H10 n-C5H12 n-C6H14 16.043 28.054 30.070 42.081 44.097 58.124 72.151 86.178 - 161.495 - 103.68 - 88.60 - 47.72 - 42.045 -0.50 36.064 68.732
• 馏分油裂解装置裂解气预分馏过程
水在0.038MPa,沸点75℃;0.057MPa,沸点85 ℃ ; 0.025MPa,沸点65 ℃ 。
4.1 裂解气预分馏
• 油洗塔
水洗塔分离C5,C6
烃的名称 CH4 C2H4 C2H6 C3H6 C3H8 n-C4H10 n-C5H12 n-C6H14 常压下沸点℃ -161.495 -103.68 -88.60 -47.72 -42.045 -0.50 36.064 68.732
THR-DC (管式固定床催化裂解) 裂解条件
原料 裂解温度,℃ 裂解压力,℃ 停留时间,s 蒸汽/原料中碳 气化率,%(vol) 石脑油 850 800 煤油 820 831 轻柴油 890 750 减压柴油 840 900
0.098 0.333 0.098 0.098 0.098 0.098 0.098 0.392 0.068 0.215 1.02 1.64 0.20 1.17 0.169 0.130 0.348 0.015 0.035 0.54 1.09 0.55 0.59 1.15
度(沸点)的混合
液或混合气
• 精馏分离目的
– 将混合物分离成符
合标准的各产品。
2 精馏分离方法
2.1 分离过程的发展现状 2.2 精馏分离方法
2.1 分离过程的发展现状
2.2 精馏分离方法 用于分离物系沸点较低
名 称 操作压力 加压 操作流程 间歇式 蒸馏方式 简单蒸馏 分离组分 双组分
分馏用于混合物各组 分沸点相差很大的分 离
理论板及分离效果
• 对一定的物系,操作
条件恒定,理论板
(梯级数)越多,xD
越高,xW越低,说明 分离效果好。
• 平衡线和操作线间距
表示理论板分离效果。
理论板与塔内温度分布
3.4 理论板数对精馏分离效率 的影响
• 在进料热状况和
回流比不变的条
件下,理论板减
少,分离效率降
低。
3.5 操作条件对精馏分离效率 的影响——操作压力
原料 相对密度d420 馏程 ℃ 元素 分析 %(wt) IBP 50% EP C H S 石脑油 0.674 39.00 73.00 102.00 84.36 14.37 0.17 煤油 0.783 178.50 204 86.06 13.73 0.29 轻柴油 0.823 260.50 308.50 85.67 13.40 0.79 86.49 12.74 0.77 减压柴油 0.898
