高中化学必修一物质的量练习题有答案
人教版高中化学必修一物质的量同步试题(含有答案)

高中化学学习材料金戈铁骑整理制作§1-2物质的量(1)一、选择题1.下列叙述正确的是( )A .每摩尔物质约含有6.02×1023个粒子B .摩尔是七个基本物理量之一C .摩尔是物质的质量单位D .摩尔是物质的数量单位解析:根据物质的量的概念要点分析,每摩尔物质约含有6.02×1023个粒子,故A 项正确;物质的量是七个基本物理量之一,摩尔是其单位,故B 项错;摩尔是物质的量的单位,而不是质量和数量的单位,质量的单位是kg ,数量是一个值,无单位,故C 、D 两项均错。
答案:A2.(双选题)下列说法正确的是( )A .H 2的摩尔质量是2 gB .1 mol H 2O 的质量是18 gC .氧气的摩尔质量是32 g·mol -1D .2 g H 2含1 mol H解析:摩尔质量的单位是g·mol -1,故A 项错误,C 项正确;1 mol H 2O 的质量是18 g ,故B 项正确;2 g H 2的物质的量是1 mol ,含有2 mol H ,故D 项错误。
答案:BC3.设N A 为阿伏加德罗常数的值,下列说法错误的是( )A .32 g O 2所含的原子数目为N AB .0.5 mol H 2O 含有的原子数目为1.5 N AC .1 mol SO 2含有的SO 2分子数目为N AD .0.5 N A 个Cl 2的物质的量是0.5 mol 解析:32 g÷32 g/mol =1 mol ,故32 g O 2所含分子数为N A ,原子数为2N A ,A 项错误。
答案:A4.下列物质含分子数最多的是( )A .0.8 mol SO 2B .1.806×1022 H 2OC .11.2 g COD .32 g SO 2解析:根据公式计算,B 项是0.3 mol ,C 项是0.4 mol ,D 项是0.5 mol 。
答案:A5.1 mol MgSO 4·7H 2O 含有结晶水的质量为( )A .16 gB .18 gC .112 gD .126 g答案:D6.在0.1 mol Na 2SO 4中所含Na +数目为( )A .6.02×1022 个B .1.202×1023 个C .0.1个D .0.2个解析:0.1 mol Na 2SO 4中含Na +0.2 mol,0.2×6.02×1023=1.204×1023个。
高考化学物质的量综合经典题及答案

高考化学物质的量综合经典题及答案一、高中化学物质的量练习题(含详细答案解析)1.(1)在标准状况下①6.72L CH 4②3.01×1023个HCl 分子③13.6g H 2S ④0.2mol NH 3,体积最大的是____,密最大的是度___,质量最小的是___,氢原子个数最多的是____。
(填写序号)(2)等温等压下,质子数相等的CO 、N 2两种气体,质量之比为____,体积之比为____,摩尔质量之比____。
(3)某物质在一定条件下加热分解,产物都是气体。
分解方程式为:3A =B +3C +2D 。
测得生成的混合气体的平均相对分子质量为2a ,则A 的摩尔质量为____。
【答案】② ② ④ ① 1:1 1:1 1:1 4a g/mol【解析】【详解】(1)①6.72L CH 4中:n(CH 4)= 6.72L 22.4L/mol=0.3mol ,m(CH 4)=0.3mol×16g/mol=4.8g ,ρ(CH 4)= m m M 16==g/L V V 22.4,N(H)=4N(CH 4)=1.2N A ; ②3.01×1023个HCl 分子中:n(HCl)=23233.01106.0210⨯⨯=0.5mol ,V(HCl)=0.5mol×22.4L/mol=11.2L ,ρ(HCl)=m m M 36.5==g/L V V 22.4,m(HCl)=0.5mol×36.5g/mol=18.25g ,N(H)=N(HCl)=0.5N A ; ③13.6g H 2S 中:n(H 2S)=13.6g 34g/mol=0.4mol ,V(H 2S)=0.4mol×22.4L/mol=8.96L ,ρ(H 2S)= m m M 34==g/L V V 22.4,N(H)=2N(H 2S)=0.8N A ; ④0.2mol NH 3中:m(NH 3)=0.2mol×17g/mol=3.4g ,V(NH 3)=0.2mol×22.4L/mol=4.48L ,ρ(NH 3)= m m M 17==g/L V V 22.4,N(H)=3N(NH 3)=0.6N A . 所以:体积最大的是②,密度最大的是②,质量最小的是④,含氢原子数最多的是①; (2)CO 、N 2两种气体涉及的元素有C 、O 、N 质子数分别为6、8、7,所以两种气体的分子的质子数分别为:14、14,质子数相等的CO 、N 2,物质的量相等;CO 、N 2摩尔质量分别为28g/mol 、28g/mol ,故摩尔质量之比1:1;根据m=nM 知:质量之比与摩尔质量成正比为28:28=1:1;根据阿伏伽德罗定律,相同条件下物质的量相等的气体具有相同的体积,故体积之比为1:1;(3)化学方程式系数的意义:表示物质的量。
高中化学必修一 物质的量浓度 练习解析版)

2.3.3 物质的量浓度练习(解析版)1.下列溶液中,Cl﹣的物质的量浓度最小的是()A.1 L 1 mol•L﹣1的NaCl溶液B.0.1 L 2 mol•L﹣1的KCl溶液C.0.1 L 1 mol•L﹣1的MgCl2溶液D.10 mL 1 mol•L﹣1的AlCl3溶液【答案】A【详解】A. 1 L 1 mol•L﹣1的NaCl溶液中,c(Cl-):c(NaCl)=1:1,则c(Cl-)为1mol/L;B. 0.1 L 2 mol•L﹣1的KCl溶液中,c(Cl-):c(KCl)=1:1,则c(Cl-)为2mol/L;C. 0.1 L 1 mol•L﹣1的MgCl2溶液中,c(Cl-):c(MgCl2)=2:1,则c(Cl-)为2mol/L;D. 10 mL 1 mol•L﹣1的AlCl3溶液中,c(Cl-):c(AlCl3)=3:1,则c(Cl-)为3mol/L;总上所述,氯离子浓度最小的为1mol/L,答案为A。
2.下列各溶液中n(Na+)与100 mL 0.1 mol/L Na2SO4溶液中n(Na+)相同的是A.100 mL 0.1 mol/L NaCl 溶液B.50 mL 0.2 mol/L NaNO3溶液C.100 mL 0.1 mol/L NaHSO4溶液D.200mL 0.2mol/L HCl溶液与100 mL 0.2 mol/L NaHCO3溶液混合【答案】D【详解】100 mL 0.1 mol/L Na2SO4溶液中n(Na+)=0.1 mol/L×100 mL×2=0.02mol。
A.100 mL 0.1 mol/L NaCl溶液中n(Na+) = 0.1 mol/L×100 mL×1=0.01mol。
B.50 mL 0.2 mol/L NaNO3溶液中n(Na+) = 0.2 mol/L×50 mL×1=0.01mol。
2020年新教材高中化学必修一物质的量计算习题带答案

一、单选题1.用N A表示阿伏德罗常数的值,下列叙述正确的是()A.N A个CO2分子占有的体积约为22.4LB.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 N AC.标准状况下,22.4LH2O含有的分子数为N AD.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-个数为N A2.下列叙述正确的是()A.1 mol H2O的质量为18 g/mol B.CH4的摩尔质量为16 gC.3.01×1023个SO2分子的质量为32g D.标准状况下,1 mol任何物质体积均为22.4 L3.下列物质中,含氧原子最多的是()A.标准状态时,22.4L的CO2 B.200g 49%的H3PO4 C.32g的SO2气体D.3.01×1023个O2分子4.用N A表示阿伏加德罗常数的值,下列叙述正确的是()A.含有N A个氦原子的氦气在标准状况下的体积约为11.2L B.25℃,1.01×105Pa,44gCO2中含有的原子数为3N A C.在常温常压下,11.2L Cl2含有的分子数为0.5N A D.标准状况下,11.2LH2O含有的分子数为0.5N A 5.N A是阿伏加德罗常数的值。
下列说法正确的是()A.100g质量分数为46%的酒精水溶液含有4N A个分子B.用1L1mol/LFeCl3溶液充分反应制备氢氧化铁胶体,该体系中含氢氧化铁胶体粒子数目为N AC.1L0.01mol/L氨水溶液中含NH3•H2O数目为0.01N AD.用浓盐酸分别与MnO2、KClO3反应制备1mol氯气,转移的电子数均为2N A6.阿伏伽德罗常数的值为N A。
下列说法正确的是()A.18 g H2O、D2O组成的物质中含有的电子数为10N A B.0.2 mol铁在足量的氧气中燃烧,转移电子数为0.6N A C.50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3N AD.0.1 mol 熔融的KHSO4中含有0.1N A个阳离子7.0.2mol/LAl2(SO4)3溶液100mL与0.3mol/L K2SO4200mL混合,则所得溶液中硫酸根离子的物质的量浓度为()A.1.2mol/L B.0.9mol/L C.0.3mol/L D.0.4mol/L8.用N A表示阿伏加德罗常数,下列叙述正确的是()A.标准状况下,2gH2含有的原子数为N A B.等质量的O2和O3中所含的氧分子数相同C.常温常压下,14gN2含有电子数为7N A D.等质量的CO与CO2中所含碳原子数之比为7﹕119.由硝酸钠、氯化钡和氯化钠组成的混合溶液,其中n(Na+)=0.6mol,n(Ba2+)=0.1mol,n(Cl-)=0.3mol,则NO)为()A.0.1mol B.0.3mol C.0.5mol D.0.15moln(-310.下列说法不正确的是( )A.磷酸的摩尔质量与6.02×1023个磷酸分子的质量在数值上相等B.6.02×1023 个N2 和6.02×1023个H 2 的质量比等于14∶1C.1 mol臭氧和1.5 mol氧气含有相同数目的氧原子D.常温、常压下,0.5×6.02×1023 个一氧化碳分子质量是28g11.下列说法不正确的是( )A.1 molH2的质量只有在标准状况下才约为2gB.在标准状况下,1mol任何气体的体积都约为22.4LC.273 ℃,1.01×105 Pa状态下,1 mol气体体积大于22.4LD.标准状况下,0.5 molO2和0.5 molN2组成的混合气体体积约为22.4L12.实验室配制0.1000mol·L-1的H2SO4溶液,下列图示操作不需要的是()A.B.C.D.13.配制一定物质的量浓度的某溶液,下列情况会使配制结果偏高的是()A.未冷却即转移、定容B.称最时将物体与砝码的位置放反C.定容时仰视刻度线观察液面D.容量瓶中原有少量蒸馏水14.实验室欲用232Na CO 10H O ⋅晶体配制100mL 1mol/L 的23Na CO 溶液,下列说法正确的是( )A .要完成实验需称取10.6g 232Na CO 10H O ⋅晶体B .本实验需用到的仪器有天平、药匙、玻璃棒、烧杯、500mL 容量瓶C .配制时若容量瓶不干燥,含有少量蒸馏水会导致溶液浓度偏低'D .定容时俯视刻度线会导致溶液浓度偏高15.具备基本的化学实验技能是进行科学探究的基础和保证。
高考化学物质的量的综合题试题及答案解析
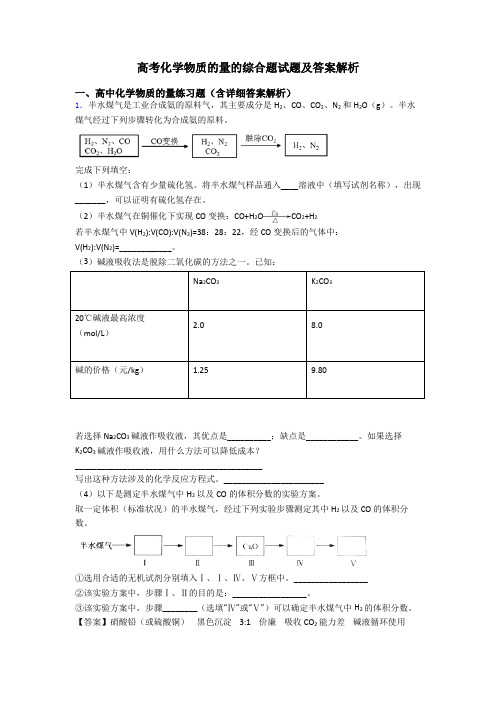
高考化学物质的量的综合题试题及答案解析一、高中化学物质的量练习题(含详细答案解析)1.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g)。
半水煤气经过下列步骤转化为合成氨的原料。
完成下列填空:(1)半水煤气含有少量硫化氢。
将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明有硫化氢存在。
(2)半水煤气在铜催化下实现CO变换:CO+H2O CO2+H2若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=____________。
(3)碱液吸收法是脱除二氧化碳的方法之一。
已知:Na2CO3K2CO320℃碱液最高浓度(mol/L)2.08.0碱的价格(元/kg) 1.259.80若选择Na2CO3碱液作吸收液,其优点是__________;缺点是____________。
如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?___________________________________________写出这种方法涉及的化学反应方程式。
_______________________(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数。
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
_________________②该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
③该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数。
【答案】硝酸铅(或硫酸铜)黑色沉淀 3:1 价廉吸收CO2能力差碱液循环使用2KHCO3→K2CO3+CO2↑+H2O除去半水煤气中的CO2(包括H2S)和H2O IV【解析】【分析】【详解】(1)硫化氢能与重金属生成沉淀,所以将半水煤气样品通入硝酸铅(或硫酸铜)溶液中,出现黑色沉淀可以证明有硫化氢存在。
高中化学(新人教版)必修第一册课后习题:物质的量在化学方程式计算中的应用(课后习题)【含答案及解析】

物质的量在化学方程式计算中的应用课后篇素养形成合格考达标练1.(2020辽宁锦州高一检测)实验室利用反应2KClO32KCl+3O2↑制取氧气,已知有24.5 g KClO3参加反应,则得到标准状况下的氧气的体积是()A.2.24 LB.4.48 LC.44.8 LD.6.72 L3的物质的量是24.5g122.5g·mol-1=0.2 mol,2KClO32KCl+3O2↑2 mol3 mol0.2 mol n(O2)2 mol∶0.2 mol=3 mol∶n(O2),则n(O2)=0.3 mol,故产生的氧气在标准状况下的体积是0.3mol×22.4 L·mol-1=6.72 L。
2.2 mol·L-1的盐酸和稀硫酸各100 mL,分别加入等质量的铁粉,反应后生成的气体质量之比为2∶3,则向盐酸中加入的铁粉的物质的量为()A.0.05 molB.0.075 molC.0.15 molD.0.2 mol(HCl)=0.2 mol,n(H2SO4)=0.2 mol。
若酸均不足,即完全反应生成H2的质量之比为1∶2;若酸均过量,即金属不足,则生成H2的质量之比为1∶1。
现生成H2的质量之比为2∶3,则说明盐酸不足,硫酸过量;根据盐酸中HCl的物质的量可求出生成H2 0.1 mol,则H2SO4反应生成0.15 mol H2,则铁粉的物质的量为0.15 mol。
3.将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是()A.1∶2∶3B.6∶3∶2C.3∶1∶1D.1∶1∶1解析根据金属与酸反应的实质2M+2n H+2M n++n H2↑可知三种金属都过量,而铝、镁都不与H2O 反应,按盐酸计算,两者产生气体的物质的量都为0.05 mol,金属钠可继续与H2O反应最终产生0.15 mol H2,即同温同压下产生气体的体积比为0.15 mol∶0.05 mol∶0.05 mol=3∶1∶1。
高考化学物质的量综合经典题及详细答案
高考化学物质的量综合经典题及详细答案一、高中化学物质的量练习题(含详细答案解析)1.实验室配制500mL0.1mol/LNa2CO3溶液,回答下列问题(1)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、___。
(2)容量瓶上标有刻度线、___,使用前要___。
(3)需用托盘天平称取Na2CO3____g。
(4)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?A.加水时超过刻度线___,B.溶解后未冷却到室温就转入容量瓶___,C.容量瓶内壁附有水珠而未干燥处理___,D.定容时仰视___,E.上下颠倒摇匀后液面低于刻线___。
(5)若实验室中要用浓度为16mol/L的浓硫酸配制480mL2.0mol/L的稀硫酸,则需要量取浓硫酸的体积为___mL。
【答案】500mL容量瓶、玻璃棒、胶头滴管温度、容积检漏 5.3 偏低偏高不变偏低不变 62.5【解析】【分析】配制一定物质的量浓度溶液步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,分析误差时可根据c=nV判断。
【详解】(1)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、初步摇匀、定容、摇匀、装瓶可知所需的仪器有:托盘天平、烧杯、玻璃棒、药匙、500mL容量瓶和胶头滴管,缺少的仪器:500mL容量瓶、胶头滴管、玻璃棒;(2)容量瓶上标有温度、刻度线、容积;容量瓶带有瓶塞,为防止使用过程中漏液,使用前应查漏;(3)配制500mL 0.1mol/LNa2CO3,需要 Na2CO3的质量为:0.5L×0.1mol/L×106g/mol=5.3g;(4)A.加水时超过刻度线,导致溶液体积偏大,溶液浓度偏低;B.溶解后未冷却到室温就转入容量瓶,冷却后溶液体积偏小,溶液浓度偏高;C.容量瓶内壁附有水珠而未干燥处理,对溶质物质的量和溶液体积都不产生影响,溶液浓度不变;D.定容时仰视,导致溶液体积偏大,溶液浓度偏低;E.上下颠倒摇匀后液面低于刻线,属于正常操作,溶液浓度不变;(5)若实验室中要用浓度为16mol/L 的浓硫酸配制480mL 2.0mol/L 的稀硫酸,应选择500mL 容量瓶,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质物质的量不变得:16mol/L×V=500mL 2.0mol/L,解得V=62.5mL。
高一物质的量练习题及答案
高中化学必修一《物质的量综合复习题》1.下列叙述中,正确的是()A.12g碳所含的原子数就是阿伏加德罗常数 B.阿伏加德罗常数没有单位C.“物质的量”指物质的质量D.摩尔表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒2.下列说法正确的是()A.1 molH2的质量是1 g B.1 mol HCl的质量是36.5 g·mol-1C.Cl2的摩尔质量等于它的相对分子质量 D.硫酸根离子的摩尔质量是96 g·mol-1 3.下列说法错误的是()A.1 mol 氢B.1 mol 的氧原子C.1 mol 二氧化碳D.1 mol水4.下列各组物质中,含原子数最多的是()A.0.4 mol NH3B.4℃时5.4 mL水 C.10 g氖气 D.6.02×1023个硫酸分子5.铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯。
如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg。
那么一个铅笔字含有的碳原子数约为()A.2.5×1019个B.2.5×1022个 C.5×1019个D. 5×1022个6.下列说法错误的是()A.6.02×1023是阿伏加德罗常数的近似值B.1 mol 12C的质量是12 gC.含有阿伏加德罗常数个粒子的物质就是1 molD.1 mol O2含有6.02×1023个氧原子7.下列物质里含氢原子数最多的是()A.1 mol H2 B.0.5molNH3C.6.02×1023个的CH4分子 D.0.3molH3PO48.0.1 mol NaHCO3中含有()A.0.2 mol Na+B.0.05 mol CO 23C.6.02×1023个 O D.0.1 mol H9.1g O2和1g O3相比,下列表述正确的是()A.所含分子数相同 B.所含原子数相同C.所含原子数不同 D.1g O3中所含分子数较多10. 2.16 g X2O5中含有0.1 molO,则X的相对原子质量为()A.21.6B.28C.14D.3111.某气体物质质量为6.4 g,含有6.02×1022个分子,则该气体的相对分子质量为() A. 64 B. 32 C.96 D.3212.如果1g水中含有n个氢原子,则阿伏加德罗常数是()A.1/n mol-1 B.9n mol-1 C.2n mol-1 D.n mol-113.①1molH2O约含个H2O;②1molO约含个e-;③2molH+约含个H+;④ 3× 6.02×1023个电子的物质的量是 mol e-;⑤1.204×1024个水分子的物质的量为mol。
新教材人教版化学必修一第二章第3节物质的量习题含答案
B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中
D.向容量瓶中转移溶液要用玻璃棒引流
(4)下列情况中,所配制的稀硫酸浓度偏大的是__________。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
A.常温常压下,2.24 L CO气体g 的分子数是1NA,其体积是22.4L
C.常温常压下,48 g O3中含有的氧原子数为3NA
D.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
二、实验题
17.用质量分数为36.5%的盐酸(密度为1.16g·cm-3)配制1mol·L-1的稀盐酸。现实验室仅需要这种盐酸220mL,试回答下列问题:
D.12 g金刚石中含有化学键的数目为4NA
9.NA是阿伏加德罗常数的值。下列说法正确的是()
A.12 g石墨烯和12 g金刚石均含有NA个碳原子
B.0.1 mol D2O中所含质子数为0.8NA
C.8.7 g MnO2与含0.4 mol HCl的浓盐酸在加热条件下反应,转移电子数为0.2NA
D.标准状况下2.24 L Cl2完全溶于水时,所得溶液中含氯微粒总数为0.2NA
(3)下列操作对所配浓度有何影响(填写字母)
偏大的有_______________;偏小的有____________;无影响的有________________。
A.称量用了生锈的砝码;
B.将NaOH放在纸张上称量;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D.往容量瓶转移时,有少量液体溅出
B.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3mol·L -1
高考化学复习《物质的量》专项综合练习
高考化学复习《物质的量》专项综合练习一、高中化学物质的量练习题(含详细答案解析)1.(1)在标准状况下①6.72L CH 4②3.01×1023个HCl 分子③13.6g H 2S ④0.2mol NH 3,体积最大的是____,密最大的是度___,质量最小的是___,氢原子个数最多的是____。
(填写序号)(2)等温等压下,质子数相等的CO 、N 2两种气体,质量之比为____,体积之比为____,摩尔质量之比____。
(3)某物质在一定条件下加热分解,产物都是气体。
分解方程式为:3A =B +3C +2D 。
测得生成的混合气体的平均相对分子质量为2a ,则A 的摩尔质量为____。
【答案】② ② ④ ① 1:1 1:1 1:1 4a g/mol【解析】【详解】(1)①6.72L CH 4中:n(CH 4)= 6.72L 22.4L/mol=0.3mol ,m(CH 4)=0.3mol×16g/mol=4.8g ,ρ(CH 4)= m m M 16==g/L V V 22.4,N(H)=4N(CH 4)=1.2N A ; ②3.01×1023个HCl 分子中:n(HCl)=23233.01106.0210⨯⨯=0.5mol ,V(HCl)=0.5mol×22.4L/mol=11.2L ,ρ(HCl)=m m M 36.5==g/L V V 22.4,m(HCl)=0.5mol×36.5g/mol=18.25g ,N(H)=N(HCl)=0.5N A ; ③13.6g H 2S 中:n(H 2S)=13.6g 34g/mol=0.4mol ,V(H 2S)=0.4mol×22.4L/mol=8.96L ,ρ(H 2S)= m m M 34==g/L V V 22.4,N(H)=2N(H 2S)=0.8N A ; ④0.2mol NH 3中:m(NH 3)=0.2mol×17g/mol=3.4g ,V(NH 3)=0.2mol×22.4L/mol=4.48L ,ρ(NH 3)= m m M 17==g/L V V 22.4,N(H)=3N(NH 3)=0.6N A . 所以:体积最大的是②,密度最大的是②,质量最小的是④,含氢原子数最多的是①; (2)CO 、N 2两种气体涉及的元素有C 、O 、N 质子数分别为6、8、7,所以两种气体的分子的质子数分别为:14、14,质子数相等的CO 、N 2,物质的量相等;CO 、N 2摩尔质量分别为28g/mol 、28g/mol ,故摩尔质量之比1:1;根据m=nM 知:质量之比与摩尔质量成正比为28:28=1:1;根据阿伏伽德罗定律,相同条件下物质的量相等的气体具有相同的体积,故体积之比为1:1;(3)化学方程式系数的意义:表示物质的量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物质的量练习题
一、选择题(每小题1~2个正确答案)
1、下列关于摩尔质量的说法正确的是()
A、氯气的摩尔质量是71克
B、氯化氢的摩尔质量为g/moL
C、1摩氢气的质量为2克
D、O2的摩尔质量为16 g/moL。
2、对于相同质量的二氧化硫和三氧化硫来说,下列关系正确的是()
A、含氧原子的个数比为2∶3
B、含硫元素的质量比是5∶4
C、含氧元素的质量比为5∶6
D、含硫原子的个数比为1∶1
3、1克氯气含有n个Cl2分子,则阿佛加德罗常数可表示为()
A、71n
B、(1/71)n
C、
D、(1/.n
4、将a g氯化钾溶于水中,恰使K+离子数与水分子数之比为1∶100,则a值为()
A.B.C.39 D.
5、在一定体积的容器中加入mol氙气(Xe)和mol氟气,于400 ℃和2633 kPa压强下加
热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比是()
A.1∶2 B.1∶3 C.1∶4 D.1∶6
6、下列各指定粒子数目不等于阿伏加德罗常数值的是()
A.1 g H2所含的原子个数
B.4 g氦气所含的原子个数
C.23 g金属Na全部转变为金属离子时失去的电子个数
D.16 g O2所含的分子个数
7、过氧化钠与水反应时,氧化剂与还原剂物质的量之比是()
A.1:1 B.1:2 C.2:1 D.2:3
8、设N A表示阿伏加德罗常数,下列说法中正确的是()
A.N A个N2分子和N A个CO分子质量比为1∶1
B.1 mol H2O的质量等于N A个H2O质量的总和
C.在任何条件下1mol H2所含的原子数为N A
D.1 mol H2SO4中所含的粒子数目一定是N A
9、若某氖原子质量是a g,12C的原子质量是b g,N A是阿伏加德罗常数的值,下列说法正
确的是()
A.氖元素的相对原子质量一定是12a/b B.该氖原子的摩尔质量是a N A g C.Wg该氖原子的物质的量一定是W/(a N A)mol D.Wg该氖原子所含质子数是10W/a 10、a mol H2和2a mol氦气具有相同的()
A.分子数B.原子数C.质子数D.质量
11、下列说法错误的是()
A.1 mol任何物质都含有约×1023个原子
B.kg12C约含有×1023个碳原子
C.使用物质的量时,应用化学式指明粒子的种类
D.1mol H2的质量是1g
二、判断正误
1、摩尔是七个物理量之一()
2、摩尔是物质的质量单位()
3、摩尔是物质的数量单位()
4、1摩尔小麦含有×1023个麦粒()
5、3 mol氢()
6、mol NH3( )
7.摩尔是国际科学界建议采用的一种物理量( ) 8.摩尔是物质的量的单位,简称摩,符号为mol ( ) 9.我们把含有约×1023个粒子的任何粒子的集体计量为1摩尔( )
10.1mol氧含×1023个O2( )
三、填空题
1、mol H2SO4的物质的量为_____,所含H+的物质的量为____________.
硫酸根离子的物质的量为__________,所含硫酸分子的数目为_________.
2、1 mol CO和______mol CO2所含氧原子数相等?
3、mol H2O中有________mol原子.
4、mol Al2(SO4)3中含有Al3+mol、SO42-g。
5、8 g氧气为mol;氧气共有mol电子。
6、已知铁的相对原子质量是56,则1个铁原子的质量是g。
7、在60 g碳中,所有碳原子的最外层电子数共为个,质子的总
数为个。
8、某硫酸钠溶液中含有×1022个Na+,则该溶液中SO42-的物质的量是,
该溶液中Na2SO4的质量为克。
9、与16 g氧气所含有分子数相同的氨气是g,与16 g氧气所含原子总数
相同的氨气是g。
10、已知1 mol Al 所含Al原子的个数为阿佛伽德罗常数,那么mol Al 所含Al原子的个数为,2 mol Al 所含Al原子的个数为。
11、×1023个H2O的物质的量为.所含H的物质的量为所含氧原子的物质的量为.
四、计算题
1、g钠溶于多少克水中,才能使每10个H2O分子中溶有一个Na+?
2、某物质中含有×1022个Na+,则Na+ 物质的量为多少?
3、mol O2多少个O原子?
参考答案
二、1、错;2、对;3、错;4、错;5、错;6、对;7、错;8、对;9、对;10、错
三、填空题
1、;3mol;mol;N A
2、;
3、
4、;
5、;
6、56g /N A
7、20N A;30N A 8、;9、;
10、;2N A 11、mol;3 mol;mol
四、解答题
1、g;
2、;
3、5 mol。
