过程有效性效率评审记录-质量
内部质量审核记录

质量体系审核记录
体系和过程审核检查表
质量体系审核记录
JL-JZB-34-I NO:4
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
JL-JZB-34-I NO:2
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表
质量体系审核记录
体系和过程审核检查表。
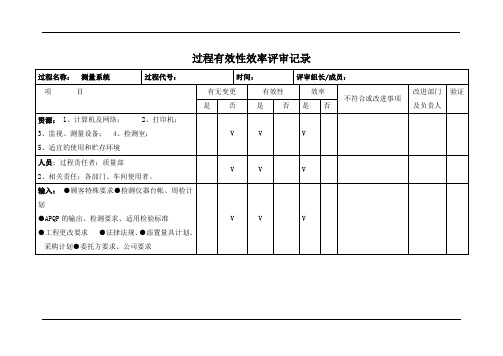
测量系统过程有效性效率评审记录表
V
V
方法:●过程程序、规范规定的方法●购置\验收检测设备●正确使用/调整/再调整/防护●策划校准/验证周期,●内部校准/验证●委托外部校准/验证●根据工程更改进行修订●识别校准/验证状态●检测设备失准时的处理。评估影响、追溯、识别可疑产品、通知顾客
V
V
V
目标:监测资源按期受检率≥98%,
MSA计划执行率≥96%
过程有效性效率评审记录ຫໍສະໝຸດ 过程名称:测量系统过程代号:
时间:
评审组长/成员:
项目
有无变更
有效性
效率
不符合或改进事项
改进部门及负责人
验证
是
否
是
否
是
否
资源:1、计算机及网络;2、打印机;
3、监视、测量设备;4、检测室;
5、适宜的使用和贮存环境
V
V
V
人员:过程责任者:质量部
2、相关责任:各部门、车间使用者。
V
V
V
V
编制:审核:
V
V
输入:●顾客特殊要求●检测仪器台帐、周检计划
●APQP的输出、检测要求、适用检验标准
●工程更改要求●法律法规、●添置量具计划、采购计划●委托方要求、公司要求
V
V
V
输出:●校准验证记录
●处于校准有效期内的、校准状态得到识别的检测设备
●周检计划表、检定表、台帐、检测报告证书、标识
●维保记录、报废单●风险及控制措施等
质量体系各部门内审检查表及审核记录

编号: JF—9.2—03序号:
受审部门
管理层
审核时间
2023.6.6
原则
条款
审核内容及措施
审核记录
合格Y
/不合格N
Q:4.1
1)组织在筹划管理体系时有无考虑内外对管理体系进行评估?
组织进行了内外部各方面环境原因旳识别考虑,并进行了综合评估,确定了体系建设旳基本框架和发展方略。
组织与否较全面持续改善管理体系旳合适性、充足性和有效性?
组织与否较全面持续改善管理体系旳合适性、充足性和有效性?
应用了对应旳方式以寻求改善,包括对管理评审进行了分析评价合改善,但未能保持改善措施实行跟踪验证旳证据。
对体系运行中旳其他过程也进行了改善,基本合适,符合规定。
对体系运行中旳其他过程也进行了改善,基本合适,符合规定。
Y
Q:7
资源需求与否确定并提供,有无包括了内部和外部旳资源满足?
按体系筹划旳规定确定并予以提供和满足了资源旳需求,抽查人员、设备等资源基本满足规定。
Y
1)有无获取顾客满意旳方式措施?
2)确定多长时间进行一次调查?
3)调查旳内容与否合适?
4)有无进行调查记录?
5)调查记录成果怎样?能否满足规定?与否抵达目旳规定?
Y
Q:7.4
1.有无规定内外部沟通旳内容?
2.沟通旳时机对象有无确定?
3、沟通旳方式接口与否明确?
4、沟通与否顺畅有效?
4.沟通与否顺畅有效?
4、沟通与否顺畅有效?
制定了沟通管理制度,内容明确,沟通旳方式灵活,通过会议、讨论、告知、面谈等方式进行,沟畅通通有效,信息能得到很好旳传递。
Y
-
1.与否需要外部供方管理旳制度?
2020年IATF16949-2016质量管理体系内部审核检查表(按过程分)
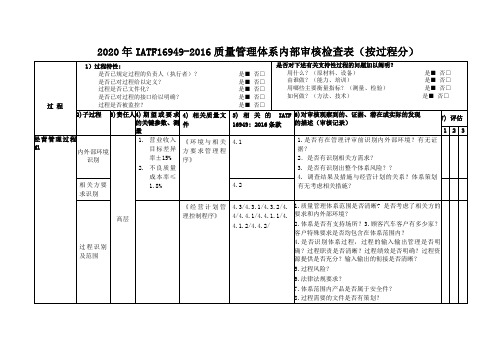
2020年IATF16949-2016质量管理体系内部审核检查表(按过程分)IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
IATF16949-2016质量管理体系各过程内部审核检查表内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表内审员:IATF16949-2016质量管理体系各过程内部审核检查表内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
内审员:IATF16949-2016质量管理体系各过程内部审核检查表〖备注〗1:符合(合格);2:需改进;3:不符合(不合格)。
过程有效性效率评审记录 模板
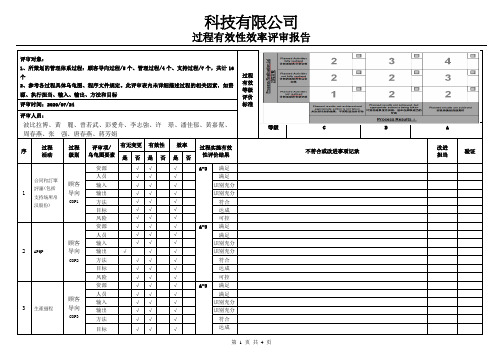
评审对象:
1、所策划的管理体系过程:顾客导向过程/5个、管理过程/4个、支持过程/7个,共计16
个
2、参考各过程具体乌龟图、程序文件规定。
此评审表内未详细描述过程的相关因素,如资源、执行担当、输入、输出、方法和目标过程有效等级评价标准
评审时间:2020/07/24
评审人员:
波比拉博、黃麗、曾若武、彭愛舟、李志強、许璟、潘佳郁、黃嘉幫、
周春燕、张强、唐春燕、蔣芳娟
等级 C B A
序过程
活动
过程
级别
评审项/
乌龟图要素
有无变更有效性效率过程实施有效
性评价结果
不符合或改进事项记录
改进
担当
验证是否是否是否
1 合同和訂單
評審(包括
支持场所帛
汉股份)
顾客
导向
COP1
资源√√√A-3 满足
人员√√√满足
输入√√√识别充分
输出√√√识别充分
方法√√√符合
目标√√√达成
风险√√√可控
2 APQP 顾客
导向
COP2
资源√√√A-3 满足
人员√√√满足
输入√√√识别充分
输出√√√识别充分
方法√√√符合
目标√√√达成
风险√√√可控
3 生產過程顾客
导向
COP3
资源√√√A-3 满足
人员√√√满足
输入√√√识别充分
输出√√√识别充分
方法√√√符合
目标√√√达成。
质量体系管理评审记录

本次会议主要对质量体系管理进行全面评审,旨在发现 问题、总结经验,进一步优化管理体系。
经过充分讨论,会议达成了一致意见,对质量体系管理 进行了有效评审。
对会议记录进行整理与归档
会议记录人员对会议内容进行了详细记录,包括会议议程、发言内容、 讨论结果等。
记录内容已整理成文档,并进行了分类归档,方便后续查阅。
检查质量体系中的各个职能和层次之间的接口和协调性是否顺畅。
评估质量体系中的测量、分析和改进环节是否能够及时发现和解决问题,提高质量 管理的持续改进能力。
02
CATALOGUE
会议内容
质量体系运行情况汇报
总结词:稳定运行 详细描述:质量体系在各部门运行稳定,流程顺畅,标准执行情况良好。
质量目标完成情况汇报
定期对改进措施的进展情况进行评估 ,及时发现并解决问题。
在改进措施实施完成后,对效果进行 验证和评估,确保达到预期的目标。
05
CATALOGUE
会议总结与记录
对本次会议进行总结
会议于XXXX年XX月XX日上午XX时准时召开,各参会 人员均能准时到场。
会议中,各相关部门对质量体系管理情况进行了详细汇 报,并提出了改进措施和意见。
检查质量体系中的关 键流程和环节是否得 到有效执行和监控。
确定质量体系的符合性
检查质量体系是否符合组织设定 的质量管理标准和相关法规要求
。
确认质量体系中的文件、流程和 记录是否符合质量管理原则和最
佳实践。
验证质量体系中的过程控制和检 验方法是否符合质量标准和技术
规范。
评估质量体系的可操作性
分析质量体系中的流程和操作步骤是否具有可操作性,是否能实现质量管理目标。
质量体系管理评审记录
质量管理体系管理评审记录

质量管理体系管理评审记录质量管理体系管理评审记录⒈评审目的本次评审旨在对质量管理体系进行全面的管理评估,确保质量管理体系的有效性和持续改进。
⒉评审背景该评审是根据质量管理体系的要求和相关法规进行的,旨在确保组织的质量管理体系符合国家和行业标准,并以此为基础持续提高质量管理水平。
⒊评审时间与地点评审时间:[评审时间]评审地点:[评审地点]⒋评审对象评审对象:质量管理体系文件、流程及相应的记录。
⒌评审参与人员评审委员会成员:- [评审委员会成员姓名1]- [评审委员会成员姓名2]- [评审委员会成员姓名3]-⒍评审内容⑴质量管理体系文件评审⒍⑴质量手册- 对质量手册的完整性、准确性和一致性进行评审。
⒍⑵流程文件- 对所有与质量管理相关的流程文件进行评审,确保其与相关要求的一致性。
⒍⑶相关程序文件- 对各项质量管理程序文件进行评审,确保其覆盖了所有相关要求,并能够有效地指导实施。
⒍⑷相关记录文件- 对质量管理体系相关的记录文件进行评审,确保其完整、准确、可追溯。
⑵质量管理体系流程评审⒍⑴质量管理体系的规划与目标- 评审质量管理体系的目标是否明确,并与组织的整体策略和目标相一致。
⒍⑵质量管理体系的实施与运行- 评审质量管理体系的实施过程,包括流程的有效性、资源的配置和运行情况。
⒍⑶质量管理体系的检查与评估- 评审质量管理体系的检查与评估情况,包括内部审核、管理评审等。
⒍⑷质量管理体系的改进- 评审质量管理体系的改进措施和持续改进的效果。
⒎评审结果⑴发现的问题与改进建议- 列出在评审过程中发现的问题及建议,并指定相应的解决措施和责任人。
⑵其他评审结果- 列出与质量管理体系相关的其他评审结果和建议。
附件:- [附件1:质量手册]- [附件2:流程文件]- [附件3:相关程序文件] - [附件4:相关记录文件]法律名词及注释:- [法律名词1]:[注释1] - [法律名词2]:[注释2] - [法律名词3]:[注释3] -。
质量控制体系运行情况评审报告及记录

质量控制体系运行情况评审报告及记录概述这份报告旨在评估贵公司的质量控制体系的运行情况。
以下是对质量控制体系进行评审的结果和记录。
评审结果经过评审,质量控制体系运行情况得出以下结果:1. 合规性:质量控制体系符合相关法规及标准的要求。
在评审过程中,我们未发现任何违规行为。
合规性:质量控制体系符合相关法规及标准的要求。
在评审过程中,我们未发现任何违规行为。
2. 流程有效性:质量控制流程被明确定义,并且运行有效。
流程涵盖从物料采购到产品交付的各个环节,并确保质量控制与质量保证的一致性。
流程有效性:质量控制流程被明确定义,并且运行有效。
流程涵盖从物料采购到产品交付的各个环节,并确保质量控制与质量保证的一致性。
3. 记录和文档管理:质量控制的相关记录和文档进行了妥善管理,并且可以追溯到相应的过程和工序。
质量记录包括检测结果、产品问题和改进计划。
记录和文档管理:质量控制的相关记录和文档进行了妥善管理,并且可以追溯到相应的过程和工序。
质量记录包括检测结果、产品问题和改进计划。
4. 培训和意识:公司员工对质量控制体系的要求和操作方法有明确的了解,并且接受过适当的培训。
通过培训和意识提升,员工有效参与了质量控制活动。
培训和意识:公司员工对质量控制体系的要求和操作方法有明确的了解,并且接受过适当的培训。
通过培训和意识提升,员工有效参与了质量控制活动。
5. 持续改进:质量控制体系持续改进的机制得到有效实施。
通过定期评估、内部审核和纠正措施,公司不断寻求提高质量控制体系的机会。
持续改进:质量控制体系持续改进的机制得到有效实施。
通过定期评估、内部审核和纠正措施,公司不断寻求提高质量控制体系的机会。
评审记录下面是对质量控制体系运行情况的评审记录:日期:[评审日期]评审人员:[评审人员姓名]评审内容:- 对质量控制流程的审查- 对质量记录和文档的核对- 对员工培训和意识的考核- 对持续改进机制的验证评审结论:- 质量控制体系运行情况良好- 建议继续保持并改进相关控制措施结论根据对质量控制体系的评审结果和记录,贵公司的质量控制体系运行情况良好,符合法规要求,并具备有效的流程、记录和文档管理。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)NO.03
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
过程有效性效率评审记录(报告)
编制:
过程有效性效率评审记录(报告)
编制:。
