晶体结构练习试题
晶体结构测试题(含答案)

晶体结构测试题(含答案)晶体结构与性质单元测试出题⼈:陈冰测试时间:120分钟可能⽤到的原⼦量:H:1 C;12 N:14 O:16 Na:23第Ⅰ卷(选择题共60分)⼀、选择题(本题包括15⼩题,每⼩题3分,共45分。
每⼩题只有⼀个....选项符合题意。
)1.下列化学式能真实表⽰物质分⼦组成的是A.NaOH B.SO3C.CsCl D.SiO22.下列晶体中不属于原⼦晶体的是A.⼲冰B.⾦刚砂C.⾦刚⽯D.⽔晶3.⽀持固态氨是分⼦晶体的事实是A.氮原⼦不能形成阳离⼦B.铵离⼦不能单独存在C.常温下,氨是⽓态物质D.氨极易溶于⽔4.下列分⼦晶体:①HCl ②HBr ③HI ④CO ⑤N2⑥H2熔沸点由⾼到低的顺序是A.①②③④⑤⑥B.③②①⑤④⑥C.③②①④⑤⑥D.⑥⑤④③②①5.下列的晶体中,化学键种类相同,晶体类型也相同的是A.SO2与SiO2B.CO2与H2OC.NaCl与HCl D.CCl4与KCl6.固体熔化时,必须破坏⾮极性共价键的是A.冰B.晶体硅C.溴D.⼆氧化硅7.当SO3晶体熔化或⽓化时,下述各项中发⽣变化的是A.分⼦内化学键B.核外电⼦总数C.分⼦构型D.分⼦间作⽤⼒8.已知C3N4晶体很可能具有⽐⾦刚⽯更⼤的硬度,且原⼦间均以单键结合,下列关于C3N4晶体的说法正确的是A.C3N4晶体是分⼦晶体B.C3N4晶体中,C-N键的键长⽐⾦刚⽯中的C-C键的键长要长C.C3N4晶体中每个C原⼦连接4个N原⼦,⽽每个N原⼦连接3个C原⼦D.C3N4晶体中微粒间通过离⼦键结合9.下列各项所述的数字不是6的是A.在NaCl晶体中,与⼀个Na+最近的且距离相等的Cl- 的个数B.在⾦刚⽯晶体中,最⼩的环上的碳原⼦个数C.在⼆氧化硅晶体中,最⼩的环上的原⼦个数D.在⽯墨晶体的⽚层结构中,最⼩的环上的碳原⼦个数10.六氟化硫分⼦呈正⼋⾯体,难以⽔解,在⾼电压下仍有良好的绝缘性,在电器⼯业有着⼴泛⽤途,但逸散到空⽓中会引起强温室效应。
晶体结构与性质练习题

晶体结构与性质练习题晶体是由一定的周期性排列的原子、分子或离子组成的固体物质。
晶体的结构与性质有着密切的联系,不同的晶体结构会导致不同的晶体性质。
为了帮助大家更好地理解晶体结构与性质之间的关系,下面将提供一些练习题,供大家进行学习和思考。
题目一:简单晶体结构1. 以NaCl为例,简述其晶体结构的特点。
2. 请说出以下晶体中的阴离子和阳离子:CaF2、K2SO4、MgO。
3. 解释为什么NaCl和KCl的晶体结构相似,但是它们的性质却有所不同。
题目二:晶体缺陷1. 什么是点缺陷?举例说明。
2. 简述晶体中的位错缺陷以及其对晶体性质的影响。
3. 解释为什么金刚石可以成为优质的宝石。
题目三:晶体的导电性1. 解释为什么金属晶体具有良好的导电性。
2. 什么是半导体晶体?举例说明其应用。
3. 简述离子晶体的导电性及其应用。
题目四:晶体的光学性质1. 什么是吸收谱和荧光谱?它们对于研究晶体结构和性质有何意义?2. 简述偏光现象产生的原因以及其应用。
3. 解释为什么金属外观呈现出不同的颜色。
题目五:晶体的热学性质1. 解释晶体的热膨胀现象及其原理。
2. 简述晶体的热导性质以及其在热散热领域的应用。
3. 解释为什么铁磁性晶体具有自发磁化特性。
题目六:晶体的力学性质1. 解释为什么晶体呈现出不同的硬度。
2. 简述晶体的弹性性质以及其应用。
3. 什么是形状记忆合金?简述其工业应用。
以上是晶体结构与性质练习题,希望能够帮助大家加深对晶体结构与性质之间关系的理解。
通过思考与学习这些问题,相信大家能够更好地掌握晶体学知识,并在实际应用中发挥自己的才能。
祝你们学习进步!。
高中化学晶体结构与性质练习题(含解析)

高中化学晶体结构与性质练习题学校:___________姓名:___________班级:_____________一、单选题1.下列关于晶体的结构,粒子间的相互作用的说法,正确的是()A.分子晶体中只存在范德华力B.离子晶体中只存在离子键C.共价晶体中都存在极性键D.金属晶体中只存在金属键2.某晶体的一部分如图所示,这种晶体中A、B、C三种微粒数之比是()A.3:9:4 B.1:4:2 C.2:9:4 D.3:8:5 3.下列各组物质的晶体中,化学键类型和晶体类型均相同的是()A.NH3和NH4Cl B.HCl和H2OC.KCl和K D.CO2和SiO24.电子表、电子计算器、电脑显示器都运用了液晶材料显示图象和文字。
有关其显示原理的叙述中,正确的是()A.施加电压时,液晶分子沿垂直于电场方向排列B.移去电压后,液晶分子恢复到原来状态C.施加电场时,液晶分子恢复到原来状态D.移去电场后,液晶分子沿电场方向排列5.下列物质的晶体类型与其他几个不同的是()A.Na2S B.MgCl2C.AlCl3D.Al2O36.下列说法中,错误的是()A.只含分子的晶体一定是分子晶体B.碘晶体升华时破坏了共价键C.几乎所有的酸都属于分子晶体D.稀有气体中只含原子,但稀有气体的晶体属于分子晶体7.美国某杂志曾经报道:在40 GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,有关原子晶体干冰的推断错误的是()A.有很高的熔点和沸点B.易汽化,可用作制冷材料C.含有极性共价键D.硬度大,可用作耐磨材料8.化学用语是学习化学的工具和基础。
下列有关化学用语的说法或使用正确的是A.稀有气体的晶体,其组成微粒是原子,晶体中不存在分子间作用力B.核素C—12的原子组成符号为C,二氧化碳分子的结构式为O=C=OC.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2OD.表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-571.6KJ/mol 9.铁元素形成的单质有三种晶胞的结构,如图所示,则下列说法正确的是()A.铁元素基态原子M层上有8对成对电子BC.三种晶胞α、β、θ中铁原子的配位数之比为4:6:3D.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体结构相同10.下列说法正确的是()A.晶体一般都是透明的B.金刚石属于混合型晶体C.区分晶体和非晶体最可靠的科学方法是对固体进行X射线衍射实验D.在[Cu(NH3)4]2+配离子中NH3与中心离子Cu2+结合的化学键是非极性键11.金属钛(Ti)与氮形成的某种化合物常被用作高温结构材料和超导材料。
【化学奥赛】晶体结构习题new!
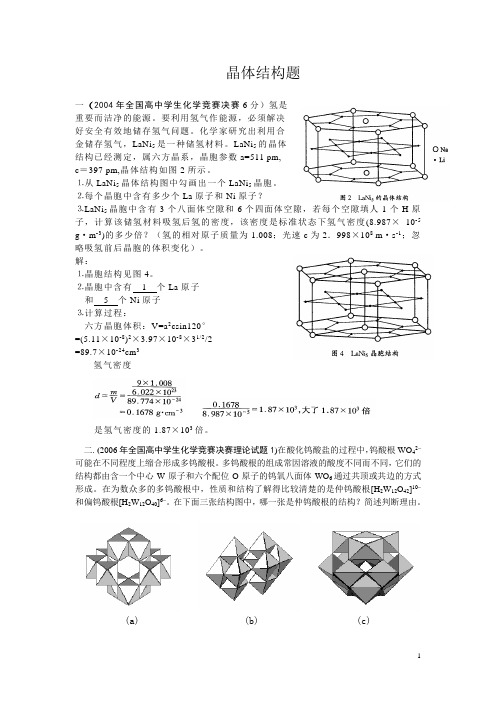
晶体结构题一(2004年全国高中学生化学竞赛决赛6分)氢是重要而洁净的能源。
要利用氢气作能源,必须解决好安全有效地储存氢气问题。
化学家研究出利用合金储存氢气,LaNi5是一种储氢材料。
LaNi5的晶体结构已经测定,属六方晶系,晶胞参数a=511 pm,c=397 pm,晶体结构如图2所示。
⒈从LaNi5晶体结构图中勾画出一个LaNi5晶胞。
⒉每个晶胞中含有多少个La原子和Ni原子?⒊LaNi5晶胞中含有3个八面体空隙和6个四面体空隙,若每个空隙填人1个H原子,计算该储氢材料吸氢后氢的密度,该密度是标准状态下氢气密度(8.987×10-5 g·m-3)的多少倍?(氢的相对原子质量为1.008;光速c为2.998×108 m·s-1;忽略吸氢前后晶胞的体积变化)。
解:⒈晶胞结构见图4。
⒉晶胞中含有1个La原子和5个Ni原子⒊计算过程:六方晶胞体积:V=a2csin120°=(5.11×10-8)2×3.97×10-8×31/2/2=89.7×10-24cm3氢气密度是氢气密度的1.87×103倍。
二. (2006年全国高中学生化学竞赛决赛理论试题1)在酸化钨酸盐的过程中,钨酸根WO42-可能在不同程度上缩合形成多钨酸根。
多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含一个中心W原子和六个配位O原子的钨氧八面体WO6通过共顶或共边的方式形成。
在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2W12O40]6-。
在下面三张结构图中,哪一张是仲钨酸根的结构?简述判断理由。
(a) (b) (c)解:提示:考察八面体的投影图,可以得到更清楚地认识。
三.(2006年全国高中学生化学竞赛决赛理论试题4)轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,它的生产以白云石(主要成分是碳酸镁钙)为原料。
全国高中生化学竞赛试题2 晶体结构(答案)

晶体结构答案第1题(6分)所有原子都是Mg (得3分)所有原子都是O (得3分)画更多原子者仍应有正确几何关系。
第2题(5分)2-1MgB 2(2分)(注:给出最简式才得分)2-2或a =b ≠c ,c 轴向上(3分)(注:任何能准确表达出Mg :B =1:2的晶胞都得满分,但所取晶胞应满足晶胞是晶体微观空间基本平移单位的定义,例如晶胞的顶角应完全相同等。
)第3题(10分)3-1①12②2③钠(各1分,共3分)3-2晶胞体积V =[2×(116pm +167pm)]3=181×106pm 3离子体积v =4×43π(116pm)3+4×43π(167pm)3=104×106pm 3v /V =57.5%(1分)(有效数字错误扣1分,V 和v 的计算结果可取4位,其中最后1位为保留数字,不扣分。
)3-3表面原子为8(顶角)+6(面心)+12(棱中心)=26总原子数为8(顶角)+6(面心)+12(棱中心)+1(体心)=27表面原子占总原子数26/27×100%=96%(1分)注:26和27均为整数值,比值26/27是循环小数0.962,取多少位小数需根据实际应用而定,本题未明确应用场合,无论应试者给出多少位数字都应按正确结果论。
3-4计算分两个步骤:步骤一:计算表面原子数。
可用n =2、3的晶胞聚合体建立模型,得出计算公式,用以计算n =10。
例如,计算公式为:[8]+[(n -1)×12]+[n ×12]+[(n -1)2×6]+[n 2×6]+[(n -1)×n ×2×6]顶角棱上棱交点棱上棱心面上棱交点面上面心面上棱心n =10,表面原子总数为2402(2分)步骤二:计算晶胞聚合体总原子数n 3×8+[8]×7/8+[(n -1)×12]×3/4+[n ×12]×3/4+[(n -1)2×6]/2+[n 2×6]/2+[(n -1)×n ×2×6]/2=8000+7+81+90+243+300+540=9261(2分)表面原子占总原子数的百分数:(2402/9261)×100%=26%(1分)(注:本题计算较复杂(还有更简单的计算方法),若应试者用其他方法估算得出的数值在26%左右2个百分点以内可得3分,3个百分点以内可得2分,其估算公式可不同于标准答案,但其运算应无误。
人教版高中化学选修3第三章《 晶体结构与性质》测试题(含答案)

第三章《晶体结构与性质》测试题一、单选题1.下列有关晶体的说法中正确的是A.某晶体固态不导电,水溶液能导电说明该晶体是离子晶体B.原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力C.区分晶体和非晶体最科学的方法是对固体进行X﹣射线衍射实验D.任何晶体中,若含有阳离子也一定含有阴离子2.下列每组物质发生所述变化克服的作用属于同种类型的是()A.氯化铝和干冰升华B.钠和硫熔化C.食盐和氯化氢溶解于水D.二氧化硅和二氧化硫熔化3.对于氯化钠晶体,下列描述正确的是A.它是六方紧密堆积的一个例子B.58.5 g氯化钠晶体中约含6.02×1023个NaCl分子C.与氯化铯晶体结构相同D.每个Na+与6个Cl-作为近邻4.碳化硅(SiC)常用于电炉的耐火材料。
关于SiC说法正确的是A.易挥发B.能导电C.熔化时破坏共价键D.属于分子晶体5.下面有关晶体的叙述中,不正确的是A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子B.氯化钠晶体中,每个Na+周围距离相等且紧邻的Na+共有6个C.在冰中,每1molH2O分子形成2mol氢键D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子6.下列各组物质中,化学键类型相同,晶体类型也相同的是()A.C(金刚石)和CO2B.CH4和H2O C.NaBr和HBr D.Cl2和KCl 7.磷化硼是一种超硬耐磨涂层材料。
如图为其晶体结构中最小的重复单元。
下列有关说法正确的是B PA.磷化硼的化学式为2B.磷化硼晶体的熔点高,且熔融状态下能导电C.磷化硼晶体属于共价晶体D.磷化硼晶体在熔化时需克服范德华力8.下列各组顺序的排列错误的是A.半径:F—>Na+>Mg2+>Al3+B.沸点:H2O<H2S<H2SeC.酸性:HClO4>H2SO4>H3PO4D.熔点:SiO2>NaCl>CO29.北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。
奥赛晶体结构试题
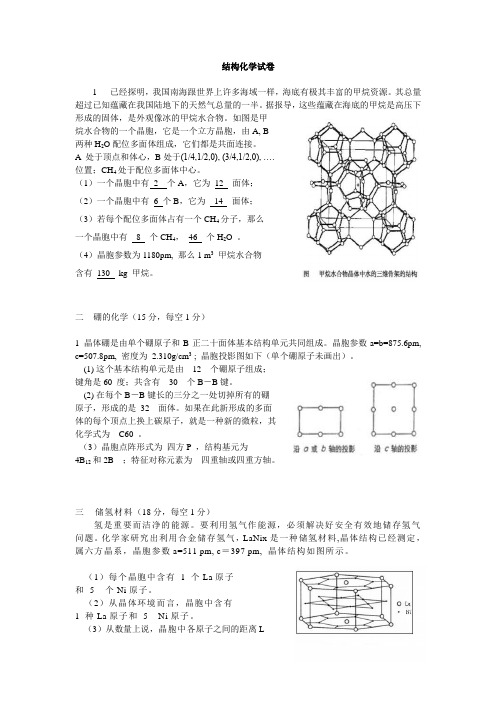
结构化学试卷1 已经探明,我国南海跟世界上许多海域一样,海底有极其丰富的甲烷资源。
其总量超过已知蕴藏在我国陆地下的天然气总量的一半。
据报导,这些蕴藏在海底的甲烷是高压下形成的固体,是外观像冰的甲烷水合物。
如图是甲烷水合物的一个晶胞,它是一个立方晶胞,由A, B两种H2O配位多面体组成,它们都是共面连接。
A 处于顶点和体心,B处于(1/4,1/2,0), (3/4,1/2,0), ….位置;CH4处于配位多面体中心。
(1)一个晶胞中有2 个A,它为12 面体;(2)一个晶胞中有6 个B,它为14 面体;(3)若每个配位多面体占有一个CH4分子,那么一个晶胞中有8 个CH4,46 个H2O 。
(4)晶胞参数为1180pm, 那么1 m3甲烷水合物含有130 kg 甲烷。
二硼的化学(15分,每空1分)1 晶体硼是由单个硼原子和B正二十面体基本结构单元共同组成。
晶胞参数a=b=875.6pm, c=507.8pm, 密度为2.310g/cm3 ; 晶胞投影图如下(单个硼原子未画出)。
(1) 这个基本结构单元是由12 个硼原子组成;键角是60 度;共含有30 个B-B键。
(2) 在每个B-B键长的三分之一处切掉所有的硼原子,形成的是32 面体。
如果在此新形成的多面体的每个顶点上换上碳原子,就是一种新的微粒,其化学式为C60 。
(3)晶胞点阵形式为四方P ,结构基元为4B12和2B ;特征对称元素为四重轴或四重方轴。
三储氢材料(18分,每空1分)氢是重要而洁净的能源。
要利用氢气作能源,必须解决好安全有效地储存氢气问题。
化学家研究出利用合金储存氢气,LaNix是一种储氢材料,晶体结构已经测定,属六方晶系,晶胞参数a=511 pm, c=397 pm, 晶体结构如图所示。
(1)每个晶胞中含有 1 个La原子和 5 个Ni原子。
(2)从晶体环境而言,晶胞中含有1 种La原子和 5 Ni原子。
(3)从数量上说,晶胞中各原子之间的距离L共有8 种;最小的L La-La值为397pm ; 最小的L La-Ni值为295.03pm ;最小的L Ni-Ni值为226.19pm ;。
固体物理 第一章 晶体结构习题

第一章晶体结构1.试述晶态、非晶态、准晶、多晶和单晶的特征性质。
解:晶态固体材料中的原子有规律的周期性排列,或称为长程有序。
非晶态固体材料中的原子不是长程有序地排列,但在几个原子的范围内保持着有序性,或称为短程有序。
准晶态是介于晶态和非晶态之间的固体材料,其特点是原子有序排列,但不具有平移周期性。
另外,晶体又分为单晶体和多晶体:整块晶体内原子排列的规律完全一致的晶体称为单晶体;而多晶体则是由许多取向不同的单晶体颗粒无规则堆积而成的。
2.晶格点阵与实际晶体有何区别和联系?解:晶体点阵是一种数学抽象,其中的格点代表基元中某个原子的位置或基元质心的位置,也可以是基元中任意一个等价的点。
当晶格点阵中的格点被具体的基元代替后才形成实际的晶体结构。
晶格点阵与实际晶体结构的关系可总结为:晶格点阵+基元=实际晶体结构3.晶体结构可分为Bravais格子和复式格子吗?解:晶体结构可以分为Bravais格子和复式格子,当基元只含一个原子时,每个原子的周围情况完全相同,格点就代表该原子,这种晶体结构就称为简单格子或Bravais格子;当基元包含2个或2个以上的原子时,各基元中相应的原子组成与格点相同的网格,这些格子相互错开一定距离套构在一起,这类晶体结构叫做复式格子。
解:(a)“面心+体心”立方不是布喇菲格子。
从“面心+体心”立方体的任一顶角上的格点看,与它最邻近的有12个格点;从面心任一点看来,与它最邻近的也是12个格点;但是从体心那点来看,与它最邻近的有6个格点,所以顶角、面心的格点与体心的格点所处的几何环境不同,即不满足所有格点完全等价的条件,因此不是布喇菲格子,而是复式格子,此复式格子属于简立方布喇菲格子。
(b)“边心”立方不是布喇菲格子。
从“边心”立方体竖直边心任一点来看,与它最邻近的点子有八个;从“边心”立方体水平边心任一点来看,与它最邻近的点子也有八个。
虽然两者最邻近的点数相同,距离相等,但他们各自具有不同的排列。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
解答
1 、 晶 胞 图 中 , CH4 被 包 含 在 五 角 十 二 面 体 〔512〕 和十四面体〔51262〕中,五角十二面体位于顶角和 体心,所以共包含2个;十四面体有共包含六个。 所以答案:8CH4·46H2O(n=8)
2、按晶体的理想组成和晶胞参数,可算得晶胞体积V和晶 胞中包含CH4的物质的量n(CH4): V=a3=(1180pm)3=1.64×103pm3=1.64×10-27m3
键长为:
15c350p5m 18p9m 8 8
练习题六
(2003江苏选拔赛)甲烷水合物(nCH4·46H2O)是一种具 有重要经济价值的化合物,在海洋深处蕴藏量非常大,是 未来的重要能源之一。它的晶体结构可看作由五角十二面 体〔512〕和十四面体〔51262〕共面连接堆积形成。在立方晶 胞中,〔512〕的中心处在顶角和体心位置;〔51262〕中心位 置在面上,坐标为(1/4,1/2,0)、(3/4,1/2,0)、(0, 1/4,1/2)、(0,3/4,1/2)、(1/2,0,1/4)、(1/2,0, 3/4)计6个。它们彼此共用六角形面连成柱体,再和五角十 二面体共面连接。右图所示出甲烷水合物中水骨架的结构。
晶体结构练习题
练习题一
题目:研究离子晶体,常考察以一个离子 为中心时,其周围不同距离的离子对它的 吸引或排斥的静电作用力。设氯化钠晶体 中钠离子跟离它最近的氯离子之间的距离 为d,以钠离子为中心,则: [1]第二层离子有 12 个,离中心离子的距 离为 2d ,它们是 钠 离子。
[2]已知在晶体中Na+离子的半径为116pm,CI-离 子的半径为167pm,它们在晶体中是紧密接触的。 求离子占据整个晶体空间的百分数。
n(CH4)==1.33×10-23mol 1m3甲烷水合物晶体中含CH4的物质的量为: n=×1.33×10-23mol=8.11×103mol 它 相 当 于 标 准 状 态 下 的 甲 烷 气 体 V = 8.11×103×22.4m3 = 182m3
3、文献报导值比实际值小,说明甲烷分子在笼 形多面体中并未完全充满,即由于它的晶体中 CH4没有达到理想的全充满的结构。
2 ,1 ,1 338
。
(1) 按比例画出SiC六方晶胞;
(2)每个晶胞中含有SiC
个。
(3)晶体中Si的堆积型式是
பைடு நூலகம்
。
C填充的空隙类型是
。
(4)列式计算C—Si键长。
解答
(1)SiC六方晶胞
解答
(2)每个晶胞中含有2个SiC。 (3)Si原子作六方最密堆积,C原子填
充在Si围成的四面体空隙中。 (4)由(1)中晶胞图可以看出,Si-C
实际上甲烷水合物晶体结构形成时,并不要求 〔512〕全部都充满CH4分子,它的实际组成往 往介于6CH4·46H2O和8CH4·46H2O之间。
解答
1、
解答
2.晶胞中含有1个La原子和5个Ni原子。 3.计算过程: 六 方 晶 胞 体 积 : V = a2csin120° = (5.11×10-8)2 ×3.97×10-8×31/2/2=89.7×10-24cm3
dV m 9 1 .8 0.7 9 0 6 7 .0 1 8 4 2 2 0 1 42 2 0 3 0 .16 gc 7 m 3
硼化镁的晶体结构投影图
由图5—l可确定硼化镁的化学式为: 画出硼化镁的一个晶胞的透视图,标出该 晶胞内面、棱、顶角上可能存在的所有硼 原子和镁原子(镁原子用大白球,硼原子 用小黑球表示)。
[1] MgB2 [2]
解答
无 厘 头 幽 默的 搞笑个 性句子 1、 数 学 老 师带我 们遨游 在知识的海洋,他上 岸 了,我 们却溺 死在海 里 2、睢这 长相, 肯定你 妈生你 的时候 着急了 。 3、 你 穿 的 那 么 清爽, 长得那 么败火 。 4、 不 以 淫 荡惊 天下, 就以风骚动世人!问 世 间 谁 最 风 骚、直 叫我当 仁不让 ! 5、 你 这 破 相, 严重的 影响了我这一天的心 情 。 6、 古 人 云 ,鲜花 插在牛 粪上, 是因为 牛粪养 料极高 。 7、 无 论 你 是 怎 样 转 身 的 ,你的 眼睛始 终在你 的前面 。 8、 人 生 就 像打 电话,不是你先挂, 就 是我先 挂 9、世界 是我们 的,也 是儿子 们的, 但最终 是那帮 孙子的 。 10、 我 视 金 钱 如 粪土我 爸视我 为化粪 池。 11、 做 一 个 吃货无 忧无虑 ,当一 个痴货 无 牵 无 挂 。 12、 你 肺 活 量是 多少啊 ,能把 牛B吹 的这么 大。 13、 原 谅 你 是 上 帝 的 事 ,我所 能做的 就是送 你去见 上帝。 14、 为 什 么 我看 了那么 久都看 不 懂 你 的 心 ?因为 。我近 视。 15、 露 出 半 个屁股 不代表 你性感 ,只能 说明你 内 裤 买 小 了 16、 你 跟 我 装逼 ,只是 因为你 没逼而 已,你 跟我装 纯,只 是因为 你 不 纯 罢 了 。 17、 山 外 青 山 楼外楼 ,你不 爱我我 不愁; 世上美 女多的 是,她
解答
[1] 12, 2d ,钠离子 [2] V晶胞=[2(116pm+167pm)]3=181 106pm3
V离子=4 (4/3)(116pm)3+ 4 (4/3)(167pm)3 =104106 pm3
V离子/ V晶胞=57.5%
练习题二
(2001年省级赛区试题)
题目:今年3月发现硼化镁在39K呈超导性, 可 能是人类对超导认识的新里程碑。在硼化镁晶体 的理想模型中,镁原子和硼原子是分层排布的, 像维夫饼干,一层镁一层硼地相间,图5—l是该 晶体微观空间中取出的部分原于沿C轴方向的投 影,白球是镁原子投影,黑球是硼原子投影,图 中的硼原子和镁原子投影在同一平面上。
1、CH4分子由于体积较小,可包合在这两种多面体中,若 全部充满时,确定晶胞的组成为(即n值)。
2、已知该晶胞参数a=1180pm,计算1m3甲烷水合物晶体中 可释放CH4的体积(标准状况下)。 3、有的文献中报导开采1m3的甲烷水合物晶体可得到164m3 的甲烷气体,请根据2的结果给出一合理解释。
是氢气密度的1.87×103倍。
练习题五
题目:SiC具有高硬度、高耐磨性、高耐腐蚀
性及较高的高温强度等特点,已成为一种重要
的工程材料。其晶体具有六方ZnS型结构,晶
胞参数为a=308pm,c=505pm,已知C原子的分
数坐标为0,0,0和 2 , 1 , 1 ;Si原子的分数坐
332
标为 0 ,0 , 5 和 8
会 比 你 更 温 柔! 18、 现 在 什 么时代 ,杂乱 无章, 猛然一
练习题三
练习题四
题目:氢是重要而洁净的能源。要利用氢 气作能源,必须解决好安全有效地储存氢 气问题。化学家研究出利用合金储存氢气, LaNi5是一种储氢材料。LaNi5的晶体结构已 经测定,属六方晶系,晶胞参数a=511pm, c=397pm, 晶体结构如图所示:
LaNi5晶体结构图
O La ● Ni
1.从LaNi5晶体结构图中勾画出一个LaNi5晶胞。 2.每个晶胞中含有多少个La原子和Ni原子?
3.LaNi5晶胞中含有3个八面体空隙和6个四面体空隙, 若每个空隙填入1个H原子,计算该储氢材料吸氢后氢的 密度,该密度是标准状态下氢气密度(8.98710-5g·cm-3) 的 多 少 倍 ? ( 氢 的 相 对 原 子 质 量 为 1.008 ; 光 速 c 为 2.998×108m·s-1;忽略吸氢前后晶胞的体积变化)。
