第02章 热力学第一定律作业
第二章 热力学第一定律

第二章 热力学第一定律英文习题1. Cooling of a hot fluid in a tankA rigid tank contains a hot fluid that is cooled while being stirred by apaddle wheel. Initially, the internal energy of the fluid is 800 kJ. During the cooling process, the fluid loses 500 kJ of heat, and the paddle wheel does 100 kJ of work on the fluid. Determine the final internal energy of the fluid. Neglect the energy stored in the paddlewheel.2. Heating of a gas by a resistance heaterA piston-cylinder device initially contains 0.5 m 3of nitrogen gas at 400 kPa and 27℃. An electric heater within the device is turned on and is allowed to pass a current of 2 A for 5 min from a 120-V source. Nitrogen expands at constant pressure, and a heat loss of 2800 J occursduring the process. Determine the final temperature of nitrogen.3. Cooling of an iron block by watercontains 0.5 A 50-kg iron block at 80℃ is dropped into an insulated tanks that equilibriumm 3of liquid water at 25℃. Determine the temperature when thermal is reached.4. Deceleration of air in a diffuserAir at 10℃ and 80 kPa enter the diffuser of a jet engine steadily with a velocity of 200 m/s. The inlet area of the diffuser is 0.4 m 2. The air leaves the diffuser with a velocity that isvery small compared with the inlet velocity. Determine (a) themass flow rate of the air and (b) the temperature of the air leaving the diffuser.5. Energy balance in turbineConsider a gas turbine power plant with air as the working fluid, Air enters at 100 kPa, 20ºC (ρ=1.19 kg/m 3), with a velocity of 130m/s through an opening 0.112 m 2cross-sectional area. After being compressed, heated and expanded through a turbine, the air leaves at 180 kPa, 150ºC (ρ=1.48 kg/m 3), through an opening of 0.100 m 2cross-sectional area. The power output of the plant is 375 kW. The internal energy and enthalpy of the air are given in kJ/kg byU=0.717T and h=1.004T, where T istemperature on the Kelvin scale. Determine the net amountofheatadded tothe air in kJ/kg.FIGURE 2-1FIGURE 2-2FIGURE 2-3FIGURE 2-42113111112.0/130/19.120100mA s m c m k g CT k Pa p f ===︒==ρ2112WsQ223222100.0/48.1150180m A m kg CT kPap ==︒==ρFIGURE 2-56. Air is compressed in a frictionless steady-flow processAir is compressed in a frictionless steady-flow process from 90 kPa, 150ºC (v=0.918 m 3/kg) to 130 kPa in such a manner that p(v+0.250)=constant, where v is in m 3/kg, inlet velocity is negligible small, and discharge velocity is 110 m/s. Calculate the work required per kilogram of air.7. Mixture processA mixture of air and water vapor with an enthalpy of 120 kJ/kg enters the dehumidifying section of an air-conditioning system at a rate of 320 kg/hr, liquid water drains out of the dehumidifier with an enthalpy of 42 kJ/kg at a rate of 7.0 kg/hr. An air vapor mixture leaves with an enthalpy of 47 kJ/kg.Determine the rate of heat removal from the fluids passing through the dehumidifier.8. Reviews problemA piston-cylinder device contains helium gas initially at 150 kPa, 20℃, and0.5 m 3. The helium is now compressed in a polytropic process (PV n=constant) to 400 kPa and 140℃. Determine the heat loss or gainduring this process.9. Two rigid tanks are connected by a valve. Tank Acontains 0.2 m 3of water at 400 kPa and 80 percent quality. Tank B contains 0.5 m 3of water at 200 kPa and 250℃. The valve is now opened, and the two tanks eventually come to the same state. Determine the pressure and the amount of heat transfer whenthe system reaches thermal equilibrium with the surrounding at 25 ℃.10. Consider a well-insulated horizontal rigid cylinder that isdividedm m 112233dehumidifierkgkJ h hrkg /126/32011==∙kgkJ h hr kg /42/0.722==∙kgkJ h /473=FIGURE 2-7FIGURE 2-8W in1122/918.0901311===f c kg m v kPa p sm c kPa p f /11013022==FIGURE 2-6FIGURE 2-9FIGURE 2-10into two compartments by a piston that is free to move but does not allow either gas to leak into the other side. Initially, one side of the piston contains 1 m 3of N 2 gas at 500 kPa and 80℃ while the other side contains 1 m 3of He gas at 500 kPa and 25℃. Now thermal equilibrium is established in the cylinder as a result of heat transfer through the piston. Using constant specific heats at room temperature, determine the final equilibrium temperature in the cylinder. What would your answer be if the piston were not free to move?工程热力学与传热学第二章 热力学第一定律 习题1. 一绝热刚性容器,中间用隔板分为两部分,左边盛有空气,右边为真空,抽掉搁板,空气将充满整个容器。
《物理化学》第二章热力学第一定律练习题(含答案)

《物理化学》第二章热力学第一定律练习题(含答案)第二章练习1,填入1,根据系统与环境之间的能量和物质交换,系统可分为,,2,强度性质显示了体系的特征,与物质的量无关。
容量属性体现了系统的特征,它与物质的数量有关,具有性别。
3年,热力学平衡态同时达到四种平衡,即,,,4,系统状态改变称为进程常见的过程有、、、和,5.从统计热力学的观点来看,功的微观本质是热的微观本质6,每种气体的真空膨胀功w = 0.7,在绝热钢瓶内的化学反应△ u = 0.8,焓定义为2.真或假:1。
当系统的状态不变时,所有状态函数都有一定的值(√) 2。
当系统的状态改变时,所有状态函数的值也相应地改变。
(χ) 3。
因为=δH和=δU,所以和都是状态函数(χ)4,密闭系统在恒压过程中吸收的热量等于系统的焓(χ)误差只有当封闭系统不做非膨胀功等压过程δH = QP5且状态被给定时,状态函数才有固定值;在状态函数被确定之后,状态也被确定(√) 6。
热力学过程中的W值由具体过程(√)7和1摩尔理想气体从同一初始状态经过不同的循环路径后返回初始状态决定,其热力学能量保持不变(√) 3。
单一主题1。
系统中的以下几组物理量都是状态函数:(C) A,T,P,V,Q B,M,W,P,H C,T,P,V,N,D,T,P,U,W2,对于内能是系统的单值函数的概念,误解是(C)系统A处于某一状态,某一内能B对应于某一状态,内能只能有一个值,不能有两个以上的值c的状态改变,内部能量也必须随着对应于内部能量值的d而改变。
可以有多种状态3以下语句不具有状态函数的特征:(d)当系统A的状态确定后状态函数值也确定时,状态函数值的变化值只由系统C的恒定状态通过循环过程来确定。
状态函数值是常数。
D态函数的可加性为4。
在下面的描述中正确的是(a)A物体的温度越高,它的内能越大,B物体的温度越高,它包含的热量越多。
当系统温度升高时,一定是它吸收了热量。
当系统温度恒定时,解释它既不吸热也不放热。
第二章 热力学第一定律自测题资料讲解

第二章热力学第一定律自测题一、选择题1.物质的量为n的理想气体,该气体的下列物理量中,其值确定后,其他状态函数方有定值的是()。
(a) p(b) V(c) T, U(d) T, p2.有一真空绝热瓶子,通过阀门和大气相隔。
当阀门打开时,大气(视为理想气体)进入瓶内,此时瓶内气体的温度将()。
(a) 升高(b) 降低(c) 不变(d) 不确定3.公式 H=Q p适用于下列过程中的()。
(a) 理想气体从1013.25kPa反抗恒定的外压101.325kPa膨胀(b) 273K,101.325kPa下冰融化成水(c) 298K,101.325kPa下电解CuSO4水溶液(d) 气体从状态Ⅰ等温可逆变化到状态Ⅱ4.反应C(金刚石) + 0.5O2(g)—CO(g)的热效应为△rHmθ,问此△rHmθ值为()A CO(g) 的生成焓B C(金刚石)的燃烧焓C C的燃烧焓D 全不是5.对于一定量的理想气体,有可能发生的过程是()。
(1)对外做功且放出热量(2)恒容绝热升温、无非膨胀功(3)恒压绝热膨胀(4)恒温绝热膨胀(a) (1),(4) (b) (2),(3) (c) (3),(4) (d) (1),(2) 6.实际气体经节流膨胀后,( )。
(a) Q <0, ∆H =0, ∆p <0 (b) Q =0, ∆H =0, ∆T <0 (c) Q =0, ∆H <0, ∆p <0 (d) Q =0, ∆H =0, ∆p <07.某气体的状态方程为pV m =RT +bp (b 为大于零的常数),此气体向真空绝热膨胀后的温度将( )。
(a) 不变 (b) 上升 (c) 下降 (d) 不确定 8.根据定义等压膨胀系数pT V V ⎪⎭⎫⎝⎛∂∂=1α,等容压力系数V T p p ⎪⎭⎫⎝⎛∂∂=1β,等温压缩系数Tp V V ⎪⎪⎭⎫⎝⎛∂∂-=1κ。
α,β,κ 三者间的关系为( )。
第二章 热力学第一定律自测题

第二章热力学第一定律自测题与答案. I选择题1.物质的量为n的纯理想气体,该气体的下列物理量中,其值确定后,其他状态函数方有定值打得是(d)。
(a)p(b)V (c)T,U (d)T,p2.有一真空绝热瓶子,通过阀门和大气相隔。
当阀门打开时,大气(视为理想气体)进入瓶内,此时瓶内气体的温度将(a)。
(a)升高(b)降低(c)不变(d)不确定3.公式∆H=Q p适用于下列过程中的(b)。
(a)理想气体从1013.25 kPa反抗很定的外压101.325 kPa膨胀(b)273 K,1013.25 kPa下冰融化成水(c)298 K,下电解CuSO4水溶液(d)气体从状态I等温可逆变化到状态II4.可逆机的效率为η,冷冻机的冷冻系数为β,则β和η的数值满足(d)。
(a)η<1,β<1 (a)η<1,β<1(a)η<1,β>1 (a)η<1,β可能小于、等于或大于15.对于一定量的理想气体,有可能发生的过程是(a)。
(1)对外做功且放出热量(2)很容绝热升温、无非膨胀功(3)恒压绝热膨胀(4)恒温绝热膨胀(a)(1),(4)(b)(2),(3)(c)(3),(4)(d)(1),(2)6.实际气体经节流膨胀后,(d)。
(a)Q<0,∆H=0,∆p<0(a)Q=0,∆H=0,∆T<0(a)Q=0,∆H<0,∆p<0(a)Q=0,∆H=0,∆p<07.某气体的状态方程为pV m=RT+bp(b为大于零的常数)。
此气体向真空绝热膨胀后的温度将(a)。
(a)升高(b)降低(c)不变(d)不确定8.根据定义:等压膨胀系数1=pVV Tα∂⎛⎫⎪∂⎝⎭,等容压力系数1=Vpp Tβ∂⎛⎫⎪∂⎝⎭,等温压缩系数1=TVV pκ⎛⎫∂⎪∂⎝⎭。
,,αβκ三者间的关系为(d)。
(a)α⋅β=p⋅κ(b)α⋅β⋅κ=1(c)α⋅κ=β/p(d)α=p⋅β⋅κ9.van der waals 气体经Joule实验后(绝热向真空膨胀),气体的温度将(b)。
第二章 热力学第一定律-2
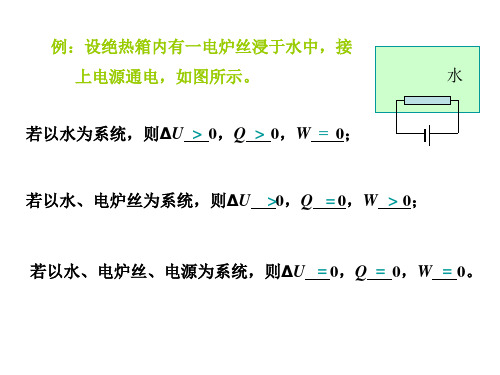
压力下, 例 在0℃,1000kPa压力下,10.00dm3理想气体经下列三 ℃ 压力下 种途径膨胀至压力为100kPa的末态,求各过程的。 种途径膨胀至压力为100kPa的末态,求各过程的。设该 100kPa的末态 体的C ,m 气 体的 V,m=12.471kJ.mol-1. ⑴等温可逆膨胀; 等温可逆膨胀; ⑵绝热可逆膨胀; 绝热可逆膨胀; ⑶在恒定外压为100kPa下绝热膨胀。 在恒定外压为100kPa下绝热膨胀。 100kPa下绝热膨胀 解:气体的物质的量为
理想气体 : dU = CV dT nRT nCV ,m dT = − dV V dT dV CV ,m = −R T V CV ,m d ln T + Rd ln V = 0
d ln T = −(γ − 1)d ln V V2 T2 ln = ln V T1 1 T2 V2 T V 1 1
W = ∆U = nCV ,m (T2 − T1 )
可逆条件: 用过程方程解出T 用过程方程解出T2和 便可得W. T1,便可得W.
p1 ,V1 , T
p
Q= 0
T = 常数 p2 ,V2 , T
p2,V',T'
V
例2.6.1. 某双原子理想气体4mol, 从始态50kPa, 160dm 经绝热可逆 某双原子理想气体4mol, 从始态50kPa, 求末态温度T 及过程的W, W,△ 压缩到末态压力=200kPa,求末态温度T2及过程的W,△U及△H. 分析: 分析: n=4mole n=4mole
(完整版)《物理化学》第二章热力学第一定律练习题(含答案)

(完整版)《物理化学》第⼆章热⼒学第⼀定律练习题(含答案)第⼆章练习题⼀、填空题1、根据体系和环境之间能量和物质的交换情况,可将体系分成、、。
2、强度性质表现体系的特征,与物质的数量⽆关。
容量性质表现体系的特征,与物质的数量有关,具有性。
3、热⼒学平衡状态同时达到四种平衡,分别是、、、。
4、体系状态发⽣变化的称为过程。
常见的过程有、、、、。
5、从统计热⼒学观点看,功的微观本质是,热的微观本质是。
6、⽓体各真空膨胀膨胀功W= 07、在绝热钢瓶中化学反应△U= 08、焓的定义式为。
⼆、判断题(说法对否):1、当体系的状态⼀定时,所有的状态函数都有⼀定的数值。
(√)2、当体系的状态发⽣变化时,所有的状态函数的数值也随之发⽣变化。
(χ)3.因= ΔH, = ΔU,所以与都是状态函数。
(χ)4、封闭系统在压⼒恒定的过程中吸收的热等于该系统的焓。
(χ)错。
只有封闭系统不做⾮膨胀功等压过程ΔH=Q P5、状态给定后,状态函数就有定值;状态函数确定后,状态也就确定了。
(√)6、热⼒学过程中W的值应由具体过程决定( √ )7、1mol理想⽓体从同⼀始态经过不同的循环途径后回到初始状态,其热⼒学能不变。
( √ )三、单选题1、体系的下列各组物理量中都是状态函数的是( C )A 、T、P、V、QB 、m、W、P、HC、T、P、V、n、D、T、P、U、W2、对于内能是体系的单值函数概念,错误理解是( C )A体系处于⼀定的状态,具有⼀定的内能B对应于某⼀状态,内能只能有⼀数值不能有两个以上的数值C状态发⽣变化,内能也⼀定跟着变化D对应于⼀个内能值,可以有多个状态3下列叙述中不具有状态函数特征的是(D )A体系状态确定后,状态函数的值也确定B体系变化时,状态函数的改变值只由体系的始终态决定C经循环过程,状态函数的值不变D状态函数均有加和性4、下列叙述中正确的是( A )A物体温度越⾼,说明其内能越⼤B物体温度越⾼,说明其所含热量越多C凡体系温度升⾼,就肯定是它吸收了热D凡体系温度不变,说明它既不吸热也不放热5、下列哪⼀种说法错误( D )A焓是定义的⼀种具有能量量纲的热⼒学量B只有在某些特定条件下,焓变△H才与体系吸热相等C焓是状态函数D焓是体系能与环境能进⾏热交换的能量6、热⼒学第⼀定律仅适⽤于什么途径(A)A同⼀过程的任何途径B同⼀过程的可逆途径C同⼀过程的不可逆途径D不同过程的任何途径7. 如图,将CuSO4⽔溶液置于绝热箱中,插⼊两个铜电极,以蓄电池为电源进⾏电解,可以看作封闭系统的是(A)(A) 绝热箱中所有物质; (B) 两个铜电极;(C) 蓄电池和铜电极;(D) CuSO4⽔溶液。
热力学第一定律作业

第二章热力学第一定律1.始态为25 °C,200 kPa的5 mol某理想气体,经途径a,b两不同途径到达相同的末态。
途经a先经绝热膨胀到-28.47 °C,100 kPa,步骤的功;再恒容加热到压力200 kPa的末态,步骤的热。
途径b为恒压加热过程。
求途径b的及。
2. 2 mol某理想气体,。
由始态100 kPa,50 dm3,先恒容加热使压力体积增大到150 dm3,再恒压冷却使体积缩小至25 dm3。
求整个过程的。
文档来自于网络搜索3.单原子理想气体A与双原子理想气体B的混合物共5 mol,摩尔分数,始态温度,压力。
今该混合气体绝热反抗恒外压膨胀到平衡态。
求末态温度及过程的。
文档来自于网络搜索4. 1.00mol(单原子分子)理想气体,由10.1kPa、300K按下列两种不同的途径压缩到25.3kPa、300K,试计算并比较两途径的Q、W、ΔU及ΔH。
文档来自于网络搜索(1)等压冷却,然后经过等容加热;(2)等容加热,然后经过等压冷却。
5.在一带活塞的绝热容器中有一固定的绝热隔板。
隔板靠活塞一侧为2 mol,0 °C的单原子理想气体A,压力与恒定的环境压力相等;隔板的另一侧为6 mol,100 °C的双原子理想气体B,其体积恒定。
今将绝热隔板的绝热层去掉使之变成导热板,求系统达平衡时的T及过程的。
文档来自于网络搜索6.1mol 理想气体从300K,100kPa下等压加热到600K,求此过程的Q、W、∆U、∆H。
已知此理想气体C p,m=30.0 J·K-1·mol-1。
文档来自于网络搜索7. 5 mol双原子气体从始态300 K,200 kPa,先恒温可逆膨胀到压力为50 kPa,在绝热可逆压缩到末态压力200 kPa。
求末态温度T及整个过程的及。
文档来自于网络搜索8.一水平放置的绝热恒容的圆筒中装有无摩擦的绝热理想活塞,活塞左、右两侧分别为50 dm3的单原子理想气体A和50 dm3的双原子理想气体B。
热力学第一定律作业

热力学第一定律作业一、 选择题(每题2分,共20分)1.1mol 单原子理想气体经一循环过程后,W =400J ,则该过程的Q 为:( )A 、 0B 、因未指明是可逆过程,无法确定C 、400 JD 、–400 J2.理想气体经一不可逆循环( )。
A 、ΔU >0,ΔH =0B 、ΔU >0,ΔH >0C 、ΔU =0,ΔH =0D 、ΔU=0,ΔH >03.物质的量为n 的理想气体的何组物理量确定后,其它状态函数方有定值:( )A 、pB 、VC 、T ,UD 、T ,p4.在一带活塞的绝热气缸中发生某一化学反应,系统终态温度升高,体积增大,则此过程的S ∆( )。
A 、大于零B 、小于零C 、等于零D 、无法确定5.下列各摩尔反应焓中,属于摩尔生成焓的是( )。
A 、2222()()2()H g O g H O g +→B 、221()()()2CO g O g CO g +→ C 、2221()()()2H g O g H O l +→ D 、2222443()()()C H g C H g C H g +→+6.在一保温良好、门窗紧闭的房间内,放有电冰箱,若将电冰箱门打开,不断向冰箱供给电能,室内的温度将( )A 、 逐渐降低B 、 逐渐升高C 、不变D 、无法确定7.甲烷燃烧反应:4222CH (g)+2O (g)=CO (g)+2H O(l),在绝热恒压条件下反应,终态温度升高,体积增大,其过程的ΔU 和ΔH 分别为( )。
A 、=0,>0B 、<0,=0C 、=0,<0D 、无法确定8.下列物质中,“完全氧化”后的最终产物错误的是( )。
2232A C CO (g)B H H O(l)C S SO (g)D N N (g)→→→→、、、、9.理想气体从同一始态(p 1,V 1,T 1)出发,分别经恒温可逆压缩(T)、绝热可逆压缩(i)到终态体积为V 2时,环境对体系所做功的绝对值比较( )。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物理化学---热力学第一定律作业题
习题1 看仿P27-29所有课后习题,参考答案及解题思路见书后
习题2 (1)如果一系统从环境接受了160J 的功,内能增加了200J ,试问系统将吸收或是放出多少热?(2)一系统在膨胀过程中,对环境做了10540J 的功,同时吸收了27110J 的热,试问系统的内能变化为若干?
[答案:(1) 吸收40J ;(2) 16570J]
习题3 一蓄电池其端电压为12V ,在输出电流为10A 下工作2小时,这时蓄电池的内能减少了1265000J ,试求算此过程中蓄电池将吸收还是放出多少热?
[答案:放热401000J]
习题4 体积为4.10dm 3的理想气体作定温膨胀,其压力从106 Pa 降低到105 Pa,计算此过程所能作出的最大功为若干?
[答案:9441J]
习题5 在25℃下,将50gN 2作定温可逆压缩,从105Pa 压级到2×106Pa ,试计算此过程的功。
如果被压缩了的气体反抗恒定外压105Pa 作定温膨胀到原来的状态,问此膨胀过程的功又为若干?
[答案:–1.33×104J ;4.20×103J]
习题6 计算1mol 理想气体在下列四个过程中所作的体积功。
已知始态体积为25dm 3终态体积为100dm 3;始态及终态温度均为100℃。
(1)向真空膨胀;
(2)在外压恒定为气体终态的压力下膨胀;
(3)先在外压恒定为体积等于50dm 3时气体的平衡压力下膨胀,当膨胀到50dm 3(此时温度仍为100℃)以后,再在外压等于100 dm 3时气体的平衡压力下膨胀;
(4)定温可逆膨胀。
试比较这四个过程的功。
比较的结果说明了什么问题?
[答案:0;2326J ;310l J ;4299J]
习题7 试证明对遵守范德华方程的1mol 实际气体来说,其定温可逆膨胀所作的功可用下式求算。
)11()ln(2
,12,1,2,V V a b V b V RT W m m m -----= 已知范德华方程为 RT b V V a p m m
=-+))((2 习题8 1mol 液体水在100℃和标准压力下蒸发,试计算此过程的体积功。
(1)已知在100℃和标准压力下,水蒸气的比体积(体积除以质量)为1677cm 3·g -1,水的比体积为1.043cm 3·g -1。
(2)假设水的体积比之蒸气的体积可略去不计,蒸气作为理想气体。
比较两者所得的结果,说明(2)的省略是否合理。
[答案:3.057×103J ;3.101×103J]
习题9 在373K 和标推压力下,水的蒸发热为 4.067×104J·mol -1,1mol 液态水体积为18.08cm 3,蒸气则为30200cm 3。
试计算在该条件下1mol 水蒸发成气的ΔU 和ΔH 。
[答案:3.761×104J ;4.067×104J]
习题10 试由0=⎪⎭⎫ ⎝⎛∂∂T V U 及0=⎪⎭⎫ ⎝⎛∂∂T V H 证明理想气体的 0=⎪⎪⎭⎫ ⎝⎛∂∂T p U 及
0=⎪⎪⎭⎫ ⎝⎛∂∂T
p U 习题11 有1mol 单原子分子理想气体在0℃,105Pa 时经一变化过程,体积增大一倍,△H =2092J ,Q=1674J 。
(1)试求算终态的温度、压力及此过程的△U 和W ;(2)如果该气体经定温和定容两步可逆过程到达上述终态,试计算Q 、W 、△U 和△H 。
[答案:(1)373.7K ,6.84×104Pa ,1255J ,419J , (2)2828J ,1573J ,1255J, 2092J]
习题12 已知任何物质的 TV C C v p β
α2
=- 其中α为膨胀系数,β为压缩系数。
现已查得25℃时液体水的定容热容C v,m =75.2J·K -1·mol -1, α=2.1×10-4K -1, β=4.44×10-10Pa -1,而水的V m =18×10-6m 3·mol -1。
试计算液体水在25℃时的C p,m 。
[答案:75.7J·K -1·mol -1 ]
习题13 已知N 2和O 2的定压摩尔热容与温度的关系式分别为
113
2,)1027.487.27()(---⋅⋅⨯+=mol K J K T N C p m 1121
32,))
/(1031.410845.0162.31()(----⋅⋅⨯-⨯+=mol K J K T K T O C p m 试求空气的C p,m 与温度的关系式应为如何?
习题14 某理想气体的C p,m =35.90J·K -1·mol -1,⑴当2mol 此气体在25℃,1.5×106 Pa 时,作绝热可逆膨胀到最后压力为5×105 Pa ;⑵当此气体在外压恒定为5×105 Pa 时作绝热快速膨胀;试分别求算上述两过程终态的T 和V 及过程的W 、△U 和△H 。
[答案:⑴231K ;7.68dm 3;-3697J ;-3697J ;-4811J ;⑵252K ;8.38 dm 3;2538J ;-2538J ;-3303J]
习题15 已知下列反应在25℃时的热效应为
1
221
422142221
23.92);()(2
1)(21)4(8.1382);()(2)()(2)3(8.800);()(2)()()2(411);()(2
1)()1(-Θ-Θ-Θ-Θ⋅-=∆=+⋅-=∆=++⋅-=∆=++⋅-=∆=+m ol kJ H g HCl g Cl g H m ol kJ H s SO Na g O s S s Na m ol kJ H l SO H g O s S g H m ol kJ H s NaCl g Cl s Na m r m r m r m r
计算反应2NaCl(s)+H 2SO 4(l)=Na 2SO 4(s)+2HCl(g)在25℃时的Θ∆m r H 和Θ∆m r U
[答案:55.4; 50.4 kJ·mol -1]
习题16 已知反应
(1)C(金刚石)+O 2(g)=CO 2(g); )298(K H m r Θ∆=-395.4kJ·mol -1
(2) C(石墨)+O 2(g)=CO 2(g); )298(K H m r Θ∆=-393.5kJ·mol -1
求C(石墨)=C(金刚石)的 )298(K H m r Θ∆
[答案: 1.9kJ·mol -1]
习题17 利用下列数据计算HCl(g)的生成焓
1
3221
42221441
1
331
4302.46)298();()(2
3)(21)6(8.313)298();()(2
1)(2)(21)5(32.16)298();,()()4(22.73)298();,()()3(56.35)298();,()()2(21.50)298();,(),(),()1(-Θ-Θ-Θ-Θ-Θ-Θ⋅-=∆=+⋅-=∆=++⋅=∆∞=+⋅-=∆∞=+⋅-=∆∞=+⋅-=∆∞=∞+∞m ol kJ K H g NH g H g N m ol kJ K H s Cl NH g Cl g H g N m ol kJ K H aq Cl NH s Cl NH m ol kJ K H aq HCl g HCl m ol kJ K H aq NH g NH m ol kJ K H aq Cl NH aq HCl aq NH m r m r m r m r m r m r 水水水
[答案:-92.5kJ·mol -1]
习题18 试计算在20 ℃及标准压力下,1mol 液态水蒸发成水蒸气的气化焓。
已知100 ℃ 焓及及标准压力下液态水蒸发成水蒸气的气化焓为2259J·g -1,在此温度区间内,水和水蒸气的平均摩尔等压热容分别为75.3 J·K -1·mol -1和 33.2 J·K -1·mol -1。
[答案:43.8kJ·mol -1]
习题19 某工厂中生产氯气的方法如下:将比例为1:2的18℃的氧气和氯化氢混合物连续地通过一个386℃的催化塔。
如果气体混合物通得很慢,在塔中几乎可达成平衡,即有80%的HCl 转化成Cl 2和H 2O(g)。
试求算欲使催化塔温度保持不变,则每通过1molHCl 时,需从系统取出多少热?
[答案:约7kJ]。
