选修五化学方程式
选修5 第三章 第二节 乙醛

4、乙醛与氢气在一定条件下反应生成乙醇, 此反应属于: AC A、还原反应 B、氧化反应 C、加成反应 D、消去反应 5、下列有机物在反应中被氧化的是 BD A、CH2=CH2转化成CH3CH3 B、CH3CH2OH转化成CH3CHO C、CH3CHO转化成CH3CH2OH D、CH3CHO转化成CH3COOH
H
O
R-CH-C-H
R-CH-C-H
△ -H2O
O R-CH2-CH=C-C-H R O
以乙烯合成1-丁醇 资料36页 15题 现有一化合物A,是由B、C两物质通 过上述原理的反应生成的。试根据A的结 构式写出B、C的结构式 CH3 CH3CHO A:CH3 C CH2CHO O OH CH3 C CH3
聚甲醛, 假象牙,是一 种很好的有机塑料 nHC≡CH
一定条件
— [ CH=CH— ]n 聚乙炔,导电塑料
苯酚与甲醛的缩聚反应
OH
n
O + n HCH
OH
]n -CH2-
缩聚反应——单体间相互反应生成高分子 化合物的同时还生成小分子的反应 条件: 每一种单体必须有能够形成两条 半键的原子或原子团
-
1mol 甲醛~
2
mol Cu2O
若分子中有1个醛基: 若1个分子中有 1mol该醛 —— 2mol Ag 多个醛基,依 若分子中有2个醛基: 次类推 1mol该醛 —— 4mol Ag 所以可根据醛的物质的量和生成的Ag 的物质的量的关系,可知醛分子中所含醛 基的个数 但需注意:甲醛(HCHO)是一元醛,分子中 只有1个醛基,但在发生氧化反应时,相当 于二元醛,如与银氨溶液反应时: 1mol HCHO —— 4mol Ag
了解 2、乙醛也可和HX、HCN加成 O OH CH3CH + HX
高中化学选修5化学方程式总汇

1. 2. 3.+Br 2(液溴)FeCl3■NO 2+H 2O有机化学方程式(选修五)烷烃(甲烷为例)1. CH 4+C12光照「CH 3cl +HCl.2. CH ,+(3n +1)/2O,点燃-nCO.+(n +1)HO n2n+2222烯烃(乙烯为例)1. CH 2=CH 2+Br 2-CH 2Br —CH 2Br2. CH 2=CH 2+H 2O 催化剂.CH 3CH 2OH3. CH 2=CH 2+HCl 催化剂qCH 3cH 2cl5. nCH 2=CH 2催化剂.KH 2—CH 2t6.C n H2n+3n/2O2n CO 2+n H 2O炔烃(乙炔为例)2. CH 三CH +HCl 催化剂=CH 2=CHCl △3. CH 三CH +Br 2-CHBr=CHBr4. CH 三CH +2Br 2-CHBr 2—CHBr 25. nCH 2=CHCl 催化剂.[CH 2—fHi n 催化剂Cl6. C 4H 104t 一小二C 9H ,十CH410加热、加压2426苯4. CH 2=CH 2+H 2 催化剂A△CH 3—CH 31.CH 三CH +2H 2催化剂-*CH 3—CH+HNO 3浓硫酸 55〜60℃—Br +HBr2催化剂A△1. CH 3cH 2Br +NaOH H ‘O「CH 3cH 20H +NaBr△醇2. CHCHBr +NaOH 7~~^CHRH 9f+NaBr +HO32△22醇1.2CH 3cH 20H +2Na -2CH 3cH 2ONa +H 2T2. CH 3cH 2OH +HBr —△--CH 3CH 2Br +H 20浓硫酸3. CH 3CH 2OH 丁CH 2=CH 2T+H 2O170催化剂2CHCHOH +O 。
x2CHCHO +2HO322△32催化剂2CHCH(OH)CH +O,■2CHCOCH +HO332y^3327.C (CH 3)3OH +O 2催化剂.很难被氧化△酚(苯酚为例) +2Na -2ONa+H 2TfONa3.2+凡。
高中化学选修五-第三章第四节-有机合成
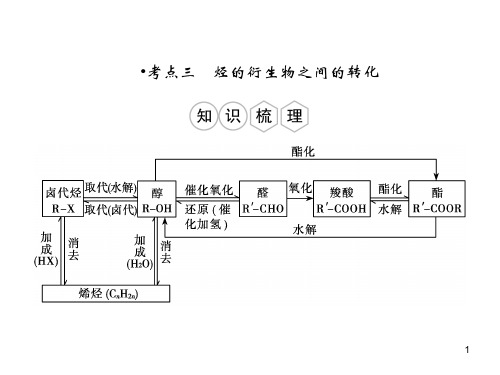
③2mol-OH或2mol-COOH与活泼金属反应放出1molH2。
④1mol-COOH与碳酸氢钠溶液反应放出1molCO2
⑤1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子 质量将增加42,1mol二元醇与足量乙酸反应生成酯时,其相 对分子质量将增加84。
解析:由题意可知,C不是甲酸,E为酮(分子中含碳原子数≥3),
故A可能为
或
。
• 答案:B
25
解有机物综合推断类试题的常用方法 (1)逆推法。由产物推断未知反应物或中间产物时叫逆推法。 (2)根据反应条件推断。在有机合成中,可以根据一些特定反应的 条件,推出未知有机物的结构简式。如“N―aO― △H→/醇”是卤代烃消去的条 件;“ N―aO△―H→/水 ”是卤代烃水解的条件,“ 浓― 17―硫0 →℃酸 ”是乙醇消去的条 件,“浓硫酸,△”是羧酸和醇发生酯化反应的条件。
(1).碳骨架构建:构建方法会以信息形式给出。 包括碳链增长和缩短 、成环和开环等。
(2.官能团的引入和转化: (1)官能团的引入:
思考与交流
1、引入碳碳双键的三种方法: 卤代烃的消去;醇的消去;炔烃的不完全加成。
2、引入卤原子的三种方法:
醇(或酚)的取代;烯烃(或炔烃)的加成;
烷烃(或苯及苯的同系物)的取代。
•2020/2/14 ⑩遇浓硝酸变黄的有机物为: 蛋白质
1717
寻找题眼.确定范围---【有机物·条件】
①当反应条件为NaOH醇溶液并加热时,必定为 卤代烃的消去反应。 ②当反应条件为NaOH水溶液并加热时,通常为 卤代烃或酯的水解反应。
③当反应条件为浓H2SO4并加热时,通常为
糖类油脂化学方程式

高三化学复习化学方程式5 班级姓名学号选修5有机化学基础(第四章生命中的基础有机化学物质)1、葡萄糖与氧气反应 (有氧呼吸和无氧呼吸)C6H12O6 (s)+ 6O2(g)→6CO2(g) + 6H2O(l)2、葡萄糖的氧化反应:(Ⅰ)与新制Cu(OH)2作用CH2OH-(CHOH)4-CHO + 2Cu(OH)2CH2OH-(CHOH)4-COOH + Cu2O↓+2 H2O (II)银镜反应(离子方程式)CH2OH-(CHOH)4-CHO + 2[Ag(NH3)2]+ + 2OH-CH2OH-(CHOH)4-COO- + NH4+ +2Ag↓+ H2O + 3NH3(产物记忆为:一水二银三氨葡萄糖酸铵)3、葡萄糖的酯化反应: 与乙酸作用生成葡萄糖五乙酸酯4、蔗糖水解C12H22O11 + H2O →C6H12O6 + C6H12O6 (催化剂:稀硫酸)(蔗糖) (葡萄糖) (果糖)5、麦芽糖水解C12H22O11 + H2O →2 C6H12O6 (催化剂:稀硫酸)(麦芽糖) (葡萄糖)6、淀粉水解2(C6H10O5)n + nH2O →nC12H22O11(催化剂:稀硫酸或酶)淀粉麦芽糖C12H22O11 + H2O →2C6H12O6 (稀硫酸或酶)C6H12O6→2C2H5OH+2CO2(催化剂:酒化酶)麦芽糖葡萄糖葡萄糖酒精(乙醇)7、油脂酸性条件下的水解8、油脂的皂化:油脂在碱性(NaOH)条件下的水解反应中生成的高级脂肪酸钠盐是肥皂的主要成分。
所以将油脂在碱性条件下的水解反应称为皂化反应硬脂酸甘油酯硬脂酸钠甘油可以理解为油脂水解产生的高级脂肪酸再与NaOH反应而得到的产物。
9、油脂的氢化:实质是与氢气发生加成反应。
也称油脂的硬化。
油酸甘油酯(油)硬脂酸甘油酯(脂肪)+ 3H2C17H33COOCH2C17H33COOCHC17H33COOCH2催化剂加热加压C17H35COOCH2C17H35COOCHC17H35COOCH2。
化学选修5有机化学方程式汇总

化学选修五方程式汇总一、烷烃1、取代反应①甲烷与氯气的取代(只写出第一步反应)注:但共有种产物,其中的产量最多,有种有机产物。
2、氧化反应①不能使酸性高锰酸钾溶液褪色。
②甲烷燃烧:③烷烃燃烧通式:3、分解反应①甲烷高温下分解:②十六烷催化裂解:③丁烷催化裂化:一、烯烃1、加成反应①乙烯与溴水(或溴的四氯化碳)的加成反应:②乙烯制工业酒精:③乙烯与氢气反应:④乙烯与氯化氢反应:⑤1,3-丁二烯与氯气发生1,2-加成:⑥1,3-丁二烯与氯气发生1,4-加成:2、氧化反应①使酸性高锰酸钾溶液褪色。
②乙烯燃烧:③烯烃燃烧通式:④乙烯氧化法制乙醛:3、加聚反应①乙烯发生加聚反应:②2-丁烯发生加聚反应:③乙烯与苯乙烯发生共聚反应:一、炔烃实验室制备乙炔:1、加成反应①乙炔与溴水(或溴的四氯化碳)1:1加成反应:②乙炔与溴水(或溴的四氯化碳)1:2加成反应:③乙炔与氢气1:1反应:④乙炔与氯化氢1:1反应:2、氧化反应①使酸性高锰酸钾溶液褪色。
②乙炔燃烧:③炔烃燃烧通式:3、加聚反应①乙炔发生加聚反应:②丙炔发生加聚反应:三、芳香烃1、取代反应①卤代:苯与液溴、铁粉的取代反应②硝化:苯与浓硫酸、浓硝酸共热③磺化:苯与浓硫酸共热④甲苯与浓硫酸、浓硝酸共热发生硝化反应⑤甲苯与氯气光照:(1:1)⑥甲苯与氯气氯化铁催化:(1:1)2、氧化反应①苯不能使酸性高锰酸钾溶液褪色,甲苯或乙苯能使酸性高锰酸钾溶液褪色,生成苯甲酸。
②苯在空气中燃烧③苯和苯的同系物在空气中燃烧通式④烃(C x H y)燃烧通式3、加成反应①苯与氢气加成:②甲苯与氢气加成:四、卤代烃1、水解反应①溴乙烷的水解②1,2-二氯乙烷的水解2、消去反应①溴乙烷的消去反应②2-氯丙烷的消去反应③1,2-二溴乙烷的消去反应五、醇1、置换反应①乙醇与金属钠的置换反应②乙二醇与金属钠的置换反应③丙三醇与金属钠的置换反应2、消去反应①乙醇与浓硫酸共热170℃(实验室制备乙烯)②2-丙醇与浓硫酸共热发生消去反应3、取代反应①乙醇与浓氢溴酸混合共热②乙醇与浓硫酸共热140℃③乙醇与乙酸发生酯化反应④乙二醇与足量的乙酸发生酯化4、氧化反应①乙醇在空气中燃烧:②乙醇催化氧化:③2-丙醇催化氧化:④乙醇能被酸性重铬酸钾溶液氧化,能使酸性高锰酸钾溶液褪色。
高中化学方程式总结

高中化学方程式总结第一部分无机方程式1、钠与空气常温下反应4Na+O2==2Na2O2、钠再空气中加热过氧化钠为黄色固体2Na+O2==Na2O2加热或点燃3、钠与水反应现象浮、游、熔、响、红2Na+2H2O==2NaOH+H2↑4、铁与水蒸气反应3Fe+4H2Og==Fe3O4+4H2加热5、铝与氢氧化钠溶液反应2Al+2NaOH+2H2O==2NaAlO2+3H2↑2Al+2OH-+2H2O==2AlO-+3H2↑6、氧化钠与水反应Na2O+H2O==2NaOH7、氧化钠与二氧化碳反应Na2O+CO2==Na2CO38、过氧化钠与水反应反应放出大量的热2Na2O2+2H2O==4NaOH+O2↑9、过氧化钠与二氧化碳反应应用于防毒面具与潜水艇制氧气2Na2O2+2CO2==2Na2CO3+O210、碳酸钠俗称:苏打、纯碱与盐酸反应注意“互滴”时的现象少量盐酸:Na2CO3+HCl==NaCl+NaHCO3CO32--+H+==HCO3-NaHCO3+HCl==NaCl+H2O+CO2↑HCO3-+H+==H2O+CO2↑过量盐酸:Na2CO3+2HCl==2NaCl+H2O+CO2↑CO32-+2H+==H2O+CO2↑11、碳酸氢钠俗称:小苏打与盐酸反应NaHCO3+HCl==NaCl+H2O+CO2↑HCO3-+H+==H2O+CO2↑12、向碳酸钠溶液中通入二氧化碳Na2CO3+H2O+CO2==2NaHCO3CO32-+H2O+CO2==2HCO3-13、碳酸钠加热分解2NaHCO3==Na2CO3+H2O+CO2↑加热14、碳酸氢钠溶液加入氢氧化钠NaHCO3+NaOH==Na2CO3+H2OHCO3-+OH-==CO32-+H2O15、氧化铝与盐酸反应Al2O3+6HCl==2AlCl3+3H2OAl2O3+6H+==2Al3++3H2O16、氧化铝与氢氧化钠溶液反应Al 2O 3+2NaOH==2NaAlO 2+H 2OAl 2O 3+2OH -==2AlO 2-+H 2O17、实验室制取氢氧化铝用可溶性铝盐和氨水反应Al 2SO 43+6NH 3·H 2O==2AlOH 3↓+3NH 42SO 4Al 3++ 3NH 3·H 2O ==AlOH 3↓+3NH 4+18、氢氧化铝与盐酸反应AlOH 3+3HCl==AlCl 3+3H 2OAlOH 3+3H +==Al 3++3H 2O19、加热氢氧化铝分解2AlOH 3==Al 2O 3+3H 2O 加热20、偏铝酸钠溶液与盐酸反应NaAlO 2+HCl+H 2O==NaCl+AlOH 3↓AlO 2-+H ++H 2O==AlOH 3↓21、偏铝酸钠溶液中通入二氧化碳二氧化碳少量:2NaAlO 2+CO 2+3H 2O==Na 2CO 3+2AlOH 3↓2AlO 2-+CO 2+3H 2O==CO 32-+2AlOH 3↓二氧化碳过量:NaAlO 2+CO 2+2H 2O==AlOH 3↓+NaHCO 3AlO 2-+CO 2+2H 2O==AlOH 3↓+HCO 3-22、氧化亚铁与盐酸反应FeO+2HCl==FeCl 2+H 2OFeO+2H +==Fe 2++H 2O23、氧化铁与盐酸反应Fe 2O 3+6HCl==2FeCl 3+3H 2OFe 2O 3+6H +==2Fe 3++3H 2O24、四氧化三铁与盐酸反应Fe 3O 4+8HCl==FeCl 2+2FeCl 3+4H 2OFe 3O 4+8H +==Fe 2++2Fe 3++4H 2O25、硫酸亚铁与氢氧化钠反应FeSO 4+2NaOH==FeOH 2↓+Na 2SO 4Fe 2++2OH -==FeOH 2↓26、实验室制取氢氧化铁红褐色FeCl 3+3NaOH==FeOH 3↓+3NaClFe 3++3OH -==FeOH 3↓27、氢氧化亚铁被氧化现象:灰白色沉淀迅速变成灰绿色最终变成红褐色 4FeOH 2+O 2+2H 2O==FeOH 328、Fe 3+的检验生成血红色物质 切记不是沉淀Fe 3++3SCN -==FeSCN 329、铁离子与铜反应常用于腐蚀印刷电路板2FeCl 3+Cu==2FeCl 2+CuCl 22Fe 3++Cu==2Fe 2++Cu 2+30、铁离子与锌反应锌少量:2FeCl 3+Zn==2FeCl 2+ZnCl 2 2Fe 3++Zn==2Fe 2++Zn 2+锌过量:2FeCl 3+3Zn==2Fe+3ZnCl 2 2Fe 3++3Zn==2Fe+3Zn 2+31、氯化铁溶液里加铁粉2FeCl 3+Fe==3FeCl 22Fe 3++Fe==3Fe 2+32、氢氧化铁加热分解2FeOH 3==Fe 2O 3+3H 2O 加热33、用氢氟酸雕刻玻璃SiO 2+4HF==SiF 4↑+2H 2O34、二氧化硅与氢氧化钠反应因此保存氢氧化钠溶液应用橡胶塞SiO 2+2NaOH==Na 2SiO 3+2H 2O35、制取硅酸硅酸钠水溶液成为水玻璃Na 2SiO 3+2HCl==H 2SiO 3↓+2NaCl 沉淀符号可加可不加,以学校为准SiO 32-+2H +==H 2SiO 3↓36、水玻璃中通入二氧化碳可以验证碳酸酸性比硅酸强Na 2SiO 3+H 2O+CO 2==Na 2CO 3+H 2SiO 3↓SiO 32-+H 2O+CO 2==CO 32-+H 2SiO 3↓注意:若二氧化碳过量则生成碳酸氢盐37、实验室制取氯气MnO 2+4HCl 浓==MnCl 2+Cl 2↑+2H 2O 加热38、磷与氯气反应氯气少量:2P+3Cl 2==2PCl 3氯气足量:2P+5Cl 2==2PCl 5PCl 3为液态,PCl 5为固态39、氯气与水反应Cl2+H 2O==HClO+HCl40、氯气光照分解2HClO==2HCl+O 2↑光照41、氯气通入氢氧化钠溶液中生成物为84消毒液主要成分Cl 2+2NaOH==NaClO+NaCl+H 2OCl 2+2OH -==ClO -+Cl --+H 2O42、将氯气通入石灰乳中制漂白粉漂白粉主要成分是氯化钙和次氯酸钙,有效成分是次氯酸钙CaOH 2+2Cl 2==CaClO 2+CaCl 2+2H 2O43、漂白粉工作原理CaClO 2+2HCl==2HClO+CaCl 2ClO -+H +==HClO44、漂白粉再空气中变质可证明碳酸酸性强于次氯酸CaClO 2+CO 2+H 2O==CaCO 3↓+2HClOCa 2++2ClO -+CO 2+H 2O==CaCO 3↓+2HClO注意:若二氧化碳过量则生成碳酸氢盐45、高锰酸钾与浓盐酸反应2KMnO 4+16HCl 浓==2KCl+2MnCl 2+5Cl 2↑+8H 2O46、卤素之间的置换反应Cl 2+2Br -==Br 2+2Cl -Cl 2+2I -==I 2+2Cl -Br 2+2I -==I 2+2Br -47、硫与氧气点燃S+O2==SO2点燃48、二氧化硫溶于水SO2+H2O==H2SO3可逆号49、用氢氧化钠吸收二氧化硫SO2+2NaOH==Na2SO3+H2OSO2+2OH-==SO32-+H2O50、向亚硫酸钠溶液中继续通入二氧化硫Na2SO3+SO2+H2O==2NaHSO3SO32-+SO2+H2O==2HSO3-51、二氧化硫与氧化钙反应SO2+CaO==CaSO3高温52、氯水中通入二氧化硫,漂白性消失Cl2+2H2O+SO2==H2SO4+2HClCl2+2H2O+SO2==4H++SO42-+2Cl-52、实验室制取二氧化硫Na2SO3+H2SO4浓==Na2SO4+SO2↑+H2O53、工业制硫酸2SO2+O2==2SO3可逆号催化剂、加热SO3+H2O==H2SO454、三氧化硫与氧化钙反应SO3+CaO==CaSO455、用熟石灰吸收三氧化硫SO3+CaOH2==CaSO4+H2O56、向硫化氢的水溶液俗称氢硫酸中通入二氧化硫2H2S+SO2==3S↓+2H2O57、硫化氢与氧气反应氧气少量:2H2S+O2==2S↓+2H2O点燃氧气足量:2H2S+3O2==2H2O+2SO2点燃58、硫于氢氧化钠反应3S+6NaOH==2Na2S+Na2SO3+3H2O3S+6OH-==2S2-+SO32-+3H2O59、二氧化硫和过氧化钠反应SO2+Na2O2==Na2SO460、大气固氮NO是无色无味气体,有毒N 2+O2==2NO高温或放电61、一氧化氮被氧化NO2是红棕色有刺激性气味有毒气体2NO+O2==2NO262、二氧化氮溶于水3NO2+H2O==2HNO3+NO63、一氧化氮与氧气4:3溶于水4NO+3O2+2H2O==4HNO364、二氧化氮与氧气4:1溶于水4NO2+O2+2H2O==4HNO365、工业制氨气N 2+3H2==2NH3可逆号高温高压催化剂66、氨气溶于水NH 3+H 2O==NH 3·H 2O 可逆号67、氨气和氯化氢反应产生白烟NH3+HCl==NH 4Cl68、碳酸氢铵俗称碳铵加热分解NH 4HCO 3==NH 3↑+H 2O ↑+CO 2↑加热69、硝酸铵与氢氧化钠混合加热NH 4NO 3+NaOH==NaNO 3+H 2O+NH 3↑加热70、实验室制取氨气2NH 4Cl+CaOH 2==CaCl 2+2H 2O+2NH 3↑加热71、氨的催化氧化4NH 3+5O 2==4NO+6H 2O 催化剂、加热72、浓硫酸和铜反应Cu+2H 2SO 4浓==CuSO 4+SO 2↑+2H 2O 加热73、铁与浓硫酸加热2Fe+6H 2SO 4浓==Fe 2SO 43+3SO 2↑+6H 2O 加热74、碳与浓硫酸反应C+2H 2SO 4浓==CO 2↑+2H 2O+SO 2↑加热75、硫于浓硫酸反应S+2H 2SO 4浓==3SO 2↑+2H 2O 加热76、硫化氢与浓硫酸反应H 2S+H 2SO 4浓==2H 2O+SO 2+S ↓加热77、铜与浓硝酸反应Cu+4HNO 3浓==CuNO 32+2NO 2↑+2H 2OCu+4H ++2NO 3-==Cu 2++2NO 2↑+2H 2O78、铜与稀硝酸反应3Cu+8HNO 3稀==3CuNO 32+2NO ↑+4H 2OCu+8H ++2NO 3-==3Cu 2++2NO ↑+4H 2O79、浓硝酸与碳反应C+4HNO 3==CO 2↑+4NO 2↑+2H 2O 加热80、硝酸见光分解4HNO 3==4NO 2↑+O 2↑+2H 2O 光照或加热81实验室制取氯化氢NaCl+H 2SO 4浓==NaHSO 4+HCl ↑加热82、制取水煤气C+H 2Og==CO+H 2高温83、铝热反应3Fe 3O 4+8Al==4Al 2O 3+9Fe 高温84、向氯化亚铁中滴入氯水2FeCl 2+Cl 2==2FeCl 32Fe 2++Cl 2==Fe 3+第二部分 有机方程式必修部分1、烃燃烧C x H y +x+y/4O 2→xCO 2+y/2H 2O 点燃2、甲烷与氯气发生取代反应CH 4+Cl2→CH 3Cl+HCl 光照CH 3Cl+Cl 2→CH 2Cl 2+HCl 光照CH 2Cl 2+Cl 2→CHCl 3+HCl 光照CHCl 3+Cl 2→CCl 4+HCl 光照2、乙烯与溴水加成CH 2=CH 2+Br 2→CH 2BrCH 2Br3、乙烯和氢气加成CH 2=CH 2+H 2→CH 3CH 3一定条件4、乙烯与氯化氢加成CH 2=CH 2+HCl →CH 3CH 2Cl 一定条件5、乙烯和水加成CH 2=CH 2+H 2O →CH 3CH 2OH 一定条件6、乙烯的加举反应一定条件7、苯燃烧2C 6H 6+15O 2→12CO 2+6H 2O 点燃8、苯与液溴取代9、苯的硝化反应10、苯与氢气加成11、乙醇燃烧CH 3CH 2OH+3O 2→2CO 2+3H 2O 点燃12、乙醇与钠反应2CH 3CH 2OH+2Na →2CH 3CH 2Na+H 2↑13、乙醇的催化氧化2CH 3CH 2OH+O 2→2CH 3CHO+2H 2OCu 或Ag 、加热14、乙醇与氧化铜反应CH 3CH 2OH+CuO →CH 3CHO+H 2O 加热15、乙醇的消去反应实验室制乙烯CH 3CH 2OH →CH 2=CH 2↑+ H 2O 浓硫酸、170℃16、乙酸与镁反应2CH 3COOH+Mg →CH 3COO 2Mg+H 2↑17、乙酸与乙醇发生酯化反应CH 3COOH+ CH 3CH 2OH →CH 3COOC 2H 5+H 2O 可逆号浓硫酸、加热18、蔗糖水解C 12H 22O 11蔗糖+H 2O →C 6H 12O 6葡萄糖+C 6H 12O 6果糖稀硫酸、加热19、麦芽糖水解C 12H 22O 11麦芽糖+H 2O →2C 6H 12O 6葡萄糖稀硫酸、加热20、淀粉水解C 6H 10O 5n 淀粉+nH 2O →nC 6H 12O 6葡萄糖稀硫酸、加热第三部分 电离水解方程式1、醋酸的电离CH 3COOH==CH 3COO -+H +可逆号2、碳酸的电离H 2CO 3==H ++HCO 3-可逆号HCO 3-== H ++CO 32-可逆号3、氢氧化铁的电离FeOH 3==Fe 3++3OH -可逆号4、碳酸根水解CO 32-+H 2O==HCO 3-+OH -HCO 3-+H 2O==H 2CO 3+H 2O5、铁离子的水解Fe 3++3H 2O==FeOH 3+3H +6、碳酸根与铁离子双水解3CO 32-+2Fe 3++3H 2O==2FeOH 3↓+3CO 2↑7、碳酸氢根与铁离子双水解3HCO 3-+Fe 3+==FeOH 3↓+3CO 2↑8、偏铝酸根与铝离子双水解Al 3++3AlO 2-+6H 2O==4AlOH 3↓9、水的电离H 2O==H ++OH -可逆号第四部分电化学方程式 1、铜锌原电池硫酸做电解液负极:Zn-2e -==Zn 2+正极:2H ++2e -==H 2↑总反应:Zn+2H +==Zn 2++H 2↑2、铅蓄电池放电负极:Pb+SO 42--2e -==PbSO 4正极:PbO+4H ++SO 42-+2e -==PbSO 4+2H 2O总反应:PbO 2+Pb+2H 2SO 4==2PbSO 4+2H 2O3、铅蓄电池充电阴极:PbSO 4+2e -==Pb+SO 42-阳极:PbSO 4+2H 2O-2e -==PbO+4H ++SO 42-总反应:2PbSO 4+2H 2O==PbO 2+Pb+2H 2SO 44、氢氧燃料电池酸性电解质溶液负极:H 2-2e -==2H +正极:O 2+4e -+4H +==2H 2O总反应:2H 2+O 2==2H 2O5、氢氧燃料电池碱性电解质溶液负极:H 2-2e -+2OH -==2H 2O正极:O 2+4e -+2H 2O==4OH -总反应:2H 2+O 2==2H 2O6、电解氯化铜溶液阴极:Cu 2++2e -==Cu阳极:2Cl --2e -==Cl 2↑总反应:CuCl 2== Cu+Cl 2↑电解7、电解氯化钠溶液氯碱工业、工业制氯气阴极:2H ++2e -==H 2↑阳极:2Cl --2e -==Cl 2↑总反应:2NaCl+2H 2O==2NaOH+H 2↑+Cl 2↑电解8、电解硫酸亚铁溶液阴极:Fe 2++2e -==Fe阳极:4OH --4e -==O 2↑+2H 2O总反应:2FeSO 4+2H 2O==2Fe+O 2↑+2H 2SO 4电解9、 电解氢氧化钠溶液阴极:2H ++2e -==H 2↑阳极:4OH --4e -==O 2↑+2H 2O总反应:2H 2O==2H 2↑+O 2↑电解10、向铜上镀银镀件做阴极,镀层金属做阳极,镀层金属盐溶液做电解质溶液 阴极:Ag ++e -==Ag阳极:Ag-e -==Ag +11、精炼铜反应粗铜做阳极,精铜做阴极阴极:Cu 2++2e -==Cu阳极:Cu-2e -==Cu 2+12、析氢腐蚀负极:Fe-2e -==Fe 2+正极:2H ++2e -==H 2↑总反应:Fe+2H +==Fe 2++H 2↑13、吸氧腐蚀负极:2Fe-4e -==2Fe 2+正极:2H 2O+O 2+4e -==4OH -总反应:2Fe+O 2+2H 2O==2FeOH 24FeOH 2+O 2+2H 2O==4FeOH 3第五部分 选修三1、制取银氨溶液AgNO 3+NH 3·H 2O==AgOH ↓+NH 4NO 3AgOH+2NH 3·H 2O==AgNH 32OH+2H 2OAg ++ NH 3·H 2O===AgOH ↓+NH 4+AgOH+2NH3·H2O==AgNH 322++2H 2O+2OH -2、制取四氨合氢氧化铜Cu 2++2NH 3·H 2O==CuOH 2↓+2NH 4+CuOH 2+4NH3·H2O==CuNH 342++2OH -+4H 2O。
化学选修五(有机化学基础)----芳香烃
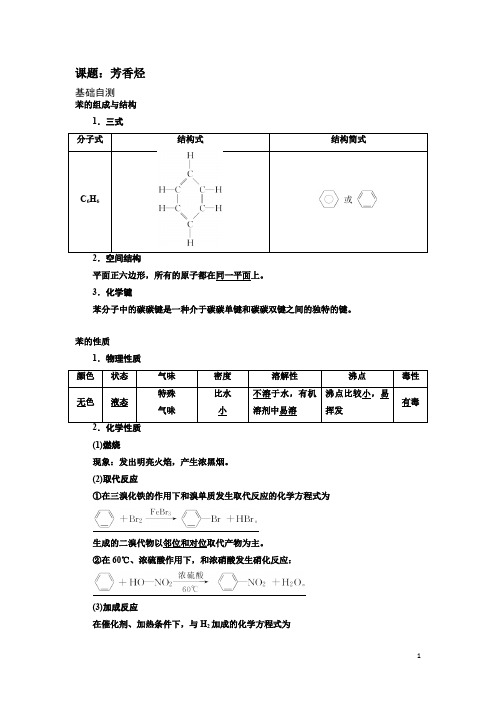
课题:芳香烃基础自测苯的组成与结构1.三式平面正六边形,所有的原子都在同一平面上。
3.化学键苯分子中的碳碳键是一种介于碳碳单键和碳碳双键之间的独特的键。
苯的性质1.物理性质(1)燃烧现象:发出明亮火焰,产生浓黑烟。
(2)取代反应①在三溴化铁的作用下和溴单质发生取代反应的化学方程式为生成的二溴代物以邻位和对位取代产物为主。
②在60℃、浓硫酸作用下,和浓硝酸发生硝化反应:(3)加成反应在催化剂、加热条件下,与H2加成的化学方程式为(4)苯的特性①苯不与高锰酸钾酸性溶液和溴水反应,由此可知苯在化学性质上与烯烃有很大的差别。
②苯在催化剂(Fe或FeBr3)作用下与液溴发生取代反应,说明苯具有烷烃的性质。
③苯又能够与H2或Cl2分别在催化剂作用下发生加成反应,说明苯具有烯烃的性质。
④苯容易发生取代反应,而难于发生加成反应,难被氧化,其化学性质不同于烷烃、烯烃和炔烃。
溴苯、硝基苯的制备将反应后的液体倒入一个盛有冷水芳香烃的来源与苯的同系物1.芳香烃的来源(1)芳香烃最初来源于煤焦油中,现代主要来源于石油化学工业中的催化重整和裂化。
苯、乙苯和对二甲苯是应用最多的基本有机原料。
(2)工业上,乙苯、异丙苯主要通过苯与乙烯、丙烯反应获得。
苯与乙烯反应的化学方程式为。
2.苯的同系物(1)概念:苯环上的氢原子被烷基取代后的产物。
(2)结构特点:分子中只有1个苯环,侧链是烷烃基。
(3)通式:C n H2n-6(n≥7)。
苯的同系物与芳香烃的关系(1)分子式与苯(C6H6)相差一个或若干个“CH2”原子团的物质,如甲苯(C7H8)、二甲苯(C8H10)等都是苯的同系物,它们也都属于芳香烃。
(2)苯的同系物都是芳香烃,但芳香烃不一定是苯的同系物。
如属于芳香烃,但不是苯的同系物。
(3)苯的同系物的通式都为C n H2n-6(n≥7),但通式符合C n H2n-6的烃不一定是苯的同系物。
如的分子式为C10H14,它不属于苯的同系物。
选修五第三章羧酸--酯分解

+2CH3CH2OH
+ 2H2O
4.多元酸与多元醇之间的酯化反应
多元酸与多元醇之间的酯化反应有多种形式,可以得到普 通酯、环状酯和高聚酯。
+
HOOCCOOCH2CH2OH+H2O
+
+2H2O
nHOOC—COOH+nHOCH2—CH2OH
+(2n-1)H2O
5.羟基酸自身的酯化反应
羟基酸自身的酯化反应也有多种形式,可以得到普通酯、 环状酯和高聚酯。
(3)乳酸在浓硫酸存在下,3 分子相互反应,生成物为链状, 其结构简式可表示为:__________________________________。
(4)乳酸在浓硫酸存在下,2 分子相互反应,生成物为环状, 其结构简式可表示为___________________________________。
解,而在酸荡、均匀碱性条件下易水解?
实验步骤2 将三支试管同时放入70~80℃的水浴里加热约5
min,闻各试管里乙酸乙酯的气味
实验现象 实验结论
6、化学性质:(水解反应)
O
稀H2SO4
CH3—C—O—C2H5 + H2O
O
O
CH3—C—OH+H—O—C2H5 O
CH3—C—OC2H5 + NaOH
3、乙酸的化学性质
(1) 弱酸性:
CH3COOH A、使紫色石蕊试液变色: B、与活泼金属反应:
CH3COO-+H+
2CH3COOH + Fe = Fe (CH3COO)2+H2↑ C、与碱性氧化物反应:
2CH3COOH+Na2O=2CH3COONa+2H2O D、与碱反应:
CH3COOH + NaOH = CH3COONa+ H2O E、与某些盐反应:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
选修五化学方程式甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
CH4→C+2H2(条件为高温高压,催化剂)甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HClCH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HClCHCl3+Cl2→CCl4+HCl (条件都为光照。
)实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br乙烯和水CH2=CH2+H20→CH3CH2OH (条件为催化剂)乙烯和氯化氢CH2=CH2+HCl→CH3-CH2Cl乙烯和氢气CH2=CH2+H2→CH3-CH3 (条件为催化剂)乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)氯乙烯聚合nC H2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃)乙炔和溴水C2H2+2Br2→C2H2Br4乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2乙炔和氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6 (条件为催化剂)实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。
CaCO3 === CaO + CO2 2CaO+5C===2CaC2+CO2CaC2+2H2O→C2H2+Ca(OH)2C+H2O===CO+H2-----高温C2H2+H2→C2H4 ----乙炔加成生成乙烯C2H4可聚合苯燃烧2C6H6+15O2→12CO2+6H2O (条件为点燃)苯和液溴的取代C6H6+Br2→C6H5Br+HBr苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)苯和氢气C6H6+3H2→C6H12 (条件为催化剂)乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃)乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)乙醇发生消去反应的方程式CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸170摄氏度)两分子乙醇发生分子间脱水2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸140摄氏度)乙醇和乙酸发生酯化反应的方程式CH3COOH+C2H5OH→CH3COOC2H5+H2O乙酸和镁Mg+2CH3COOH→(CH3COO)2Mg+H2乙酸和氧化钙2CH3COOH+CaO→(CH3CH2)2Ca+H2O乙酸和氢氧化钠CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH乙酸和碳酸钠Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑甲醛和新制的氢氧化铜HCH O+4Cu(OH)2→2Cu2O+CO2↑+5H2O乙醛和新制的氢氧化铜CH3CHO+2Cu→Cu2O(沉淀)+CH3COOH+2H2O乙醛氧化为乙酸2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)烯烃是指含有C=C键的碳氢化合物。
属于不饱和烃。
烯烃分子通式为CnH2n,非极性分子,不溶或微溶于水。
容易发生加成、聚合、氧化反应等。
乙烯的物理性质通常情况下,无色稍有气味的气体,密度略小比空气,难溶于水,易溶于四氯化碳等有机溶剂。
1) 氧化反应:①常温下极易被氧化剂氧化。
如将乙烯通入酸性KMnO4溶液,溶液的紫色褪去,由此可用鉴别乙烯。
②易燃烧,并放出热量,燃烧时火焰明亮,并产生黑烟。
2) 加成反应:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应。
3) 聚合反应:2.乙烯的实验室制法(1)反应原理:CH3CH2OH===CH2=CH2↑+H2O (条件为加热,浓H2SO4)(2)发生装置:选用“液液加热制气体”的反应装置。
(3)收集方法:排水集气法。
(4)注意事项:①反应液中乙醇与浓硫酸的体积比为1∶3。
②在圆底烧瓶中加少量碎瓷片,目的是防止反应混合物在受热时暴沸。
③温度计水银球应插在液面下,以准确测定反应液温度。
加热时要使温度迅速提高到170℃,以减少乙醚生成的机会。
④在制取乙烯的反应中,浓硫酸不但是催化剂、吸水剂,也是氧化剂,在反应过程中易将乙醇氧化,最后生成CO2、CO、C等(因此试管中液体变黑),而硫酸本身被还原成SO2。
SO2能使溴水或KMnO4溶液褪色。
因此,在做乙烯的性质实验前,可以将气体通过NaOH溶液以洗涤除去SO2,得到较纯净的乙烯。
乙炔又称电石气。
结构简式HC≡CH,是最简单的炔烃。
化学式C2H2分子结构:分子为直线形的非极性分子。
无色、无味、易燃的气体,微溶于水,易溶于乙醇、丙酮等有机溶剂。
化学性质很活泼,能起加成、氧化、聚合及金属取代等反应。
能使高锰酸钾溶液的紫色褪去。
乙炔的实验室制法:CaC2+2H2O→Ca(OH)2+C2H2↑化学性质:(1)氧化反应:a.可燃性:2C2H2+5O2 → 4CO2+2H2O现象:火焰明亮、带浓烟。
b.被KMnO4氧化:能使紫色酸性高锰酸钾溶液褪色。
(2)加成反应:可以跟Br2、H2、HX等多种物质发生加成反应。
现象:溴水褪色或Br2的CCl4溶液褪色与H2的加成CH≡CH+H2 → CH2=CH2与H2的加成两步反应:C2H2+H2→C2H4C2H2+2H2→C2H6 (条件为催化剂)氯乙烯用于制聚氯乙烯C2H2+HCl→C2H3Cl nCH2=CHCl→=-[-CH2-CHCl-]n- (条件为催化剂)(3)由于乙炔与乙烯都是不饱和烃,所以化学性质基本相似。
金属取代反应:将乙炔通入溶有金属钠的液氨里有氢气放出。
乙炔与银氨溶液反应,产生白色乙炔银沉淀.1、卤化烃:官能团,卤原子在碱的溶液中发生“水解反应”,生成醇在碱的醇溶液中发生“消去反应”,得到不饱和烃2、醇:官能团,醇羟基能与钠反应,产生氢气能发生消去得到不饱和烃(与羟基相连的碳直接相连的碳原子上如果没有氢原子,不能发生消去)能与羧酸发生酯化反应能被催化氧化成醛(伯醇氧化成醛,仲醇氧化成酮,叔醇不能被催化氧化)3、醛:官能团,醛基能与银氨溶液发生银镜反应能与新制的氢氧化铜溶液反应生成红色沉淀能被氧化成羧酸能被加氢还原成醇4、酚,官能团,酚羟基具有酸性能钠反应得到氢气酚羟基使苯环性质更活泼,苯环上易发生取代,酚羟基在苯环上是邻对位定位基能与羧酸发生酯化5、羧酸,官能团,羧基具有酸性(一般酸性强于碳酸)能与钠反应得到氢气不能被还原成醛(注意是“不能”)能与醇发生酯化反应6、酯,官能团,酯基能发生水解得到酸和醇物质的制取:实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4 (条件是CaO 加热)实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑工业制取乙醇:C2H4+H20→CH3CH2OH (条件为催化剂)乙醛的制取乙炔水化法:C2H2+H2O→C2H4O(条件为催化剂,加热加压)乙烯氧化法:2 CH2=CH2+O2→2CH3CHO(条件为催化剂,加热)乙醇氧化法:2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂,加热)乙酸的制取乙醛氧化为乙酸:2CH3CHO+O2→2CH3CO OH(条件为催化剂和加温)加聚反应:乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)氧化反应:甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃)苯燃烧2C6H6+15O2→12CO2+6H2O (条件为点燃)乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃)乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)乙醛的催化氧化:CH3CHO+O2→2CH3COOH (条件为催化剂加热)取代反应:有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应叫做取代反应。
甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HClCH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HClCHCl3+Cl2→C Cl4+HCl(条件都为光照。
)苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)苯与苯的同系物与卤素单质、浓硝酸等的取代。
如:酚与浓溴水的取代。
如:烷烃与卤素单质在光照下的取代。
如:酯化反应。
酸和醇在浓硫酸作用下生成酯和水的反应,其实质是羧基与羟基生成酯基和水的反应。
如:水解反应。
水分子中的-OH或-H取代有机化合物中的原子或原子团的反应叫水解反应。
①卤代烃水解生成醇。
如:②酯水解生成羧酸(羧酸盐)和醇。
如:乙酸乙酯的水解:CH3COOC2H5+H2O→CH3COOH+C2H5OH(条件为无机酸式碱)加成反应。
不饱和的碳原子跟其他原子或原子团结合生成别的有机物的反应。
乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br乙烯和水CH2=CH2+H20→CH3CH2OH (条件为催化剂)乙烯和氯化氢CH2=H2+HCl→CH3-CH2Cl乙烯和氢气CH2=CH2+H2→CH3-CH3 (条件为催化剂)乙炔和溴水C2H2+2Br2→C2H2Br4乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2乙炔和氢气两步反应:C2H2+H2→C2H4---------C2H2+2H2→C2H6 (条件为催化剂)苯和氢气C6H6+3H2→C6H12 (条件为催化剂)消去反应。
有机分子中脱去一个小分子(水、卤化氢等),而生成不饱和(含碳碳双键或碳碳三键)化合物的反应。
乙醇发生消去反应的方程式CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸170摄氏度)两分子乙醇发生分子间脱水2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸140摄氏度)。
