乙酸和乙醇的酯化反应
乙醇与乙酸发生酯化反应方程式

乙醇与乙酸发生酯化反应方程式
摘要:
I.乙醇与乙酸的酯化反应基本概念
- 酯化反应的定义
- 酯化反应的类型
II.乙醇与乙酸发生酯化反应的化学方程式
- 乙醇与乙酸酯化反应的化学方程式
- 乙醇与乙酸酯化反应的机理
III.乙醇与乙酸酯化反应的条件
- 反应温度和压力
- 催化剂的作用
IV.酯化反应在实际应用中的重要性
- 酯化反应在医药工业中的应用
- 酯化反应在食品工业中的应用
正文:
I.乙醇与乙酸的酯化反应基本概念
酯化反应是一种有机化学反应,指醇与羧酸或含氧无机酸生成酯和水的反应。
这种反应属于酸碱中和反应的一种,但酸与醇的反应并不一定是酯化反应,只有当醇是羟基氢的来源时,反应才能进行。
在有机化学中,乙醇与乙酸发生的酯化反应是最常见的反应之一。
II.乙醇与乙酸发生酯化反应的化学方程式
乙醇与乙酸发生酯化反应的化学方程式如下:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
在这个反应中,乙酸(CH3COOH)与乙醇(C2H5OH)发生反应,生成乙酸乙酯(CH3COOC2H5)和水(H2O)。
III.乙醇与乙酸酯化反应的条件
乙醇与乙酸的酯化反应一般在有催化剂存在的条件下进行。
常用的催化剂有硫酸、氢氧化钠、醇钠和酸酐等。
反应的温度和压力也会影响反应的进行,一般情况下,反应温度越高,反应速率越快;反应压力越大,反应速率也越快。
IV.酯化反应在实际应用中的重要性
酯化反应在医药工业和食品工业中具有非常重要的应用价值。
在医药工业中,酯化反应常被用于合成药物,例如,抗炎药布洛芬就是通过酯化反应合成的。
高中化学乙酸与乙醇的酯化反应

乙酸与乙醇的酯化反应1.酯化反应是一个可逆反应。
为了提高酯的产量,必须尽量使反应向有利于生成酯的方向进行。
一般是使反应物酸和醇中的一种过量。
在工业生产中,究竟使哪种过量为好,一般视原料是否易得。
价格是否便宜以及是否容易回收等具体情况而定。
在实验室里一般采用乙醇过量的办法。
乙醇的质量分数要高,如能用无水乙醇代替质量分数为95%的乙醇效果会更好。
催化作用使用的浓硫酸量很少,一般只要使硫酸的质量达到乙醇质量的3%就可完成催化作用,但为了能除去反应中生成的水,应使浓硫酸的用量再稍多一些。
但一般老师的体会是:最好使用冰醋酸(冬天是固体,夏天可能是液体)和无水乙醇。
同时采用乙醇过量的办法。
只须加入2 滴浓硫酸,多了效果反而不好。
2.制备乙酸乙酯时,反应温度不宜过高,保持在60℃~70℃,不能使液体沸腾。
温度过高时会产生乙醚和亚硫酸等杂质。
液体加热至沸腾后,应改用小火加热。
事先可在试管中加入几片碎瓷片,以防止液体暴沸(一般是没有加碎瓷片,因此加热过猛时有暴沸产生)。
3.使用无机盐Na2CO3溶液吸收挥发出的乙酸。
蒸馏出的乙酸乙酯中因混有乙酸和乙醇,故不能闻到明显的酯的果香味。
此时必须振荡试管,使饱和碳酸钠跟乙酸反应将其吸收,这样既溶解了乙醇又降低酯的溶解性,让酯浮在液面上便于闻其香味,观察色、态。
Na2CO3溶液的作用是:(1)乙酸乙酯在无机盐Na2CO3溶液中的溶解度减小,容易分层析出。
(2)Na2CO3能跟挥发出的乙酸反应,生成没有气味的乙酸钠,便于闻到乙酸乙酯的香味。
4.导气管不要伸到Na2CO3溶液中去,防止由于加热不均匀,造成Na2CO3溶液倒吸入加热反应物的试管中。
5.该实验也可以用中圆底烧瓶作反应物的容器,这时反应物的量要大一些。
我的体会是可按书上装置进行,所得乙酸乙酯量也不少,效果也明显。
一般是加热沸腾,让其反应,使乙酸乙酯蒸发出来。
一般未加碎石,要出现暴沸。
[注意事项]乙醛的银镜反应1.不能用久置起沉淀的乙醛。
乙酸和乙醇的酯化反应机理

乙酸与乙醇酯化反应机理
说起乙酸跟乙醇那个酯化反应,咱们得先从它是个啥子反应讲起。
乙酸,就是咱们说的醋酸,乙醇呢,就是酒里面的主要成分酒精。
这两个东西搁一块儿,加点催化剂,比如浓硫酸,再加热一下,就能反应生成乙酸乙酯跟水。
这个反应的过程,说起来也简单。
先是乙酸在催化剂的作用下,变得更容易被乙醇攻击。
乙酸把个质子丢给乙醇,自己变成了乙酰离子,乙醇呢,就变成了带正电的乙铵离子。
这时候,乙酰离子就像个亲核试剂,去攻击乙铵离子的氧原子,两个东西就缠到一块儿,形成了一个四面体的中间体。
但是呢,这个中间体不稳定,它会把个水分子丢出去,就变成了咱们要的乙酸乙酯。
这个过程,就像两个人先拉近距离,再互相配合,最后分出个结果来。
为啥子说这个过程重要呢?因为乙酸乙酯这个东西,用处可大了。
它是个重要的有机溶剂,还能用来做香精、香料,甚至涂料、油墨里头都要用到它。
所以,咱们得把这个反应搞透了,才能想办法提高产率,做出更多更好的乙酸乙酯来。
当然了,这个反应也不是一帆风顺的。
温度、压力、催化剂的种类跟用量,都能影响到反应的速率跟产率。
所以,科学家们一直都在研究,怎么优化这些条件,才能让反应更加高效、环保。
总的来说,乙酸跟乙醇的酯化反应,就是个典型的有机化学反应,里头涉及到的机理,也是咱们化学里头的基础知识。
虽然说起来有点复杂,但是只要咱们理解了,就能更好地掌握它,为咱们的生产生活服务。
乙酸与乙醇的酯化反应的副反应

乙酸与乙醇的酯化反应的副反应
乙酸与乙醇酯化反应是一种常见的有机化学反应,通常用于合成酯类化合物。
然而,这种反应在实际应用中存在一些副反应,这些副反应会影响反应的效率和产物的纯度。
其中一种常见的副反应是消耗醇反应。
在乙酸与乙醇进行酯化时,有些乙醇通过消耗反应与乙酸反应,产生大量副产物水和二乙酸。
消耗反应的一个常见机制是醇脱水作用,即乙醇中的羟基被脱除,形成乙烯气体和水。
这种消耗反应通常会导致反应的低收率和产品的低纯度。
另一种副反应是逆酯化反应。
逆酯化反应是酯键反向断裂并释放酸和醇。
它通常由酸中水分的存在引起。
在酯化反应中,加入一些水可以促进逆酯化反应,导致产物中出现未反应的乙酸和乙醇。
逆酯化反应也会导致产物与理论收率之间的差异。
在一些脱度缩合反应中出现的副反应在酯化反应中也可能会出现,例如产生醇和酸的缩合反应。
这种反应是通过酸催化作用引起的,会形成酮或醛。
如果缩合反应产生的产物没有被进一步反应掉,产品的纯度也会受到负面影响。
除了上述副反应,还有其他少见的副反应,例如酸水解反应,即酸催化下产物被水分硬化成醇与酸;以及酶水解反应,即产生酯醇浆料转变至醇酸浆料。
这些副反应通常由反应条件和催化剂的选择等因素影响。
为了控制这些副反应并提高反应效率和产物的纯度,反应条件需要进行优化。
例如,可以控制反应中水分和催化剂的量,以避免逆酯化和消耗反应的发生。
此外,通过在反应中加入分子筛等干燥剂,可以有效地减少水分的存在,从而抑制逆酯化反应的发生。
乙酸和乙醇的酯化反应
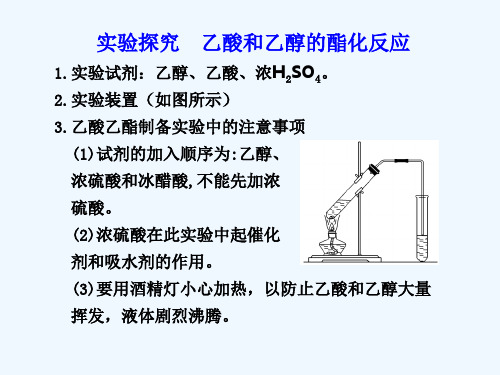
写出制取乙酸乙酯的化学方程式:________________ ___________________________________________。 (2)上述实验中饱和碳酸钠溶液的作用是(填字母) _________。 A.中和乙酸和乙醇 B.中和乙酸并吸收部分乙醇 C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中
_____________________________________________
___________________________________________。
解析 (1)配制乙醇、浓硫酸、乙酸混合液时,各试 剂加入试管的顺序依次为:CH3CH2OH→浓硫酸 →CH3COOH。将浓硫酸加入乙醇中,边加边振荡是 为了防止混合时产生的热量导致液体飞溅造成事故; 将乙醇与浓硫酸的混合液冷却后再与乙酸混合,是为 了防止乙酸的挥发造成原料的损失。在加热时试管 中所盛溶液不能超过试管容积的 1 。 因为试管容积
实验探究 乙酸和乙醇的酯化反应
1.实验试剂:乙醇、乙酸、浓H2SO4。 2.实验装置(如图所示) 3.乙酸乙酯制备实验中的注意事项
(1)试剂的加入顺序为:乙醇、 浓硫酸和冰醋酸,不能先加浓 硫酸。 (2)浓硫酸在此实验中起催化 剂和吸水剂的作用。 (3)要用酒精灯小心加热,以防止乙酸和乙醇大量 挥发,液体剧烈沸腾。
【实验探究2】已知下列数据:
物质 熔点(℃) 沸点(℃) 密度(g/cm3)
乙醇 -117.0
78.0
0.79
乙酸
16.6
117.9
1.05
乙酸乙酯 -83.6
77.5
0.90
浓硫酸
-
(98%)
338.0
1.84
乙酸的酯化反应方程式

乙酸的酯化反应方程式乙酸的酯化反应是一种常见的有机合成反应。
酯化反应是一种醇和酸发生酯结合的化学反应。
在乙酸的酯化反应中,乙酸与一种醇反应生成酯,并释放水分子。
这种反应通常需要酸催化剂的存在,常用的酸催化剂包括硫酸、磷酸等。
乙酸的酯化反应可以用以下方程式表示:酸 + 乙醇→ 乙酸乙酯 + 水在这个方程式中,酸可以是无机酸,如硫酸、磷酸等,也可以是有机酸,如乙酸、苯甲酸等。
乙醇是一种醇,也就是乙酸的醇基。
乙酸乙酯是生成的酯,它由乙酸和乙醇的醇基通过酯结合形成。
水是酯化反应中生成的副产物,它由醇和酸反应生成。
乙酸的酯化反应是一种平衡反应,反应达到平衡时,生成物和反应物的浓度将保持不变。
在这种情况下,反应的方向取决于反应物的浓度。
如果反应物中酸或醇的浓度较高,反应将向右进行,生成更多的酯。
相反,如果生成物中酯的浓度较高,反应将向左进行,生成更多的反应物。
乙酸的酯化反应在有机合成中有广泛的应用。
酯是一类重要的有机物,它们具有多种用途,包括作为溶剂、香料、润滑剂和某些药物的原料等。
乙酸乙酯是一种常用的溶剂,在油漆、涂料和胶水等工业中广泛使用。
此外,乙酸乙酯还可以作为合成某些药物的中间体。
乙酸的酯化反应可以通过不同的方法进行改变和控制。
一种常见的方法是改变反应物的摩尔比例,通过控制乙酸和乙醇的比例来控制生成物的产量。
此外,可以调节反应的温度、反应时间和酸催化剂的浓度等参数,以优化反应条件,提高产率和选择性。
乙酸的酯化反应是一种常见的有机合成反应,通过乙酸和乙醇的酯化反应,可以合成乙酸乙酯等酯类化合物。
这种反应在化工和制药工业中具有广泛的应用,通过调节反应条件和反应物的比例,可以控制反应的产率和选择性。
乙酸和乙醇反应的活化能

乙酸和乙醇反应的活化能
乙酸和乙醇之间的反应通常是酯化反应,其中乙酸和乙醇反应生成乙酸乙酯(常称为醋酸乙酯)和水。
这种反应是一个酸催化的酯化反应,通常使用硫酸等酸性催化剂。
酯化反应的活化能主要与反应的催化剂、反应条件以及反应物的性质有关。
由于这是一个催化反应,酸性催化剂通常能够降低反应的活化能,促使反应更容易发生。
在实际化学反应中,活化能的具体数值会受到多种因素的影响,因此具体数值可能会有所不同。
这包括反应条件(温度、压力等)、使用的催化剂类型和浓度、反应物浓度等。
总体而言,酸催化的酯化反应通常是相对较容易进行的反应,催化剂有助于降低反应的活化能,使反应在温和的条件下进行。
实验探究 乙酸和乙醇的酯化反应
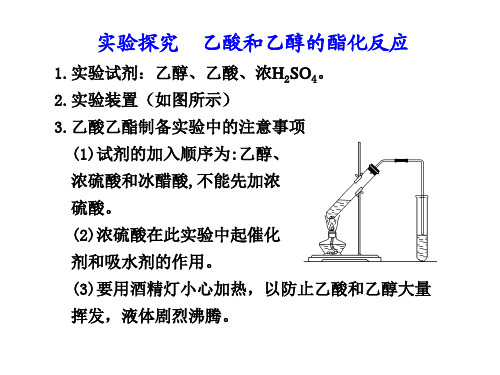
(2)在试管a中加入几粒沸石(或碎瓷片) (2)在试管a中加入几粒沸石(或碎瓷片) 在试管 (3)① (3)①加快反应速率 ②及时将产物乙酸乙酯蒸出, 及时将产物乙酸乙酯蒸出, 以利于平衡向生成乙酸乙酯的方向移动 (4)吸收随乙酸乙酯蒸出的少量乙酸和乙醇并减少乙 (4)吸收随乙酸乙酯蒸出的少量乙酸和乙醇并减少乙 酸乙酯的溶解 (5)b中的液体分层,上层是透明的油状液体 (5)b中的液体分层, 规律技巧 实验室制取乙酸乙酯时, 实验室制取乙酸乙酯时,为 防止倒吸,可用干燥管(如图)、倒扣 防止倒吸,可用干燥管(如图)、倒扣 )、 的漏斗等装置来替代图中的竖立的导管。 的漏斗等装置来替代图中的竖立的导管。
实验探究
乙酸和乙醇的酯化反应
1.实验试剂:乙醇、乙酸、 1.实验试剂:乙醇、乙酸、浓H2SO4。 实验试剂 2.实验装置(如图所示) 2.实验装置(如图所示) 实验装置 3.乙酸乙酯制备实验中的注意事项 3.乙酸乙酯制备实验中的注意事项 (1)试剂的加入顺序为:乙醇、 (1)试剂的加入顺序为:乙醇、 试剂的加入顺序为 浓硫酸和冰醋酸,不能先加浓 浓硫酸和冰醋酸, 硫酸。 硫酸。 (2)浓硫酸在此实验中起催化 (2)浓硫酸在此实验中起催化 剂和吸水剂的作用。 剂和吸水剂的作用。 (3)要用酒精灯小心加热,以防止乙酸和乙醇大量 (3)要用酒精灯小心加热, 要用酒精灯小心加热 挥发,液体剧烈沸腾。 挥发,液体剧烈沸腾。
mL,那么所盛溶液不超过10 mL,按体积比1:4:4 为30 mL,那么所盛溶液不超过10 mL,按体积比1:4:4
1 3
Hale Waihona Puke 的比例配浓硫酸、乙酸和乙醇的混合溶液, 的比例配浓硫酸、乙酸和乙醇的混合溶液,由此可 知,对应的浓硫酸、乙酸和乙醇的体积为1 mL、 对应的浓硫酸、乙酸和乙醇的体积为1 mL、 mL、 mL。既然在题中已经给定的是30 mL的大 4 mL、4 mL。既然在题中已经给定的是30 mL的大 试管,那就不能用其他规格的试管, 试管,那就不能用其他规格的试管,在答题时要特别
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6. 酯化反应原理:
HO ①
H —C—C—O—H
方式一:酸脱氢、醇脱羟基 H
②
+ + CH3COOH
HOCH2CH3
18O
浓硫
△
酸
CH3COOCH2CH3
H2O
18O
方式二:酸脱羟基、醇脱氢
+ + CΒιβλιοθήκη 3COOHHOCH2CH3
18O
浓硫
△
酸
CH3COOCH2CH3
18O
H2O
7.酯化反应在生活中的应用: ❖ 做鱼时加醋加酒味道香醇。
2.实验现象:
饱和碳酸钠溶液的液面上有透明的油状液体,并可闻到香味。
3.实验结论:
乙酸与乙醇在浓硫酸加热的条件下生成了一种具有香味的油状液体
4.反应方程式:
+ + CH3COOH
HOCH2CH3
浓硫
△
酸
CH3COOCH2CH3
H2O
酸
醇
酯
水
5.酯化反应概念:
酸与醇反应生成酯和水的反应 逆反应为酯的水解反应。
酒越陈越香 醋能解酒吗? 香醋
在身体发生酯化反应微乎其微,所以用 醋解酒,不可靠。
祝同学们学习进步!
再见
高中化学
酯化反应
乾县杨汉高中 刘 敏
做鱼时加一点 醋,加一点酒, 做出的鱼味道 特别香醇。你 想知道是为什 么吗?
酒越陈越香
1982年的拉菲
醋能解酒,是什么原因呢? 因为发生了酯化反应
乙酸的酯化反应
1.实验:
在一支试管中加入3mL乙醇,然 后边加边震荡试管边慢慢加入2mL 浓硫酸和2mL冰乙酸,按图连接好 装置,用酒精灯缓慢加热,将产生 的蒸汽经导管通到饱和碳酸钠溶液 的液面上,观察现象。
