铝三角铁三角化学方程式总结
铁三角铝三角金属钠

Fe3Fe+4H2O(g)高温Fe3O4+4H2Fe + 2H+ = Fe2+ + H2↑Fe + Cu2+ == Cu + Fe2+Fe + 2Fe3+ == 3Fe2+Fe2+ + 2OH- == Fe(OH)2↓4Fe(OH)2 + O2 + 2H2O == 4 Fe(OH)3(生成白色沉淀,迅速变成灰绿色,最后变成红褐色)2Fe2+ + Cl2 == 2Fe3+ + 2Cl-2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2OFe3+ + 3OH- == Fe(OH)3↓2Fe3+ + 3CO32- + 3H2O == 2Fe(OH)3↓ + 3CO2↑(双水解)2Fe3+ + Cu == 2Fe2+ + Cu2+2Fe3+ + 2I- == 2Fe2+ + I2Fe3+ + 3SCN- == Fe(SCN)3 (红色溶液,Fe3+离子检验)Fe3+ + 3H2O Fe(OH)3(胶体) + 3H+ (氢氧化铁胶体制备)FeO + 2H+ == Fe2+ + H2O Fe2O3 + 6H+ == Fe3+ + 3H2OFe3O4 + 8H+ == Fe2+ + 2Fe3+ + 4H2OAl2Al + 6H+ == 2Al3+ + 3H2↑2Al + 2OH- + 2H2O == 2AlO2- + 3H2↑Al3+ + 3H 2O Al(OH)3(胶体)+ 3H+(明矾净水)Al3+ + 3OH- == Al(OH)3↓Al3+ + 4OH- == AlO2- + 2H2OAl3+ + 3NH3.H2O == Al(OH)3↓+ 3NH4+(实验室制备氢氧化铝,白色胶状沉淀)2Al3+ + 3CO32- + 3H2O == 2Al(OH)3↓ + 3CO2↑ (双水解)2Al3+ + 3S2- + 6H2O == 2Al(OH)3↓ + 3H2S↑(双水解)Al3+ + 3AlO2- + 6H2O== 4Al(OH)3↓(双水解)2AlO2- + CO2 + 3H2O ==2 Al(OH)3↓+ CO32-(CO2少量)AlO2- + CO2 + 2H2O == Al(OH)3↓+ HCO3-(CO2过量)Al2O3 + 6H+ == 2Al3+ + 3H2OAl2O3 + 2OH- == 2AlO2- + H2OAl(OH)3 + 3H+ == Al3+ + 2H2OAl(OH)3 + 2OH- == AlO2- + 2H2O①过量OH —②过量H +③H + ④OH—⑤H + ⑥OH — 2Al+Fe 2O 3高温Al 2O 3+2Fe (铝热反应)Al+3O 2点燃2Al 2O 3(纯氧) 2Al(OH)3 △Al 2O 3+3H 2OFe 或Al 与H 2SO 4(浓)或HNO 3(浓)室温下钝化Na2H 2O + 2Na = 2Na + +2OH - + H 2↑ 4Na+TiCl 4(熔融)=4NaCl+Ti 2H 2O + 2Na 2O 2 = 4NaOH+ O 2↑ 2Na 2O 2+2CO 2=2Na 2CO 3+O 2 2NaR+ Ca 2+ = CaR 2 +2Na +2NaR+ Mg 2+ = MgR 2 +2Na + ( 离子交换法软化水) CaR 2 +2Na + =2NaR+ Ca 2+ (再生) NaH + H 2O = NaOH + H 2↑CO 2+NH 3+NaCl+H 2O =NaHCO 3↓+NH 4Cl (侯氏制碱法)一、镁、铝的工业制法1、镁的工业制法:(从海水中提取镁)2、铝的工业制法:(以铝土矿为原料)二、铝三角及应用1、三角关系:Al 3+、Al(OH)3与AlO 2—相互转化的关系Al 3+Al(OH)3AlO 2— 石灰过滤 海水 Mg(OH)2 盐酸 MgCl 2 电解 熔融Mg铝土矿 除杂质 Al 2O 3 熔融、电解冰晶石作熔剂 Al有关离子方程式:A 、Al 3+与AlO 2—的相互转化①Al 3+→AlO 2—: ②AlO 2—→Al 3+: B 、AlO 2—与Al(OH)3的相互转化③AlO 2—→Al(OH)3: ④Al(OH)3→AlO 2—: C 、Al 3+与Al(OH)3的相互转化⑤Al(OH)3→Al 3+: ⑥Al 3+→Al(OH)3: 2、铝三角的应用①制取Al(OH)3Al 3+ + 3NH 3·H 2O == Al(OH)3↓+3NH 4+(常用方法) AlO 2—+ CO 2 + 2H 2O == Al(OH)3↓+ CO 32—②离子共存问题:a 、Al 3+与OH —、S 2—、AlO 2—、HCO 3—、CO 32—、HSO 32—等离子因生成沉淀或双水解而不能大量共存;b 、AlO 2—与Al 3+、H +、NH +、Fe 3+等离子因生成沉淀或双水解反应而不能大量共存。
铝 铁三角

鋁的化學方程式(1) 2Al + 2NaOH + 2H2O === 2NaAlO2 + 3H2(上升)(2) 4Al + 3O2 === 2Al2O3(條件:點燃)[2Al + Fe2O3 === Al2O3 + 2Fe(條件:高溫)](3) 2Al2O3 === 4Al + 3O2(上升)(條件:電解)(4) 2Al + 3Cl2 === 2AlCl3(條件:點燃)[2Al + 6HCl === 2AlCl3 + 3H2(上升)](5) Al2O3 + 2NaOH === 2NaAlO2 + H2O(6) Al2O3 + 6HCl === 2AlCl3 + 3H2O(7) NaAlO2 + HCl + H2O === NaCl + Al(OH)3(沉淀)(8) Al(OH)3 + NaOH === NaAlO2 + 2H2O(9) 2Al(OH)3 === Al2O3 + 3H2O(條件:加熱)(10)Al(OH)3 + 3HCl === AlCl3 + 3H2O(11)AlCl3 + 3NH3.H2O === Al(OH)3(沉淀) + 3NH4Cl[AlCl3 + 3NaOH === Al(OH)3(沉淀) + 3NaCl](12)NaAlO2 + HCl(過) === AlCl3 + NaOH + H2O铝热反应可简单认为是铝与某些金属氧化物(如Fe2O3、Fe3O4、Cr2O3、V2O5等)在高热条件下发生的反应。
铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应实验反应化学方程式:氧化铁:2Al+Fe2O3=Al2O3+2Fe四氧化三铁:8Al+3Fe3O4=4Al2O3+9Fe二氧化锰:4Al+3MnO2=2Al2O3+3Mn(反应条件都为高温)(铝热反应配平技巧:取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,底下便可得到Al为4,Fe为9)鐵的反應方程式(1) FeS + H2SO4 === FeSO4 + H2S(上升)(2) FeSO4 + NaOH === Fe(OH)2(沉淀) + Na2SO4(3) Fe(OH)2 + H2SO4 === Fe(OH)2(沉淀) + Na2SO4(4) Fe + S === FeS(加熱)(5) FeO + H2SO4 === FeSO4+H2O(6) Fe(OH)2 + O2 + H2O === Fe(OH)3(沉淀)(7) FeO + CO === (高溫) Fe +CO2(8) 2Fe + O2 === (加熱) FeO(9) Fe +2HCl === FeCl2 + H2(上升)(10) 2Fe + 3Cl2 === (加熱)2FeCl3(11) Fe3O4 + 4CO === (加熱) 2FeCl3(12) 3Fe + 2O2 === (點燃) Fe3O4(13) Fe2O3 + 3CO === (加熱) 2FeCl3 +3H2O(14) Fe2O3 + 6HCl === 2FeCl3 + 3H2O(15) Fe(OH)3 === (加熱) Fe2O3 + 3H2O(16) 2FeCl3 + Fe === 3FeCl2(17) 2FeCl2 + Cl2 === 2FeCl3(18) Fe(3+) + SCN(-) ==== [Fe(SCN)](2+)(19) Fe(OH)3 + 3HCl === FeCl3 + 3H2O(20) FeCl3 + 3NaOH === Fe(OH)3 (沉淀) + 3NaCl。
初三化学三角关系化学方程式及反应类型总结
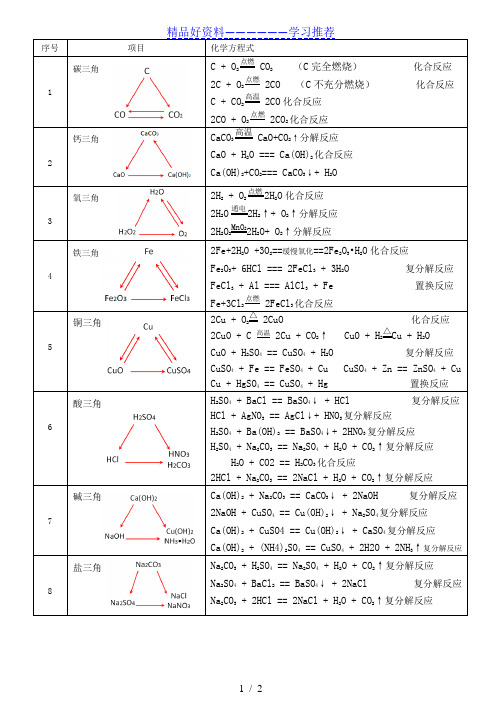
序号项目化学方程式1 碳三角 C + O2点燃 CO2(C完全燃烧)化合反应2C + O2点燃 2CO (C不充分燃烧)化合反应C + CO2高温 2CO化合反应2CO + O2点燃 2CO2化合反应2 钙三角CaCO3高温CaO+CO2↑分解反应CaO + H2O === Ca(OH)2化合反应Ca(OH)2+CO2=== CaCO3↓+ H2O3 氧三角2H2 + O2点燃2H2O化合反应2H2O通电2H2↑+ O2↑分解反应2H2O2MnO22H2O+ O2↑分解反应4 铁三角2Fe+2H2O +3O2==缓慢氧化==2Fe2O3•H2O化合反应Fe2O3+ 6HCl === 2FeCl3 + 3H2O 复分解反应FeCl3 + Al === AlCl3 + Fe 置换反应Fe+3Cl2点燃 2FeCl3化合反应5 铜三角2Cu + O2△ 2CuO 化合反应2CuO + C 高温 2Cu + CO2↑ CuO + H2△Cu + H2OCuO + H2SO4 == CuSO4 + H2O 复分解反应CuSO4 + Fe == FeSO4 + Cu CuSO4 + Zn == ZnSO4 + CuCu + HgSO4 == CuSO4 + Hg 置换反应6 酸三角H2SO4 + BaCl == BaSO4↓ + HCl 复分解反应HCl + AgNO3 == AgCl↓+ HNO3复分解反应H2SO4 + Ba(OH)2 == BaSO4↓+ 2HNO3复分解反应H2SO4 + Na2CO3 == Na2SO4 + H2O + CO2↑复分解反应H2O + CO2 == H2CO3化合反应2HCl + Na2CO3 == 2NaCl + H2O + CO2↑复分解反应7 碱三角Ca(OH)2 + Na2CO3 == CaCO3↓ + 2NaOH 复分解反应2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO4复分解反应Ca(OH)2 + CuSO4 == Cu(OH)2↓ + CaSO4复分解反应Ca(OH)2 + (NH4)2SO4 == CuSO4 + 2H2O + 2NH3↑复分解反应8 盐三角Na2CO3 + H2SO4 == Na2SO4 + H2O + CO2↑复分解反应Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl 复分解反应Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑复分解反应9 盐三角CaCO3 + 2HCl == CaCl2 + H2O + CO2↑复分解反应CaCl2 + 2AgNO3 == 2ACl↓ + Ca(NO3)2复分解反应CaCO3 + 2HNO3 == Ca(NO3)2 + H2O + CO2↑复分解反应。
铁三角的化学方程式

引言概述:化学方程式是描述化学反应的重要工具,通过化学方程式可以清晰地了解反应物与物之间的转化关系以及反应的定量比例关系。
铁三角是指整个方程式中的反应物、物和反应条件。
本文将继续介绍铁三角的化学方程式的相关知识,包括5个大点的详细阐述。
正文内容:1.氧化反应(OxidationReaction)1.1铁的氧化反应(IronOxidation)铁能与氧反应铁的氧化物,反应方程式可以表示为:2Fe+O2→2FeO1.2锌的氧化反应(ZincOxidation)与铁类似,锌也能与氧发生反应,锌的氧化物,反应方程式可表示为:2Zn+O2→2ZnO1.3铝的氧化反应(AluminumOxidation)铝在氧气中也会发生氧化反应,铝的氧化物,化学方程式可表示为:4Al+3O2→2Al2O32.还原反应(ReductionReaction)2.1铁的还原反应(IronReduction)铁的氧化物可以还原为纯铁,反应方程式可表示为:FeO+CO→Fe+CO22.2锌的还原反应(ZincReduction)锌的氧化物也可以通过还原反应得到纯锌,反应方程式可表示为:ZnO+C→Zn+CO2.3铝的还原反应(AluminumReduction)铝的氧化物也可以还原为纯铝,化学方程式可表示为:2Al2O3+3C→4Al+3CO23.置换反应(DisplacementReaction)3.1铁的置换反应(IronDisplacement)铁可以与其他金属离子发生反应,进行置换反应,反应方程式可表示为:Fe+CuSO4→FeSO4+Cu3.2锌的置换反应(ZincDisplacement)类似地,锌也能通过置换反应与其他金属离子反应,反应方程式可表示为:Zn+2HCl→ZnCl2+H23.3铝的置换反应(AluminumDisplacement)铝也能与其他金属离子进行置换反应,化学方程式可表示为:2Al+3CuCl2→2AlCl3+3Cu4.酸碱反应(AcidBaseReaction)4.1铁的酸碱反应(IronAcidBaseReaction)铁可以与酸发生酸碱反应,反应方程式可表示为:Fe+2HCl→FeCl2+H24.2锌的酸碱反应(ZincAcidBaseReaction)锌也与酸发生酸碱反应,反应方程式可表示为:Zn+2HCl→ZnCl2+H24.3铝的酸碱反应(AluminumAcidBaseReaction)铝同样能与酸发生酸碱反应,化学方程式可表示为:2Al+6HCl→2AlCl3+3H2铁能与氧气燃烧成铁的氧化物,反应方程式可表示为:4Fe+3O2→2Fe2O3锌的燃烧反应同样能锌的氧化物,反应方程式可表示为:2Zn+O2→2ZnO铝也能与氧气燃烧铝的氧化物,化学方程式可表示为:4Al+3O2→2Al2O3总结:铁、锌和铝是铁三角中的常见金属元素,在不同反应条件下,它们能参与氧化反应、还原反应、置换反应、酸碱反应和燃烧反应。
铁三角化学方程式

铁三角化学方程式关于铁三角的所有化学方程式如下:一、Fe和Fe²⁺的相互转换。
1、Fe到Fe²⁺的离子或化学方程式。
2Fe³⁺+Fe=3Fe²⁺。
Cu²⁺+Fe=Fe²⁺+Cu。
2H⁺+Fe=Fe²⁺+H₂。
S+Fe=(加热)FeS。
I₂+Fe=FeI₂。
2、Fe²⁺到Fe的离子或化学方程式。
Zn+Fe(NO₃)₂=Zn(NO₃)₂+Fe。
2Al+3Fe(NO₃)₂=2Al(NO₃)₃。
C+2FeO=(加热)2Fe+CO₂。
CO+FeO=(加热)Fe+CO₂。
H₂+FeO=(加热)Fe+H₂O。
二、Fe和Fe³⁺的相互转换。
1、Fe到Fe³⁺的离子或化学方程式。
3Cl₂+2Fe=2FeCl₃。
3Br₂+2Fe=2FeBr₃。
6HNO₃+Fe=Fe(NO₃)₃+3H₂O+3NO₂。
浓6H₂SO₄+2Fe=Fe₂(SO₄)₃+6H₂O+3SO₂。
2Ag⁺+Fe=Fe²⁺+2Ag(只有Ag⁺是不可能生成Fe³⁺的)。
2、Fe³⁺到Fe的离子或化学方程式。
3Zn+2Fe³⁺=3Zn²⁺+2Fe。
Al+Fe³⁺=Al³⁺+Fe。
3CO+Fe₂O₃=2Fe+3CO₂。
3C+2Fe₂O₃=4Fe+3CO₂。
3H₂+Fe₂O₃=2Fe+3H₂O。
三、Fe²⁺和Fe³⁺的相互转换。
1、Fe²⁺到Fe³⁺的离子或化学方程式。
O₂+4FeO=2Fe₂O₃。
Cl₂+FeCl₂=2FeCl₃。
Br₂+FeBr₂=2FeBr₃。
8HNO₃+2FeO=2Fe(NO₃)₃+4H₂O+2NO₂。
H₂O₂+2Fe²⁺=2Fe³⁺+2(OH)⁻。
2、Fe³⁺到Fe²⁺的离子或化学方程式。
