初中化学各知识点树状图
九年级化学各单元知识点框架图

初三新的一门课程——化学,很多孩子不喜欢这门学科,因为有太多枯燥繁琐的需要记忆的东西。
其实,初三的化学知识点都是很基础的东西,今天我特意分享了一份初三各单元知识表,里面囊括了所以化学重点及简易运算法则,希望能对孩子有所帮助!
第一单元:走进化学世界
第二单元:我们周围的空气
第三单元:自然界的水
第四单元:物质构成的奥秘
第五单元:化学方程式
第六单元:碳和碳的氧化物
第七单元:燃料及其利用
第八单元:金属和金属材料
第九单元:溶液。
初中化学各单元知识框架图
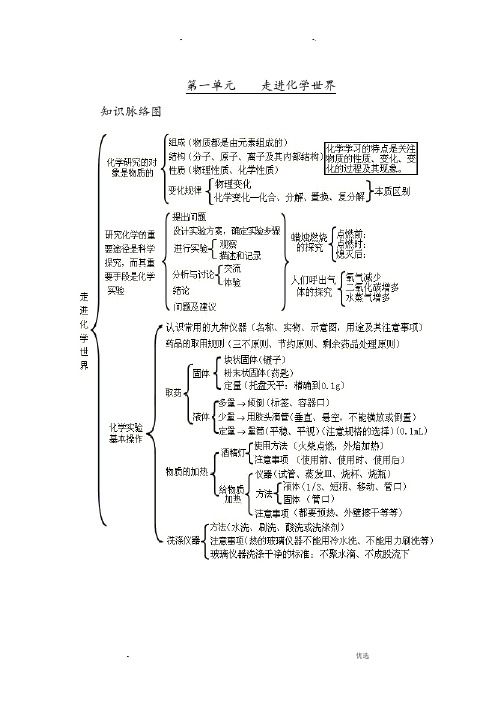
第一单元走进化学世界知识脉络图第二单元我们周围的空气知识脉络图第三单元自然界的水知识脉络图第四单元物质构成的奥秘知识脉络图第五单元化学方程式知识脉络图第六单元碳和碳的氧化物知识脉络图第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐氧化物、酸、碱和盐的知识点可以从以下十个方面掌握:一、化学用语1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分生石灰:CaO熟石灰、消石灰、石灰水的主要成分:Ca(OH)2石灰石、石:CaCO3食盐的主要成分:NaCl纯碱、口碱:Na2CO3烧碱、火碱、苛性钠:NaOH 胆矾、蓝矾:CuSO4.5H2O碳酸钠晶体:Na2CO3.10H2O 氨水:NH3.H2O二、化合物的分类三、金属活动性1、金属活动性顺序:KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
四、酸、碱、盐的溶解性1、常见盐与碱的溶解性:(如果不读出括号中的字,是不是一个较好记忆的顺口溜):钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙氢氧化镁、氢氧化铜、氢氧化铁四微溶物:Ca(OH)2(石灰水注明“澄清〞的原因)CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:所谓的氢氧化银、碳酸铝、碳酸铁五、分解反响发生的条件反响后有气体、水或沉淀生成。
初级中学化学各单元学习知识框架图
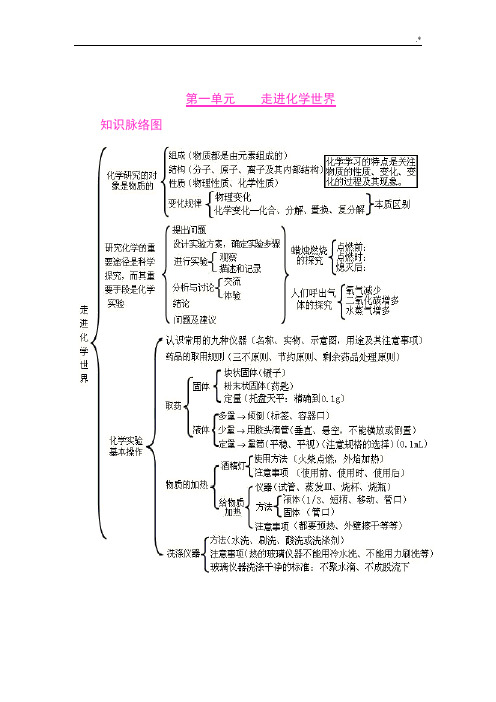
第一单元走进化学世界知识脉络图第二单元我们周围的空气知识脉络图第三单元自然界的水知识脉络图第四单元物质构成的奥秘知识脉络图第五单元化学方程式知识脉络图第六单元碳和碳的氧化物知识脉络图第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐氧化物、酸、碱和盐的知识点可以从以下十个方面掌握: 一、化学用语 1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分生石灰??CaO 熟石灰、消石灰、石灰水的主要成分??Ca(OH)2石灰石、大理石??CaCO3食盐的主要成分??NaCl 纯碱、口碱??Na2CO3烧碱、火碱、苛性钠??NaOH 胆矾、蓝矾??CuSO4.5H2O 碳酸钠晶体??Na2CO3.10H2O 氨水??NH3.H2O二、化合物的分类三、金属活动性1、金属活动性顺序:KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
四、酸、碱、盐的溶解性1、常见盐与碱的溶解性:(如果不读出括号中的字,是不是一个较好记忆的顺口溜?)钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:所谓的氢氧化银、碳酸铝、碳酸铁五、分解反应发生的条件反应后有气体、水或沉淀生成。
初中化学1至12单元知识框架图(全)(打印)

第一单元 走进化学世界f 育法(水洗、刷洗、酸洗或洗涤剂)洗涤仪器彳注意事项(热的玻璃仪器不能用冷水i 总 不能用力刷洗等〉I 玻璃仪器洗涤干净的标准:不聚水辖U 不成股流下1锅炉爆炸、轮胎爆炸是物理变化,可燃性物质导致的爆炸是化学变化,如氢气爆炸,烟花爆炸等。
2、 催化剂能加快和减慢反应速率,其质量和化学性质反应前后不变,物理性质,如形状、状态可能改 变 3、 由一种元素组成的物质可能为单质,也可能为混合物。
如氧气02和臭氧03两种单质混合得到混合物,也只由氧(O )元素组成。
金刚石C 和石墨C 的混合物,只由碳(C )元素组成等。
只有说由一种元素 组成的纯净物,才能说一定是单质。
冰水混合物是纯净物,冰是水的固态,还是水。
优学研究的对象是物质的 组成(物质都是由元素组成的〉结构(分子、原子、离子及其商部结构) 〈性质(物理性质、化学隍质)变化规律r 物理变化[化学变化一k 合、分摒、置换、复分解}本质区别走 进 化 学 世 界硏究化学的重 要途径是科学 探究,而其重 要r提出间題设计实验有案.确定貓歩骤 迸行实验・ 分析与讨论* 结论I 间题及建议r 观察1摊述和记录交赢 体■验J 占嵌时.、、体的探究峙二氧化碳增多 水蒸气增多/认识常用的九种仪器(名称、实物、示宜图,用途及其注言事项〉 药品的取用规则(三不原则、节约J®则、剩余葯品处理原则)取药&化学实验J基耳操作%. 「块状固您(辍子)固体・粉耒状固悴(药匙)L 定量(托盘天平:精确到0*1或「多壘-倾倒(:标签,容器口)襪体{少壘T 用胶头滴管〔垂宜、悬空,不能横放或倒置) ' L 定堇一壘筒(平稳、平视)(注意规格的选择)(0. ImL )「使用右法〔火柴点燃,外焰加热〉 I 注意車项〔使用前、使用时、使用后〉 「仪器■(试管、葵发皿、烧杯、烧瓶) 、吐J 液体茨短柄、移动、管口) 万京1固体(管口)I 注意事项(都要预热、外壁擦干等等)广酒周丁 物I 质的加热J4、原子是化学变化中的最小粒子。
(完整版)初中化学全册十个知识框架图

初中化学全册10个知识框架图,轻松拿高分!化学好老师第一单元:走进化学世界第二单元:我们周围的空气第三单元:自然界的水第四单元:物质构成的奥秘第五单元:化学方程式第六单元:碳和碳的氧化物第七单元:燃料及其利用第八单元:金属和金属材料第九单元:溶液第十单元:酸碱盐一、化学用语1、电离方程式:2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4·5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O。
二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na 除外)。
三、酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁四、复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物。
初中化学全册10个知识框架图(新)

初中化学全册10个知识框架图第一单元:走进化学世界第二单元:我们周围的空气第三单元:自然界的水第四单元:物质构成的奥秘第五单元:化学方程式第六单元:碳和碳的氧化物第七单元:燃料及其利用第八单元:金属和金属材料第九单元:溶液第十单元:酸碱盐1、电离方程式:2、物质的俗称和主要成分:生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4·5H2O;碳酸钠晶体Na2CO3.10H2O;氨水NH3.H2O1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物。
九年级化学知识结构图

化学反应的基本类型
化学反应可分为化合反应、分解反应、 置换反应和复分解反应四种基本类型。
溶液、酸碱盐基础
溶液的概念和组成
溶液是一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物,由溶质和溶剂 组成。
酸碱盐的定义和性质
酸指电离时产生的阳离子全部都是氢离子的化合物;碱指电离时产生的阴离子全部都是氢 氧根离子的化合物;盐指电离时生成金属阳离子(或铵根离子)和酸根离子的化合物。酸 碱盐具有不同的化学性质。
九年级化学知识结构图
目 录
• 基础知识概述 • 微观世界探秘 • 宏观物质变化规律 • 实验技能与科学探究 • 环境保护与可持续发展观念培养 • 总结回顾与拓展延伸
01 基础知识概述
物质的组成与分类
01
02
03
物质的组成
物质由元素组成,元素是 同一类原子的总称,原子 由质子、中子和电子构成。
物质的分类
化学键
分子或离子之间通过相互 作用力形成的稳定结构, 包括离子键、共价键和金 属键等。
微观粒子间相互作用力
离子键
由阴、阳离子之间通过静电作用 所形成的化学键,如NaCl中的离
子键。
共价键
原子之间通过共用电子对所形成 的化学键,如HCl中的共价键。
分子间作用力
分子之间存在着相互作用的弱力, 包括范德华力和氢键等,影响物
氧化还原反应
化学反应中元素化合价发生变化的反应称为氧化还原反应, 其中失去电子(或化合价升高)的过程称为氧化,得到电 子(或化合价降低)的过程称为还原。
原电池与电解池
利用氧化还原反应将化学能转化为电能的装置称为原电池; 利用电能引起氧化还原反应的装置称为电解池。
电极反应与电池反应
