碳酸钠和碳酸氢钠教学设计(广大附中 胡国良)
碳酸钠和碳酸氢钠教学设计

《碳酸钠和碳酸氢钠》教学设计【教学目标】1.了解碳酸钠和碳酸氢钠的物理性质和化学性质;2.掌握碳酸钠和碳酸氢钠鉴别及相互转化的常见方法;3.在实验探究、列表比较碳酸钠、碳酸氢钠性质的过程中,感受科学探究的一般方法,体验对比实验在研究物质性质中的重要作用。
【教学重点】碳酸钠和碳酸氢钠的化学性质【教学难点】碳酸钠和碳酸氢钠的热稳定性、与酸的反应【教学过程】【活动一:我说你猜】它是制作面包的发酵粉、食用它可治疗胃酸过多、它可制作泡沫灭火器。
它是__________【活动二:分组探究实验1】比较Na 2CO 3和NaHCO 3物理性质的异同药品和仪器:Na 2CO 3和NaHCO 3固体、蒸馏水、试管、胶头滴管【活动三:探究实验2】比较Na 2CO 3和NaHCO 3的热稳定性233写在表格最后一列。
药品和仪器:Na 2CO 3和NaHCO 3固体、澄清石灰水、试管、酒精灯步骤:如左图所示,取2支洁净干燥的试管,将Na 2CO 3和NaHCO 3分别进行加热,观察实验现象。
这一反应可用于鉴别Na 2CO 3和NaHCO 3。
【活动四:分组探究实验3】比较Na2CO3和NaHCO3与稀盐酸的反应药品和仪器:Na2CO3和NaHCO3固体、稀盐酸、试管、胶头滴管233【思考与交流4】等质量Na2CO3和NaHCO3与足量相同的稀盐酸反应,谁生成气体更多?为什么?【使用反馈】1、下列关于碳酸钠和碳酸氢钠的比较中,不准确的是( )A.二者在水中的溶解度不同,碳酸氢钠的溶解度小于碳酸钠B.二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠C.二者都能与盐酸反应放出二氧化碳气体,等质量时生成CO2的量一样多D.二者在一定条件下能够相互转化2、有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有4位同学为鉴别它们采用了以下不同的方法,其中不可行的是( )A.分别配成溶液,再加入澄清石灰水B.分别配成溶液,再加入CaCl2溶液C.分别加热,再检验是否有使澄清石灰水变浑浊的气体产生D.分别取固体样品,滴加同浓度盐酸,观察产生气泡的快慢3。
碳酸钠与碳酸氢钠教案
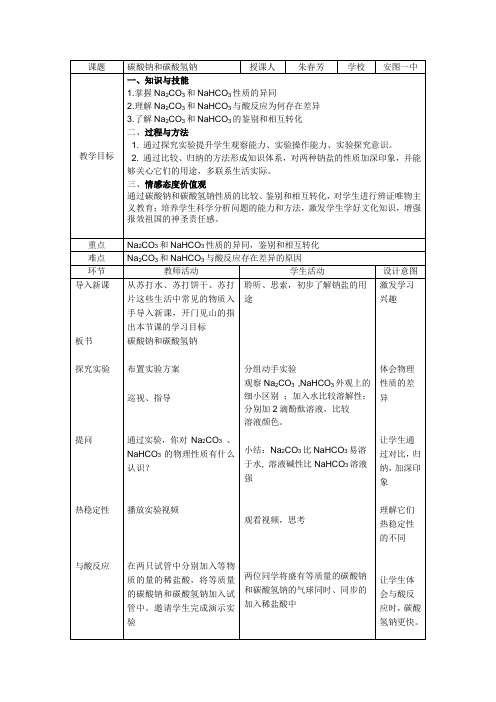
小结:Na2CO3比NaHCO3易溶于水,溶液碱性比NaHCO3溶液强
观看视频,思考
两位同学将盛有等质量的碳酸钠和碳酸氢钠的气球同时、同步的加入稀盐酸中
分组实验:奇数组的同学把稀盐酸逐滴滴入2mLNa2CO3溶液的试管中,边滴边振荡;偶数组的同学把Na2CO3溶液逐滴滴2mL稀盐酸溶液的试管中,边滴边振荡
设计意图
导入新课
板书
探究实验
提问
热稳定性
与酸反应
设疑
与碱的反应
与盐的反应
鉴别和转化
总结
从苏打水、苏打饼干、苏打片这些生活中常见的物质入手导入新课,开门见山的指出本节课的学习目标
碳酸钠和碳酸氢钠
布置实验方案
巡视、指导
通过实验,你对Na2CO3、NaHCO3的物理性质有什么认识?
播放实验视频
在两只试管中分别加入等物质的量的稀盐酸,将等质量的碳酸钠和碳酸氢钠加入试管中。邀请学生完成演示实验
CaCI2白色沉淀不反应
教学
反思
同时和酸反应,碳酸钠慢,为什么呢?
和学生分析,讨论并利用坐标来解释现象。
引导学生思考:与NaOH、
Ca(OH)2反应时的异同
讲述:Na2CO3与可溶性的钙盐、钡盐反应生成沉淀
指导、评价
侯德榜及侯氏制碱法
聆听、思索,初步了解钠盐的用途
分组动手实验
观察Na2CO3,NaHCO3外观上的细小区别;加入水比较溶解性;分别加2滴酚酞溶液,比较
课题
碳酸钠和碳酸氢钠授课人源自朱春芳学校安图一中
教学目标
1、知识与技能
1.掌握Na2CO3和NaHCO3性质的异同
2.理解Na2CO3和NaHCO3与酸反应为何存在差异
碳酸钠和碳酸氢钠教学设计
碳酸钠和碳酸氢钠
【教学目标】
知识与技能:通过教师的演示实验,学生学习碳酸钠和碳酸氢钠的区别,对照记忆相关的物理性质和化学性质,并学会定量滴定离子方程式的
书写。
过程与方法:学生通过观察分析教师的实验探究过程,学习探究物质差异的一般方法(从物理性质和化学性质上进行分析)。
情感态度价值观:通过对碳酸钠和碳酸氢钠的学习,学生树立探究物质内部差异的学习兴趣,同时通过对碳酸钠和碳酸氢钠与盐酸的反应,培
养学生严谨的理性思考习惯。
【教学重点】
碳酸钠与碳酸氢钠溶解度、热稳定性、与盐酸反应的差异
【教学难点】
碳酸钠、碳酸氢钠与盐酸反应现象不同的本质原因。
【教学过程设计】
【板书设计】
1、溶解度 Na
2CO
3
> NaHCO
3
溶液都呈碱性
2、热稳定性 Na
2CO
3
< NaHCO
3
2NaHCO
3△
Na
2
CO
3
+ CO
2
↑+ H
2
O
3.与盐酸的反应
NaHCO
3: HCO
3
-+ H+ = CO
2
↑+ H
2
O
Na
2CO
3
: CO
3
2-+ H+ = HCO
3
-
HCO
3-+ H+ = CO
2
↑+ H
2
O。
碳酸钠和碳酸氢钠教学设计

《碳酸钠和碳酸氢钠》教学设计一、教材分析《几种重要的金属化合物》是新教材中有关金属及其化合物性质的重要的学习内容之一。
金属在自然界基本以化合态形式存在,因此第一节介绍金属单质的性质后,第二节重点讲述了钠、铝、铁的化合物性质。
在这一节内容里,新教材安排了精彩的图片和丰富的实验探究。
旨在强调学生的主体学习能力,倡导学生主动参与,乐于探究,培养学生探究、分析和解决问题的能力、以及交流与合作的能力,对提高学生全面的科学素养具有十分重要的作用。
《碳酸钠与碳酸氢钠》本节内容在呈现方式上有以下特点:图画较多,有利于引起学生的学习兴趣,对所学知识留下深刻的印象;活动较多,有利于培养学生的各种能力。
在介绍碳酸钠和碳酸氢钠时,采用科学探究的形式,突出实验引探功能;利用对比的方法,让学生填写表格,可使学生在比较中学习。
教学重点是碳酸钠和碳酸氢钠的性质,难点是如何引导学生正确观察实验现象,并分析这些现象的本质,对碳酸钠和碳酸氢钠的性质作出正确的判断。
二、教学设计思路:《碳酸钠和碳酸氢钠》这部分内容,其性质并不是本单元教学的难点,知识层面要求不高。
教材的设计是以列表的形式提供信息,由学生进行实验方案的设计,且实验都是简单易做,学生可以通过努力独立完成或者小组合作完成。
根据以上特点,我淡化了Na2CO3和NaHCO3化学性质的教学,将本节的教学目标定位在“让学生体验科学探究的过程,学会科学探究的一般方法”,并且将科学精神、探究精神融入教学当中。
从生活引入,以实验探究、讨论式教学法的形式展开,特别是设计学案,辅助教学,引导和启发学生进行主动建构,充分发挥学生课堂主体地位,又可充分发掘教师的辅导作用,这样更能激发学生学习的兴趣和情感。
本节教学设计的主线是:创设情境—猜想设疑—实验探究—小组讨论--得出结论——总结内容--习题巩固。
充分利用多媒体课件,运用引导-实验探究、对比的教学方法进行边讲边实验教学。
这在教学中突出学生动手能力、合作交流能力、观察能力、对比能力、分析问题和解决问题能力的培养。
碳酸钠与碳酸氢钠的教案

碳酸钠与碳酸氢钠的教案教案标题:碳酸钠与碳酸氢钠的教案教学目标:1. 了解碳酸钠和碳酸氢钠的化学性质和常见用途。
2. 掌握碳酸钠和碳酸氢钠的化学式、分子结构和物理性质。
3. 能够区分碳酸钠和碳酸氢钠,并能够正确使用它们。
教学重点:1. 碳酸钠和碳酸氢钠的化学性质和常见用途。
2. 碳酸钠和碳酸氢钠的化学式、分子结构和物理性质。
教学准备:1. PowerPoint演示文稿。
2. 实验器材和化学试剂:碳酸钠、碳酸氢钠、酚酞指示剂、醋酸。
教学过程:一、导入(5分钟)1. 利用图片或实物引入碳酸钠和碳酸氢钠的概念,让学生猜测它们的用途和性质。
2. 引导学生思考碳酸钠和碳酸氢钠在日常生活中的应用。
二、讲解碳酸钠和碳酸氢钠的化学性质和常见用途(15分钟)1. 通过PPT演示,向学生介绍碳酸钠和碳酸氢钠的化学性质,如溶解性、酸碱性等。
2. 列举碳酸钠和碳酸氢钠在日常生活中的常见用途,如烹饪调料、清洁剂、药品等。
三、介绍碳酸钠和碳酸氢钠的化学式、分子结构和物理性质(20分钟)1. 解释碳酸钠和碳酸氢钠的化学式及其分子结构。
2. 通过实验演示或图片展示,展示碳酸钠和碳酸氢钠的物理性质,如颜色、形状、溶解度等。
四、实验操作(15分钟)1. 将一定量的碳酸钠和碳酸氢钠溶解于水中,观察其溶解性和酸碱性变化。
2. 使用酚酞指示剂和醋酸进行酸碱中和反应,观察反应现象。
五、总结与拓展(10分钟)1. 总结碳酸钠和碳酸氢钠的化学性质和常见用途。
2. 提出拓展问题,如碳酸钠和碳酸氢钠在环境保护中的应用等。
六、作业布置(5分钟)布置相关作业,如写一篇关于碳酸钠和碳酸氢钠的小结,或者设计一个实验来验证碳酸钠和碳酸氢钠的某一性质。
教学评估:1. 课堂参与度:观察学生在课堂上的积极参与程度。
2. 实验操作:观察学生在实验中的操作技能和实验报告的准确性。
3. 作业完成情况:评估学生对碳酸钠和碳酸氢钠的理解和应用能力。
教学延伸:1. 邀请相关专业人士进行讲座,深入了解碳酸钠和碳酸氢钠在工业生产中的应用和环境影响。
2.1课时3碳酸钠与碳酸氢钠教学设计2024-2025学年高一上学期化学人教版(2019)必修第一册

选择几个典型的碳酸钠和碳酸氢钠应用案例进行分析。
详细介绍每个案例的背景、特点和意义,让学生全面了解碳酸钠和碳酸氢钠的多样性或复杂性。
引导学生思考这些案例对实际生活或学习的影响,以及如何应用碳酸钠和碳酸氢钠解决实际问题。
4. 学生小组讨论(10分钟)
目标:培养学生的合作能力和解决问题的能力。
过程:
2.多媒体课件:用于辅助讲解和展示实例。
3.实物模型:展示碳酸钠和碳酸氢钠的微观结构。
七、教学策略
1.采用问题驱动的教学方法,引导学生主动探究碳酸钠和碳酸氢钠的知识。
2.通过生活实例,激发学生的学习兴趣,提高学生的实践能力。
3.利用多媒体课件和实物模型,增强学生的直观感受,帮助学生更好地理解知识。
八、教学注意事项
c. 碳酸钠常用于洗涤剂的制造。
d. 碳酸氢钠的溶解度大于碳酸钠的溶解度。
- 填空题:根据所学知识,填写下列空白。
a. 碳酸钠的化学式为__________。
b. 碳酸氢钠在生活中的应用包括__________和__________。
c. 碳酸钠与盐酸反应生成__________、__________和__________。
(二)存在主要问题
1. 教学管理:在教学管理方面,存在一些问题,如课堂纪律不够严格,学生的注意力不够集中,需要加强课堂管理,提高学生的学习积极性。
2. 教学组织:在教学组织方面,存在一些问题,如课堂活动安排不够合理,学生的参与度不够高,需要合理安排课堂活动,提高学生的参与度。
3. 教学方法:在教学方法方面,存在一些问题,如讲授法过于单一,学生的主动性和创造性得不到充分发挥,需要丰富教学方法,激发学生的学习兴趣和主动性。
其他学生和教师对展示内容进行提问和点评,促进互动交流。
碳酸钠和碳酸氢钠》教学设计文档
《碳酸钠和碳酸氢钠》教学设计一、课程标准、教材以及学生分析1.课程标准和教材分析课程标准:根据生产、生活中的应用实例或通过实验探究,了解钠及其重要化合物的主要性质。
教材分析:在进行教学设计之前,我参考了三套教材并对其中的相同与不同之处做了分析:人教版:碳酸钠和碳酸氢钠是放在离子反应之后的。
设计了3个实验:(1)取固体分别溶解,滴加酚酞观察颜色;(2)分别加热;(3)分别与稀盐酸反应。
探究了3种性质:碳酸钠和碳酸氢钠的溶解性、碳酸钠和碳酸氢钠的热稳定性、二者与盐酸反应。
苏教版:碳酸钠的性质与应用是放在离子反应之前的。
设计了3个实验:(1)分别向澄清石灰水和CaCl2中滴加碳酸钠溶液;(2)使碳酸钠与浓盐酸反应;(3)测定碳酸钠溶液的pH(用试纸);用碳酸钠溶液洗沾有油污的铜片,通过这三个实验探究碳酸钠中CO32-与Ca2+、H+的反应,以及其碱性。
探究了3种性质:碳酸钠与钙离子生成沉淀;碳酸钠与氢离子反应生成气体;碳酸钠溶液的碱性。
另外涉及到如何由碳酸钠制备碳酸氢钠。
鲁科版:在碳酸钠和碳酸氢钠的主要性质安排在研究物质性质的基本程序和离子反应的相关内容之后。
让学生自己设计实验。
探究了3种性质:碳酸钠和碳酸氢钠与稀盐酸的反应;碳酸氢钠与氢氧化钠反应;碳酸氢钠受热分解。
还涉及到如何由碳酸钠溶液得到碳酸氢钠,以及碳酸氢钠溶液如何得到碳酸钠。
三种教材的相同点和不同点见表1。
表1 三套教材关于碳酸钠和碳酸氢钠的相同与不同之处2.学生分析(1)高中生普遍具有的特点:高中学生的认知发展水平已经到一定的高度,因此学生对知识的学习也有了更高的要求:不喜欢单纯记忆知识而不深入理解。
高中生对物质的兴趣不局限在表面,而是对更本质的知识产生极大的兴趣。
他们希望能够从更本质的角度去看问题。
而化学就是从分子、原子水平来研究物质的科学,因此我们从微观离子之间的反应来解释现象。
不喜欢盲目地做实验而没有一定的方法。
常常会遇到学生上课学得很好,但是一到实验室头脑一片空白,不知道从哪里入手。
碳酸钠和碳酸氢钠教案
碳酸钠和碳酸氢钠教案教案标题:碳酸钠和碳酸氢钠教案教学目标:1. 了解碳酸钠和碳酸氢钠的化学性质和常见用途;2. 能够区分碳酸钠和碳酸氢钠的区别;3. 掌握碳酸钠和碳酸氢钠的制备方法;4. 了解碳酸钠和碳酸氢钠在日常生活中的应用。
教学准备:1. 实验室设备和材料:试剂瓶、试剂盒、试管、酒精灯、试剂(碳酸钠、碳酸氢钠)、酚酞指示剂等;2. PPT或黑板、粉笔等;3. 学生实验报告模板。
教学过程:一、导入(5分钟)1. 利用PPT或黑板,简要介绍碳酸钠和碳酸氢钠的化学性质和常见用途,引发学生的兴趣。
二、理论讲解(15分钟)1. 通过PPT或黑板,详细介绍碳酸钠和碳酸氢钠的结构、性质、制备方法和应用领域。
2. 强调两者之间的区别,包括化学式、酸碱性质、溶解度等。
三、实验演示(20分钟)1. 展示碳酸钠和碳酸氢钠的制备方法,如碳酸钠的烧碱法和碳酸氢钠的中和法。
2. 演示实验过程中,注意安全操作,提醒学生注意实验室安全知识。
四、实验操作(30分钟)1. 学生分组进行实验操作,制备碳酸钠和碳酸氢钠。
2. 学生在实验过程中,记录实验数据和观察现象。
五、实验结果分析与讨论(15分钟)1. 学生根据实验结果,进行数据分析和讨论。
2. 引导学生思考实验中可能出现的误差和原因。
六、知识总结(10分钟)1. 学生通过小组讨论,总结碳酸钠和碳酸氢钠的制备方法和应用。
2. 教师进行知识点的巩固和补充。
七、作业布置(5分钟)1. 布置学生实验报告的撰写任务,要求学生结合实验结果和理论知识,撰写实验报告。
2. 布置相关练习题,巩固学生对碳酸钠和碳酸氢钠的理解。
教学反思:1. 在实验演示和实验操作环节,要保证学生的安全意识和实验操作技能。
2. 教学过程中,要及时引导学生思考和讨论,激发学生的学习兴趣。
碳酸钠和碳酸氢钠教案
碳酸钠和碳酸氢钠教案一、教学目标1.了解碳酸钠和碳酸氢钠的基本性质和用途。
2.掌握碳酸钠和碳酸氢钠的制备方法。
3.能够进行碳酸钠和碳酸氢钠的实验操作,并能够正确记录实验数据。
4.培养学生的实验操作能力和科学探究精神。
二、教学重点1.碳酸钠和碳酸氢钠的制备方法。
2.碳酸钠和碳酸氢钠的实验操作。
三、教学难点1.碳酸钠和碳酸氢钠的制备方法的理解和掌握。
2.实验操作中的注意事项和实验数据的正确记录。
四、教学内容1. 碳酸钠和碳酸氢钠的基本性质和用途碳酸钠碳酸钠,化学式为Na2CO3,是一种白色晶体或粉末状物质。
它是一种重要的化工原料,广泛用于玻璃、纺织、造纸、化肥、洗涤剂等行业。
此外,碳酸钠还可以用于制备其他化学品,如碳酸氢钠、硼酸、过氧化氢等。
碳酸氢钠碳酸氢钠,化学式为NaHCO3,是一种白色粉末状物质。
它是一种重要的食品添加剂,可以用于面包、饼干、蛋糕等烘焙食品的发酵剂。
此外,碳酸氢钠还可以用于制备其他化学品,如碳酸钠、氯化钠、碳酸钙等。
2. 碳酸钠和碳酸氢钠的制备方法碳酸钠的制备方法碳酸钠的制备方法有多种,其中比较常用的是氨法和索达法。
氨法氨法是将氨气通过食盐水溶液,使其与食盐反应生成氯化铵,再将氯化铵与石灰石反应生成氨气和氯化钙,最后将氨气通过浓碱液,使其与二氧化碳反应生成碳酸钠。
氨法的反应方程式如下:2NH3 + 2NaCl + CO2 + H2O → 2NaHCO3 + 2NH4Cl索达法索达法是将石灰石和食盐在高温下反应生成氯化钙和二氧化碳,再将氯化钙与氨水反应生成氯化铵和氢氧化钙,最后将氯化铵与石灰石反应生成氨气和氯化钙,最终将氨气通过浓碱液,使其与二氧化碳反应生成碳酸钠。
索达法的反应方程式如下:CaCO3 + 2NaCl → Na2CO3 + CaCl2CaCl2 + 2NH3 + 2H2O → Ca(OH)2 + 2NH4Cl2NH4Cl + CaCO3 → CaCl2 + 2NH3 + H2O + CO22NH3 + CO2 + H2O → (NH4)2CO3(NH4)2CO3 + Na2CO3 → 2NaHCO3 + 2NH3碳酸氢钠的制备方法碳酸氢钠的制备方法有多种,其中比较常用的是反硝化法和氨法。
碳酸钠和碳酸氢钠性质的探究教学教案
碳酸钠和碳酸氢钠性质的探究教学教案教学目标:1.了解碳酸钠和碳酸氢钠的基本性质;2.能够通过实验观察和记录数据,推测碳酸钠和碳酸氢钠的化学反应;3.培养学生的科学思维和实验动手能力。
教学重点:1.掌握碳酸钠和碳酸氢钠的基本性质;2.在实验中观察和推测化学反应。
教学难点:1.实验设计;2.数据记录和观察。
教学准备:教学过程:Step 1:导入(5分钟)通过观察碳酸钠溶液和碳酸氢钠溶液的外观和性质,让学生比较它们的异同点。
Step 2:实验设计与观察(25分钟)1.学生分组进行实验,每个小组准备一个试管,分别放入碳酸钠溶液和碳酸氢钠溶液。
2.观察不同溶液的外观和颜色的变化,记录观察结果。
3.利用酚酞溶液分别滴在两个试管中,观察颜色的变化。
4.用酸碱指示剂纸测量不同溶液的酸碱性质,记录结果。
5.通过观察和数据记录,让学生推测碳酸钠和碳酸氢钠之间是否存在化学反应,并解释。
Step 3:实验总结(10分钟)1.让学生回答实验中观察到的现象和实验结果。
2.引导学生总结碳酸钠和碳酸氢钠的基本性质和化学反应。
3.让学生归纳和总结碳酸钠和碳酸氢钠的性质差异。
4.展示学生总结的结果,并让他们互相核对。
Step 4:拓展实验(15分钟)让学生对比不同浓度的碳酸钠和碳酸氢钠溶液的性质差异,进行实验观察和记录,进一步探究碳酸钠和碳酸氢钠的性质。
Step 5:实验报告(10分钟)要求学生根据实验过程和观察结果,撰写实验报告。
报告的要求包括实验目的、实验原理、实验步骤、实验结果分析和结论等。
Step 6:小结与评价(5分钟)总结本节课的主要内容,回答学生的问题,并对学生在实验中的表现进行评价。
教学延伸:1.拓展实验:可以进一步比较不同温度下碳酸钠和碳酸氢钠的溶解度差异。
2.课外拓展:让学生了解碳酸钠和碳酸氢钠在生活中的应用和重要性。
教学反思:本节课通过实验的方式,让学生亲自观察和推测化学反应,培养了他们的实验动手能力和科学思维。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
必修1第三章第二节《碳酸钠、碳酸氢钠》教学设计广州大学附属中学胡国良一、教学目标1. 知识与技能:(1)准确的描述Na2CO3与NaHCO3的物理性质(溶解性、状态)。
(2)正确书写Na2CO3和NaHCO3的电离方程式,准确判断能否与盐酸、石灰水、CaCl2反应,准确描述实验现象和书写方程式。
(3)准确描述酸氢钠受热分解实验现象和书写方程式,正确书写Na2CO3转化为NaHCO3的方程式。
(4)归纳酸式盐代表物碳酸氢盐的结构和性质2. 过程与方法:(1)通过Na2CO3和NaHCO3的性质的科学探究,掌握研究物质性质的基本方法。
以Na2CO3和NaHCO3为载体,先观察外观,实验研究物理性质(状态、溶解性),再分析结构(组成、类别、化合价)预测可能的化学性质,实验研究化学性质。
(2)通过Na2CO3、NaHCO3、H2CO3组成对比,理解NaHCO3的两性,并归纳出酸式盐代表物碳酸氢盐的性质。
(3)通过Na2CO3、NaHCO3溶液中滴加酚酞、再逐滴加入稀盐酸的实验,体验微观离子的反应过程。
3. 情感态度与价值观:通过预测和实验探究结果产生矛盾,感受化学魅力,提高学生对“化学是一门以实验为基础的科学”的认识。
通过本节课的学习,增强学生的民族自豪感,培养爱国主义高尚情操。
二、教学重难点教学重点:碳酸钠和碳酸氢钠的性质比较和鉴别方法教学难点:HCO3-的性质、通过Na2CO3、NaHCO3溶液中滴加酚酞、再逐滴加入稀盐酸的实验,体验微观离子的反应过程。
三、本节承载的化学核心观念、化学思想和方法微粒观:盐是由离子基本微粒构成的,盐的性质应该更多的从离子角度思考。
体验微观离子的反应过程,加深对宏观实验的认识。
对比法:将结构相似的物质从相同的角度进行比较,使共同点和差异更加突出,加深对知识的了解,提高学习效率。
陌生物质性质研究方法:陌生物质性质研究是由外观观察,实验研究物理性质(状态、溶解性),再分析结构(组成、类别、化合价)预测可能的化学性质,实验研究化学性质;具体物质各有不同的侧重点。
变化观:化学反应是在一定条件下发生的,不同条件下化学变化可能不同,通过化学反应人们可以获得或消除物质。
CO32-和HCO3-的相互转化是在不同条件下的反应物与产物的互换,转化法可用于物质的除杂。
化学反应是有规律的,Na2CO3和NaHCO3在水溶液中的反应都遵循离子反应规律。
四、教学过程教学环节一:讨论实验方案[引入]:通过前面的学习我们已经知道Na是一种非常活泼的金属元素,在自然界中均以化合态存在。
在钠的诸多化合物中,有着小有名气的"苏氏三姐妹"。
我们首先来认识她们。
化学式小苏打碳酸氢钠NaHCO3苏打碳酸钠Na2CO3说到苏打,他还有一个俗名叫纯碱纯碱和我国著名化学家侯德榜先生讲解:侯德榜,杰出科学家。
他为祖国的化工事业奋斗终生。
并以独创的联合制碱工艺闻名世界。
1926年,他研制的"红三角"牌中国纯碱在美国费城举办的万国博览会上获得了金质奖章,并被誉为"中国工业进步的象征"。
[学生]……[教师]这两个结构决定性质,学习分类法的时候我们了解到,类别相同的物质,性质上有一定的相似之处,碳酸钠大家比较熟悉,我们可以由此推测碳酸氢钠的性质。
[教师]事实是否如我们所预测呢?请大家进行实验设计。
首先考虑物理性质,颜色、状态?都可以直接观察,那么水溶性呢?[学生]……[教师]化学性质应该从哪些方面进行比较?应该选择什么试剂?[学生]……[教师]所以我们应该挑选典型的酸、碱、盐分别去与碳酸钠、碳酸氢钠溶液反应。
这就是我们接下来将要进行的实验。
教学环节二:学生分组实验[教师]我们来研究它们的物理性质,请大家观察所展示的碳酸钠和碳酸氢钠的颜色,状态,并通过实验去了解它们的溶解性。
化学性质我们先做一个钠盐与酸反应的对比实验,请完成分组实验,并把你观察到的现象填在学案中。
[学生]分组实验:[教师](投影分组实验)23323NaHCO3的溶解度是9.6g。
所以相同温度时,Na2CO3比NaHCO3更易溶于水。
(2) Na2CO3和Na2CO3·XH2O是两种不同的纯净物。
Na2CO3溶液结晶生成Na2CO3·XH2O:Na2CO3+ XH2O = Na2CO3·XH2O,Na2CO3·XH2O在空气中易发生风化变成Na2CO3粉末:Na2CO3·XH2O =Na2CO3+ XH2O(失水),属于化学变化。
[教师]小结:同为钠盐的碳酸钠和碳酸氢钠,在化学性质上有不少相同之处,但是也略有差异。
(1)盐不一定都是中性的,为什么Na2CO3和NaHCO3这两种盐的Array水溶液会呈碱性?在选修4会进行研究。
(2)Na2CO3和NaHCO3都能与稀盐酸反应,从基本反应类型的角度看,它们都是复分解反应,请写出反应的离子方程式。
(3)从微观上理解为什么现象会不同:H+和CO32-反应有阶段性,先生成HCO3-,红色变浅,HCO3-和H+再继续反应生成CO2气体,红色褪去。
如图所示。
教学环节三:学生演示实验[教师]盐除了可以与酸反应之外,还可以与碱、盐溶液发生反应,接下来我们通过一个实验来一起研究。
[学生]演示实验①②[教师]小结:(1)碳酸钠溶液中滴加氯化钙溶液,有白色沉淀,而碳酸氢钠溶液无明显现象,因为碳酸钙是难溶于水,碳酸氢钙是可溶盐。
(2)碳酸钠和澄清石灰水反应生成的白色沉淀是碳酸钙,碳酸氢钠和澄清石灰水混合,为什么也会产生白色沉淀呢?该沉淀是什么呢?OH -+HCO 3-=CO 32-+H 2O, CO 32-+Ca 2+=CaCO 3由以上实验可知HCO 3-和H +、OH -不能共存,与Ca 2+或Ba 2+能共存课堂练习一.下列表述中正确的是( )A .碳酸钠和碳酸氢钠可以用澄清石灰水鉴别它们的溶液B .向无色溶液滴加足量盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,则无色溶液中一定有CO 32-C .Na +、Ca 2+、OH -、HCO 3-能大量共存 D .碳酸钠和碳酸氢钠均可与硫酸反应制备CO 2[教师]我们研究某种固体物质,除了从组成上研究通性之外,往往还要研究它的热稳定性,就是在受热的时候,该固体是否容易发生分解反应,接下来我们通过一个实验来一起研究。
[学生]请一个学生上来加热固体,另一个学生观察现象并进行描述。
[教师]该实验表明碳酸氢钠的热稳定性较弱,2NaHCO 3 ===Na 2CO 3 + H 2O + CO 2↑,碳酸氢钠分解可以变成碳酸钠,碳酸钠在在某些条件下可以转化成碳酸氢钠吗?层,久而久之,就形成了溶洞,CaCO 3+H 2O+CO 2=Ca 2++2HCO 3(1)写出Na 2CO 3溶液中通入二氧化碳时反应的化学方程式和离子方程式:______________________________________________________________________________ (2)据此,为什么除去二氧化碳气体中混有的少量氯化氢等酸性气体时,用饱和NaHCO 3溶液而不用Na 2CO 3溶液_____________________________________________________________ [教师]碳酸钠和碳酸氢钠在一定条件下可以相互转化。
[教师]根据碳酸钠与碳酸氢钠各自不同的性质,二者有什么用途呢? [学生]归纳二者的主要用途:发酵粉、药剂、去污剂、灭火剂……提问:根据以上分析,请同学们根据Na 2CO 3和NaHCO 3性质的不同,设计出多种不同的实验方案来鉴别Na 2CO 3和NaHCO 3。
回答:方案一,方案二..........小结:根据同学们讨论的结果,将鉴别Na 2CO 3和NaHCO 3的方法总结如下: PPt :(1):利用两者溶解性的不同讲解: 20℃时,称量约20g Na 2CO 3和NaHCO 3固体,逐渐加入盛有100g 水的烧杯中,不断搅拌至不再溶解。
有固体剩余的是NaHCO3固体,全部溶解的是Na 2CO 3固体。
(2):利用两者水溶液pH 的不同用固体配成等物质的量浓度的溶液 ,测定其水溶液的pH (3):利用两者热稳定性的不同采用如下装置(将装置课前准备好,放在讲台上),分别加热两种固体,能产生使澄清石灰水变浑浊的气体的是NaHCO 3固体,没有变化的是Na 2CO 3固体。
(4):利用两者与酸反应速率的不同在小试管中分别加入Na 2CO 3和NaHCO 3固体(盖满试管底部即可)。
然后倒入稀盐酸,比较两者反应速率的不同。
反应速率较大的是NaHCO3固体,速率较慢的是Na2CO3固体。
(5):鉴别碳酸钠和碳酸氢钠溶液因为Ca(HCO3)2可溶,所以NaHCO3不会和CaCl2反应生成沉淀。
故可以用CaCl2溶液来鉴别Na2CO3和NaHCO3溶液。
方法:分别取样于两支试管中,加入CaCl2溶液,产生白色沉淀的是Na2CO3,没有明显变化的是NaHCO3溶液。
教学环节四:总结规律[教师]本节课我们再一次按规律研究了两种物质,这个规律是什么?[学生]先研究物理性质,然后研究化学性质,分别从组成着手去研究通性和特性,最后研究用途。
[教师]本节课我们通过实验研究了碳酸氢钠的性质,请从组成上对比碳酸钠和碳酸,小结碳酸氢盐性质。
教学反思今年的市发言《碳酸钠和碳酸氢钠》进度的原因,是在没有上氧化钠和过氧化钠的前提下,把碳酸钠和碳酸氢钠提前上了。
于是这堂课作为元素化合物的第一堂课,承担了帮助学生理清研究陌生物质的思路的重要任务。
从上课情况看,整堂课的思路还是非常的清晰,从物理性质——化学性质(组成的角度)——用途,能够给学生提供一个较完整较系统的研究陌生物质的思路。
但是这样实验的容量比较大,40分钟的时间捉襟见肘。
课前学案能够让学生在知识基础方面进行较好的学前准备,但是从实验探究的角度来看,因为对学案的讨论不充分,学生依旧对实验设计没有太多的自主思考,课堂实验中还是有不少学生不清楚实验如何操作,药品应取何用量,究其关键还是对实验目的、实验设计本身没有进行充分探究,有些赶鸭子上架。
教师要引导学生分析方案设计时应考虑的实际问题,完善实验方案。
这次教学中已经渗透研究物质的思路,那么研究物质的基本思路在本节内容设计上属于观念的强化,因此在教学过程中可以赋予其他的化学观念,适当建立宏观与微观的交互,从宏观现象到微观结构或形态的想象,有利于学生感性想象力的发展,从微观结构到宏观性质的推理,有助于学生逻辑推理能力的提升。
向滴有酚酞的的碳酸氢钠溶液中滴加盐酸——立刻出现大量气泡,向滴有酚酞的碳酸钠溶液中滴加盐酸,溶液先颜色变浅,再出现大量气泡。
