吡格列酮杂质总结经验分享
替普瑞酮杂质经验总结分享

替普瑞酮杂质总结分享
序号
名称
CAS
分子式
规格
用途
结构式
1
Teprenone Impurity 1
3879-23-0C23H38O
10mg 25mg 50mg 100mg
研发申报
2
Teprenone Impurity 2
1117-52-8C18H30O
10mg 25mg 50mg 100mg
研发申报
3
Teprenone Impurity 3
40716-66-3C15H26O
10mg 25mg 50mg 100mg
研发申报
4
Teprenone Impurity 4
1117-51-7C18H30O
10mg 25mg 50mg 100mg
研发申报
5
Teprenone Impurity 5
3790-78-1C15H26O
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①伏立康唑杂质②尼莫地平杂质③阿立哌唑杂质④瑞格列奈杂质⑤培美曲塞杂质q:300-
⑥氟维司群杂质⑦地西他滨杂质⑧佐匹克隆杂质⑨长春瑞滨杂质⑩恩杂鲁胺杂质-8058-⑪醋丁洛尔杂质⑫倍他米松杂质
⑬塞来昔布杂质
⑭西酞普兰杂质
⑮氯吡格雷杂质
-303
⑯硫酸益康唑杂质......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。
国产与进口盐酸吡格列酮片的质量考查

日获美 国 F A批准上市 , D 文献资料显示 , 盐酸吡格 本 武 田公 司首先 研制 开 发 的一种 新 型噻 唑 烷 二酮 类 抗 列酮可有效降低 Ⅱ型糖 尿病人 的空腹 血糖、 后 2h 餐 血糖和糖化 血红蛋 白, 常适用 于 Ⅱ型糖尿病 人 。 非 糖尿病药物 , 属胰岛素增敏剂 。该药于 19 年 7月 l 99 5
关键词 盐 酸吡格列酮片 , 出度 , 溶 有关 物质 , 含量均匀度 , 质量考查
中图分 类号 : 97 1 R 2 .1
文献标识码 : A
文章编号 :0 65 8 (0 9 0 -0 50 10 —6 7 20 )30 1 - 4
Qul yE  ̄ ai nD me Nhomakorabea n mp re igi zn d ohoieT bes a t v u t n o o s ca dI otdPo la o eHy r c l d a l i o i t r t
天津药 学
Taj P am c 20 i i hr ay 0 9年 nn
第2 1卷第 3期
1 5
a , rn放冷 , i 再称定各 自重量, 甲醇补足各 自减失的重 用 量, 摇匀 , 滤过 , 取续滤液 , 测定 。结果含量虽然基本相 同, 但考虑到供试品溶液制备中剪碎的粗细 , 超声处理 时位置不同等各种因素, 以甲醇为提取溶剂 , 故 采取超 声处理 3 i, 0mn 作为本方法的提取时间。 3 4 柚皮 苷 含量 测定粗 放度 试 验 取 同一 批样 品 , . 分 别 考查 Da os 1 20mm× . m, m) P e im niC8 5 l ( 4 6m 5 与 h-
n m nx C 8 2 0 mm ×4 6 mm, m)色 谱 柱 , o e e 1 ( 5 . 5
基因毒性杂质

什么是基因毒性杂质对于基因毒性杂质的定义主要是指:在以DNA 反应物质为主要研究对象的体内/ 体外试验中,如果发现它们对DNA 有潜在的破坏性,那可称之为基因毒性。
对没有进行体内实验的情况下,也可以根据关联系做一些相关的体外实验去评估该物质在体内的毒性。
如果没有关联评估的,体外基因毒性物质经常被考虑为假定的体内诱变剂和致癌剂。
GUIDELINE ON THE LIMITS OF GENOTOXIC IMPURITIES ( EMEA/CHMP/QWP/251344/2006 )基因毒性杂质的风险按照目前的法规来说,(体内)基因毒性物质在任何摄入量水平上对DNA 都有潜在的破坏性,这种破坏可能导致肿瘤的产生。
因此,对于基因毒性致癌物,不能说“不存在明显的阀值,或是任何的摄入水平都具有致癌的风险”。
可接受风险的摄入量对于那些可以与DNA 进行反应的化合物,由于在较低的剂量时机体保护机制可以有效的运行,按照摄入量由高到低所造成的影响进行线性推断是很困难的。
目前,对于一个给定诱变剂,我们很难从实验方面证明它的基因毒性存在一个阀值。
特别是对某些化合物,它们可以与非DNA 靶点进行反应,或一些潜在的突变剂,在与关键靶位结合之前就迅速失去了毒性。
由于缺乏支持基因毒性阀值存在的有力证据,而使得我们很难界定一个安全的服用量。
所以有必要采取一个新观点:确定一个可接受其风险的摄入量。
可接受其风险的摄入量即毒理学阈值一般通用的被定义为Threshold of Toxicological Concern (TTC)。
具体含义为:一个“ 1.5ug/day ”的TTC 值,即相当于每天摄入1.5ug 的基因毒性杂质,被认为对于大多数药品来说是可以接受的风险(一生中致癌的风险小于100000 分之1 )。
按照这个阀值,可以根据预期的每日摄入量计算出活性药物中可接受的杂质水平。
在特定的条件下一些基因毒性杂质也可以有较高的阈值。
吡格列酮临床研究总结

吡格列酮
C 研究结果 吡格列酮组患者胰岛素敏感性(Matsuda指数)增加显著高于安慰剂组(P<0.001)
C 研究结果 治疗后,吡格列酮组患者TG水平较基线比显著下降,而安慰剂组无显著性差异
P=0.007
P=0.90
C 研究结果
治疗后,吡格列酮组患者较安慰剂组更显著升高HDL-C水平(P=0.008)
2008 吡格列酮延缓高风险的2型糖尿病患者粥样斑的进展——PERISCOPE研究
2007
吡格列酮降低心脏复合终点、致死性或非致死性心梗、致死性卒中或复发性卒中风险—— PROactive研究亚组分析 吡格列酮降低死亡/心梗/中风风险达18%,但增加心力衰竭发生率——Lincoff荟萃分析
2006 吡格列酮延缓动脉粥样硬化的进展——CHICAGO研究
吡格列酮临床研究总结
吡格列酮的历史
胰岛素抵抗是 2 型糖尿病和心血管疾病共同的病理生理基础。改善胰岛素抵抗应贯穿 2 型糖尿病
治疗的全程,噻唑烷二酮类药物(TZDs)是目前的一类胰岛素增敏剂。然而吡格列酮作为重要
TZD药物之一,发展历程却跌宕起伏,但随着各项临床研究的开展而最终证明了自己的地位!
2019 吡格列酮可能对卒中/短暂性脑缺血发作和糖尿病前期患者的二级预防有效——IRIS研究分析
吡格列酮组 安慰剂组
D 研究意义
ACT NOW研究证实:
吡格列酮早期干预显著延缓糖尿病前期患者疾病进展,降低
T2DM风险72%。
1
ACT NOW研究进一步证实:
吡格列酮能升高HDL,降低TG,针对T2DM的血脂紊乱特点。
2
三、KPNC研究
A
研究背景
B
研究方案
降糖药吡格列酮合成方法的比较与评价

都 需要 繁 琐 的 后处 理 过 程及 高 温 高 压 的苛 刻 条 件 .收 率较 低 , 用有 毒 和 昂贵 的试 剂 , 业应 用受 限 。 使 工
总 之 , 法 工 艺 路 线较 长 , 期对 主 原 料 1 该 后 7消 耗 很大 , 生 产成 本相 对较 高 。 方 法 5 2与 4 氟 苯 甲腈 ( 8 : 一 1 )在 钠 氢 作 用下 得 4 『一 一2 (一 5 乙基 吡 啶一 一 ) 氧 基1 甲腈 ( 9 ,9经 雷 尼 镍 和 甲 2基 乙 苯 1 )1
2若 直接 参 与 成酚 醚 反应 则需 要 很 苛刻 的反 应条 件 , 因 而 有必 要 对 其进 行 活 化 。该 法 使用 2的 甲磺 酸酯 或 对 甲苯 磺 酸酯 为 原料 , 酸 酯 的形 式 活 化 了 2的 醇 羟基 , 加 了成 磺 增 酚 醚反 应 的 活性 . 虽然 避 免 了 危 险试 剂 氢 化钠 . 用 了 较短 采 的工 艺路 线 , 在 制 备 1时 仍 采用 水 解 方 法 , 同样 会 使产 但 也
。
~
1 R= e Ts 0 K= M l ,s
… 。 ,
。
”
1 R=M e Ts 0
,
1 3
l 5
。 . 。
一 。
哌啶
6 % 4
一ห้องสมุดไป่ตู้
。
泄
+
一H P2 d. ] C ,
图 4 方 法 3合 成 路 线 图 图 5 方 法 4合 成 路 线 图
该法 特 点基 本 同 “ 方法 2 ,但 对 硝 基苯 酚 容 易氧 化 聚 ”
吡格列酮药典杂质5-羟基吡格列酮的一锅法合成

境因素相互作用引起的胰岛素分泌和(或)作用缺 的碱、还原剂、溶剂和反应温度等影响因素进行筛
陷导致的一组以慢性血葡萄糖升高为特征的代谢 选优化,可通过“一锅法”高效便捷地合成 5羟基
异常综合症[3]。最新的调查结果显示我国成人糖 吡格列酮。
尿病的患病率已达 9 7% [4]。同时,有研究[5 ~ 表7] 明,合并糖尿病的重症患者,易发生压疮,痊愈过
反应也可能会发生氧化生成相应氧化降解杂质。 效构建 CO 键的方法[14],可以实现氧原子的高选
对此类杂质药典[2]明确指出需要进行定性和定量 择性插入[15]。受 Hodney 等[16]应用氧气氧化的启
研究。
发,我们以吡格列酮盐酸盐为原料,采用廉价的、
糖尿病(diabetes , )是 mellitus DM 由遗传和环 来源丰富的氧气作为氧化剂,通过对反应体系中
第203231卷年第6 6月期
化 学 研 究 与 应 用 化 学 研 究 与 应 用
Chemical Research and Application
第,, 卷 VJoul.n3e320N32o13. 6
文章编号: ( ) 10041656 2021 06119205
吡格列酮药典杂质 5羟基吡格列酮的一锅法合成
吴国芳1,邓建梅2,廖永志3
(1. 攀枝花学院附属医院,四川 攀枝花 ; 617000 2. 攀枝花学院生物与化学工程学院,四川 攀枝花 ; 617000 3. 攀枝花学院数学与计算机学院,四川 攀枝花 ) 617000
摘要:5羟基吡格列酮是治疗糖尿病原料药吡格列酮及其制剂氧化降解研究的必备杂质,而其合成方法未见 文献报道。本文以盐酸吡格列酮为起始原料,利用 KHMDS/ O2 / ( ) P OMe 3 氧化体系,通过去质子化、氧气氧化 和还原反应可“一锅法”合成克级规模的 5羟基吡格列酮。通过对反应所需的碱、还原剂、溶剂和温度等条件 进行优化,确定最佳反应条件为:四氢呋喃为溶剂,KHMDS 为碱,亚磷酸三甲酯为还原剂,反应温度为70 oC。 收率可达 82% ,其结构经1H 、 NMR 13 、 CNMR HMBC 和 HRMS(ESI)确证。 关键词:5羟基吡格列酮;氧化;吡格列酮;糖尿病 中图分类号:O621 254 文献标志码:A
瑞舒伐他汀Rosuvastatin全套杂质结构列表
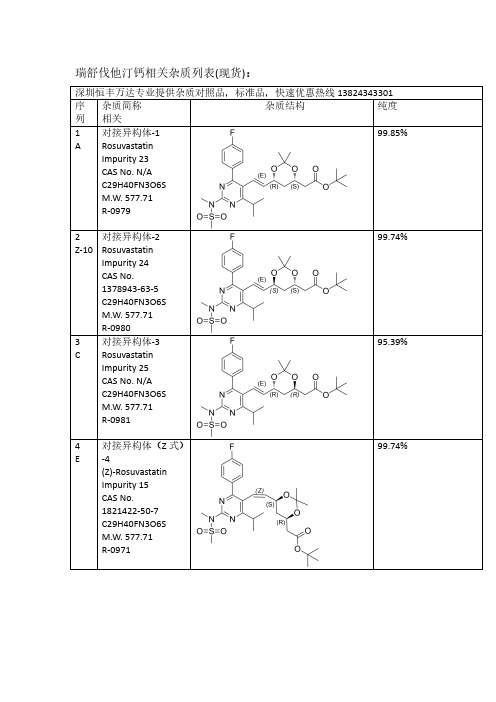
瑞舒伐他汀钙相关杂质列表(现货):深圳恒丰万达专业提供杂质对照品,标准品,快速优惠热线138****3301序列杂质简称相关杂质结构纯度1A 对接异构体-1RosuvastatinImpurity 23CAS No.N/A C29H40FN3O6S M.W.577.71R-097999.85%2Z-10对接异构体-2RosuvastatinImpurity 24CAS No.1378943-63-5C29H40FN3O6S M.W.577.71R-098099.74%3C 对接异构体-3RosuvastatinImpurity 25CAS No.N/A C29H40FN3O6S M.W.577.71R-098195.39%4E对接异构体(Z 式)-4(Z)-Rosuvastatin Impurity 15CAS No.1821422-50-7C29H40FN3O6S M.W.577.71R-097199.74%5Q对接光降解-1CAS No.N/A C29H40FN3O6S M.W.577.71R-099099.31%6P对接光降解-2CAS No.N/A C29H40FN3O6S M.W.577.71R-099299.69%7I丙酮加合物CAS No.N/A C32H46FN3O7S M.W.635.7998.23%8Z-12对接脱氟CAS No.N/AC29H41N3O6S M.W.559.72R-099399.46%9Z-16双键环氧脱丙酮叉CAS No.N/AC29H40FN3O7S M.W.593.7199.18%10B脱丙酮叉异构体-1ent-Rosuvastatin tert-Butyl Ester CAS No.615263-60-0C26H36FN3O6S M.W.537.65R-091899.90%11Z-11脱丙酮叉异构体-2(3S,5S)-Rosuvastatintert-Butyl Ester CAS No.2185805-16-5C26H36FN3O6S M.W.537.65R-097699.66%12D 脱丙酮叉异构体-3(3R,5R)-tert-ButylRosuvastatin (Rosuvastatin Impurity)CAS No.2162136-65-2C26H36FN3O6S M.W.537.65R-0911100%13F 脱丙酮叉异构体(Z 式)-4CAS No.1821422-51-8C26H36FN3O6S M.W.537.65R-099699.44%14S脱丙酮叉光降解-1CAS No.N/A C26H36FN3O6S M.W.537.65R-098999.61%15R脱丙酮叉光降解-2CAS No.N/A C26H36FN3O6S M.W.537.65R-099199.20%16J丙酮加合物脱丙酮叉Rosuvastatin EP Impurity A CAS No.1714147-49-5C29H42FN3O7S M.W.595.72R-099799.65%17Z-13无氟脱丙酮叉CAS No.N/AC26H37N3O6S M.W.519.65R-099599.17%18Z-255-甲氧基脱叉杂质RosuvastatinImpurity 42CAS No.N/A C27H38FN3O6S M.W.551.67R-0910098.80%19Z-263-甲氧基脱叉杂质RosuvastatinImpurity 47CAS No.N/A C27H38FN3O6S M.W.551.67R-0910598.65%203,5-二甲氧基脱叉杂质Rosuvastatin Impurity 44CAS No.N/A C28H40FN3O6S M.W.565.70R-0910698%21G钙盐异构体-1Rosuvastatin EP Impurity G Calcium Salt CAS No.1242184-42-4(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.88%22Z-1钙盐异构体-2(3S,5S)Rosuvastatin Calcium Salt CAS No.1584149-34-7(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.04R-091598.15%23H钙盐异构体-3Rosuvastatin EP Impurity B Calcium Salt(3R,5R)-Rosuvastatin Calcium Salt CAS No.1422515-55-61094100-06-7(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.04R-091296.13%24V钙盐异构体(Z 式)-4Rosuvastatin Z-Isomer Calcium Salt CAS No.1444772-08-01445208-17-2(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.51%25Z-245-甲氧基钠盐CAS No.N/AC23H29FN3NaO6S M.W.517.5599.50%26Z-273-甲氧基钠盐CAS No.N/AC23H29FN3NaO6S M.W.517.5596.83%27Z-293,5-二甲氧基钠盐CAS No.N/AC24H31FN3NaO6S M.W.531.5797.78%28U钙盐异构体光降解-5RosuvastatinImpurity 1Calcium Salt CAS No.854898-49-0854898-48-9(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.75%29T 钙盐异构体光降解-6RosuvastatinImpurity 2Calcium Salt CAS No.854898-50-3854898-53-6(free base)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.83%30Z-18钠盐异构体光降解-7(混合物)RosuvastatinImpurity 1Calcium SaltCAS No.N/A C22H27FN3O6S.1/2Ca M.W.480.5420.04R-093499.16%31Z-20钙盐异构体光降解-8Rosuvastatin Impurity CAS No.N/A C22H26FN3O6S M.W.479.5296.69%32Z-14钙盐无氟DesfluoroRosuvastatin Calcium Salt CAS No.N/A847849-66-5(acid)C22H28N3O6S.1/2Ca M.W.462.5420.04R-099499.78%33K 丙酮加合物钙盐Rosuvastatin EPImpurity A Calcium Salt CAS No.1714147-47-31715120-13-0(free acid)C25H33FN3O7S.1/2Ca M.W.538.6120.04R-092599.46%34M 内酯Rosuvastatin EPImpurity D CAS No.503610-43-3C22H26FN3O5S M.W.463.52R-09199.46%35N 内酯异构体CAS No.N/AC22H26FN3O5S M.W.463.5299.46%36内酯异构体CAS No.N/A C22H26FN3O5S M.W.463.5297%37Z-283-甲氧基内酯CAS No.N/AC23H28FN3O5S M.W.477.5598.97%38L5-氧代Rosuvastatin EP Impurity C freed acid CAS No.1620823-61-1(sodium salt)1422619-13-3(acid)C22H26FN3O6S M.W.479.5297.92%39Z-63-氧代3-Oxo Rosuvastatin Sodium Salt CAS No.1346606-28-71346747-49-6(acid)C22H25FN3O6S.Na M.W.478.5222.99R-091798.61%40O内酯脱水Rosuvastatin2,6-Diene Lactone Impurity CAS No.1246665-85-9C22H24FN3O4S M.W.445.5299.36%R-094141Z-44,6-二烯Rosuvastatin4,6-Diene Impurity CAS No.1422954-13-9C22H26FN3O5S M.W.463.53R-092795.44%42Z-152,6-二烯CAS NO.1422954-12-8(free acid)C22H26FN3O5S R-092695.70%43Z-8脱甲基二钠盐(体内代谢产物)N-Desmethyl Rosuvastatin Disodium Salt CAS No.371775-74-5(free base)C21H24FN3O6S.2Na M.W.465.50222.99R-09598.87%44W光降解内酯CAS No.854898-47-8C22H26FN3O5S M.W.463.5299.80%45X 光降解内酯CAS No.854898-46-7C22H26FN3O5S M.W.463.5297.84%46Z-2Z 式异构体内酯CAS No.N/A C22H26FN3O5S M.W.463.5296.52%47Z-9脱甲基内酯(体内代谢产物)N-Desmethyl Rosuvastatin Lactone CAS:1797419-58-9C21H24FN3O5S M.W.449.5097.42%48Z-7基因毒性杂质(体内代谢产物)Rosuvastatin Impurity 28CAS No.N/A C22H28FN3O7S M.W.497.54R-098498.94%49Z-5母核烯醛(工艺相关杂质)CAS No.890028-66-7C18H20FN3O3S M.W.377.4398.85%50Z-42母核无氟膦盐CAS No.N/A C34H35BrN3O2PS M.W.660.6099.14%51Y 本体脱丙酮叉CAS No.N/A C26H36FN3O6S M.W.537.6599.74%更多其他项目:雷西纳德,阿格列汀,依鲁替尼,唑吡坦,利奈唑胺,西他沙星,沙丁胺醇,罗替戈汀,丙戊酸钠,左乙拉西坦,西格列汀,特地唑胺,帕瑞昔布钠,帕布昔利布,赛乐西帕,伏硫西汀,曲格列汀,米拉贝隆,沙芬酰胺,达泊西汀,吡格列酮,达泊西汀,吉非替尼,去甲肾上素,阿昔洛韦,文拉法辛,普拉洛芬,普拉克索,曲唑酮,茚达特罗,阿扎胞苷,酮替芬,依折麦布,西那卡塞,氨曲南,替诺福韦,厄多司坦,孤法辛,雷贝拉唑,阿法替尼,依达拉奉,帕利哌酮,达比加群酯,鲁拉西酮,尼非卡兰,瑞巴派特,苯达莫司汀,利伐沙班,法舒地尔,普拉格雷,维格列汀,索非布韦,文拉法辛等。
盐酸吡格列酮USP标准翻译

▲盐酸吡格列酮定义以干燥品计,盐酸吡格列酮含C19H20N2O3S²HCl不少于98.0%不大于102.0%。
鉴别²A.红外吸收《197》²B.常规鉴别氯化物《191》:称取25mg盐酸吡格列酮溶解于0.5ml硝酸,加入2ml稀硝酸。
结果符合氯化物检验的要求。
²C.照含量测定项下记录色谱图,供试品溶液的主峰保留时间与标准品溶液的主峰保留时间一致。
含量测定²操作流动相:乙腈-0.1M醋酸铵-冰醋酸(25:25:1)标准品溶液:制备一份USP盐酸吡格列酮标准品溶液,先用甲醇稀释浓度为0.5mg/mL,再用流动相稀释制成含盐酸吡格列酮50ug/mL的溶液。
系统适用性储备液:用甲醇配制含USP盐酸吡格列酮标准品0.5mg/mL和含二苯甲酮0.13mg/mL的溶液。
系统适用性溶液:用流动相将系统适用性储备液稀释成含盐酸吡格列酮50ug/mL和含二苯甲酮13ug/mL的溶液。
样品溶液:用甲醇配制一份含盐酸吡格列酮0.5mg/mL的溶液,再用流动相稀释成含盐酸吡格列酮50ug/mL的溶液。
色谱系统(见色谱《621》,系统适用性。
)方法:液相色谱法检测器:UV 269nm色谱柱:4.6mm³15cm;5um 填料 L1柱温:25±2.5°流速:0.7mL/min。
[注:调整流速使吡格列酮峰的保留时间在7min左右。
]进样量:20uL系统适用性样品:系统适用性溶液和标准品溶液[注:吡格列酮和二苯甲酮的相对保留时间分别约为1.0和2.6。
]适用性要求拖尾因子:系统适用性溶液中,吡格列酮和二苯甲酮的拖尾因子不大于1.5分离度:系统适用性溶液中,吡格列酮和二苯甲酮之间的分离度不小于15相对标准偏差:标准品溶液六次重复进样的相对标准偏差不大于2.0%分析样品:标准品溶液和样品溶液通过下列公式计算盐酸吡格列酮中含C19H20N2O3S²HCl的百分比:结果=(r U/ r S)³(c U/c S)³100r U=样品溶液的峰响应值r S =标准品溶液的峰响应值c S=标准品溶液中USP盐酸吡格列酮标准品的浓度(ug/mL)c U=样品溶液中盐酸吡格列酮的浓度(ug/mL)可接受标准:干燥品含量为98.0%—102.0%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
名称
CAS
分子式
规格
1
Hydroxy Pioglitazone
M-IV
10mg
146062-44-4
C19H20N2O 4S
25mg 50mg
100mg
Pioglitazone 2 Ketone (from
M-II)
10mg
N/A
C19H18N2O 25mg
4S
50mg
100mg
3
Pioglitazone Sulfonic Impurity
625853-74-9
C19H20N2O 4S
25mg 50mg
100mg
10mg
9
Pioglitazone EP Impurity B
136401-69-9
C19H18N2O 3S
25mg 50mg
100mg
10mg
10
Pioglitazone EP Impurity C
952188-00-0
C28H31N3O 3S
⑭帕博西尼杂质 ⑮地奈德杂质
⑯阿托伐他汀杂质 ......等更多项目品种欢迎咨询!
并代理其他品牌:EP/USP/TRC/TLC/MC/LGC/RHINO等 欢迎咨询!
25mg 50mg
100mg
10mg
11
Pioglitazone Ketone (M-III)
146062-45-5
C19H19N2O 4S
25mg 50mg
100mg
10mg
12
Pioglitazone EP Impurity D
868754-41-0
C21H26N2O 4S
25mg 50mg
100mg
......更多相关杂质对照品持续供应
湖北瑞诺医药---专注杂质对照品、标准品
优势供应:
①阿加曲班杂质
②雷尼替丁杂质 ③克林Βιβλιοθήκη 素磷酸酯杂质④阿卡波糖杂质
⑤阿曲库铵杂质 ⑥舒更葡糖钠杂质
⑦阿扎胞苷杂质
⑧恩替卡韦杂质 ⑨沙库巴曲杂质(LCZ696)
⑩替诺福韦杂质
⑪普瑞巴林杂质 ⑫克拉维酸钾杂质
⑬利伐沙班杂质
10mg
625853-73-8
C18H22N2O 5S
25mg 50mg
100mg
4
Pioglitazone Bromo Impurity
669716-58-9
C15H16BrN O
10mg 25mg 50mg 100mg
Pioglitazone
5
Imino
Impurity
10mg
N/A
C19H21N3O 25mg
2S
50mg
100mg
结构式
Pioglitazone
6
Fluoro
Impurity
10mg
N/A
C10H8FNO2 25mg
S
50mg
100mg
7
Pioglitazone Metabolite
M1
74772-78-4
10mg
C10H9NO3S
25mg 50mg
100mg
10mg
8
Pioglitazone Impurity A
